Servicios Personalizados
Revista
Articulo
Indicadores
 Citado por SciELO
Citado por SciELO  Accesos
Accesos
Links relacionados
 Citado por Google
Citado por Google  Similares en
SciELO
Similares en
SciELO  Similares en Google
Similares en Google
Compartir
Revista Colombiana de Química
versión impresa ISSN 0120-2804
Resumen
MENDOZA, Johanna; RODRIGUEZ, Oscar y AGREDA, Jesús A. ESTUDO TERMOCINÉTICO DAS REAÇÕES DE ORDEM ZERO, UM E DOIS NUM CALORÍMETRO PSEUDOADIABÁTICO: aproximação numérica e dados experimentais. Rev.Colomb.Quim. [online]. 2012, vol.41, n.1, pp.111-122. ISSN 0120-2804.
O sinal produzido por um calorímetro pseudoadiabático foi simulado mediante a solução numérica das equações dife-renciais que modelam a cinética química [1], as propriedades térmicas da célula calorimétrica [2] e da resposta do termis-tor que foi usado como sensor termométrico [3]. 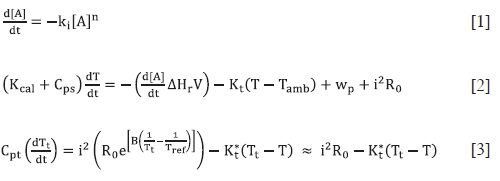 Os resultados obtidos das simulações foram usados para realizar urna compa-ração entre os sinais das três cinéticas básicas (ordem zero, um e dois). Isso serviu para estabelecer um protocolo de estudo da cinética de uma reação a partir de medidas calorimétricas, o qual resulta fundamental, já que como se vê nas equações anteriores, a relação entre a ordem de reação e o sinal calorimétrico não é simples. Para esclarecer este ponto, foi realizado o estudo dos sinais calorimétricos simulados usando o método das velocidades iniciais e compa-raram-se os resultados assim obtidos (ordem de reação e constante cinética) com os valores usados para as simulações. Como era de esperar, as ordens de reação "calorimétricas" não coincidiram com as ordens cinéticas usadas nas simulações, como sucede no caso de dados espectrofotométricos. No entanto, foi possível estabelecer uma relac" o linear entre a ordem "calorimétrica e a ordem cinética que permite obter a ordem de reação de um processo que se estuda com um calorímetro. Finalmente, o procedimento desenvolvido foi aplicado aos resultados calorimétricos experimentais da decomposição de H2O2 catalisada em fase homogênea com Fe3+ e em fase heterogênea com carvão ativado, encontrando as ordens de reação e as constantes cinéticas respectivas de cada processo global, os quais apresentaram boa coincidência com os valores reportados na literatura.
Os resultados obtidos das simulações foram usados para realizar urna compa-ração entre os sinais das três cinéticas básicas (ordem zero, um e dois). Isso serviu para estabelecer um protocolo de estudo da cinética de uma reação a partir de medidas calorimétricas, o qual resulta fundamental, já que como se vê nas equações anteriores, a relação entre a ordem de reação e o sinal calorimétrico não é simples. Para esclarecer este ponto, foi realizado o estudo dos sinais calorimétricos simulados usando o método das velocidades iniciais e compa-raram-se os resultados assim obtidos (ordem de reação e constante cinética) com os valores usados para as simulações. Como era de esperar, as ordens de reação "calorimétricas" não coincidiram com as ordens cinéticas usadas nas simulações, como sucede no caso de dados espectrofotométricos. No entanto, foi possível estabelecer uma relac" o linear entre a ordem "calorimétrica e a ordem cinética que permite obter a ordem de reação de um processo que se estuda com um calorímetro. Finalmente, o procedimento desenvolvido foi aplicado aos resultados calorimétricos experimentais da decomposição de H2O2 catalisada em fase homogênea com Fe3+ e em fase heterogênea com carvão ativado, encontrando as ordens de reação e as constantes cinéticas respectivas de cada processo global, os quais apresentaram boa coincidência com os valores reportados na literatura.
Palabras clave : termocinética; calorímetro pseudoadiabático; cinéticas de ordem zero; um e dois; simulações; de-composição de H2O2.













