Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
DYNA
versão impressa ISSN 0012-7353versão On-line ISSN 2346-2183
Dyna rev.fac.nac.minas v.73 n.148 Medellín jan./abr. 2006
CARACTERIZACIÓN TEXTURAL Y QUÍMICA DE CATALIZADORES TI-SIO2 CRISTALINOS USADOS EN LA EPOXIDACIÓN DE ÉSTERES GRASOS
TEXTURAL AND CHEMICAL CHARACTERIZATION OF CRYSTALLINE Ti-SiO2 CATALYSTS USED IN THE EPOXIDATION OF FATTY ESTERS
LUIS RIOS
Grupo Procesos Fisicoquímicos Aplicados, Departamento de Ingeniería Química, Universidad de Antioquia, Medellín larios@udea.edu.co
GLORIA RESTREPO
Grupo Procesos Fisicoquímicos Aplicados, Departamento de Ingeniería Química, Universidad de Antioquia, Medellín gloma@udea.edu.co
RICARDO SUÁREZ
Grupo Procesos Fisicoquímicos Aplicados, Departamento de Ingeniería Química, Universidad de Antioquia, Medellín
ROSARIO CAICEDO
Grupo Procesos Fisicoquímicos Aplicados, Departamento de Ingeniería Química, Universidad de Antioquia, Medellín
PAULA MAZO
Grupo Procesos Fisicoquímicos Aplicados, Departamento de Ingeniería Química, Universidad de Antioquia, Medellín
ALEXANDER FRANCO
Grupo Procesos Fisicoquímicos Aplicados, Departamento de Ingeniería Química, Universidad de Antioquia, Medellín
DAVID ECHEVERRI
Grupo Procesos Fisicoquímicos Aplicados, Departamento de Ingeniería Química, Universidad de Antioquia, Medellín
Recibido para revisar 19 de Abril de 2005, aceptado 29 de Agosto de 2005, versión final 13 de Septiembre de 2005
RESUMEN: Centros discretos de TiIV dispersos en una matriz de SiO2 actúan como fuertes aceptores de electrones por lo cual son útiles para la activación de moléculas o funciones químicas densas en electrones. La cantidad de estos centros, su dispersión, accesibilidad y coordinación, determinan su eficiencia química; para determinar estas propiedades, varios materiales Ti-MCM-41 se caracterizaron mediante DRX, FTIR, UV-Vis e isotermas de adsorción de N2; también se determinaron la cristalinidad, porosidad y superficie específica de la matriz SiO2 permitiendo correlacionar el ambiente fisicoquímico del titanio y las propiedades texturales del catalizador, con su efectividad en la activación de enlaces O-O presentes en moléculas tipo peróxidos, usados en la epoxidación de aceites vegetales. Los resultados sugieren que la presencia de poros cristalinos, en la epoxidación del metiléster del ácido oleico con TBHP y catalizada con Ti-MCM-41, no es necesaria, puesto que la reacción ocurre principalmente en el área externa a los poros. Lo realmente importante es tener centros de Ti finamente dispersos sobre una área superficial alta y accesible. Por otro lado, la temperatura de reacción deber estar por debajo de 70°C para minimizar la formación de subproductos (cetona).
PALABRAS CLAVE: Ti-SiO2, Ti-MCM-41, epoxidación, aceites.
ABSTRACT: Discrete TiIV centers dispersed in a SiO2 matrix acts as strong electron acceptors, therefore, they are useful in activating molecules or moieties which are electron-rich. The amount, dispersion, accessibility and coordination of these centers determine their chemical efficiency. Several Ti-MCM-41 materials where characterized using DRX, FT-IR, UV-Vis and nitrogen adsorption to evaluate the dispersion, coordination and accessibility of Ti centers as well as the crystallinity, porosity and surface area of the SiO2 matrix. This study allows a correlation between the chemical environment of titanium, textural properties of the catalyst and its performance in the activation of O-O bonds present in peroxides, used for the epoxidation of plant oils. Results suggest that the presence of crystalline pores, in the epoxidation of oleic acid methylester with TBHP catalyzed by Ti-MCM-41, is not necessary, because the reaction occurs in large extension on the external surface area. The important issue is to have the titanium centers finely dispersed on a relatively high surface area. Temperature should be below 70°C to minimize the ketone formation.
KEYWORDS: Ti-SiO2, Ti-MCM-41, epoxidation, oils
1. INTRODUCCIÓN
La epoxidación de aceites vegetales (figura 1) es una reacción comercialmente importante porque los epóxidos obtenidos a partir de estas materias primas renovables tienen diversas aplicaciones tales como plastificantes y estabilizadores de polímeros [1]. Adicionalmente, estos epóxidos pueden ser usados como intermedios para la producción de una gran variedad de derivados debido a la alta reactividad que presenta el anillo epóxico. Por ejemplo, a través de las reacciones de apertura del anillo epóxico con los reactivos adecuados se podrían producir mono-alcoholes, dioles, alkoxialcoholes, hidroxiésteres, N-hidroxialquilamidas y mercaptoalcoholes [2].
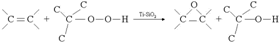
Figura 1. Esquema general de reacción de epoxidación.
Figure 1. General path of epoxidation reaction
Ha sido reportado que Ti-SiO2 en su forma cristalina hexagonal, conocido como Ti-MCM-41, es un catalizador muy efectivo para activar peróxidos durante la epoxidación de alquenos de gran tamaño molecular, debido a la gran accesibilidad al titanio que brindan sus amplios poros (20-40 Å de diámetro) [3]. También es ampliamente conocido que solo átomos de titanio que están
en coordinación tetraedral dentro de la matriz de SiO2 son activos para esta reacción [4,5]. Sin embargo, no se ha estudiado en detalle el efecto de las propiedades texturales del catalizador en la eficiencia química para este tipo de reacciones. En este trabajo se estudiaron las propiedades texturales y químicas más importantes que inciden sobre la actividad de Ti-MCM-41 para la epoxidación de alquenos voluminosos tales como el oleato de metilo (diámetro molecular promedio de 9 Å).
2. EXPERIMENTAL
Los materiales Ti-MCM-41 se prepararon siguiendo el procedimiento desarrollado por Nießen et al. [6] usando sílica Aerosil (Degussa 200), bromuro de tetradeciltrimetilamonio (purum, Fluka), hidróxido de tetraetilamonio (Fluka, 40 % en agua) y (NH4)3[TiO2F5] [7]. Se sintetizaron cuatro catalizadores Ti-MCM-41 cambiando la cantidad de la fuente de Ti adicionada al gel de síntesis: Ti-MCM-41(0.8), Ti-MCM-41(2.2), Ti-MCM-41(2.7), Ti-MCM-41(2.9). El número en paréntesis denota la relación molar Ti/Si x100, determinada mediante análisis químico global (ICP-AES). Los patrones de difracción de rayos X se tomaron en un difractómetro con radiación CuKa (Siemens D5000). Los análisis de composición química global se realizaron por espectroscopía de emisión atómica (ICP-AES, Spectroflame D, Spectro). Los análisis FT-IR se realizaron en un equipo Nicolet Protégé 460, mediante la técnica de transmisión, los espectros fueron tomados a temperatura ambiente bajo un flujo de aire seco. Los espectros UV-Vis se tomaron por la técnica de reflectancia difusa en un equipo Lambda 7 (Perkin Elmer), usando BaSO4 como referencia. Las isotermas de adsorción-desorción de N2 se midieron en un equipo Coulter Omnisorp, antes de la medición las muestras fueron desgasificadas durante 4 h a 200°C y 10-2 Pa.
Las mezclas reaccionantes se analizaron por cromatografía gaseosa en un equipo Hewlet Packard HP 6890 usando la columna FS-SE54 ( 60 m). Los productos puros de caracterizaron mediante GC-Mass Spectrometry (GC Varian 3400 CX, MS Varian Saturn 3 at 70 eV and electron ionization), FT-IR (Nicolet Protégé 460, NaCl windows) así como por 1H (300 MHz) y13C NMR (75 MHz) con experimentos dept90 y dept135. La concentración del hidroperóxido se determinó por iodometría. Las epoxidaciones se realizaron en reactores de vidrio de fondo redondo localizados en un baño de aceite el cual se mantuvo a la temperatura deseada. La agitación se realizó usando barras magnéticas recubiertas con teflón. El sustrato usado fue el metiléster del ácido oleico (Fuchs Petrolub AG, 97 wt.% metiléster del ácido cis-9-octadecenóico). Todos los catalizadores fueron evacuados a 120°C y alto vacío. Las solución del hidroperóxido en tolueno se deshidrató sobre malla molecular UOP-3A.
3. RESULTADOS Y DISCUSIÓN
3.1 Caracterización de los catalizadores Ti-MCM-41El arreglo cristalino hexagonal de los catalizadores fue confirmado por los patrones de difracción de rayos X (figura 2). En todos los catalizadores se observa un pico a 2.2 grados el cual se debe al plano de difracción 1-0-0, e indica la simetría hexagonal. En el caso de Ti-MCM-41(2.7) y Ti-MCM-41(2.9) se obtuvieron dos picos adicionales de alto orden, asociados a los planos 1-1-0 y 2-0-0.
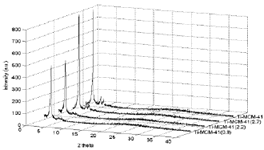
Figura 2. Espectros DRX para el catalizador Ti-MCM-41
Figure 2. DRX spectra of Ti-MCM-41 catalysts
Se realizaron análisis FT-IR y UV/Vis para evaluar el estado del Ti en la red del catalizador. Los resultados de estos análisis se discuten en detalle porque ellos son cruciales para entender el comportamiento catalítico mostrado más adelante. Los resultados FT-IR se presentan en la figura 3; se observan cuatro bandas de absorción características. La banda centrada a 810 cm-1 se debe al estiramiento/doblamiento simétrico de los enlaces Si-O-Si. La banda a 1085 cm-1 con el hombro a 1220 cm-1 se origina del estiramiento asimétrico Si-O-Si. La banda más importante en este contexto, la banda a 960 cm-1, es una evidencia, aunque no decisiva, de la incorporación de Ti en posiciones tetraedrales de la red de SiO2. Esta banda resulta de la superposición de modo de estiramiento de los grupos silanol Si-(OH) con el modo de estiramiento asimétrico de los grupos Si-O-Ti [8].
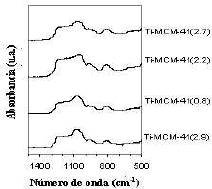
Figura 3. Espectros FT-IR de los catalizadores Ti-MCM-41
Figure 3. FT-IR spectra of Ti-MCM-41 catalysts
La asignación de esta banda a los sitios con Ti ha sido objeto de debate, sin embargo hay pruebas muy concluyentes que permiten hacer esta asignación [9]. La ausencia de la banda a 960 cm-1 indicaría, sin duda alguna, la no incorporación del Ti, pero su presencia no es suficientemente concluyente para probar la incorporación de Ti. Otro aspecto importante es que ninguno de los catalizadores muestra bandas de absorción en la región 700-400 cm-1, rango en el cual el TiO2, como una fase separada, absorbe.
Los resultados de los análisis UV/Vis se presentan en la figura 4. Ninguna de las muestras presenta absorción alrededor de 340 nm, que es la longitud de onda a la cual absorben la anatasa y estructuras TixOy relativamente grandes formadas por octaedros condensados de Ti [9]. Todas las muestras tienen un máximo de absorción entre 208-220 nm, el cual está asociado a la transición de nivel a nivel debido a centros aislados de Ti [10]; por ejemplo, Ti[OCH(CH3)2]4 tiene un pico de absorción centrado a 222 nm.
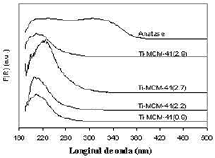
Figura 4. Espectros UV/Vis de los catalizadores Ti-MCM-41
Figure 4. UV/Vis spectra of Ti-MCM-41 catalysts
Los análisis de adsorción de N2 se realizaron para determinar algunos parámetros físicos importantes tales como área superficial, volumen de mesoporos y diámetro promedio de mesoporo. Estos resultados, junto con los de otros análisis como DRX y densidad de sólido, permitieron la determinación de las propiedades texturales que ayudarán a explicar la actividad catalítica. La figura 5 muestra las isotermas de adsorción-desorción de nitrógeno para los catalizadores Ti-MCM-41.
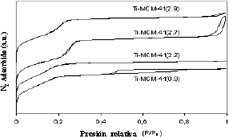
Figura 5. Isotermas de adsorción-desorción de N2
Figure 5. N2 Adsorption-desorption isoterms
Tres de los materiales muestran los típicos lazos de histéresis en forma de triángulo y paralelogramo, el último de los cuales corresponde al tipo I (IUPAC). El lazo de histéresis está ausente en Ti-MCM-41(2.2), esto es una indicación del pequeño tamaño de poro de este material [11], un hecho que se confirmará más adelante. Tal como se mencionó anteriormente, las propiedades texturales de los catalizadores Ti-MCM-41 se determinaron para establecer su influencia en la actividad catalítica. Estas propiedades se calcularon siguiendo el método propuesto por Fenelovov et al. [12] y los resultados se resumen en la tabla I.
Tabla 1. Propiedades texturales de los catalizadores Ti-MCM-41
Table 1. Textural properties of Ti-MCM-41 catalysts
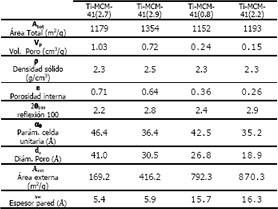
El área superficial total se calculó usando la ecuación BET, el volumen total de poro se calculó con el método BJH, la densidad del sólido se midió en un auto-picnómetro con helio a 26°C, el ángulo 2q para la reflexión 1-0-0 se determinó a partir de patrón XRD, los otros parámetros de la tabla fueron calculados de acuerdo con el modelo de Fenelovov.
3.2 Resultados catalíticos con Ti-MCM-41Después de la caracterización de los catalizadores Ti-MCM-41, se discute sobre la actividad de estos materiales en la epoxidación del oleato de metilo y su correlación con todos los análisis previos. En primer lugar, se revisó el efecto de la temperatura; el aumento de temperatura desde 25°C hasta 100°C produce una caída en la selectividad de alrededor de un 10%, mientras que la conversión se incrementa desde un 10% hasta un 90%. El mecanismo propuesto para la epoxidación del aceite se presenta en la figura 6 en base a los centros discretos de Ti en una matriz de SiO2 cuyo subproducto obtenido se identificó como la cetona, obtenida mediante el rearreglo del epóxido. Aunque el rearreglo de epóxidos pequeños es una reacción bien documentada [13], hasta donde nuestro conocimiento llega, el rearreglo de aceites epoxidados no ha sido aun reportado; usualmente, los únicos subproductos reportados son los que provienen de las reacciones de apertura del epóxido. Haciendo un compromiso entre conversión y selectividad se seleccionó 70°C como la temperatura óptima para realizar las reacciones en las que se compararán los diferentes catalizadores. La figura 7 muestra los resultados obtenidos en la epoxidación del oleato de metilo catalizada por los materiales Ti-MCM-41.
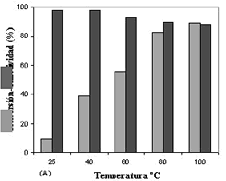
Figura 6. Mecanismo molecular de epoxidación catalizada con centros de Ti en presencia de TBHP.
Figure 6. Molecular mechanism of epoxidation catalyzed by Ti centers in presence of TBHP
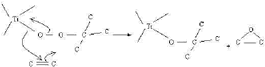
Figura 7. Efecto de la temperatura en la conversión y la selectividad de la epoxidación del oleato de metilo con Ti-MCM-41(2.7). TBHP/C=C 1.1 mol/mol, oleato/catalizador= 20 g/g, tolueno/oleato= 1 g/g, tiempo= 25 h.
Figure 7. Temperature effect over conversion and
selectivity of methyl oleate epoxidation by Ti-MCM-41(2.7).TBHP/C=C 1.1mol/mol, oleate/ catalyst=20 g/g, toluene/oleate= 1 g/g, time= 25 h
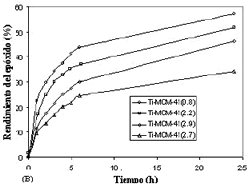
Figura 8. Comparación de los catalizadores Ti-MCM-41 en la epoxidación de oleato de metilo, TBHP/oleato= 1.1 mol/mol, oleato/catalizador=20 g/g, tolueno/oleato= 1 g/g, temp.= 70°C, Selectividad al epóxido mayor de 98%.
Figure 8. Comparison of TI-MCM-41 catalysts for methyl oleate epoxidation, TBHP/oleate= 1.1 mol/mol, oleate/catalyst= 20 g/g, toluene/oleate= 1 g/g, temp.= 70°C, epoxide selectivity >98%
Las diferentes actividades observadas muestran ser una función del nivel de dispersión de Ti (molecular) y de las propiedades texturales de los soportes, especialmente del área superficial externa. Esta última propiedad usualmente no ha sido tenido en cuenta para explicar la actividad de catalizadores mesoporosos, pero en esta investigación demostró que es crucial. Ti-MCM-41(2.7) es el catalizador menos activo a pesar de que tiene la mayor carga de Ti. Esta actividad inferior puede ser consecuencia de dos factores: (a) Ti está menos disperso que en todos los otros catalizadores porque la banda de absorción en el espectro UV es la más desplazada hacia las mayores longitudes de onda, y (b) aunque el área superficial total de Ti-MCM-41(2.7) es comparable a la de Ti-MCM-41(0.8) y Ti-MCM-41(2.2), su área superficial externa es la más pequeña (ver tabla I). La relevancia del área superficial externa para esta reacción se confirma cuando se comparan Ti-MCM-41(2.2) y Ti-MCM-41(2.9). Aunque el último catalizador tiene una mayor carga de Ti, en un grado de dispersión similar (según los espectros UV e IR), y una mayor área superficial total, es menos activo que el primero. Una posible explicación para esta menor actividad es la menor área superficial externa que tiene Ti-MCM-41(2.9) comparada con la de Ti-MCM-41(2.2). Otro aspecto importante en la figura 4-B es la actividad superior de Ti-MCM-41(0.8). Basándose en los espectros UV e IR, así como en la baja carga de Ti que tiene este catalizador (la menor de todas), se puede concluir que tiene la mayor dispersión de Ti. Además, este catalizador tiene una alta área superficial externa, similar a la de Ti-MCM-41(2.2).
Un parámetro que es de extrema importancia para la aplicación industrial de las tecnologías de epoxidación es la eficiencia en el consumo del hidroperóxido, la cual debe ser maximizada. Las selectividades del hidroperóxido de tertbutilo (TBHP) en los experimentos que se mostraron en la figura 7 fue en todos los casos mayor del 97% (calculada mediante la titulación iodométrica del peróxido). Esta alta selectividad del TBHP podría ser consecuencia de una rápida difusión de la olefina hacia el complejo peroxo-Ti-TBHP (figura 6), del cual toma el oxígeno antes de que sea emitido al gas (descomposición del peróxido).
4. CONCLUSIONESLos resultados sugieren que la presencia de poros cristalinos, en la epoxidación del metiléster del ácido oleico con TBHP y catalizada con Ti-MCM-41, no es necesaria, puesto que la reacción ocurre principalmente en el área externa a los poros. Lo que realmente es importante es tener los centros de Ti finamente dispersos sobre un área superficial alta y accesible. Después de esta conclusión tan importante, resulta obvio pensar que una simple sílica amorfa cargada con Ti podría ser también un catalizador eficiente, siempre y cuando el Ti esté disperso adecuadamente y el área superficial sea alta. Actualmente se está estudiando la reacción con catalizadores de este tipo. Por otro lado, la temperatura de reacción deber estar por debajo de 70°C para minimizar la formación de subproductos (cetona).
AGRADECIMIENTOS
Los autores agradecen el apoyo de la Universidad de Antioquia y COLCIENCIAS para la realización de esta investigación.
REFERENCIAS [ Links ][2]














