Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
DYNA
versão impressa ISSN 0012-7353versão On-line ISSN 2346-2183
Dyna rev.fac.nac.minas v.74 n.151 Medellín jan./abr. 2007
SENSORES DE GAS DEL SISTEMA Sn-Sb
USE OF CHEMICAL METHODS TO OBTAIN Sn-Sb GAS
SENSOR
ALEJANDRA MONTENEGRO
Grupo CYTEMAC. Departamento de Física, Universidad del Cauca, amontenegro@unicauca.edu.co
MIGUEL PONCE
Instituto de Investigaciones en Ciencia y Tecnología de Materiales, INTEMA, Mar del Plata, Argentina. mponce@fi.mdp.edu.ar
MIRIAM CASTRO
Instituto de Investigaciones en Ciencia y Tecnología de Materiales, INTEMA, Mar del Plata, Argentina. mcastro@fi.mdp.edu.a
JORGE RODRÍGUEZ
Grupo CYTEMAC. Departamento de Física, Universidad del Cauca, jnpaez@unicauca.edu.co
Recibido para revisar 21 de Noviembre de 2005, aceptado 11 de Julio de 2006, versión final 15 de Agosto de 2006
RESUMEN: Los sensores de gas basados en óxidos semiconductores presentan un cambio en la resistencia cuando son expuestos a ciertos gases. El óxido de estaño, SnO2, es el compuesto más utilizado en la fabricación de sensores de gas, y con el fin de mejorar su eficiencia normalmente se le adicionan óxidos de paladio, bismuto, antimonio entre otros. Durante el desarrollo de este trabajo se realizó la síntesis de polvos cerámicos del sistema SnO2 –Sb2O3 utilizando los métodos de precipitación y precursor polimérico (Pechini). Los polvos cerámicos fueron caracterizados con ATD/TG, DRX y FTIR. Además, se muestra la microestructura obtenida por MEB y el comportamiento eléctrico de películas gruesas conformadas con los polvos cerámicos obtenidos sobre substratos de alúmina, determinando el cambio de la resistencia eléctrica del sistema en función del tiempo de exposición a una atmósfera (oxígeno o monóxido de carbono). El principal interés de este trabajo fue determinar el efecto del método de síntesis, así como el de la concentración de Sb2O3 como aditivo, sobre las propiedades sensoras de sistemas con base en SnO2.
PALABRAS CLAVE: Sensor de gas; Síntesis; SnO2 - Sb2O3; Precipitación; Precursor Polimérico.
ABSTRACT: Semiconductor metal oxide-based gas sensors change their resistance when they are exposed to certain gases. Tin oxide, SnO2, is the dominant compound in gas sensors production; however its efficiency is generally improved by adding additives as palladium, bismuth, antimony oxides among others. In this work, SnO2-Sb2O3 ceramic powders were obtained by using precipitation methods and polymeric precursor (Pechini) methods. The ceramic powders were characterized through DTA/TG, XRD and FTIR. Using the resulting powders, thick films were conformed onto alumina substrates. SEM micrographs and electrical response at several atmospheres, sensitivity and stability of the gas sensor were recorder. This paper focuses on the influence of the synthesis method, as well as the effect of the Sb2O3 concentration on the sensor properties.
KEY WORDS: Gas sensor; Synthesis; SnO2 – Sb2O3; Precipitation; Polymeric precursor
1. INTRODUCCION
El SnO2 es un semiconductor tipo n con gran estabilidad química y mecánica, propiedades que lo hacen útil para diferentes usos tecnológicos, entre ellos como sensor de gas [1,2]. La sensibilidad del óxido de estaño a la presencia de gases reductores es el resultado de una reacción química del oxígeno quimisorbido sobre su superficie con gases como el hidrógeno, el monóxido de carbono o los hidrocarburos [3,4]. El oxígeno adsorbido en la superficie del SnO2 toma electrones de la banda de conducción del óxido ocasionando la disminución de su densidad de carga electrónica y por lo tanto de su conductividad [5,6].
Por otro lado, el SnO2 presenta vacancias de oxigeno que se forman durante el tratamiento térmico al que es sometido el óxido y que se puede expresar a través de la siguiente reacción:
![]()
donde V¨O representa una vacancia de oxigeno con dos cargas positivas, y SnxSn y Oxo las posiciones normales del Sn y el O en la red [7]; la generación de vacancias de oxigeno y electrones libres contribuyen al incremento de la conductividad del óxido de estaño.
La adición al SnO2 de un catión trivalente, como el Sb3+, permite incrementar el número de vacancias de oxigeno, ocasionando un incremento en la conductividad; la reacción que ocurre por la adición del Sb3+ al sistema se puede expresar así:
![]()
donde SbSn representa la sustitución del Sn4+ por el Sb3+ generándose una vacancia de oxigeno en cualquier lugar. Si en el sistema estuviera presente el Sb5+, la conductividad del estaño aumentaría debido a la generación de electrones libres [8]:
![]()
Lo anterior muestra que las propiedades eléctricas de los cerámicos policristalinos de SnO2 dependen fuertemente de la química de defectos que pueda ocurrir en ellos y que ellas se ven afectadas por el método de preparación del polvo cerámico, la temperatura y atmósfera utilizadas para realizar el tratamiento térmico del compuesto. Considerando concretamente la síntesis de los polvos cerámicos de SnO2, puro o dopado, los métodos más importantes que se han utilizado para obtenerlos son: sol-gel, coprecipitación de oxalatos o hidróxidos, precursor polimérico, reacciones en estado sólido a través de la descomposición de carbonatos, deposición en fase vapor y la oxidación de SnO (a) a SnO2 por crecimiento epitaxial [9-11].
En este trabajo se utilizaron dos métodos de síntesis, precipitación y Pechini para obtener polvos cerámicos del sistema SnO2–Sb2O3 con diferentes composiciones. Los polvos cerámicos obtenidos se caracterizaron utilizando difracción de rayos X (DRX), análisis térmico diferencial (ATD) y Termogravimetrico (TG), y Espectroscopia Infrarroja con transformada de Fourier (FTIR). Los polvos cerámicos se utilizaron para conformar películas gruesas sobre sustratos de alúmina a los que previamente se les depositaron electrodos de oro. Las películas conformadas se caracterizaron mediante microscopia electrónica de barrido (MEB) y se les determinó la variación de su resistencia eléctrica al colocarlas en presencia de atmósferas de O2 y CO y someterlas a temperatura. Con base en estos últimos resultados, se determinó la sensibilidad y tiempo de estabilización del sistema SnO2 –Sb2O3 como sensor de gas.
2. PARTE EXPERIMENTAL
2.1 Obtención de los polvos cerámicos de SnO2 -Sb2O3 mediante el método de precipitación
Se prepararon separadamente soluciones acuosas 0.3 M de Sulfato de estaño (SnSO4 –Fisher Scientific 95%) y 0,1M de acetato de antimonio ((CH3CO2)3Sb-Aldrich 99.99%), con la adición de ácido nítrico (HNO3-Carlo Erba 99%). La solución del precursor de estaño se agitó constantemente a 200 r.p.m., a temperatura ambiente, hasta que no se observaron partículas en suspensión ni sedimentadas. Luego se adicionó hidróxido de amonio (NH4OH-Mallincrodt 28%) a una velocidad de 0.034 mL/seg utilizando para ello un dosificador (Metrohm Dosimat 685). La variación del pH del sistema, a medida que se adicionaba el NH4OH, se midió con un pH-metro (Metrohm 744); el pH del sistema se graficó en función del volumen adicionado de precipitante (NH4OH). Se suministró base débil a la solución hasta alcanzar un valor de pH previamente definido con base en las curvas de valoración potenciométrica del sistema de estaño. Para obtener las nanopartículas de óxido de antimonio, se diluyo el acetato de antimonio en una mezcla de etilenglicol y ácido cítrico, agitando la solución a una velocidad de 200 r.p.m.
Posteriormente se adicionó NH4OH hasta que se alcanzo un valor de pH de 8.3 conforme a estudios previos. Las soluciones obtenidas se mezclaron uniformemente utilizando un equipo de dispersión de alta cizalla, Ultraturrax Marca IKA Mod. T-50, sometiendo la mezcla a agitación a una velocidad de 4000 r.p.m., durante 3 minutos. La suspensión final se dejó envejecer 24 horas a temperatura ambiente y luego se filtró a vacío para eliminar en gran parte el solvente del sistema; el sólido húmedo se redispersó en 200 mL de agua destilada utilizando el equipo de dispersión. Este proceso se repitió dos veces más y al final el producto obtenido se secó en una estufa a 60 °C durante 12 horas.
El sólido resultante del secado se maceró utilizando un mortero de ágata. Las composiciones de los sistemas estudiados, obtenidos por precipitación, se indican en la tabla 1.
Tabla 1. Concentración de oxido de estaño y antimonio para obtener las muestras.
Table 1. Tin and antimony oxides concentrations.

2.2 Obtención de los polvos cerámicos de SnO2-Sb2O3 mediante el método de precursor polimérico (Pechini)
Para obtener el polvo cerámico por el método Pechini, inicialmente se calentaron 59,11 mL de etilenglicol (Mallinckodt 99.5%) a 70°C y se le adicionó lentamente 52,54 g. de ácido cítrico (Carlo Erba 99%) agitando continuamente la solución, hasta obtener una solución transparente. Por separado se preparó una solución acuosa 0,1M de acetato de antimonio (Aldrich 99.99%) adicionándole ácido nítrico (Carlo Erba %). A la solución de etilenglicol y ácido cítrico se le adicionaron el sulfato de estaño y la solución del precursor de antimonio.
Cuando la mezcla de los precursores con etilenglicol y el ácido cítrico quedó totalmente transparente, se redujo la temperatura a 25°C y se comenzó a adicionar NH4OH hasta llevar la solución a un pH de 9. Una vez alcanzado este valor de pH, garantizando que no se había formado ningún precipitado en el sistema, se calentó la solución a 140°C, bajo agitación constante, hasta que se formó una resina de color negra. La resina obtenida se calcinó a 350°C y el sólido resultante de esta pre-calcinación se maceró utilizando un mortero de ágata. Las composiciones de los sistemas estudiados, obtenidos por Pechini, se indican en la tabla I.
2.3 Caracterización de los polvos cerámicos obtenidos
Los polvos obtenidos, tanto por precipitación como por Pechini, fueron caracterizados inicialmente con Análisis Térmico ATD/TG, utilizando para ello un termo analizador diferencial DTA-50 Shimadzu, en una atmósfera de aire seco con flujo de 7l/min y a una velocidad de calentamiento de 10°C/min.; con esta técnica se determinaron las temperaturas donde ocurrían cambios de fase, descomposición de fase orgánica y procesos de cristalización. A partir de estos resultados se definió la temperatura a la que se deben someter los polvos cerámicos para obtener los óxidos de interés. Para la determinación de las fases cristalinas presentes en los polvos cerámicos se utilizó difracción de rayos X (DRX); el equipo que se empleo fue un difractómetro marca Philips, utilizando la radiación del Co con l igual a 1,790Å. Además, se uso Espectroscopia infrarroja con transformada de Fourier, para determinar los grupos funcionales presentes en el sistema; los espectros fueron tomados con un espectrofotómetro FTIR Nicolet Model IR200 spectrometer. La distribución de tamaño de partícula de los polvos cerámicos sintetizados se midio utilizando un equipo Micromeritics Sedigraph 5000D y el tamaño y morfología de las partículas se definieron utilizando Microscopía Electrónica de Barrido (MEB) (Jeol 6460 LV).
2.4 Caracterización eléctrica de las películas gruesas
Para la conformación de las películas gruesas se utilizaron sustratos de alúmina, a los cuales previamente se les depositaron electrodos de oro mediante la técnica de sputtering. Los polvos cerámicos de dióxido de estaño dopados con antimonio fueron mezclados con glicerol y finalmente depositados mediante la técnica de screen printing. Una vez depositados, las películas fueron calcinadas a 500?C y enfriadas rápidamente a temperatura ambiente.
Una ves obtenidas las películas se introdujeron en el equipo diseñado para las medidas. Para la medición de resistencia, en función del tiempo. Se introdujeron en la celda los sustratos de alúmina que soportan las películas de SnO2-Sb2O3 y se elevo la temperatura hasta alcanzar el valor deseado (250?C o 350?C). Se realizó vació en la celda para permitir la desorción de gases que pudieran haber quedado retenidos por la exposición de la película al medio ambiente. Posteriormente se permitió la entrada de los gases, oxígeno ( mmHg) o monóxido de carbono (mmHg). El instante en el que entra el gas a la celda define el tiempo inicial t=0 de la medida. Las medidas se llevaron a cabo hasta que los valores de resistencia alcanzaron un estado estacionario. Luego se realizo vació y se continuó con la toma de datos correspondiente.
3. RESULTADOS Y DISCUSIÓN.
3.1 Análisis térmico diferencial (ATD) y análisis termogravimétrico (TG)
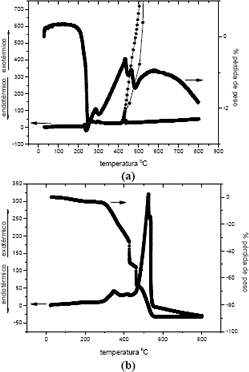
En la Figura 1(a) se indican las curvas de ATD/TG de una muestra obtenida por precipitación controlada. En esta se observa un pico endotérmico alrededor de 250°C asociado a una disminución de peso, debido posiblemente a la descomposición de compuestos oxi-hidróxidos de Sn y Sb que se habrían formado como resultado de la hidrólisis de los cationes. Alrededor de 300°C se observa un pequeño pico endotérmico, asociado a un aumento de peso, debido al cambio del estado de oxidación del antimonio: de Sb3+ a Sb4+. A 450°C se observa un gran pico exotérmico que puede indicar la cristalización de la casiterita SnO2 y la oxidación del acetato remanente. Algo similar se observa para las diferentes muestras estudiadas que contienen distintas concentraciones de antimonio.
Figura 1. Curvas de ATD y TG de la muestra con 0,5% en moles de Sb, obtenida por el método de precipitación controlada (a) y Pechini (b).
Figure 1. TG and DTA curves of sample with 0,5 mol % Sb, obtained to precipitation (a) and Pechini (b) methods.
En la Figura 1(b) se indican las curvas de ATD/TG de una muestra obtenida por el método Pechini donde se observa una gran pérdida de peso que comienza a los 350°C, asociado a dos picos exotérmicos apreciables por encima de los 400°C que debe corresponder a la descomposición de los compuestos orgánicos existentes en la muestra y a la iniciación de la cristalización del SnO2. Esto comportamiento se observa en las muestras obtenidas por este método con diferentes concentraciones de oxido de antimonio (tabla I).
3.2 Difracción de Rayos X (DRX)
Con el objetivo de identificar las principales fases cristalinas presentes en las muestras se utilizó difracción de rayos X (DRX). Los difractogramas de rayos X correspondientes a los diferentes sistemas estudiados se muestran en la figuras 2 (a) y (b).
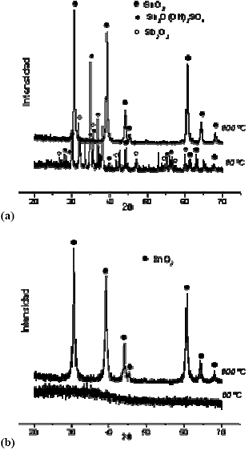
Figura 2. Difractogramas de Rayos X de la muestra con 0,5% en moles de Sb, tratada térmicamente a 60 y 600°C. Las muestras se obtuvieron por precipitación (a) y Pechini (b).
Figure 2. XRD pattern of the sample with 0,5 mol % Sb thermally treated at 60 or 600°C, obtained to precipitation (a) and Pechini (b) methods.
La figura 2(a) muestra los difractogramas de rayos X correspondientes al sistema SnO2–Sb2O3 sintetizado por el método de Precipitación Controlada. El difractograma que corresponde a la muestra sin calcinar presenta, principalmente, las siguientes fases cristalinas: SnO2 (PDF41-1445), Sn3O(OH)2SO4 (PDF30-1376) y Sb2O3 (PDF72-1334), principalmente. El difractograma de Rayos X de la muestra sometida a tratamiento térmico, a 600°C, presenta la casiterita, SnO2, como única fase cristalina, aunque no se descarta la presencia de la fase Sb2O4 (PDF80-0232). Las mismas fases cristalinas se presentaron para las diferentes composiciones de antimonio estudiadas y obtenidas utilizando el método de precipitación.
En la Figura 2(b) se indican los difractogramas de rayos X obtenidos para las muestras sintetizadas por Pechini. A partir de ellos se observa que el polvo sin tratamiento térmico es amorfo. El difractograma de rayos X del sólido tratado térmicamente a 600°C muestra que la principal fase cristalina presente es el SnO2 (41-1445). Esta fase cristalina se presento para las diferentes composiciones de antimonio estudiadas y obtenidas utilizando el método Pechini.
3.3 Espectroscopia infrarroja con transformada de Fourier
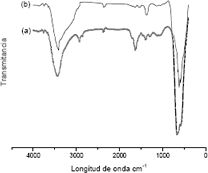
En la figura 3 se muestra el espectro correspondiente al sólido obtenido por el método de precipitación controlada (a) y método Pechini (b) con tratamiento térmico a 600°C.
Figura 3. Espectros FTIR de la muestra con 1% en moles de Sb tratada térmicamente a 600°C. La muestra se obtuvo utilizando método precipitación controlada (a) y método Pechini (b).
Figure 3. IR spectra, of the sample with 0,5 mol % Sb, obtained to precipitation (a) and Pechini (b) methods.
En los espectros se hacen evidentes las bandas a 650cm-1, correspondientes al SnO2, y la del enlace Sn-O-H a 890cm-1; por otro lado, con baja intensidad se presentan las bandas a 1060cm-1, correspondiente a sulfato monodentado, la banda asociada al (NH4)2SO4 a 1380cm-1, la del H-O-H a 1640cm-1, C-O en 2360cm-1, y las del O-H a 2860cm-1, 2930cm-1, y 3440cm-1. Además se hace evidente la banda a 1290cm-1 que corresponde al ión sulfato libre.
3.4 Morfología y tamaño de partícula de los polvos cerámicos obtenidos
Los estudios de distribución de tamaño de partícula, utilizando sedigrafía, indican que la muestra Sn1Sb obtenida por el método Pechini presenta un valor medio de tamaño de partícula de ~ 3,5 µm y el 20% y 80% de la distribución contienen tamaños entre ~ 0,7 µm y ~ 10 µm respectivamente.
Considerando los resultados anteriores se puede concluir que la ancha distribución de tamaño de partícula observada es debida a la existencia de aglomerados en el polvo cerámico, por lo que los tamaños indicados deben corresponder realmente al de estos aglomerados y no a las partículas individuales; esto se comprobó observando la micrografía de la película gruesa obtenida con MEB.
La Figura 4 muestra la micrografía obtenida con MEB de la superficie de la película conformada con polvos obtenidos por Pechini y que tienen una concentración de 3 % en moles de antimonio; en ella es evidente la presencia de aglomerados constituidos por partículas primarias de tamaño < 200nm. Este problema de aglomeración es necesario corregirlo por el efecto que tiene sobre la funcionalidad sensora de la película. Para ello se puede adicionar una etapa de molienda en atrición, para romper los enlaces entre partículas, o la adición de un surfactante, por ejemplo ácido oleico, que genere un efecto estérico e impida la unión entre ellas.
Figura 4. Micrografía obtenida con MEB, de la película conformada con la muestra que contiene 3% en moles de Sb, obtenida por el método Pechini.
Figure 4. SEM micrographs of the thick film conformed trough powders with 3% mol Sb obtained to Pechini method.
3.5 Caracterización eléctrica
Para determinar el comportamiento de las soluciones sólidas SnO2 – óxido de antimonio, como sensores de gas, se registró la variación de la resistencia de cada una de las muestras en presencia de una atmósfera predeterminada, O2 o CO, a una cierta temperatura. Para ello se obtuvieron las curvas de resistencia eléctrica de las películas gruesas, conformadas utilizando los polvos sintetizados en este trabajo, en función del tiempo de exposición a una atmósfera dada y sometidas a dos temperaturas de funcionamiento diferentes. Con base en estas curvas se determinaron los valores de sensibilidad de la muestra al cambiar la condición del entorno de vacío al de atmósfera rica en oxígeno o a monóxido de carbono; en este trabajo la sensibilidad se define como el cociente entre la resistencia estable de la película en presencia de O2, o CO (Rf), y la resistencia que ella presentaba en el vacío (Ri).
En la Figura 5, y en la Tabla 2, se indican los resultados del comportamiento sensor de las películas gruesas del sistema Sn-Sb, con 0.5% en moles de óxido de Sb, conformadas con polvos obtenidos por precipitación.
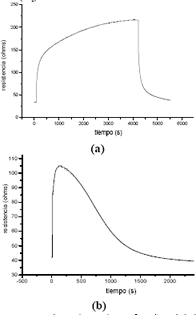
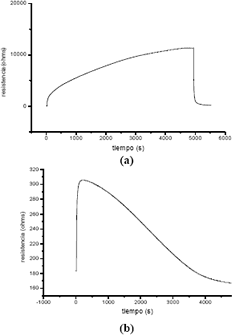
Figura 5. Curvas de resistencia en función del tiempo de exposición a una atmósfera de oxígeno (a) y a monóxido de carbono (b) a 350 °C, para la muestra con 0,5% en moles de Sb, obtenida por el método de precipitación .
Figure 5. Resistance of the film with 0,5 mol % Sb obtained to precipitation method, as a function of the exposition time to oxygen (a) and carbon monoxide (b) atmospheres.
Tabla 2. Sensibilidad y tiempo de respuesta en presencia de O2 y CO, a 250° y 350°C, de películas gruesas del sistema Sn-Sb conformadas con polvos obtenidos por el método de precipitación.
Table 2. Sensitivity and response time, of the system Sn-Sb film obtained to precipitation method, under O2 and CO, at 250°C and 350°C.
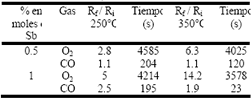
Los datos permiten concluir que al aumentar la temperatura del sistema se favorece la difusión de oxigeno, dentro de la película de SnO2, lo que genera una respuesta más rápida del dispositivo a la presencia del gas correspondiente. Se puede observar que la velocidad de respuesta del sistema no es muy alta, comportamiento que se puede justificar considerando la presencia de aglomerados.
En la Figura 6, y en la Tabla 3, se indica la variación de la resistencia con el tiempo de las películas gruesas del sistema Sn-Sb, conformadas con partículas sintetizadas por Pechini, al colocarlas a las temperaturas de 250°C y 350°C en presencia de O2 o CO.
Figura 6. Curvas de resistencia en función del tiempo de exposición a una atmósfera de oxígeno (a) y a monóxido de carbono (b) a 350 °C, para la muestra con 0,5% en moles de Sb, obtenida por el método Pechini .
Figure 6. Resistance of the film with 0,5 mol % Sb obtained to Pechini method, as a function of the exposition time to oxygen (a) and carbon monoxide (b) atmospheres.
Tabla 3. Sensibilidad y tiempo de respuesta en presencia de O2 y CO, a 250° y 350°C, de películas gruesas del sistema Sn-Sb conformadas con polvos obtenidos por el método Pechini.
Table 3. Sensitivity and response time, of the system Sn-Sb film obtained to Pechini method, under O2 and CO, at 250°C and 350°C.
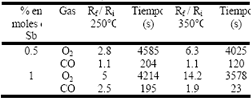
A partir de las Tablas 2 y 3 se tiene que cuando se aumenta el contenido de antimonio en las películas conformadas con polvos sintetizados mediante el método de precipitación, la sensibilidad de la película se incrementa, mientras que el tiempo necesario para alcanzar el estado estacionario disminuye. En cambio cuando las películas son conformadas a partir de polvos sinterizados por el método Pechini, la sensibilidad disminuye con el aumento en el contenido de antimonio, mientras que el tiempo necesario para alcanzar el estado estable depende del gas utilizado en el ensayo. Estos resultados indicarían que el método de síntesis tiene fuerte influencia en las características superficiales de las partículas.
Los valores del tiempo de respuesta de las muestras estudiadas son altos cuando están en presencia de oxígeno, comportamiento ocasionado principalmente por la presencia de aglomerados que generan diversos caminos para la difusión de oxígeno dentro del sólido, dificultando la llegada del O2 a la superficie de las nanopartículas. En un trabajo futuro es necesario estudiar con mayor detalle las características superficiales de las partículas, utilizando por ejemplo XPS, ya que es allí donde ocurren los procesos más importantes para el sensado de los gases.
4 CONCLUSIONES
- Durante el tratamiento térmico a que se somete el polvo cerámico sintetizado, se presenta una ganancia de peso, mostrado por las curvas de TG, debido al cambio del estado de oxidación del antimonio que pasa del Sb2O3 (Sb3+) al Sb2O4 (Sb4+).
- Las muestras sólidas del sistema Sn-Sb, independientemente del método de síntesis, presentan como fase cristalina el SnO2 (PDF-411445) al ser tratadas térmicamente a 600°C.
- Es necesario eliminar los aglomerados presentes en la muestra ya que ellos influyen negativamente en el comportamiento sensor de los sistemas estudiados.
- Los sistemas de Sn-Sb estudiados presentan cambios de su resistencia en presencia de O2 o de CO independiente del método de síntesis utilizado para obtener los polvos utilizados en la conformación de la película.
- La baja velocidad de respuesta de los sistemas, en comparación de los resultados de Ponce et. al. [2] se debe, principalmente, a la presencia de aglomerados en las muestras.
- El método de síntesis modifica la superficie de las partículas sintetizadas.
AGRADECIMIENTOS
Los autores desean agradecer al proyecto PROALERTA VIII-13 de la Red CYTED de Materiales Electrocerámicos, por la ayuda económica brindada a la Srta. Alejandra Montenegro para realizar su pasantía en la División Cerámicos del Instituto de Investigaciones en Ciencia y Tecnología de Materiales-INTEMA / Mar del Plata- Argentina
BIBLIOGRAFIA
[1] GAJDOSIK L. The concentration measurement with SnO2 gas sensor operated in the dynamic regime. Sensors and actuactors B: chemical, 106, issue, 691-694. 2005. [ Links ]
[2] PONCE M, CASTRO M, MONCADA J, ECHEVARRIA M, ALDAO C. Efectos de la exposición a vacío y aire de películas de SnO2 con distinto espesor. Mat. Res. 6, no. 4. 2003. [ Links ]
[3] SZE S.M, 1994.Semiconductors sensors, Nacional Chao Tung University, Ed. John Wiley. [ Links ]
[4] SERRINI P, BRIOIS V, Chemical composition and crystalline structure of SnO2 thin films used as gas sensor, Thin Solid Films 304, 13-122, 1997. [ Links ]
[5] HUAMÁN FERNANDO, REYES L. Detección de vapor de etanol por modificación de la conductividad eléctrica del dióxido de estaño TECNIA,Vol 8 N°01, Universidad Nacional de Ingeniería Lima – Perú, 2001. [ Links ]
[6] BERNARDI M.I.B., SOLEDADE L.E., Influence of the concentrations of Sb2O3 and the viscosity of the precursor solution and the electrical and optical properties of SnO2 thin films produced by the Pechini method, Thin solid Films 405, 228-233, 2002. [ Links ]
[7] SAMSONOV G V, 1973. The Oxide Handbook, Plenum press, New York. [ Links ]
[8] RODRIGUES E C, OLIVI P. Preparation and characterization of Sb- doped SnO2 films with controlled stoichiometry from polymeric precursors, J. Phys. Chem. Solids 64, 1105-1112, 2003. [ Links ]
[9] GIUNTINI J. C, GRANIER W, ZANCHETTA J. V. TAHA A, Sol-gel preparation and transport properties of a tin oxide, J. Mat. Sci. Lett., 9, 1383-1388, 1990. [ Links ]
[10] LEITE E. R, GOMES J. W, OLIVEIRA M. M, LEE E. J. H., LONGO E., VARELA J. A., Synthesis of SnO2 nanoribbons by a carbothermal reduction process, J. Nanosci. Nanotechn., 2, 125-128, 2002. [ Links ]
[11] ARARAT C., VARELA J.A., RODRIGUEZ P.J. Uso de métodos químicos para la obtención de polvos cerámicos del sistema (Sn,Ti)O2, Bol. Soc. Española ceram. y vidrio. 44, 215-222, 2005. [ Links ]