Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
DYNA
versão impressa ISSN 0012-7353versão On-line ISSN 2346-2183
Dyna rev.fac.nac.minas v.74 n.153 Medellín set./dez. 2007
ECUACIÓN DE CAPRISTE Y LOZANO MODIFICADA PARA PREDECIR LA ELEVACIÓN EN LA TEMPERATURA DE EBULLICIÓN EN SOLUCIONES DE CAÑA DE AZÚCAR
EQUATION OF CAPRISTE AND LOZANO MODIFIED TO PREDICT THE POINT OF BOILIG INCREASING IN SOLUTIONS OF SUGAR CANE
EVERALDO MONTES
Ingeniero Químico, Profesor Universidad de Córdoba, emontes@sinu.unicordoba.edu.co
RAMIRO TORRES
Ingeniero Químico, Profesor Universidad de Córdoba, rtorres@sinu.unicordoba.edu.co
RICARDO ANDRADE
Ingeniero Químico, Profesor Universidad de Córdoba, randrade@sinu.unicordoba.edu.co
Recibido para revisar 08 de septiembre de 2006, aceptado 02 de mayo de 2007, versión final mayo 04 de 2007
RESUMEN: La elevación en la temperatura de ebullición del jugo de la caña de azúcar, utilizando soluciones modelos con cuatro componentes (sacarosa, glucosa, fructosa y dextrana), fue medida experimentalmente en un rango de concentraciones de sólidos solubles de 30 a 60 º Brix y a presiones entre 6.2 x 103 y 7.6 x 104 Pa (abs.). Se utilizó el modelo empírico de Capriste y Lozano para representar los datos experimentales. Los datos experimentales se ajustaron mejor a un modelo modificado de Capriste y Lozano, propuesto por los autores.
PALABRAS CLAVE: Evaporación, Capriste y Lozano, presión de vapor.
ABSTRACT: Boiling temperature changes were measured experimentally for sugar cane juices using model solutions made up of four components (sucrose, glucose, fructose and dextrana), in a rank of soluble solid concentrations of 30 in 60 º Brix and pressures between 6,2 x 103 and 7,6 x 104 Pa (abs.). The empirical model of Capriste and Lozano was used to represent the experimental data. The experimental data adjusted better to a modified model of Capriste and Lozano, proposed by these authors.
KEY WORDS: Steam evaporation, Capriste and Lozano, steam pressure.
1. INTRODUCCIÓN
La producción de azúcar en Colombia, en el año 2005 fue de 2.683.203 toneladas métricas expresadas en volumen crudo (tmvc), reduciéndose 2.07% con respecto al año 2004. Sin embargo los principales indicadores de rendimiento se mantuvieron en el nivel promedio de los últimos 5 años. El 55% del azúcar producido se destina a satisfacer las necesidades del mercado interno del país, mientras que el resto se exporta a diversos países alrededor del mundo (Asocaña, 2006). Estos datos indican la gran importancia de la industria azucarera en la economía colombiana y justifican la investigación que apunta a optimizar el diseño y funcionamiento de las plantas de procesamiento.
El conocimiento de la temperatura de ebullición del jugo de caña en un amplio rango de concentraciones es importante en la industria azucarara, ya que en ésta, se hace necesario dimensionar evaporadores para la concentración del jugo y su posterior cristalización.
Trabajos anteriores han sido orientados al conocimiento del efecto de la temperatura y la concentración en las propiedades termofísicas del jugo de caña, incluyendo la densidad, calor específico, conductividad térmica, difusividad térmica, y propiedades reológicas (Telis-Romero et al., 2000 y Cabral, 2000).
No obstante, no se disponen de datos publicados de la elevación de la temperatura de ebullición a diferentes concentraciones y relaciones de los componentes de éste.
Además, las ecuaciones teóricas tienen un uso limitado, debido a la composición compleja del jugo y la falta de conocimiento de la contribución de los componentes a la elevación de la temperatura de ebullición. Los datos experimentales de esta elevación de jugos de frutas a diferentes concentraciones han sido reportados para: mandarina tailandes (Ilagantileke et al., 1991), manzana (Crapiste y Lozano, 1988 y Moresi y Spinosi, 1984), naranja (Moresi y Spinosi, 1980) y piña, mango y limón (Varshney y Barhate, 1978).
En este trabajo, se determinó la elevación de la temperatura de ebullición de soluciones modelo de jugo de caña a varias concentraciones, relaciones de componentes (sacarosa, glucosa, fructosa y dextrana) y presiones, y se comparó con datos de soluciones de sacarosa, que se usan a menudo como modelos para representar el comportamiento de alimentos fluidos, como jugos de fruta y extractos de café.
2. MATERIALES Y MÉTODOS
Preparación de la muestra
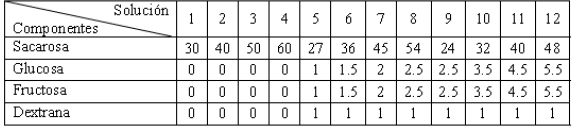
Las soluciones modelos de jugo de caña fueron preparadas con cuatro componentes (sacarosa, glucosa, fructosa y dextrana) obtenidos comercialmente, produciéndose soluciones con concentraciones de sólidos solubles en el rango de 30 a 60 ºBrix, con varias relaciones de sus componentes (tabla 1). La concentración de los sólidos solubles fue medida a 25ºC con un refractómetro Mettler Toledo Modelo 30PX.
Tabla 1. Concentraciones en ºBrix de los componentes de las soluciones modelos de jugo de caña de azúcar
Table 1. Concentrations in ºBrix of the components of the model solutions of juice of cane of sugar
Equipo y procedimiento
Un diagrama esquemático del equipo, similar al utilizado por Telis-Romero, et al. (2002), usado para las medidas experimentales se muestra en la figura 1. Consiste de un balón, de vidrio, fondo plano (F) con tres bocas. Las muestras fueron introducidas en el balón por medio del tubo A y se calentaron en un baño termostatado modelo Lauda 100, con estabilidad de temperatura de ± 0,01°C. Cuando la solución modelo de jugo de caña de azúcar alcanzó la temperatura de ebullición, se estableció un flujo de recirculación entre los tubos B y C. La mezcla líquido-vapor liberada de la superficie líquida fluyó a través del tubo B, donde se determinó la temperatura, con una termocupla, instalada en el termo pozo del tubo B, conectada a un transmisor de datos, una interface y un PC con un programa en Labview. Entretanto el condensado atrapado en el compartimiento D retornó al balón F y permitió al vapor entrar al condensador de reflujo R. El vapor condensado también retornó al balón F a través del tubo C, que tiene una válvula V para controlar la velocidad de flujo de recirculación y garantizar la concentración constante de la solución evaluada.
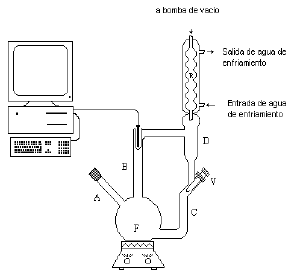
Figura 1. Diagrama esquemático del equipo usado para las medidas experimentales.
Figure 1. Schematic diagram of the team used for the experimental measures.
El condensador fue conectado a una bomba de vacío Stages Vacuum Pump Ce Modelo 2FY-2B que permitió variar la presión en el rango de 5.8 x 103 a 9.4 x 104 Pa (abs.). Un transmisor de presión diferencial fue usado para medir la presión estática en dos posiciones diferentes del tubo de vacío. La temperatura fue monitoreada con una exactitud de 0.6 ºC y la presión con una exactitud de 4.3 mPa, usando un transmisor de datos Modelo HP 75.000-B, una interface HP-BIRF y un PC con un programa escritos en IBASIC.
En cada experimento, se adicionaron 180 mL de solución modelo del jugo de caña en el balón de ebullición. Se hizo recircular agua refrigerante en el condensador de reflujo, fue encendida la bomba de vacío y se reguló la presión hasta aproximadamente 6 x 103 Pa (abs.), con una válvula reguladora, y el fluido se calentó suavemente. Se registraron continuamente temperatura y presión, y los valores finales de la temperatura de ebullición de la solución y su presión asociada, fueron las lecturas más altas registradas cuando permanecieron constantes por lo menos durante 5 minutos.
El procedimiento se repitió hasta llegar a la presión atmosférica, permitiendo medidas de temperatura de ebullición a diferentes presiones con las soluciones a evaluar. Para verificar la concentración de la solución, fue interrumpido el calentamiento periódicamente, el balón se llevó hasta temperatura ambiente, y se tomaron muestras determinando las concentraciones de sólidos solubles en ºBrix. Cuando fue necesario, la solución fue sustituida y la corrida fue repetida.
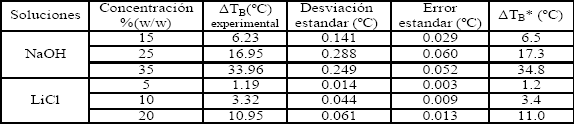
La calibración del equipo se realizó con soluciones acuosas de LiCl y NaOH, a las cuales se les conoce su temperatura de ebullición a varias concentraciones y presiones.
3. RESULTADOS Y DISCUSIÓN
La tabla 2 permite comparar los datos experimentales de la calibración del equipo y los reportados por Perry y Green (2001), mientras la figura 2 muestra un histograma típico de distribución de los datos. La buena concordancia entre los datos experimental y los reportados es resultado de la reproducibilidad del equipo, ya que el histograma muestras una distribución normal de las medidas alrededor de la media. Los valores de la desviación estándar y el error estándar, se incluyen en la tabla 2.
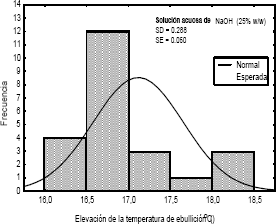
Figura 2. Histograma de distribución de la elevación de la temperatura de ebullición del NaOH.
Figure 2. Histogram of distribution of boiling point increasing of the NaOH.
Tabla 2. Elevación de la temperatura de ebullición de soluciones estándares.
Table 2. Boiling point increasing of standard solutions
Crapiste y Lozano (1988) propusieron un modelo empírico como alternativa para representar la elevación de la temperatura de ebullición de soluciones acuosas, en el cual se refleja la dependencia simultanea de la presión y la concentración de sólidos solubles, dado por la siguiente ecuación:
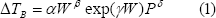
donde ΔTB = (TA - TA0) es la elevación de la temperatura de ebullición en ºC, W representa la concentración másica de sólidos solubles en ºBrix, y los parámetros α, β, γ, y δ son evaluado por regresión no lineal.
Para las soluciones modelo de jugo de caña, la ecuación (1) no representa bien los datos experimentales, ya que tiene un coeficiente de determinación bajo (R2 = 0.7166) y una mala distribución de residuos (Figura 3). Esto es explicado si se tiene en cuenta que la elevación de la temperatura de ebullición de la solución, no solo es afectada por la concentración de sólidos solubles, sino también por la influencia de los diferentes componentes de las soluciones modelo. Sin embargo la ecuación empírica de Crapiste y Lozano, representa bien los datos experimentales cuando se mantiene constante la relación (glucosa + fructosa + dextrana) / sacarosa, y solo varia la concentración de sólidos solubles en la solución, como lo indica sus altos coeficientes de determinación (soluciones 1, 2 ,3 y 4, R2 = 0,9957; soluciones 5, 6, 7 y 8, R2 = 0.9938 y soluciones 9, 10, 11 y 12, R2 = 0.9937).
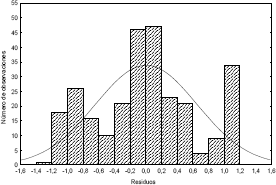
Figura 3. Distribución de residuos para la elevación de la temperatura de ebullición, de acuerdo a la ecuación (1).
Figure 3. Residuals distribution of boiling point increasing according to the equation (1).
Para tener en cuenta la influencia de los diferentes componentes de la solución fue necesario modificar el modelo propuesto por Capriste y Lozano, remplazando la concentración de sólidos solubles, W, por las sumatoria de las concentraciones de cada uno de los componentes de la solución, expresadas en términos de concentración equivalente con respecto al componente de mayor contribución (glucosa) a la elevación de la temperatura de ebullición.
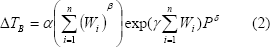
Donde Wi representa la concentración másica de sólidos solubles equivalente del componente i en ºBrix.
Los datos experimentales obtenidos para la elevación de la temperatura de ebullición de las soluciones modelo del jugo de caña, se ajustaron adecuadamente al modelo de Crapiste y Lozano modificado por los autores, ecuación (2), confirmado por el alto valor del coeficiente de determinación (R2 = 0.9747) y una buena distribución de residuos (Figura 4).
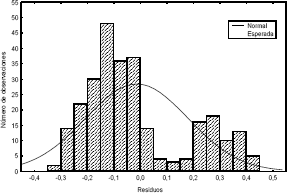
Figura 4. Distribución de residuos para la elevación de la temperatura de ebullición, de acuerdo a la ecuación (2).
Figure 4. Residuals distribution of boiling point increasing according to the equation (2).
El desempeño de la ecuación (2) para predecir la elevación de la temperatura de ebullición de las soluciones modelos de jugo de caña fue verificado graficando los datos observados (experimentales) contra los datos predichos por el modelo, figura 5. La gran mayoría de los datos está dentro de un rango de error de ±12 %, con mayores desviaciones para las Soluciones diluidas, donde el valor del aumento de la temperatura de ebullición tiende a cero.
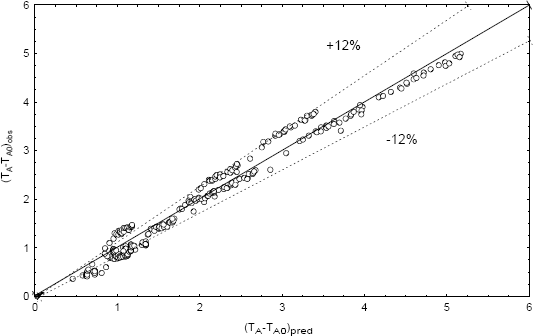
Figura 5. Elevación de la temperatura de ebullición de soluciones modelo de jugo de caña, observado contra predicho por ecuación (2).
Figure 5. Boiling point increasing of model sugar cane solutions, observed against which was predicted by equation (2)
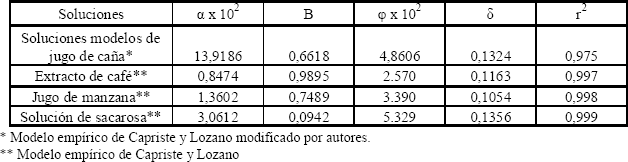
En la tabla 3 se presenta los valores numéricos de los parámetros α, β, γ, y δ, de la ecuación modificada de Crapiste y Lozano, para las soluciones modelo de jugo de caña, al igual que los parámetros de la ecuación de Crapiste y Lozano para el jugo de manzana, soluciones de azúcar (Crapiste y Lozano, 1988) y extracto de café (Telis-Romero et al., 2002). Se observó una similar magnitud de los parámetros γ y δ de las soluciones modelo de jugo de caña estudiada con los del jugo de manzana y de la solución de sacarosa, lo cual indica la poca influencia de los componentes de la solución modelo en estos parámetros. El parámetro β fue similar al del jugo de manzana, pero difiere sustancialmente al de la solución de sacarosa, esto se explica por la contribución que presentan los componentes de la solución modelo a la elevación de la temperatura ebullición.
Tabla 3. Parámetros en la ecuación de Capriste y Lozano para diferentes productos alimenticios.
Table 3. Parameters of Capriste and Lozano for different nutritious products.
4. CONCLUSIONES
Los datos experimentales de la elevación de la temperatura de ebullición para las mismas relaciones constantes de componentes se
ajustaron adecuadamente al modelo empírico propuesto por Crapiste y Lozano (1988). Sin embargo, cuando las relaciones de los componentes de la solución modelo de jugo de caña varían, esta ecuación no representa satisfactoriamente los datos.
La elevación de la temperatura de ebullición para soluciones modelos de jugo de caña, para diferentes relaciones de componentes, es descrita adecuadamente por una ecuación modificada del modelo de Crapiste y Lozano propuesta por los autores.
REFERENCIAS
[1] ASOCAÑA. Aspectos generales del sector azucarero. Disponible: http://www.asocana.org/asocana/Inf2005_2006/index.htm [citado 11 de Julio de 2006]. [ Links ]
[2] CABRAL, R. Influência da Temperatura e Fração de Água nos Parâmetros Reológicos do Extrato de Café [ Master's thesis]. São José do Rio Preto: IBILCE/UNESP, 2000. [ Links ]
[3] CRAPISTE, G. AND LOZANO, J. Effect of Concentration and Pressure on the Boiling Point Rise of Apple Juice and Related Sugar Solutions. Journal of Food Science, 53, No. 3, 865, 1988. [ Links ]
[4] ILAGANTILEKE, S., RUBA JR., A. AND JOGLEKAR, H. Boiling Point Rise of Concentrated Thai Tangerine Juices. Journal of Food Engineering, 15, 235, 1991. [ Links ]
[5] MORESI, M. AND SPINOSI, M. Engineering Factors in the Production of Concentrated Fruit Juices. 1. Fluid Physical Properties of Orange Juices, Journal of Food Technology, 15, 265, 1980. [ Links ]
[6] MORESI, M. AND SPINOSI, M. Physical Properties of Concentrated Apple Juices. In: Engineering and Food, Vol.1, Engineering Sciences in the Food Industry, edited by McKenna, B.M., Elsevier Applied Science Publishers Ltd., Essex, 475, 1984. [ Links ]
[7] PERRY, R. Y GREEN, D. MANUAL DEL Ingeniero Químico. McGraw-Hill/Interamericana de España, S. A. U. España, 2-354, 2-355, 2001. [ Links ]
[8] TELIS-ROMERO, J., GABAS, A., POLIZELLI, M. AND TELIS, V. Temperature and Water Content Influence on Thermophysical Properties of Coffee Extract. International Journal of Food Properties, 3, No. 3, 375, 2000. [ Links ]
[9] TELIS-ROMERO, J., CABRAL, R. AND KRONKA, G. Elevation on boinling point of coffe extract. Braz. J. Chem. Eng., vol.19, no.1, 119-126, 2002. [ Links ]
[10] VARSHNEY, N. AND BARHATE, V. Effect of Concentrations and Vacua on Boiling Points of Fruit Juices. Journal of Food Technology, 13, 225, 1978. [ Links ]














