Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
DYNA
versão impressa ISSN 0012-7353versão On-line ISSN 2346-2183
Dyna rev.fac.nac.minas v.75 n.156 Medellín set./dez. 2008
CARACTERIZACIÓN SUPERFICIAL, ELECTROQUÍMICA Y DE COMPOSICIÓN DE ALEACIONES ZINC NÍQUEL ELECTRODEPOSITADAS
SUPERFICIAL, ELECTROCHEMICAL AND COMPOSITIONAL CHARACTERIZATION OF ZINC nICKEL ELECTROCOATINGS
ULISES PIRATOBA
Profesor, Escuela de Física, Universidad Pedagógica y Tecnológica de Colombia Estudiante Doctorado en Física, Universidad Nacional de Colombia, upiratobam@bt.unal.edu.co
ENRIQUE VERA
Profesor, Escuela de Metalurgia, Universidad Pedagógica y Tecnológica de Colombia
CESAR ORTIZ
Profesor, Escuela de Física, Universidad Pedagógica y Tecnológica de Colombia
Recibido para revisar Octubre 02 de 2007, aceptado Febrero 04 de 2008, versión final Marzo 05 de 2008
RESUMEN: La gran demanda de láminas de acero recubiertas con Zinc o con aleaciones de Zinc, es atendida con procesos de electro deposición en continuo; estos requieren de altas densidades de corriente, obtenidas en electrolitos ácidos. En este trabajo se presenta la composición, morfología superficial y la caracterización electroquímica de aleaciones Zinc Níquel fase gamma sobre láminas de acero, depositadas con altas densidades de corriente. Estas fueron determinadas mediante Análisis de Energía Dispersa de Rayos EDX, Microscopias Electrónica de Barrido SEM y de Fuerza Atómica AFM, e Impedancia Electroquímica EI y polarización Táfel. Se encontraron recubrimientos de grano fino que se pasivan y exhiben un comportamiento anódico frente al sustrato de acero.
PALABRAS CLAVE: Galvanizado, recubrimientos Zinc Níquel, recubrimientos, corrosión.
ABSTRACT: The high request for zinc or zinc alloys electro coating steel sheets is attended by continuous electro coating process; this required high current densities obtained in acidic electrolytes. In this work, the composition, surface morphology and electrochemical characterization of gamma phase Zinc Nickel alloys on cold rolled steel sheets, obtained with high current densities is present. These were determined by Energy Dispersive X-ray Analysis EDX, Scanning Electron Microscopy SEM and Atomic Force Microscopy AFM, and Electrochemical Impedance EI and Tafel polarization. It was find passive coatings of fine grain that exhibit anodic behavior against the steel substrate.
KEYWORDS: Plating, Zinc Nickel coating, coating, corrosion.
1. INTRODUCCIÓN
Mediante los procesos de galvanizado, por inmersión o electrolítico para obtener un recubrimiento de Zinc, se logra proteger al acero de los procesos corrosivos en un proceso conocido como protección catódica. El recubrimiento adopta un comportamiento anódico y hace que el acero se comporte como el cátodo de las celdas electroquímicas donde se presentan dichos procesos.
El zinc protector se disuelve con facilidad en ambientes acuosos, siendo necesaria en algunas aplicaciones la aplicación de espesores apreciables, que dificultan procesos como el conformado de láminas en matrices, la soldadura o el pintado con recubrimientos orgánicos. Aleado con otros metales como cobalto, manganeso, hierro cobre y especialmente con el níquel, se disminuye considerablemente la velocidad de su deterioro [1,2].
En los procesos industriales mediante los cuales se recubren en continuo láminas de acero al carbono laminado en frío, con Zn o sus aleaciones, estas van pasando por series de celdas electrolíticas a velocidades iguales o superiores a unos 60 m/s; se utilizan altas densidades de corriente que solo se logran con electrolitos ácidos en flujo turbulento[3-5]. El montaje mostrado en la Figura.1 reproduce con bastante fidelidad las condiciones industriales y permite el control y estudio de los parámetros del proceso[6]; ha sido utilizado para obtener recubrimientos de aleaciones Zn-Ni (9-14%) (fase gamma de estas aleaciones electro depositadas), composición que ha mostrado las mejores características de soldabilidad, pintabilidad y protección a la corrosión [7-9]. En la electrodeposición simultanea de estos 2 metales, se presenta el fenómeno conocido como codeposición anómala[10-15], por cuanto resulta inhibida la deposición del metal más noble (Ni) y estimulada la del metal activo (Zn).
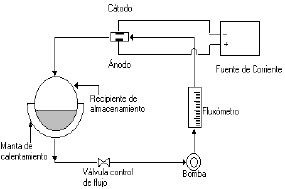
Figura 1. Esquema del equipo utilizado
Figure 1. Used system diagram
2. EQUIPOS, MATERIALES Y REACTIVOS
Para obtener los recubrimientos se utilizó el montaje mostrado en la Figura 1, construido en nuestro laboratorio; la celda de electro deposición está formada por un ánodo de plomo con área expuesta 1,2 cm2, a 1,0 cm de distancia del cátodo. Este consta de un disco cold rolled calibre 20 de 1,0 cm2 desengrasado con agua caliente jabonosa y alojado en un porta cátodos; la condición de flujo turbulento se obtiene por recirculación del electrolito en un circuito cerrado, utilizando una bomba, un flujometro y una válvula para medir y controlar el flujo. Se utilizaron 2,0 litros de electrolito obtenido por disolución en agua destilada des ionizada de NiSO4.6H2O en concentración de 152 g/L y de ZnSO4.7H2O en concentración de 156 g/L, para una relación molar Zn:Ni de 1:1; se calentó dicho electrolito hasta la temperatura de trabajo, 50 ºC, y se agregó ácido sulfúrico hasta obtener un pH de 1,3. Se utilizaron densidades de corriente de 50, 75 y 100 A/dm2. A los recubrimientos obtenidos sobre probetas de acero al carbono laminado en frío, se les analizó su topografía mediante SEM y AFM y su composición mediante EDX. Para su caracterización electroquímica, se obtuvieron mediante Impedancia Electroquímica, los diagramas de Bode para probetas del sustrato sin recubrir y recubierto con las aleaciones de Zn-Ni sumergidas en una solución de cloruro de sodio al 5%. Igualmente se obtuvieron las curvas de polarización Tafel, tanto del sustrato como del recubrimiento Zn Ni. Los espectros de impedancia y las curvas de polarización Táfel fueron obtenidos con un equipo de Gamry Instruments utilizando como electrolito una solución de NaCl 1%
3. RESULTADOS
La composición del recubrimiento (89,27 Zn, 10,36 Ni y 0,37 de Fe), obtenida por EDX cuya distribución se ilustra en la Figura 2, se halla dentro del rango asignado a la fase gamma de esta aleación electrodepositada. La micrografía SEM a 500 aumentos de la Figura 3, muestra que la aleación se ha adaptado a la topografía del sustrato generada por el proceso de laminado. Las micrografías AFM muestran recubrimientos de grano fino, con apariencia de poliedros y tamaño de grano del orden de 1 µm, (Figura 4).
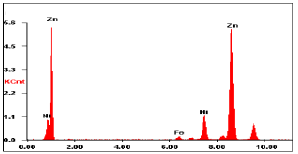
Figura 2. Composición química de los recubrimientos Zn Ni por EDX
Figure 2. Zn Ni coatings Chemical composition by EDX

Figura 3. Aspecto superficial del recubrimiento Zn Ni, obtenido por SEM
Figure 3. Surface appearance of Zn Ni coating by SEM

Figura 4. Topografía de recubrimientos ZnNi obtenidas con AFM usando sensores de: A desplazamiento y B fuerza
Figure 4 Zn Ni topography by AFM with contact sensor A and force sensor B
Se utilizó Impedancia Electroquímica para evaluar y confrontar el comportamiento electroquímico de acero con y sin recubrimiento; esta técnica permite determinar algunos parámetros dieléctricos del recubrimiento, sin causar los daños debidos a problemas de una polarización significativa típicos de los ensayos Tafel. Estas polarizaciones generan migración de iones, y posibles rupturas o formación de micro grietas o micro poros que incuban procesos de corrosión. Los diagramas de Bode de impedancia electroquímica, en solución acuosa de NaCl al 5%, se muestran en la Figura 5 para el sustrato y en la Figura 6 para el recubrimiento. Para el sustrato, solo se manifiesta el efecto capacitivo de un elemento de fase constante, atribuible a la doble capa electroquímica formada en la interfase acero/solución, un comportamiento estándar de este sistema.
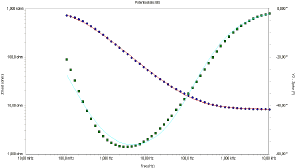
Figura 5. Diagrama de Bode del substrato de acero
Figure 5. Bode diagram of the Steel substrate
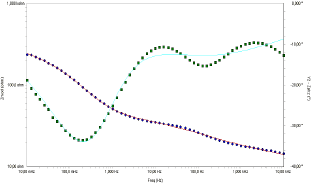
Figura 6. Diagrama de Bode del recubrimiento
Figure 6. Coating´s Bode diagram
Para el recubrimiento aparecen 2 bucles correspondientes a 2 elementos de fase constante, que evidencian la presencia de 2 interfaces; este comportamiento es típico de superficies metálicas con recubrimientos aislantes, porosos o discontinuos que pueden ser representados mediante el circuito de la Figura 7. El ajuste iterativo de estos espectros a la función de transferencia del circuito de esta Figura, arrojó los valores para los elementos del circuito que se muestran en la Tabla 1 y que se hallan representados por las líneas continuas de cada gráfica.
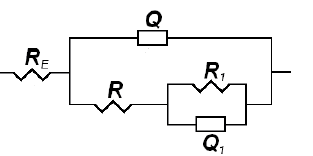
Figura 7. Circuito eléctrico que simula el comportamiento electroquímico
Figure 7. Electric circuit that simulates the electrochemical behavior
Tabla 1. Valores de los parámetros del circuito de la figura 7, para ajuste de los datos
Table 1. Circuit parameters for fitting data according to figure 7

Para el acero desnudo, el valor nulo de la resistencia R1 permite reemplazar el circuito R1Q1 por un corto circuito, quedando entonces con un solo elemento de fase constante Q. La transferencia de carga, que debe presentarse entre el metal y los iones o átomos del electrolito, se representa mediante una resistencia de transferencia de carga: R para el acero desnudo y R1 para el recubrimiento con Zn Ni. Se obtienen, para estas resistencias de transferencia de carga, valores que se hallan dentro del mismo orden de magnitud: 1095 y 440 Ω respectivamente. Las resistencias del electrolito RE en los 2 casos tienen valores muy similares. De los ensayos Tafel, cuyos resultados se muestran en la Figura 8, se dedujeron potenciales y corrientes de corrosión de -104 mV y 5,94 μA para el sustrato de acero, y de -140 mV y 6,3 μA para la aleación Zn-Ni. Valores más negativos del potencial para la aleación los justifica la presencia del Zn, metal que por ser más electronegativo que el hierro, se comporta como el ánodo de celdas de corrosión, protegiendo así al sustrato ferroso de este fenómeno. La corriente anódica para la aleación, aumenta con el sobrepotencial, aproximadamente como lo predice la ecuación de Butler Volmer [16]; alcanza un valor crítico de unos 3,54 µA a -75 mV y disminuye luego hasta 1,44 µA a 0,1 mV. Este comportamiento es típico de los metales que se pasivan y ha sido encontrado en las aleaciones de níquel [17].
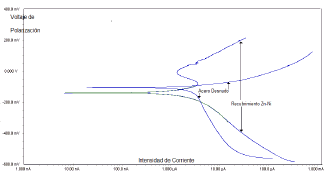
Figura 8. Diagramas Táfel de substrato y del recubrimiento
Figure 8. Táfel Diagrams of the substratum and of the coating
4. CONCLUSIONES
Las aleaciones Zn Ni fase gamma electro depositadas tienen una apariencia uniforme, forman granos finos cuyo tamaño es del orden de un micrómetro y tienen apariencia de poliedros.
Mediante Impedancia Electroquímica se obtuvo un elemento de fase constante para el acero desnudo y 2 cuando está recubierto. En este caso, la transferencia de cargas tiene lugar en 2 interfaces.
Para la aleación Zn Ni, el potencial de corrosión es más negativo que para el sustrato de acero, aportándole una protección catódica; además, el ensayo de polarización Táfel mostró un comportamiento típico de superficies que se pasivan.
5. AGRADECIMIENTOS
Al grupo de plasma de la Universidad Nacional de Colombia sede Manizales donde se realizó la caracterización topográfica, a la DIN y al grupo GSEC de la UPTC-Tunja.
REFERENCIAS
[1] GÓMEZ E. y otros, Journal of Electroanalytical Chemistry 505, 54-61, 2001. [ Links ]
[2] DURAIRAJAN A. y otros, Journal of The Electrochemical Society, 147 (5),1781-1786, 2000. [ Links ]
[3] Fabri Miranda F J; Margarit I C P; Barcia O E; Wiart R. Corrosion; Aug 1999; Vol. 55 No 8, 732-742. [ Links ]
[4] Ashassi-Sorkhabi H. et al. Surface and Coatings Technology 140 ,278-283, 2001. [ Links ]
[5] Heydarzadeh Sohi M., Jalali M. Journal of Materials Processing Technology 138 63–66, 2003. [ Links ]
[6] Jin Y.S., Kim T.Y., Kim K.Y. Surface and Coatings Technology 106, 220–227, 1998. [ Links ]
[7] Lehmberg, C.E. Lewis, D.B. Marshall G.W. Surface and Coatings Technology 192, 269-277, 2005. [ Links ]
[8] Panagopoulos, C N Georgarakis KG, Agathocleous P.E. Tribology International 36 , 619–623 , 2003. [ Links ]
[9] Zhongda Wu, L. Fedrizzi, P.L. Bonora M, Surface and Coatings Technology 85, 170-174, 1996. [ Links ]
[10] MORTAGA M. Abou-Krisha Applied Surface Science 252 , 1035–1048, 2005. [ Links ]
[11] Jing-yin Fei, Wilcox G.D. Surface and Coatings Technology 200 No 11,3533-3539, 2006. [ Links ]
[12] Elkhatabi, F. Benballa M,. Sarret M, C. MuÈller Electrochimica Acta 44 ,1645-1653, 1999. [ Links ]
[13] MuLler C., Sarret M., Benballa M. Surface and Coatings Technology 162 ,49–53, 2002. [ Links ]
[14] Benballa M. y otros. Surface and Coating Technology 123,55-61, 2000. [ Links ]
[15] GAVRILA M. et al. Surface and Coating Technology 123, 164-172., 2000. [ Links ]
[16] ALMAGRO, V. Polarografía, 1ª ed., Editorial Alhambra S. A., Madrid, 1971. [ Links ]
[17] American Society for Metals; Metals Handbook, Vol. 13 Corrosion, 9a ed. Ohio 4407, pgs 35, 466, 645. [ Links ]














