Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
DYNA
Print version ISSN 0012-7353On-line version ISSN 2346-2183
Dyna rev.fac.nac.minas vol.72 no.158 Medellín May/Aug. 2009
ESTUDIO DEL PROCESO DE PULIMENTO QUÍMICO DE PIEZAS DE JOYERÍA
STUDY OF CHEMICAL POLISHING PROCESS JEWELLER`S PIECES
OSCAR FABIÁN HIGUERA COBOS
Profesor asistente, Universidad Tecnológica de Pereira, osfahico@utp.edu.co
LUIS CARLOS FLÓREZ GARCIA
Profesor asistente, Universidad Tecnológica de Pereira, luiscar@utp.edu.co
DARIO YESID PEÑA BALLESTEROS
Profesor asistente, Universidad Industrial de Santander, dypena@uis.edu.co
Recibido para revisar marzo 26 de 200, aceptado agosto 29 de 2008, versión final septiembre 13 de 2008
RESUMEN: En este trabajo de investigación se estudiaron los aspectos fundamentales a nivel electroquímico, cinético y termodinámico del proceso de pulimento químico (proceso bomba) con el propósito de determinar las condiciones mas favorables para una posterior estandarización del mismo. El comportamiento del proceso Bomba de aleaciones de oro de 24 y 18 quilates ha sido investigado usando técnicas de voltametría cíclica mediante un electrodo de disco rotatorio. Electroquímicamente se determinaron las mejores condiciones de operación para el proceso de pulimento químico de piezas de joyería: 0.1M NaCN, 0.95M H2O2, 0 rpm y 85ºC.
PALABRAS CLAVE: Oro 24 quilates, oro 18 quilates, peróxido de hidrógeno, pulimento químico, cianuro, voltametría cíclica, electrodo de disco rotatorio (RDE).
ABSTRACT: In this investigation work the fundamental aspects were studied at electrochemical, kinetic and thermodynamic level of the process of chemical polishing (Bombing process) with the purpose of determining the favorable conditions and then standardization of the process of chemical polishing. The Bombing process behavior of 24 and 18 carat gold has been investigated using cyclic voltammetry techniques using a rotating disc electrode. Electrochemically was determined the best operation conditions for the process of chemical polishing of jeweler's pieces: 0.1M NaCN, 0.95M H2O2, 0 rpm and 85ºC
KEYWORDS: 24 carat gold, 18 carat gold, hydrogen peroxide, chemical polishing, cyanide, voltammetry cyclic, rotating disc electrode (RDE).
1. INTRODUCCIÓN
Actualmente la actividad joyera en Colombia se realiza en forma artesanal debido a que muchos de los talleres de joyería no cuentan con la infraestructura física y técnica adecuada, ni con los sistemas de control suficientes para mitigar los impactos ocasionados al medio ambiente y al mismo artesano. Este panorama muestra los escasos niveles científico y técnico con los que los procesos empleados actualmente son llevados a cabo, procesos que por otra parte conllevan desperdicio de reactivos químicos que por su
inadecuada manipulación afecta la salud de los trabajadores y aumenta los volúmenes de sustancias tóxicas que son vertidas a los alcantarillados de las ciudades. Uno de los procesos más contaminantes de esta actividad productiva es el pulimento químico que produce una gran cantidad de desechos que contienen elevadas concentraciones de cianuro y metales pesados, los cuales se movilizan a través de las fuentes hídricas. Actualmente en los talleres de joyería son utilizados dos procesos: el de armado, mas artesanal, y el de microfusión, método muy difundido a nivel mundial e indispensable en la joyería moderna; en cualquiera de ellos es el proceso de pulido químico una etapa necesaria para dar una adecuada apariencia final a la joya, llamado por los artesanos joyeros como proceso bomba, se basa en que bajo condiciones oxidantes y pHs básicos, el oro y la plata pueden ser disueltos y complejados por soluciones diluidas de cianuro para posteriormente ser recuperados de la solución. Con la adición controlada de solución diluida de peróxido de hidrógeno se logran más altos niveles de oxígeno disuelto, acelerando el proceso de disolución y disminuyendo las pérdidas de oro y de cianuro. En este trabajo de investigación se estudiaron los aspectos fundamentales a nivel electroquímico, y termodinámico del pulimento químico (proceso bomba) con el fin de predecir las mejores condiciones operativas para su posterior estandarización.
2. FUNDAMENTACIÓN TEORICA
2.1 Proceso De Cianuración
Es aquel en el cual una solución de cianuro débilmente alcalina tiene una acción preferencial para disolver el oro. En medio acuoso, en soluciones de cianuro, el oro es oxidado y disuelto a Au (I) en un complejo de cianuro Au(CN)-2. El Au(III) en el complejo de cianuro Au(CN)-4 , es también formado pero el complejo Au(I) es mas estable que la especie Au(III) a 0,5V. Para propósitos prácticos la estequiometría de la reacción de disolución puede ser asumida como:
Au + 2CN-↔ Au(CN) -2 + 1e (1)
La disolución del oro en soluciones de cianuro es un proceso electroquímico en el cual la reacción anódica es la oxidación del oro mientras la reacción catódica es la reducción del oxígeno. En cuanto a la reacción anódica se tienen los siguientes pasos en la formación del complejo de oro
Au + CN-↔ AuCN-(s) (2)
AuCN-(s) ↔ AuCN(s) + 1e- (3)
AuCN(s) + CN-↔ Au (CN)-2 (4)
donde (s) se refiere a las especies adsorbidas y AuCN es una especie neutra adsorbida sobre la superficie del oro. En cuanto a los complejos cianurados de plata, ellos tienen el mismo comportamiento que los complejos cianurados de oro, o sea:
Ag + CN-↔ AgCN-(s) (5)
AgCN-(s) ↔ AgCN(s) + 1e- (6)
AgCN(s) + CN-↔ Ag(CN)-2 (7)
La disolución de oro puede ser afectada por la disolución de elementos presentes en las aleaciones, estas reacciones son consumidoras de cianuro. Esto es favorable en el caso del proceso de pulimento químico debido a que se forman complejos cianurados de metales como el cobre que se cree es el causante del poco brillo de las joyas de oro de 18 quilates.
En cuanto a la formación de complejos cianurados de cobre se puede decir que el CuCN puede ser disuelto en la presencia de exceso de cianuro para formar iones cianocuprosos Cu(CN)-2, Cu(CN)2-3, Cu(CN)3-4 en soluciones acuosas. Estas especies siguen los siguientes pasos sucesivos de equilibrio en reacción con cianuro libre:
CuCN ↔ Cu++CN- (8)
CuCN + CN-↔ Cu(CN)-2 (9)
Cu+ + 2CN-↔ Cu(CN)-2 (10)
Cu(CN)-2+ CN-↔ Cu(CN)2-3 (11)
Cu(CN)2-3+ CN-↔ Cu(CN)3-4 (12)
HCN ↔ H++ CN- (13)
Los iones cúpricos reaccionan con el CN- y forman complejos cúpricos, los cuales son inestables y se descomponen rápidamente. Las distribuciones y los potenciales de equilibrio de las especies de cianuro de cobre son funciones de la relación molar cianuro: cobre, concentración total de cianuro, pH y temperatura. [1, 2]
3. DESARROLLO EXPERIMENTAL
3.1 Caracterización Del Proceso De Pulimento Químico De Joyas
El análisis de las muestras y las aleaciones se realizó mediante la técnica de espectroscopia de absorción atómica. Además, para comprobar la composición de las aleaciones se utilizó la técnica de microscopia electrónica de barrido.
3.2 Estudio Termodinámico Del Proceso De Pulimento Químico De Aleaciones De Oro
Se analizó la información termodinámica existente sobre el proceso de cianuración de minerales auroargentiferos con el propósito de adaptarla al proceso de pulimento químico de piezas de joyería. Además, se analizó el equilibrio de fases de las aleaciones de oro con el fin de explicar los cambios en la cinética del proceso de pulimento químico. Se construyeron diagramas Eh-pH para los sistemas Au-Ag-Cu-CN-H2O, CN-H2O los cuales son usados para estimar las especies que prevalecen en soluciones acuosas como una función del pH y del potencial químico.
3.3. Estudio Electroquímico Del Proceso De Pulimento Químico
Para este estudio se seleccionó la técnica Voltamperometría Cíclica con disco rotatorio. Las soluciones de cianuro y de peróxido de hidrógeno se prepararon con reactivos grado analítico y agua destilada. Para los ensayos experimentales se elaboraron electrodos de oro de 24 y 18 quilates. Las pruebas se realizaron a condiciones aireadas y desaireadas a una velocidad de barrido de 25 mV/s, el rango de barrido fue de -1000 a 1000 mV con dos barridos. Las condiciones experimentales generales fueron:
- Área superficial de los discos de prueba:2.011cm2
- Agitación: 0 y 450 rpm.
- Concentración de NaCN: 0.1, 0.24 y 0.6M
- Concentración de H2O2: 0.95 y 5M
- El pH fue determinado por la concentración de cianuro en solución
- Temperatura: 25 y 85°C
4. RESULTADOS Y ANALISIS
4.1 Caracterización
4.1.1. Caracterización fisicoquímica de efluentes
Se visitaron 18 talleres de joyería con el objetivo de conocer las técnicas empleadas en el proceso de pulimento químico y proceder a la toma de las muestras para análisis fisicoquímico. Se obtuvieron concentraciones de metales en los efluentes del proceso de pulimento químico: oro de 308.95mg/L, plata de 53.94 mg/L y cobre de 69.32 mg/L. Además, concentraciones de cianuro del orden de los 8700mg/L NaCN. Se deduce que las cargas son elevadas porque este balance es solo para la labor de un día en cada taller, lo cual indica que la producción mensual o anual es alta.
4.1.2 Caracterización fisicoquímica de la materia prima
Las aleaciones utilizadas para este estudio fueron, oro de 24 quilates (99.75%Au, 0.128%Ag y 0.122%Cu) y oro de 18 quilates (82.2%Au, 11.48%Ag y 6.32%Cu) Los resultados de la caracterización muestran como la composición de la aleación varia según la posición en que se analice, esto se resume enla Figura 1.
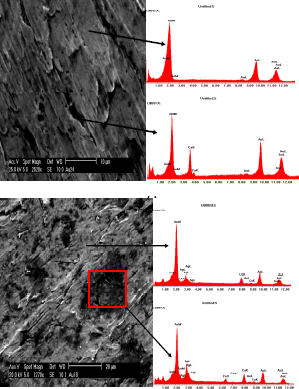
Figura 1. Microscopia electrónica de barrido. (a) Oro 24 quilates, (b) Oro 18 quilates
Figure 1. Scanning electron microscopy. (a) 24 gold carat, (b) 18 gold carat
4.2 Estudio Termodinámico
4.2.1 Termodinámica del sistema Au-Cu-Ag
En el sistema Au-Ag-Cu ocurren tres casos particulares: Au-Ag donde se presenta una solubilidad total en estado sólido en todo el rango de composición (solución sólida α); Ag-Cu donde hay un comportamiento eutéctico con la presencia de un campo binario de alfa y beta (α + β); Au-Cu tiene el comportamiento mas complejo debido a la presencia de compuestos de AuCu I y AuCu II , AuCu3, Au3Cu. Al unir estos sistemas binarios para el estudio de un sistema ternario como es el caso de las aleaciones utilizadas en los procesos de joyería, se logra un mejor entendimiento en los niveles del campo de miscibilidad en el sistema Au-Cu-Ag.
Cuando el sistema se sitúa en la intersección del campo de una sola fase y el campo de dos fases, la fase α se separa en α1, fase rica en Au-Ag, y α2, fase rica en Au-Cu. Se debe tener cuidado en la nomenclatura utilizada, ya que algunas veces estas fases separadas son expresadas como αAu-Ag y αAu-Cu. Sin embargo, en el caso actual el intervalo de miscibilidad es más complicado porque las fases ordenadas AuCu y AuCu3, también se pueden presentar en una pequeña extensión, localizada en el prisma que representa el sistema binario Au-Cu. Esto significa que la fase α2 se puede transformar ella misma a AuCu II, AuCu I o AuCu3, dependiendo de la composición. La Figura 2 muestra una versión simplificada del comportamiento del sistema Au-Cu-Ag a 300ºC. [3]
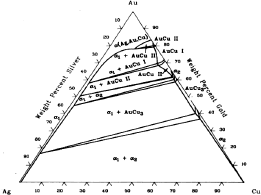
Figura 2. Diagrama de estabilidad de fases del sistema Au-Cu-Ag a 300ºC
Figure 2. Phases Stability Diagram of the system Au-Cu-Ag at 300ºC. [3]
Se observa en la Figura 2 que, la aleación de oro de 18 quilates rica en plata, presentará una sola fase de solución sólida α y su coloración será amarillo verdoso. Cuando el contenido de cobre es incrementado, el consumo de dicho cobre causa que la aleación se convierta a dos fases α1+ AuCu II, esta será la estructura del oro de 18 quilates y su coloración será amarilla.
4.2.2 Termodinámica del proceso de pulimento químico de piezas de joyería. [4]
Termodinámica del peróxido de hidrógeno. [5] La descomposición del peróxido de hidrógeno para formar oxígeno y agua con la evolución de calor se expresa con la ecuación:
2H2O2 (l) = 2H2O (l) + O2 (g) + 1240 BTU/lib 100% H2O2 (14)
Los factores primarios que deben ser controlados para impedir un aumento en la velocidad de descomposición del peróxido de hidrógeno son la temperatura, la contaminación por material orgánico e inorgánico y el pH. La descomposición homogénea frecuentemente comienza cuando otra sustancia química se introduce en un recipiente y entra en contacto directo con el peróxido de hidrógeno (o viceversa). La descomposición heterogénea del peróxido de hidrógeno está localizada en la superficie de contaminantes catalíticos sólidos, usualmente metales. El contacto del peróxido de hidrógeno con materiales de construcción impropios (cobre, latón, zinc, acero dulce, etc.) es una causa primaria de la descomposición heterogénea. La estabilidad inherente del peróxido de hidrógeno también es afectada por el pH. Normalmente, la estabilidad es mejor en la región del pH neutro. La disminución de estabilidad a un pH menor normalmente no es considerable, pero a un pH más alto ésta se deteriora muy rápidamente y el peróxido de hidrógeno alcalino puede ser muy inestable. Por consiguiente, la contaminación del peróxido de hidrógeno ocasionada por ácidos, y particularmente por álcalis, debe evitarse.
Electroquímica de las soluciones de peróxido de hidrógeno. El comportamiento electroquímico de las soluciones de peróxido de hidrógeno, no es tan simple como:
2H2O↔ H2O2 + 2H++2e- (15)
El peróxido de hidrógeno puede actuar, no solamente como un oxidante sino como un agente reductor, acorde a la reacción:
H2O2 ↔ HO2-+H+ (16)
Reducción con formación de agua.
H2O2 + 2H++2e-↔ 2H2O (17)
HO2-+ 3H++2e- ↔ 2H2O (18)
Oxidación con formación de oxígeno.
H2O2 ↔ O2 +2H++2e- (19)
HO2-↔ O2 +H+ + 2e- (20)
En la Figura 3 se observa la zona de estabilidad en la cual una solución de peróxido de hidrógeno entra en contacto con una superficie metálica, donde el potencial de electrodo se encuentra en la región de la doble inestabilidad, el H2O2 puede descomponerse espontáneamente en agua más oxígeno por la reacción:
2H2O2 ↔ O2 +2H2O (21)
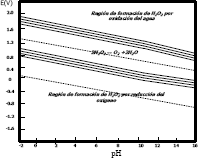
Figura 3. Diagrama Eh-ph para el sistema O2- H2O a 25ºC
Figure 3. Eh-ph Diagram for system O2- H2O to 25ºC
Mezcla Oxígeno – Peróxido. El peróxido nunca se encuentra en solución durante la oxidación anódica del agua a oxígeno, esto se puede observar durante la reducción catódica del oxígeno a agua. Aparentemente, el peróxido es un compuesto intermedio en el proceso catódico pero no en el anódico por la gran dificultad encontrada en el rompimiento del enlace doble de O-O. Cuando el oxígeno es reducido en un cátodo metálico, las moléculas de oxígeno son adsorbidas sobre la superficie del electrodo con adsorción disociativa. Si la velocidad de transferencia de electrones es mayor que la velocidad de disociación del O2 a átomos de O adsorbidos, el peróxido será formado como un intermedio estable y el O2 será reducido por un proceso de 2 electrones. Sin embargo la velocidad de disociación del O2 es mayor que la velocidad de transferencia de electrones, el peróxido no será un producto intermedio y el O2 será reducido por un proceso de 4 electrones. El valor de la energía de formación de Gibbs del H2O2 (aq), -134.1KJ/mol. Calculando para la reducción de oxigeno en soluciones ácidas:
O2 + 2H+ +2e-→H2O2 Eº = 0.695 V (dEº/Dt) (22)
En soluciones alcalinas el valor de ΔGº= -67.4 KJ/mol para el HO2-(aq).
O2 +H2O +2e-→OH- + HO2- EBº = -0.0649V (23)
Mezcla Agua- Peróxido. Calculando los potenciales estándar en la mezcla peroxido- agua en soluciones ácidas
H2O2+ 2H+ +2e-→2 H2O Eº = 1.763 V (dEº/Dt) (24)
En soluciones alcalinas
HO2-+ H2O +2e-→ 3OH- EBº = 0.867V (25)
Estos potenciales positivos tan altos sitúan al peróxido en el grupo de los más poderosos agentes oxidantes. No solamente este peróxido es inestable con respecto a la oxidación del agua, también a su propia oxidación y reducción en ambas soluciones ácidas y alcalinas.
Ión Superóxido. Cuando el ión superóxido es formado en solución de cualquiera de las dos formas, heterogéneamente por catodización de un electrodo metálico o homogéneamente por radiolisis o fotolisis de una solución alcalina saturada de oxígeno. El ión superóxido puede reaccionar con el solvente para formar un radical peroxil
O2 + e-→ O2- (26)
O2- + HA → HO2 + A- (27)
el cual puede ser reducido a un ión peroxil por transferencia de electrones, HO2 + e-→ HO2- o reacciona con otro radical como una etapa de cadena rota, HO2 + HO2 → H2O2 + O2. Para estabilizar el ión O2- en solución, el segundo paso puede ser grandemente retardado por cualquiera de los dos; por el uso de solventes apróticos o sistemas de sales fundidas o por adición de surfractantes a la solución acuosa.
Para la mezcla O2 / O2- (Eº = -0.33V), de la ionización del radical peroxil (HO2→ H+ + O2-, pk= 4.8), de la mezcla O2 / HO2- (EBº = -0.0649V), y la ionización del agua (pk= 13.995), el ΔGº de la reacción HO2 / HO2- da:
HO2 +1e-→HO2- Eº= -0.744 V (28)
El ΔGº para el radical HO2 en solución es 4.44KJ/mol. Los potenciales estándar de un número de otras mezclas que envuelven los radicales HO2 y O2-.
HO2 + H+ + 1e-→ H2O2 Eº= 1.44 V (29)
O2- + H2O + e-→ HO2- + OH- EBº = 0.2V (30)
HO2 + 3H+ + 3e-→ 2H2O Eº= 1.65 V (31)
O2- + 2H2O + 3e-→ 4OH- EBº = 0.645V (32)
O2 + H+ + e-→ HO2 Eº= -0.046 V (33)
HO2 + O2 + H+ + 1e-→ O3+ H2O Eº= 0.813 V (34)
En soluciones ácidas, el radical perihidroxil no es solamente inestable con respecto a la descomposición del ozono
2HO2 → O3 + H2O ΔGº = -65.12 KJ/mol (35)
Pero también con respecto a la descomposición a oxígeno
2HO2 → O2 + H2O2 ΔGº = -142.97 KJ/mol (36)
Sin embargo, en soluciones alcalinas, el ión O2- es mucho más estable:
2O2- + H2O → O3 + 2OH- ΔGº = 22.09 KJ/mol (37)
2O2- + H2O → O2 + HO2- + OH- ΔGº = -51.13KJ/mol (38)
Estos resultados indican que la descomposición del radical HO2 o el ión O2- sigue un camino a peróxido y O2 en lugar de ozono.
Termodinámica del cianuro. Sales simples de cianuro, tales como cianuros de sodio, potasio y calcio, disueltos e ionizados en agua para formar sus respectivos cationes metálicos e iones de cianuro libre:
NaCN ↔ Na+ + CN- (39)
Tanto el cianuro de hidrógeno como el cianuro libre pueden ser oxidados a cianato en la presencia de oxígeno y bajo condiciones oxidantes adecuados.
4HCN + 3O2 ↔ 4CNO-+ 2H2O (40)
3CN- + 2O2 + H2O ↔ 3CNO-+ 2OH- (41)
CN-+ H2O+ OH-↔ NH3+CO2 (42)
Estas reacciones son indeseables durante la disolución ya que reducen la concentración de cianuro libre y las especies de cianuro formadas no disuelven los metales básicos.
En la Figura 4 se muestran los diagramas para el sistema CN-H2O a 25ºC y 85ºC en donde se puede observar como la temperatura juega un papel muy importante, ya que la zona de estabilidad del cianuro libre al aumentar la temperatura pasa del intervalo de pH de 9.2 -14 a un intervalo de pH de 8- 14, favoreciendo el proceso. Además, se observa la presencia del amoniaco en el rango de pH en estudio; este compuesto se presenta al hidrolizarse el cianuro, proceso que ocurre muy lentamente.
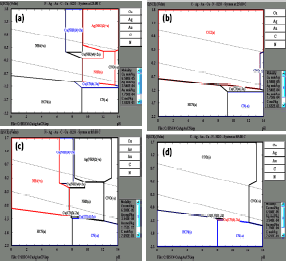
Figura 4. Diagrama Eh-ph para el sistema CN-H2O (a), (b) 25 °C y 85°C (c), (d)
Figure 4. Eh-ph Diagrams for the system CN-H2O (a), (b) 25 °C y 85°C (c), (d)
En la Figura 5 se representan los diagramas potencial vs pH para las especies metálicas de Au, Ag y Cu. En los diagramas, las líneas punteadas corresponden a los potenciales condicionales para los pares redox de Au(I)/Au(0), Ag(I)/Ag(0) y Cu(I)/Cu(0), las cuales pueden ocurrir para determinados rangos de pH, manteniendo la estabilidad del complejo formado. En este caso para las condiciones de trabajo en joyería, el pH se mantiene entre 10 a 12.5, existiendo en solución los complejos Au(CN)-2, Ag(CN)-2, Ag(CN)-23, y Cu(CN)-34.
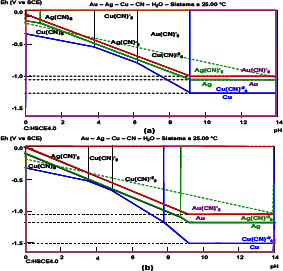
Figura 5. Diagramas Eh-pH para las especies cianuradas de oro, plata y cobre. a) CN- = 0.1 M; y b) CN- = 0.6M
Figure 5. Eh-pH Diagrams for the gold, silver and copper cyanide species. a) CN- = 0.1 M; y b) CN- = 0.6M
Según los diagramas de Pourbaix analizados, se cumple que a bajas concentraciones de cianuro y de plata, la estabilidad del complejo coordinado en el rango de pH analizado ( 10 a 12), corresponde al Ag(CN)-2, siendo este el predominante en el diagrama de distribución (Figuras 5a).Del mismo modo se observa que a medida que la concentración tanto de cianuro ( 0.6 M) como de plata en solución se incrementan, el predominio de la distribución corresponderá al complejo Ag(CN)-23, el cual es más estable a las condiciones de pH dados (Figuras 5b).
Para el caso de las especies de cobre y oro, Cu(CN)-34 y Au(CN)-2 respectivamente, se observa que son estables a las diferentes concentraciones, y en el rango de pH básico requerido para el proceso, asegurándose su estabilidad y predominio en el sistema de recuperación. El tricianuro de cobre Cu(CN)-23 es estable a condiciones de pH menores a 8, por lo cual su predominio se descarta en el proceso.
4.3 Estudio Electroquímico Del Proceso De Pulimento Químico
Efecto de la relación [NaCN]/[H2O2]. Se estudiaron diferentes relaciones [NaCN]/[H2O2], variando tanto la concentración de cianuro como la concentración de peróxido de hidrógeno, la Tabla 1 resume estos valores.
Tabla 1. Relaciones [NaCN]/[H2O2] para el estudio voltammétrico
Table 1. [NaCN]/[H2O2] Relations for voltammetry study

En la Figura 6(a) se observa el comportamiento voltamperométrico del oro de 24 quilates. En la relación 0.105 se observa la presencia de una zona pasiva en el rango de potencial entre 581-840mV y densidades de corriente bajas del orden de los 2mA/cm2 debido a la formación de Au(OH)3, este comportamiento es favorable para el proceso de pulimento químico de joyas ya que no producirá una pérdida significativa de oro. En la relación 0.2526 se presenta un pico de pasivación un poco mas marcado que el anterior a 702mV y densidades de corrientes de 2.24mA/cm2, la capa pasiva en este caso es más estable que la anterior pues produjo una disminución de la densidad de corriente a 765mV del orden de 1.83mA/cm2.
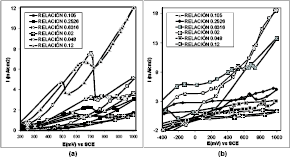
Figura 6. Efecto de la relación [NaCN]/[H2O2] sobre el comportamiento voltamétrico 0 rpm a 25ºC.(a) oro 24 quilates y (b) oro 18 quilates
Figure 6. Effect of [NaCN]/[H2O2] relation over voltammetry behavior, 0 rpm to 25ºC. (a) 24 gold carat, (b) 18 gold carat.
En la relación 0.6316 el comportamiento es más drástico; se observa un pico de pasivación a potenciales de 704 mV y densidades de corriente de 7.56 mA/cm2, la capa pasiva es estable, produciéndose la reactivación del sistema de disolución a 734 mV y 3.07 mA/cm2. En R=0.02 se observa un comportamiento muy similar al de R=0.105 aunque la zona pasiva se encuentra en el rango de potencial entre 650-899 mV, pero las densidades de corriente son menores, del orden de 1.5 mA/cm2. En R=0.048 se observa un comportamiento muy similar al de R=0.2526, pero el pico de pasivación no es tan marcado; esto se puede deber a la oxidación del cianuro. La zona pasiva se extiende entre 667-898 mV a densidades de corriente de 3.2mA/cm2.
En la relación 0.12 se presenta un comportamiento drástico y se observa un pico de pasivación a potenciales de 668 mV y densidades de corriente 6.74 mA/cm2 esta capa no es estable ya que el sistema se reactiva rápidamente a potenciales 723 mV y a densidades de corriente de 12.1 mA/cm2. También se pudo observar como al aumentar la concentración de cianuro y de peróxido de hidrógeno (R= 0.12), se presentó la disolución de cobre debido a una mayor severidad en el proceso, causada por el retroceso del barrido catódico a altas densidades de corrientes, observándose la formación de un loop.
En la Figura 6(b) se muestra el comportamiento voltamétrico para la aleación de oro de 18 quilates. Se aprecia un comportamiento muy similar entre las relaciones R=0.105 y 0.02 pero el inicio de la capa pasiva se da a potenciales mucho mas anódicos que en el oro de 24 quilates, lo que es causado por la presencia de cobre en el sistema. El cobre se introduce entre la cadena de Au-CN rompiendo la continuidad de la capa adsorbida de AuCN, formando CuCN adsorbido que posteriormente formará los diferentes complejos cianurados de cobre. La zona pasiva se encuentra en el rango de 241-1000 mV y presenta densidades de corriente del orden de 1.15 mA/cm2. Las bajas densidades de corrientes obtenidas se deben a la oxidación del cianuro por parte del peróxido de hidrógeno (5MH2O2). En cuanto a las relaciones R= 0.2526 y 0.048 el comportamiento es muy similar pero se observan mayores densidades de corriente a R=0.2526 debido a que no se presenta oxidación del cianuro, los potenciales de oxidación son mas anódicos para la relación R=0.2526, lo cual es coherente con lo encontrado en la literatura [6]. En cuanto a las relaciones 0.12 y 0.6316 se presenta un comportamiento muy similar presentándose mayores densidades de corriente para la relación 0.12 debido a las altas concentraciones de cianuro y peróxido de hidrógeno (0.6M NaCN y 5M H2O2). Además, se muestra el efecto del cobre y de los hidróxidos sobre la respuesta electroquímica de la aleación de oro de 18 quilates. A R=0.6316 (0.95M) y 0.12 (5M), se apreció el efecto de la alta concentración de OH- en el sistema; este comportamiento es concordante con Cheng et al. [6]
A densidades de corriente de 4 mA/cm2 se inició la oxidación del cobre a complejos cianurados (Cu(CN)3-2 y/o Cu(CN)4-3). Las densidades de corriente en esta región son irreproducibles, esta tendencia es característica de reacciones heterogéneas sensibles a la superficie, los resultados son consistentes con los de Hofseth y Chapman. [7] Este comportamiento es indicativo de que el paso determinante en la velocidad de disolución incluye una transferencia de electrones inicial. Además, se observó la presencia de altas concentraciones de OH- causada por el gran aumento en la densidad de corriente a potenciales 250-600 mV. También se observó por encima de este rango de potencial un incremento abrupto en la densidad de corriente que puede ser relacionado a un proceso autocatalítico. Después de esta zona de transición las corrientes se incrementaron mas lentamente, alcanzando un valor final mayor para altas concentraciones de OH-.[8]
Efecto de la temperatura. En la Figura 7 se aprecia la gran influencia de la temperatura a altas concentraciones de cianuro ( 0.24 M NaCN) tanto para el oro de 24 como el de 18 quilates. Se obtuvieron densidades de corriente para el oro de 24 quilates del orden de 35mA/cm2 y para el oro de 18 quilates del orden de los 57mA/cm2. No se nota en ninguno de los dos casos formación de capas pasivas estables debido que alta temperatura el sistema esta comandado por difusión. Este comportamiento no es favorable para el proceso de pulimento químico porque se perdería gran cantidad de material al realizar el proceso. A bajas concentraciones de cianuro 0.1M NaCN se observa un comportamiento menos drástico posiblemente debido a la formación de capas pasivas de Au(OH)3 o a la formación de AuCN adsorbido, para el oro de 24 quilates. El caso del oro de 18 quilates es mucho mas complejo pues prevalece el comportamiento electroquímico del cobre con la formación de complejos como el Cu(CN)-34, Cu(CN)3-2, Cu(CN2)- previa formación del CuCN adsorbido. [7]
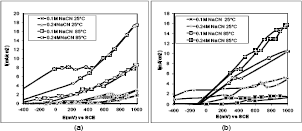
Figura 7. Efecto de la temperatura sobre el comportamiento voltamétrico del oro (a) 24 quilates y (b) 18 quilates
Figure 7. Effect of temperature over voltammetry behavior (a) 24 gold carat, (b) 18 gold carat
En cuanto a la disolución de la aleación de oro de 18 quilates a 25ºC, se observó a 200 mV la onda de oxidación del cobre a Cu(CN2)-, para posteriormente reaccionar con el cianuro libre presente en solución y oxidarlo para formar Cu(CN3)-2 o Cu(CN)4- 3. A potenciales mayores de 700 mV se presentó la destrucción de las especies cianuradas con la formación de cianato y óxido de cobre. El comportamiento de la aleación de oro de 18 quilates a 85ºC es un poco diferente ya que se presentó la formación del Cu(CN2)- a densidades de corriente de 5mA/cm2 y potenciales de 300 mV posteriormente, se formaron el Cu(CN3)-2 o Cu(CN)4-3 y al final se observó una pequeña meseta en la que se produce la destrucción del cianuro con la respectiva formación del cianato y óxido de cobre. Este comportamiento es favorecido por la agitación a 85ºC aunque su aporte no es muy significativo. [6, 7]
Efecto de la agitación. En la Figura 8 se observa que la agitación no fue un factor determinante en el proceso de pulimento químico de oro 24 y oro 18 quilates a altas temperaturas, debido a que a 85°C la movilidad atómica es mas alta por lo tanto no se presentan capas pasivas estables produciendo un aumento en la cinética de disolución de oro, plata y cobre, Se obtuvieron aumentos en la densidad de corriente a 25°C debido a que la agitación favorece el rompimiento de capas pasivas como AuCN, AgCN, CuCN y Au(OH)3. Aunque los valores obtenidos no son representativos.
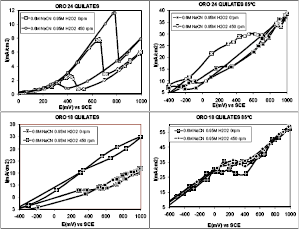
Figura 8. Efecto de la agitación sobre el comportamiento voltamétrico del oro 24 quilates y 18 quilates
Figure 8. Effect of agitation over voltammetry behavior of 24 gold carat and 18 gold carat
Efecto de la aireación. En la Figura 9 se observa la influencia que tiene el oxígeno disuelto en la solución cianurada sobre la cinética del proceso de pulimento químico de aleaciones de oro de 24 y 18 quilates en presencia de peróxido de hidrógeno. Tanto en oro de 24 como en oro de 18 quilates se observó un aumento en la densidad de corriente en soluciones desaireadas.
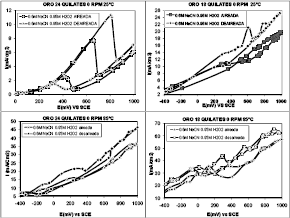
Figura 9. Efecto de la aireación sobre el comportamiento voltamétrico de la disolución de oro de 24 y 18 quilates
Figure 9. Effect of aireation over voltammetry behavior of 24 gold carat and 18 gold carat dissolution
Éste no fue el comportamiento esperado, ya que al tener mayor agente oxidante, se esperaría un corrimiento en el potencial de disolución hacia potenciales más anódicos y por ende un aumento en la cinética del proceso. Claro que este comportamiento se podría explicar de otra forma, si la concentración de agente oxidante es tan alta (soluciones aireadas) la disminución en las densidades de corriente se podría deber a la oxidación del cianuro a cianato, como lo confirman las curvas a 0.6M, tanto para oro de 24 como para oro de 18 quilates en donde se obtuvo una mayor cantidad de cianuros libres que garantizan la disolución de los metales presentes en la aleación y por ende una mayor densidad de corriente a condiciones aireadas.
5. CONCLUSIONES
Actualmente los artesanos joyeros en Colombia utilizan concentraciones entre 0.6 y 1M NaCN pero, según los resultados obtenidos experimentalmente analizados desde el punto de vista electroquímico, el proceso de pulimento químico presenta un buen comportamiento a 0.1M de NaCN y 0.95M H2O2 0 rpm y 85- 90ºC. Éste es un gran aporte desde el punto de vista ambiental y económico pues se trabaja con bajas concentraciones de cianuro, minimizando los costos y por ende el impacto ambiental de esta actividad productiva.
De conformidad con la bibliografía estudiada, se apreció que el comportamiento anódico de la aleación de oro de 18 quilates en soluciones de cianuro y en presencia de peróxido de hidrógeno es muy similar al del cobre. Además, es muy notable la gran influencia de la concentración de OH- en el comportamiento electroquímico de la aleación de oro de 18 quilates, causada por la presencia de un loop de histéresis, que va creciendo con el incremento de la concentración de cobre y por lo tanto con el decrecimiento en la relación (OH-/Cu+).
REFERENCIAS
[1] WADSWORTH M.E., ZHU X., THOMPSON J.S., PEREIRA C.J. Gold dissolution and activation in cyanide solution: kinetics and mechanism. Hidrometallurgy, 2000. [ Links ]
[2] XIAOWEI SUN, Y. CHARLES GUAN, AND KENNETH N. HAN. Electrochemical behavior of the dissolution of gold-siilver alloys in cyanide solutions. Metallurgical and materials transactions B, Volume 27B June 1996, pages 355-361. [ Links ]
[3] ASM HANDBOOK VOLUME 3 Alloy phase diagrams. ASM international 1992. [ Links ]
[4] GUZMÁN L, SEGARRA M, CHIMENOS J.M, FERNANDEZ M.A, ESPIELL F. Gold cyanidation using hydrogen peroxide. Barcelona, España. Enero 1999. [ Links ]
[5] CROISET E., RICE S., AND HANUSH R. Hydrogen peroxide decomposition in supercritical water. Aiche journal September 1997 Vol 43, No 9. [ Links ]
[6] CHENG S.C, GATTRELL M., GUENA T., MACDOUGALL B. The electrochemical oxidation of alkaline copper cyanide solutions. Electrochimica acta 47 2002. [ Links ]
[7] YICHANG GUAN AND KENNETH N. HAN. An electrochemical study on the dissolution of gold and copper from gold/copper alloys. Metallurgical and materials transactions B, Volume 25B December 1994 pages 817- 827. [ Links ]
[8] WADSWORTH M.E. Surface processes in silver and gold cyanidation. Int. J. Miner. Process. (1999). [ Links ]














