Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
DYNA
Print version ISSN 0012-7353On-line version ISSN 2346-2183
Dyna rev.fac.nac.minas vol.78 no.165 Medellín Feb./Mar. 2011
ZrO2TETRAGONAL OBTENIDO POR EL MÉTODO DE PRECIPITACIÓN CONTROLADA
TETRAGONAL ZrO2 OBTAINED BY CONTROLLED PRECIPITATION METHOD
DIEGO A. CAMPO CEBALLOS
Grupo de Ciencia y Tecnología de los Materiales Cerámicos (CYTEMAC). Universidad del Cauca. Popayán. dcampo@unicauca.edu.co
JORGE E. RODRIGUEZ PÁEZ
Grupo de Ciencia y Tecnología de los Materiales Cerámicos (CYTEMAC). Universidad del Cauca. Popayán. jnpaez@unicauca.edu.co
Recibido para revisar septiembre 18 de 2009, aceptado agosto 4 de 2010, versión final septiembre 4 de 2010
RESUMEN: En este trabajo se utilizó el método de precipitación controlada para sintetizar ZrO2 tetragonal estabilizado con óxido de calcio, CaO. Los sólidos obtenidos se caracterizaron utilizando análisis térmico diferencial y gravimétrico (ATD/TG), Espectroscopia Infrarroja con transformada rápida de Fourier (FT-IR), Difracción de Rayos X (DRX), y microscopia electrónica de transmisión (MET). Los resultados indican que al tratar el polvo cerámico a una temperatura de 600 ºC se obtiene ZrO2 con fase cristalina tetragonal; además las partículas de ZrO2 presentaron tamaño nanométrico (< 100 nm). Se prestó especial atención a los posibles mecanismos de formación de las partículas.
PALABRAS CLAVE: síntesis, ZrO2, tetragonal, precipitación controlada, caracterización
ABSTRACT: In this work, ZrO2 tetragonal stabilized with calcium oxide was synthesized by the controlled precipitation method. Ceramics powders were characterized using Differential Thermal Analysis and Thermal Gravimetry Analysis, (DTA/TG), Fourier Transform Infrared Spectroscopy (FT-IR), X-ray diffraction (XRD) and Transmission Electron Microscopy (TEM). Results show that ceramic powders treatment thermally at 600 ºC, presents ZrO2 in tetragonal crystalline phase; this powder contained particles of nanometric size. The mechanism formation of particles was discussed.
KEYWORDS: ZrO2, tetragonal, synthesis, controlled precipitation, characterization
1. INTRODUCCIÓN
El óxido de circonio, ZrO2 existe en tres formas polimórficas: monoclínica (m), tetragonal (t) y cúbica (c), siendo la m-ZrO2 la fase termodinámicamente estable a temperatura ambiente [1]. La fase monoclínica m-ZrO2 se emplea para obtener recubrimientos abrasivos, aditivos, pigmentos inorgánicos y componentes electrónicos [2]. Por otro lado, la fase tetragonal t-ZrO2, de interés para el presente trabajo, se emplea a alta temperatura en el manejo de metales fundidos, así como para fabricar troqueles de extrusión por su elevada dureza y resistencia al desgaste. Además, como es un compuesto biocompatible se usa en la fabricación de prótesis de cadera, rodilla y piezas dentales. Por la excelente conductividad iónica la fase c-ZrO2, se puede utilizar como sensor de oxígeno, capturador de gases en cámaras de vacío, cristales electrocrómicos y electrodos para celdas de combustible [2,3]. Debido a que estas dos últimas fases son de gran interés tecnológico, ellas pueden ser estabilizadas a temperatura ambiente dopando la matriz de circonia con pequeñas cantidades de óxidos estabilizadores (Y2O3, MgO, CaO y algunos óxidos de tierras raras) [4].
Dada la importancia de las características finales de los polvos cerámicos de ZrO2 sintetizados, definidas por la funcionalidad que se requiere, se han venido desarrollando diferentes métodos de obtención. Se pueden destacar los trabajos de Stevens [5] y Houchin et al [6], que utilizaron la descomposición térmica y cloración del circón para obtener el tetracloruro de circonio, para ello mezclaron el circón con carbón y posteriormente sometieron la mezcla a la acción del cloro entre 800 y 1200 ºC. Finalmente trataron el material entre 150 y 180 ºC para separar las mayores impurezas, por ejemplo, cloruros de silicio, hierro, titanio y aluminio. Este proceso permitió la obtención de tetracoluro de circonio con el cual se prepara ZrO2 con un tamaño de partícula del orden de los cientos de nanómetros.
Syamaprasad et al [7] emplearon la técnica de descomposición por plasma para obtener ZrO2, introduciendo circón en un reactor de plasma, de argón, en un rango de temperaturas alrededor de 6000 ºC; la disociación del circón ocurre favoreciéndose la formación de los óxidos constituyentes, ZrO2 y SiO2; el grado de disociación del circón depende de: el tamaño de partícula del circón, la tasa de flujo del gas Ar, la corriente, etc. La masa "descompuesta" es tratada con hidróxido de sodio (NaOH) o ácido sulfúrico (H2SO4). Bruncková et al [8] utilizaron el método sol-gel para obtener polvos cerámicos de ZrO2 de alta pureza, homogéneos y muy finos, con un tamaño de alrededor de 25 nm. El proceso se realizó utilizando una solución de los precursores metal-orgánicos utilizados, los cuales, a través de reacciones de hidrólisis y condensación llevaron a la formación del ZrO2 fase tetragonal, retenida por tamaño de partícula de aproximadamente 20 nm.
M. C. Fuertes y Porto López [9] obtuvieron circonia cúbica activando por mecanoquímica los óxidos mezclados. Luego de 6 horas de activación, a temperatura ambiente, obtuvieron una pobre solución sólida en fase cúbica, con tamaño de cristalito del orden de los nanómetros; un tratamiento térmico posterior, entre 800 y 1000 ºC, permitió un ordenamiento estructural parcial.
Debido a la relevancia de los métodos de síntesis en la obtención de ZrO2, en este trabajo se utilizó el método de precipitación controlada, ruta de naturaleza química, para sintetizar polvos cerámicos nanométricos de ZrO2 dopados con CaO. Adicional a la descripción del proceso, se realizó una breve discusión del mecanismo de formación de las partículas. Se indican los resultados más importantes de la caracterización de los polvos cerámicos sintetizados utilizando para ella, análisis térmico (ATD/TG), espectroscopia infrarroja con transformada rápida de Fourier (FT-IR), difracción de rayos X (DRX) y microscopía electrónica de transmisión (MET).
2. PROCEDIMIENTO EXPERIMENTAL
2.1 Método de síntesis: precipitación controladaPara la síntesis de la materia prima se utilizaron los siguientes precursores: oxicloruro de circonio (ZrOCl2.8H2O - Merk 99%) y acetato de calcio (Ca[CH3COO]2 - Carlo Erba 99,9%). Se tomó una solución con acetato de calcio acidificada, adicionando ácido nítrico (HNO3 - Carlo Erba 65%) en una concentración 0.3M, y se incrementó el pH del sistema utilizando hidróxido de amonio (NH4OH - Mallinckrodt 28%), a una temperatura de 60ºC. El sistema de oxicloruro se trabajó paralelamente de la misma manera, utilizando el NH4OH para incrementar su pH, pero sin ácido y a temperatura ambiente.
En trabajos previos [2,3], se estudiaron diferentes concentraciones del precursor de circonio y se determinó que la más adecuada fue la solución 0.3M, por la cantidad de material obtenido y por la baja aglomeración del polvo cerámico resultante. Para obtener la solución 0.3M se empleó el oxicloruro de circonio (ZrOCl2.8H2O - Merk 99%) disuelto en agua destilada y des-ionizada; el sistema presentó un pH inicial cercano a 1.0. El NH4OH se adicionó a una velocidad de 0.02 mL cada 15 segundos y la disolución fue llevada hasta un pH de 9 durante permanente agitación. Estas mismas condiciones de adición se utilizaron para adicionar el NH4OH a la solución 0.3M de acetato de calcio para llevarlo a un pH de 10.1. Se registró el incremento de pH con la adición de la base para los dos sistemas y así obtener las curvas de valoración potenciométrica.
Con base en los resultados obtenidos en las curvas de valoración potenciométrica obtenidas previamente, se consideró llevar el sistema precursor de circonio a un valor de pH de 4.5 (pH de equivalencia), debido a la gran cantidad de material presente y a las características de solubilidad, mientras que para el sistema de calcio se trabajó con el valor de 10.1.
Las soluciones precursoras se dejaron envejecer 24 horas (bajo condiciones ambientales) y luego se mezclaron utilizando un equipo de alta cizalla (Ultraturrax-IKA T50) a 6000 rpm, durante cinco minutos. Inmediatamente después se filtró la mezcla, y el sólido húmedo se dispersó en una solución de agua con dietilamina ([C2H5]2NH - Aldrich 98%) en concentración 0.01M (Proceso denominado lavado). Esta suspensión se dejó envejecer 24 horas y se repitió el proceso de lavado 5 veces más para eliminar los cloruros presentes en el sistema, comprobando su eliminación con el método de nitrato de plata [21].
El producto del último lavado se secó en una estufa a 80 °C durante 48 horas. El polvo cerámico obtenido se maceró en un mortero de ágata, y se sometió a tratamiento térmico a 600ºC durante una hora, para garantizar la obtención de los sólidos de interés.
En la figura 1 se indica el esquema del método de síntesis utilizado en este trabajo para la obtención de la materia prima. Las cantidades de los precursores de Zr y Ca, allí indicadas, permiten obtener un sistema de ZrO2 dopado con 6% en moles de CaO.
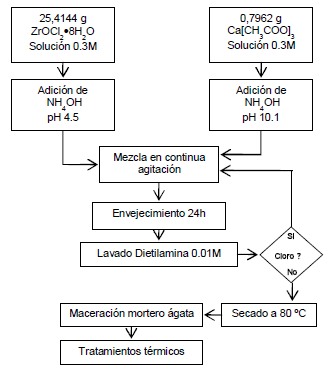
Figura 1. Etapas del procedimiento experimental del método de precipitación controlada
Figure 1. Experimental procedure of the controlled precipitation method
Los polvos cerámicos obtenidos fueron caracterizados utilizando análisis térmico diferencial y termogravimetrico (ATD/TG), para conocer el comportamiento de los polvos cerámicos frente a tratamientos térmicos utilizando para ello el equipo DSC Q100 de TA Instruments.
La espectroscopia infrarroja (FT-IR) para determinar los grupos funcionales presentes en las muestras; utilizando el espectrómetro Thermo Nicolet IR200 en un rango de medida entre 4000 y 400 cm-1.
La difracción de rayos X (DRX) para conocer las fases cristalinas presentes en las muestras, usando un difractómetro Rigaku D/MAX IIIB, utilizando la radiación Ka1 del Cu, operando a un voltaje de 40 Kv, y una corriente de 15 mA, en pasos de 0.02º (2q), tomados cada 2 segundos y en un rango de medición entre 10 y 70º (2q).
La microscopia electrónica de transmisión MET, para determinar la morfología y el tamaño de las partículas, utilizando el microscopio electrónico JEOL JEM 1200 EX.
3. RESULTADOS Y DISCUSIÓN
3.1 Curvas de Valoración Potenciométrica
3.1.1 Solución 0.3M de (ZrOCl2 - 8H2O)
La figura 2 muestra la curva de valoración potenciométrica obtenida para una concentración 0.3M de oxicloruro de circonio. Al disolverse y disociarse la sal de circonio en agua, se pudieron formar iones hidratados de circonio [Zr(OH2)8]4+ para los cuales hay que considerar que el número de coordinación del circonio es 8 [10,11]. Por otro lado, considerando la carga formal del Zr4+, se debe esperar que en el sistema predominen complejos hidroxo y oxi-hidroxo de circonio más que el complejo octa-acuo indicado anteriormente [10]. Una posible reacción que puede ocurrir, durante la disolución de la sal de circonio, es la siguiente [12]:
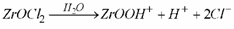 (1)
(1)
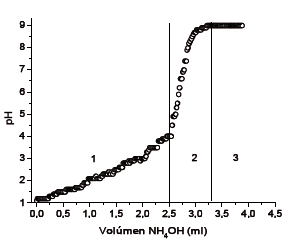
Figura 2. Curva de valoración potenciométrica para una solución 0.3M de ZrOCl2•8H2O
Figure 2. Potenciometric titration curve of 0.3M ZrOCl2•8H2O solution
Además, considerando la naturaleza del circonio, las reacciones de disociación e hidrólisis espontánea que podrían ocurrir [2,3], en el seno de la solución, son las siguientes:
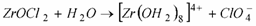 (2)
(2)
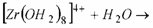
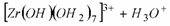 (3)
(3)
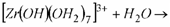
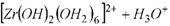 (4)
(4)
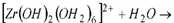
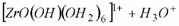 (5)
(5)
En las reacciones anteriores se produciría una gran cantidad de iones H+ lo que ocasionaría que el valor del pH inicial del sistema fuera bajo, como se evidenció experimentalmente.
Cuando se inició el proceso de adición del hidróxido de amonio, rápidamente se formaron pequeños grumos debido a la reacción entre las especies químicas presentes en la solución y el precipitante; el pH y la temperatura aumentaron lenta y gradualmente.
En un valor de pH de 1.1 se pudo observar una cantidad de partículas en la solución, aunque en general el sistema se mantuvo translúcido. Cuando el pH alcanzó un valor de 4.0, la solución se tornó opaca y de color blanco, y sobre la superficie de la suspensión se formó una delgada capa de partículas, luego se observó un rápido incremento de pH en la suspensión, pasando de 4.1 a 8.5. En este rango de pH se observó un aumento en la cantidad de fase sólida presente en el sistema; además, la capa de partículas en la superficie de la suspensión se tornó más gruesa. Finalmente, a un pH de 9, el sistema se saturó por la gran cantidad de sólidos presentes en suspensión.
Considerando la variación de la pendiente de la curva de valoración potenciométrica, figura 2, se pueden definir claramente tres zonas cuyos límites se establecieron de manera cualitativa, teniendo en cuenta el cambio brusco en la pendiente, y que deben reflejar el desarrollo de los procesos físico-químicos en el seno del sistema.
En la zona 1, la variación del pH del sistema ocurre muy lentamente debido a un alto consumo de iones OH¯ por la solución, como consecuencia del proceso de neutralización de especies de naturaleza ácida presentes en la solución que se generarían como productos de las reacciones 1 a 5, así como por el desarrollo de las reacciones de hidrólisis y condensación de las especies hidratadas de circonio. La asociación de las especies poli-nucleares de circonio favorecería la formación de embriones (aglomerados de las especies poli-nucleares).
En la zona 2 se presenta un aumento brusco del pH donde los embriones alcanzarían su tamaño crítico formándose los núcleos (embriones con estructura interna), los cuales comenzarían a crecer.
Finalmente, en la zona 3, se alcanza la saturación del sistema y los núcleos crecidos comenzarían a experimentar efectos de aglomeración y desgaste químico para formar las partículas secundarias (aglomerados de partículas primarias); las partículas secundarias sedimentarían ocasionando la separación de fases líquido-sólido, fenómeno que se observó experimentalmente.
Al adicionar la base, NH4OH, se favorece la formación del óxido hidratado, a partir de los complejos obtenidos por las reacciones de hidrólisis, por lo que la formación del óxido hidratado estaría precedida por la formación de un hidróxido de circonio, de acuerdo al siguiente mecanismo [14]:
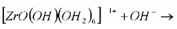
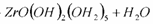 (6)
(6)
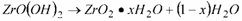 (7)
(7)
La transformación de este hidróxido a un oxi-hidróxido de circonio tendría lugar rápida e irreversiblemente, tanto que al realizar la caracterización del precipitado no se detectó la presencia del hidróxido [2, 3,14].
De acuerdo al trabajo de Zaitsev [14], este hidróxido de circonio poco estable contendría cuatro grupos hidroxilo por átomo de circonio, tal que dos de ellos podrían reaccionar con otros ligandos y los restantes permanecer inactivos, lo que permitiría establecer puentes "ol" dobles, entre cuatro átomos de circonio, dando origen a una fórmula estructural denominada "a" y que constituye a la unidad estructural del hidróxido de circonio.
Por otro lado, dado que es posible la conversión de un puente "ol" doble, a un puente "oxo", se podrían formar otros dos tipos de hidróxidos de circonio, b y g, cuyas unidades estructurales se ilustran en el trabajo de Zaitsev [14], a través de los siguientes esquemas [13,14]:
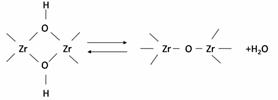 (8)
(8)
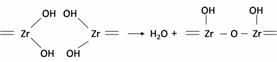 (9)
(9)
La conformación de estas unidades estructurales sería el resultado del desarrollo de las reacciones de condensación que ocurren, principalmente, en la zona 1 de la curva de valoración potenciométrica de la figura 2. Además, es posible que se formen oligómeros del siguiente tipo [14]:
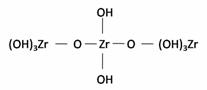 (10)
(10)
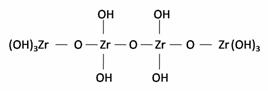 (11)
(11)
Por lo tanto, como se observa experimentalmente, al adicionar NH4OH a la solución de oxicloruro de circonio se produce un precipitado gelatinoso constituido, principalmente, por un hidróxido de circonio de naturaleza polimérica en el que los átomos de circonio estarían unidos por puentes oxo, reacciones 8 a 11, y que al filtrarlo y secarlo, al medio ambiente, se obtuvo un sólido con estructura amorfa tal como lo indican los resultados de la DRX que se muestran más adelante.
3.1.2 Solución 0.3M de Ca[CH3COO]2En la figura 3 se muestra la curva de valoración potenciométrica obtenida para una solución acidificada de Ca[CH3COO]2 0.3M.
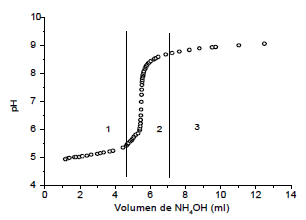
Figura 3. Curva de valoración potenciométrica para una solución 0.3M de Ca[CH3COO]2
Figure 3. Potenciometric titration curve of 0.3M Ca[CH3COO]2 solution
Considerando el comportamiento de la curva se observa que, en la región 1, figura 3, el pH se incrementó muy lentamente y fue prácticamente constante hasta la adición de 4.5 mL de la base, lo que indica que en el sistema ocurren reacciones que consumen gran cantidad de OH¯ tales como: neutralización de especies ácidas, formación de especies poli-nucleares y embriones. En la región 2 se observa un aumento brusco del pH, lo que indica que el consumo de OH¯, es mucho menor debido a que las especies ácidas han sido neutralizadas y los núcleos se han formado. Finalmente, en la región 3, se presenta una variación muy suave del pH que indica la saturación del sistema con posible precipitación de compuestos de calcio [15].
A diferencia del sistema de circonio, en el sistema con calcio no se observó un precipitado, siempre se mantuvo transparente e incoloro hasta el final del proceso. El envejecimiento de la esta disolución por un periodo de 24 horas, a temperatura ambiente, y su posterior secado a 80 °C, permitió la obtención de una fase sólida.
Con base en los datos de la literatura [15], y después de analizar el comportamiento del sistema con calcio, se establecieron las siguientes condiciones de trabajo: Utilizar una solución 0.3M de Ca[CH3COO]2 acidificada con ácido nítrico, 0.1M, y calentarla a una temperatura de 80ºC, luego adicionarle NH4OH a una velocidad de 0.2 mL cada 10 segundos, hasta que el sistema alcance un pH final de 10.1. Estas condiciones garantizan la completa disolución del precursor y una cantidad suficiente de producto.
3.2 Síntesis de los polvos cerámicos del sistema ZrO2-6%CaOPara iniciar la síntesis del óxido de circonio dopado con óxido de calcio, los sistemas de oxicloruro de circonio y de acetato de calcio, fueron preparados en recipientes separados y llevados a un pH de 4.5 y 10.1, respectivamente. Se mantuvieron en constante agitación y con las condiciones indicadas en el esquema de la figura1.
Luego se mezclaron las dos soluciones y se sometieron a agitación, utilizando el equipo de alta cizalla, a 6000 rpm durante cinco minutos; esto condujo a obtener el sistema ZrO2.6%CaO. Con los lavados hechos con dietilamina y el envejecimiento de la suspensión, se logró la eliminación de los cloruros del sistema, tal y como ocurre en otros sistemas [16], y la formación del hidróxido de circonio que favoreció la siguiente transformación en el sólido [14,17]:
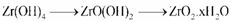 (12)
(12)
Esta última reacción conduciría a la formación de dióxido de circonio en el sistema.
3.3 Caracterización de los polvos cerámicos sintetizados
3.3.1 Análisis Térmico
En la curva de ATD, figura 4, se puede observar que se presenta un pico endotérmico alrededor de 83 ºC, que corresponde a la pérdida de agua presente en el material, el pequeño pico exotérmico alrededor de 400 °C puede indicar la cristalización de un compuesto intermedio, un oxo-hidroxo de circonio, tal como se ilustra en la reacción (12), y un pico exotérmico muy evidente a 461 ºC, que indica la cristalización del óxido correspondiente.
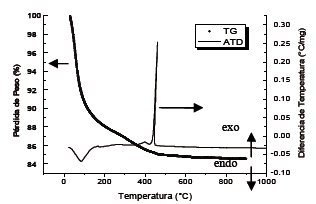
Figura 4. ATD/TG de los polvos cerámicos obtenidos
Figure 4. DTA/TG of synthesized ceramic powders
Por otro lado, en la curva TG, se observa una pérdida de peso (~12%) principalmente hasta la temperatura de 200 ºC asociada a la eliminación de agua y otros compuestos presentes en el sistema. Luego se observa una pérdida de peso menor, entre 200 y 500 °C, asociados a la eliminación de algunos residuos orgánicos usados en la síntesis del material. A partir de 500 °C, culmina la pérdida de peso, obteniendo una pérdida total de ~16% en peso, con respecto al material de partida.
Observando las curvas de ATD/TG, para los polvos cerámicos obtenidos por el método de síntesis estudiado, se puede definir que la temperatura más adecuada para la calcinación del material es ≥ 600 ºC, es decir, para temperaturas mayores a esta, todas las reacciones del sistema se han llevado a cabo y se obtiene el material cristalino.
3.3.2 Espectroscopia infrarroja
En la figura 5 se muestra la evolución de las bandas presentes en los polvos obtenidos por efecto del tratamiento térmico.
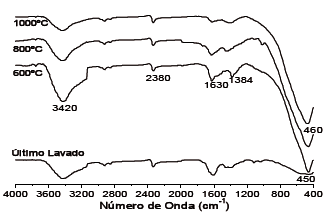
Figura 5. Espectros infrarrojos de las muestras de óxido de circonio, tratadas a diferentes temperaturas
Figure 5.Infrared spectra of zirconia samples treated thermically to different temperatures
En estos espectros es evidente la banda alrededor de 3420 cm-1 que corresponde al estiramiento del agua y al grupo hidroxilo [18], mientras la banda a alrededor de 1630 cm-1 es debido al modo de flexión del agua asociada al KBr utilizado para realizar esta prueba[19].
La banda alrededor de 2380 cm-1 es la vibración característica del CO2 presente en el ambiente. Teniendo en cuenta que el precursor de calcio es un acetato, y hay presencia de ácido nítrico, la banda ancha a ~1384 cm-1 se podría asociar al NH4NO3 debido a la competencia entre el acetato y el nitrato por enlazarse con el circonio [19].
Las bandas asociadas a los enlaces del circonio-calcio se encuentran a bajo número de onda: 450 cm-1, 460 cm-1 y un hombro a 575 cm-1 [19]. Aunque estas bandas se desplazan y se hacen más intensas a medida que la temperatura aumenta, siguen estando presentes lo que propone una forma de identificar la fase tetragonal de la circonia, posteriormente corroborada por los resultados de DRX.
3.3.3 Difracción de rayos XSe tomaron los difractogramas de rayos X, al sólido a temperatura ambiente, resultante del último lavado con la solución 0.01M de dietilamina, y a los polvos tratados a 600, 800 y 1000 ºC. En la figura 6 se muestra la superposición de los difractogramas de los sólidos de interés.
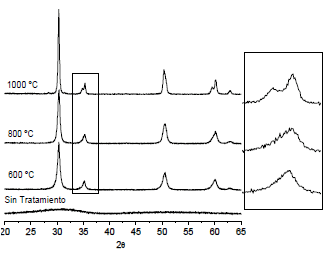
Figura 6. Difractogramas de los polvos de circonia tratados a diferentes temperaturas
Figure 6. XRD of zirconia powders treated thermically to different temperatures
Al tratar térmicamente la muestra a 1000 ºC, es evidente el desdoblamiento de los picos a ~35º y a ~60º en 2q, que corresponden a los picos característicos del óxido de circonio tetragonal [20,21].
Cabe mencionar que existe una dificultad generalizada para diferenciar con precisión la fase cúbica de la fase tetragonal, ya que los picos de las dos estructuras difieren sólo en algunas décimas de grado.
Sin embargo, el desdoblamiento de dichos picos y un análisis del difractograma utilizando el Refinamiento Rietveld [20,21] con el software FullProf Suite y tomando como patrón la estructura cristalina tetragonal de la circonia (grupo espacial P42/nmc)[20], figura 7, se verifica la presencia de la fase tetragonal de la circonia, como única fase cristalina en el sólido obtenido.
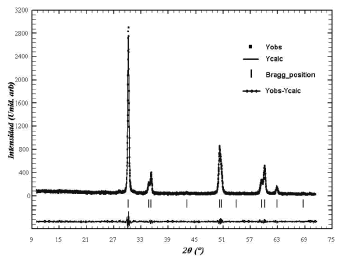
Figura 7. Refinamiento Rietveld de la muestra a 1000 ºC.
Figure 7. Rietveld refinement of sample at 1000 ºC.
En la figura 8 se muestra la micrografía MET de los polvos cerámicos de circonia, dopados con óxido de calcio, sintetizados utilizando el método de precipitación controlada y tratados térmicamente a 600 °C. A primera vista hay gran cantidad de aglomerados de partículas con tamaños entre 200 y 500 nm (zonas más grandes y oscuras), que se forman por la unión de partículas primarias que a su vez forman aglomerados blandos debido a que estas partículas son muy reactivas.

Figura 8. Fotografía MET de la muestra a 600 ºC
Figure 8. MET Micrograph of sample at 600 ºC
Observando cuidadosamente, las partículas primarias forman aglomerados blandos, como el indicado con un rombo en la micrografía, que tienen morfología irregular con diferentes tamaños en el rango de 10 y 100 nm.
4. CONCLUSIONES
Con base en los resultados obtenidos en este trabajo se puede concluir lo siguiente:
Las curvas de valoración obtenidas en este trabajo permitieron establecer un medio de control del proceso y definir sus etapas, con las cuales se propusieron los posibles fenómenos fisicoquímicos que en ellas pueden ocurrir, y considerando resultados de la literatura y los obtenidos en este trabajo, se planteó la propuesta del mecanismo de formación de las partículas cuando se utiliza el método de precipitación controlada para la obtención de circonia tetragonal.
Utilizando el método de síntesis, precipitación controlada, se pudieron obtener polvos cerámicos de ZrO2 dopado con 6 % en moles de CaO, de tamaño nanométrico, y donde prevaleció la fase tetragonal de la circonia. El difractograma del sólido obtenido a 1000 ºC, mostró que la fase cristalina del ZrO2 fue la tetragonal. Aunque en el difractograma de los sólidos tratados a 600 y 800ºC también se pudo identificar esta fase, fue necesario considerar el desdoblamiento de los picos a 35º y a 60º, y además de relacionarlo con el análisis de infrarrojo considerando la presencia de tres bandas en el espectro infrarrojo alrededor de 575 cm-1, 490 cm-1 y 450 cm-1 y así obtener una plena identificación de la fase tetragonal.
Las micrografías de los polvos cerámicos sintetizados evidenciaron la obtención de nanopartículas entre 10 nm y 100 nm de morfología no definida y con tendencia a formar aglomerados de tamaños superiores a 200 nm.
AGRADECIMIENTOS
A la VRI de la Universidad del Cauca y a la bióloga Patricia Mosquera, de la Unidad de Microscopia de la Universidad del Cauca, por la colaboración con el estudio con MET.
REFERENCIAS
[1] M. RÜHLE AND A. H. HEUER, "Phase transformations in ZrO2-containing ceramics: II, the martensitic reaction in t-ZrO2", Adv. Ceram. 12, 14 - 32. 1984. [ Links ]
[2] J. J. CABRERA, "Síntesis y Caracterización de Óxido de Circonio", Tesis de Pregrado, Facultad de Ciencias Naturales, Exactas y de la Educación, Universidad del Cauca, 2003. [ Links ]
[3] J. L. NARVÁEZ, "Obtención de Conductores Iónicos con Base en el Sistema de Óxido de Circonio", Tesis de Pregrado, Facultad de Ciencias Naturales, Exactas y de la Educación, Universidad del Cauca, 2006. [ Links ]
[4] R. H. J. HANNINK, P. M. KELLY AND B. C. MUDDLE, "Transformation toughening in zirconia-containing ceramics", J. Am. Ceram. Soc., 83 (3), 461 - 487. 2000. [ Links ]
[5] R. STEVENS, "Zirconia and Zirconia Ceramics", Magnesium Elektron Ltd., U. K., 1986. [ Links ]
[6] M. R. HOUCHIN, D. H. JENKINS AND H. N. SINHA, "Production of high-purity zirconia from zircon", Am. Ceram. Soc. Bull., 69, 1706 - 1710, 1990. [ Links ]
[7] U. SYAMAPRASAD, S. BHATTACHARJEE, R. K. GALGALI AND B. C. MOHANTY, "Zirconia ceramics by thermal plasma", Trans. Ind. Ceram. Soc., 52, 35 - 46, 1993. [ Links ]
[8] H. BRUNCKOVÁ, L'. MEDVECKÝ, J. BRIANCIN, K. SAKSL, "Influence of hydrolysis conditions of the acetate sol-gel process on the stoichiometry of PZT powders", Ceram. Int., 30, 453 - 460, 2004. [ Links ]
[9] M. C. FUERTES, J.M. PORTO LÓPEZ, "Mechanochemical synthesis and thermal evolution of La3+-ZrO2 cubic solid solutions", Ceram. Int., 30, 2137 - 2142, 2004. [ Links ]
[10] J. P. JOLIVET, M. HENRY AND J. LIVAGE, "Metal Oxide Chemistry and Synthesis", John Wiley & Sons Ltd, New York, 2000. [ Links ]
[11] J. OTTERSTEDET, D. A. BRANDRETH, "Small particles technology", Plenum Press, New York, 1998. [ Links ]
[12] W. B. BLUMENTHAL, "The Chemical Behaviour of Zirconium", (Translated into Russian), Inostr. Lit. Moscow, 1963. [ Links ]
[13] L. M. ZAITSEV, "Peculiarities in the Behaviour of Zirconyl in Solutions", Russian J. Inorg. Chem., 411 - 414, 1962. [ Links ]
[14] L. M. ZAITSEV, "Zirconium Hydroxides", Russian J. Inorg. Chem., 11 [7], 900 - 904, 1964. [ Links ]
[15] L. M. AHUMADA, "Síntesis y Caracterización de Silicatos de Calcio Utilizando Como Precursor de Sílice la Cascarilla de Arroz", Tesis de Pregrado, Facultad de Ciencias Naturales, Exactas y de la Educación, Universidad del Cauca, 2005. [ Links ]
[16] C. ARARAT IBARGUEN. Synthesis of SnO2 nanoparticles through the controlled precipitation route. Materials Chemistry and Physics. Volume 101, Issues 2-3, 15, Pages 433-440. Febrero de 2007. [ Links ]
[17] C. F. BAES, R. E. MESMER, "The Hydrolisis of Cations", John Wiley & Sons, New York, (1976). [ Links ]
[18] J.J. CABRERA LÓPEZ. "Síntesis de ZrO2 nanométrico utilizando precipitación controlada". Rev. Fac. Ing. Univ. Antioquia N° 47.Marzo 2009. [ Links ]
[19] K. NAKAMOTO, "Infrared and Raman Spectra of Inorganic and Coordination Compounds", part A, John Wiley & Sons, Inc., 5ta edition, 1978. [ Links ]
[20] International Centre for Diffraction Data (JCPDS-ICDD) PDF2 Software. [ Links ]
[21] D.A. CAMPO CEBALLOS. "Efecto del Método de Síntesis Sobre las Propiedades Mecánicas del Óxido de Circonio", Tesis de Pregrado, Facultad de Ciencias Naturales, Exactas y de la Educación, Universidad del Cauca, 2009. [ Links ]














