Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
DYNA
versão impressa ISSN 0012-7353
Dyna rev.fac.nac.minas v.78 n.169 Medellín out. 2011
CARACTERIZACIÓN DE POLVOS DE ACERÍA ELÉCTRICA PRODUCIDOS EN VENEZUELA Y EVALUACIÓN PRELIMINAR DE SU LIXIVIABILIDAD CON ÁCIDOS ORGÁNICOS DILUIDOS
CHARACTERIZATION OF ELECTRIC ARC FURNACE STEEL DUST GENERATED IN VENEZUELA AND PRELIMINARY ASSESSMENT OF ITS LEACHABILITY WITH DILUTED ORGANIC ACIDS
PEDRO DELVASTO
Dr., Profesor, Universidad Simón Bolívar, Caracas, Venezuela. delvasto@usb.ve
BETTIANA IBAÑEZ ALDAO
Ing. Materiales, Universidad Simón Bolívar, Caracas, Venezuela.
DANIELA SANDOVAL RAVOTTI
Ing. Materiales, Universidad Simón Bolívar, Caracas, Venezuela.
Recibido para revisar Junio 6 de 2011, aceptado Agosto 30 de 2011, versión final Septiembre 14 de 2011
RESUMEN: Se estudiaron polvos de acería cuyo análisis químico reveló un contenido (en peso) de: 27,0 % de Fe; 7,1 % de Mg; 4,9 % de Zn; 4,0 % de Ca y 0,5 % de Pb. La difracción de rayos X y la espectroscopía infrarroja, permitió identificar en los polvos las siguientes fases: espinelas, Fe3O4, CaCO3, SiO2, ZnO y PbO. El análisis microscópico de estos residuos indicó que están formados por agregados de partículas esferoidales cuyo tamaño varía entre 120 y 0,25 µm. La lixiviabilidad de los mismos se evaluó durante 28 días en columnas de percolación, empleando agua y disoluciones de ácidos orgánicos como agentes lixiviantes. El objetivo fue evaluar el comportamiento del residuo bajo condiciones similares a las que generan los microorganismos naturales del suelo. Se encontró que la lixiviabilidad de Zn y Pb varió entre 80 y 16 mg mensuales por kilogramo de polvo de acería.
PALABRAS CLAVE: Polvos de acería eléctrica, caracterización, lixiviación, metales pesados, ácidos orgánicos.
ABSTRACT: Electric arc furnace dust from steelmaking were studied. The chemical analysis of the dusts was as follows (by weight): 27.0 % Fe; 7.1 % Mg; 4.9 % Zn; 4.0 % Ca and 0.5 % Pb. Spinels, Fe3O4, CaCO3, SiO2, ZnO and PbO were the main mineral phases identified in the dusts through X-ray diffraction and Fourier transform infrared spectroscopy. Scanning electron microscopy showed that dusts comprised agglomerated spheroidal particles, whose sized ranged from 120 to 0.25 µm. The leachability of the dust was assessed during 28 days in percolation columns. Water and diluted organic acids were employed as leaching agents. The objective was to evaluate the behavior of this residue under conditions similar to those encountered in soils, as a consequence of microbial activity. The leachability of Zn and Pb was found to be between 80 and 16 mg per kg of dusts, per month.
KEYWORDS: Electric arc furnace dust, characterization, leaching, heavy metals, organic acids.
1. INTRODUCCIÓN
los polvos de acería son residuos sólidos complejos [1-9], que provienen de los sistemas de limpieza de las corrientes gaseosas que se generan durante las operaciones de fusión y afino del acero, en hornos de arco eléctrico (EAF, por sus siglas en inglés). La química y mineralogía de dichos residuos es variable, y depende, tanto de las condiciones operativas particulares de cada planta siderúrgica, como de las materias primas utilizadas en el proceso. Sin embargo, suelen estar constituidos, fundamentalmente, por partículas discretas de óxidos metálicos simples o complejos [3,5]. Si bien los componentes mayoritarios de los polvos de EAF son óxidos de hierro, los mismos se caracterizan por presentar un contenido importante de metales pesados, como Pb, Zn y Cd, lo que los cataloga como residuos peligrosos [1-9]. El contenido en metales pesados de esta clase de residuos puede resultar particularmente elevado, llegando a rondar un 25 % en peso, en operaciones siderúrgicas basadas, exclusivamente, en fusión de chatarra. La razón de esto, radica en que la chatarra de acero puede tener múltiples procedencias y, al derivarse de componentes manufacturados desechados, tienden a venir contaminados con metales pesados. Tal es el caso, por ejemplo, de los componentes de acero galvanizado, cuyo contenido en Zn resulta particularmente alto [1].
Sin embargo, no todas las operaciones de fusión de acero en hornos de arco eléctrico están basadas en la fusión de chatarra. En países que cuentan con hierro de reducción directa (DRI, por sus siglas en inglés), los EAF se alimentan en porcentajes variables con esta materia prima, haciendo que el consumo de chatarra sea menor. En particular, para el caso venezolano (país productor de DRI), una práctica metalúrgica usual de producción de acero estructural convencional, conlleva una carga al horno de 20 % de chatarra y 80 % de DRI. Es de esperarse, por tanto, que prácticas de esta naturaleza conduzcan a polvos de EAF con menores contenidos en metales pesados, aunque, en realidad, poco se conoce acerca de los polvos generados por operaciones siderúrgicas en las cuales el patrón de cargas al horno eléctrico esté fundamentado en hierro de reducción directa. En las siderúrgicas venezolanas, se estima la producción de polvos de EAF entorno a los 25 kg por tonelada de acero líquido producida.
Si bien en los países desarrollados existe la combinación de una legislación ambiental estricta con la disponibilidad de diferentes procesos industriales para recuperar metales no férreos a partir de esta clase de residuos [1,2], en los países emergentes la situación no es la misma, y muchas veces los polvos de EAF son dispuestos en vertederos o rellenos sanitarios, a veces en condiciones poco controladas. La situación se agrava cuando estos residuos entran en contacto directo con los suelos, bien por el mismo proceso de elaboración del relleno o cuando el polvo es transportado por los vientos o las aguas de escorrentía a lugares adyacentes del depósito inicial. En este caso, resulta factible que los residuos entren en contacto con la microbiota (seres vivos) del suelo, creando interacciones que pueden impactar, negativamente, sobre la movilidad de los metales pesados en las aguas de percolación, pudiéndose facilitar la extensión del eventual daño medioambiental. Se conoce que, como consecuencia de sus procesos metabólicos, los microorganismos del suelo (bacterias, hongos, levaduras, algas, etc.) son capaces de producir diversos ácidos orgánicos (p. ej. acético, cítrico, oxálico, tartárico, fórmico, glucónico, entre otros)[10-12, 14,15]. Los ácidos orgánicos de esta naturaleza presentan la particularidad de que pueden atacar a las matrices minerales de los óxidos metálicos - como las que se encuentran presentes en los polvos de EAF - de dos formas, por ataque protónico y por complejación de los metales con los aniones orgánicos de dichos ácidos, haciendo que esta clase de residuos puedan resultar lixiviables bajo condiciones naturales [10-12, 14, 15].
Con base en la realidad anteriormente plasmada, en el presente trabajo se estudió una muestra de polvos de EAF provenientes de una acería venezolana dedicada a la producción de acero al carbono estructural, cuya práctica metalúrgica conlleva, principalmente, la fusión de DRI (80 % de la carga a los hornos). En la primera parte del trabajo, los polvos de partida se caracterizaron, química, mineralógica y morfológicamente, por medio de las técnicas de espectroscopía de absorción atómica (AAS, por sus siglas en inglés), difracción de rayos X (XRD, por sus siglas en inglés), espectroscopía infrarroja por transformada de Fourier (FT-IR, por sus siglas en inglés), microscopía electrónica de barrido (SEM, por sus siglas en inglés) con microanálisis químico por espectroscopía de energías dispersivas (EDS, por sus siglas en inglés) y se determinó su pH de contacto. En la segunda parte del trabajo, los polvos se sometieron a un proceso de lixiviación estática en columnas de percolación, utilizando ácidos orgánicos diluidos como agentes lixiviantes, a fin de evaluar el comportamiento del residuo bajo condiciones de acidez y presencia de aniones orgánicos, similares a la que pueden generar los microorganismos naturales del suelo; simulando así una situación de disposición final de este residuo en vertederos. El fin último del estudio es tratar de establecer las cantidades de metales pesados (Zn y Pb) que se pueden movilizar a partir de polvos de EAF provenientes de procesos de fusión de DRI, bajo estas condiciones tan particulares.
2. PROCEDIMIENTO EXPERIMENTAL
2.1 Caracterización de los polvos de acería
Para el análisis químico de los principales metales que componen a los polvos de EAF estudiados, se digirieron (por cuadruplicado) 100 mg de polvo en 100 ml de agua regia, en un reactor calentado eléctricamente, equipado con un condensador para evitar la pérdida de vapores. El líquido se filtró y diluyó con agua destilada en un balón volumétrico de 500 ml, para posteriormente ser analizados sus cotenidos de Fe, Zn, Pb, Mg, Cr, Cu y Ca mediante la técnica de AAS, en un espectrómetro Shimadzu AA-6200.
El análisis mineralógico por XRD se realizó empleando un difractómetro X’PERT Pro Philips, empleando radiación de cobalto (l = 1,79 Å) y un barrido de ángulos 2θ entre 5º y 90º. La identificación de los compuestos se efectuó por comparación con las fichas estándar del International Centre for Diffraction Data (ICDD).
El análisis por FT-IR se llevó a cabo triturando en un mortero de ágata KBr y polvo de EAF en una proporción en peso de 98:2. La mezcla se comprimió en una prensa manual hasta obtener una pastilla de 3 mm de diámetro, cuyo espectro infrarrojo se obtuvo en un equipo BRUKER Tensor 2, empleando el software OPUS, con corrección de línea base y compensación atmosférica de CO2, ajustando la resolución espectral en 2 cm-1 y 32 barridos por espectro.
Para la obtención de imágenes por SEM de los polvos, muestras del mismo se recubrieron con grafito conductor mediante sputtering, y se llevaron a un microscopio JEOL JSM-6390, equipado con una sonda EDS para microanálisis químico, el cual operó a un voltaje de aceleración de 25 kV. La medición del tamaño de las partículas se efectuó mediante un software de análisis de imágenes. Finalmente, se determinó el pH de contacto de los polvos de acería, suspendiendo 70 g de polvos en 1 L de agua destilada bajo agitación mecánica por 120 min., para luego medir el pH del líquido sobrenadante con un pH metro DIGIMED-23 equipado con un electrodo combinado de Ag/AgCl.
2.2 Lixiviabilidad de los polvos de acería
La lixiviabilidad estos polvos de acería se evaluó en columnas de percolación cilíndricas, manufacturadas en plexiglás, de 45 cm de alto y 10 cm de diámetro. Como lixiviantes se emplearon agua destilada (pH=5,6) como control y soluciones diluidas de los siguientes ácidos orgánicos: cítrico (C6H8O7), oxálico (C2H2O4) y tartárico (C4H6O6). Las concentraciones de las disoluciones de dichos ácidos fueron, respectivamente 0,5 g/l, 0,2 g/l y 0,41 g/l. Dichas concentraciones garantizaron que el pH de todas las disoluciones de ácidos orgánicos usadas se mantuviera alrededor de 3 unidades.
Estas condiciones se buscan, ya que permiten evaluar el comportamiento del residuo bajo condiciones de acidez y presencia de aniones orgánicos, similares a la que pueden generar microorganismos [10-12]; simulando así una situación de disposición final de este residuo en presencia de suelo natural, eventualmente formando una mezcla con éste, por ejemplo, en vertederos poco controlados.
El lecho de las columnas estuvo constituido por 2,0 kg de una mezcla (en peso) de 80 % de polvos de acería y 20 % de arena silícea lavada, añadida para facilitar la percolación de las disoluciones y simular una columna de suelo, es decir, que la masa efectiva de residuo en cada columna fue de 1,6 kg. El volumen efectivo de la columna (i. e. ocupado por la mezcla sólida residuo/arena) fue de 3.000 mL. Luego de saturarse con agua destilada, las columnas se irrigaron cada 48 horas, con 500 mL de las soluciones lixiviantes, por un período de 4 semanas continuas (28 días). No se realizó recirculación del líquido lixiviado. Los análisis químicos para Zn y Pb, en los líquidos lixiviados recogidos, se realizaron mediante AAS. Todas las experiencias de lixiviación se realizaron por duplicado.
3. RESULTADOS Y DISCUSIÓN
3.1 Caracterización de los polvos de acería
La tabla 1 muestra la composición química general de los polvos de acería de origen venezolano, analizados en el presente trabajo, y su comparación con otros polvos de EAF originados en diversos países cuyos resultados se encuentran reportados en la literatura. Tal y como se aprecia, el polvo de acería EAF estudiado presenta un porcentaje de Zn entre cuatro y seis veces menor que el de sus contrapartes de otros países, y es, incluso, dos veces menor que el valor típico mínimo registrado para los Estados Unidos, de acuerdo con el estudio de Nyirenda [2]. Algo similar ocurre con el Pb, metal pesado para el cual el polvo de acería estudiado presenta valores porcentuales entre dos y diez veces menores a los típicos basados en procesos de fusión de chatarra de acero.
Tabla 1. Contenido en diversos metales de varios polvos de acería EAF originados en algunos países [2,5,8,9] y su comparación con los evaluados en el presente trabajo
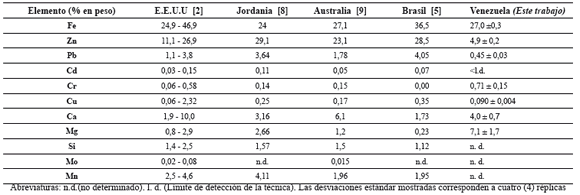
Es notorio también el hecho de que los contenidos de Cd en los polvos de EAF son menores al límite de detección de la técnica (~ 5 ppb), lo que indica que este peligroso metal pesado se encuentra prácticamente ausente del residuo. Este nivel bajo de metales pesados es consecuencia de que el patrón de cargas a los hornos de la acería de la cual provienen esté basada en el uso de hierro de reducción directa (DRI). Esta materia prima, por el contrario, suele presentar elevados contenidos de ganga no metálica, razón que podría explicar que los contenidos de Mg y Ca sean relativamente elevados en comparación con los otros polvos de acería EAF mostrados en la tabla. Resalta el caso del Mg, cuyo porcentaje en peso dentro de los polvos venezolanos supera hasta treinta veces el contenido típico de este metal en polvos de acería de otras procedencias. No obstante, faltaría establecer si los contenidos de silicio (que es un componente típico de la ganga no metálica en el DRI) en los polvos EAF estudiados en el presente trabajo son también elevados, para poder establecer una mejor relación entre estos hechos. Este análisis no fue realizado en el marco del presente trabajo.
El bajo contenido relativo de metales pesados de los polvos EAF venezolanos, hace que, de acuerdo con la clasificación hecha por Nyirenda [2], se le catalogue como un residuo de tipo intermedio (entre 1 % y 15 % en peso de Zn). Esta clase de polvos de EAF es la más difícil de reciclar y no resulta interesante para la recuperación secundaria de metales no férreos como el Zn. Su disposición en vertederos, sin embargo, podría implicar importantes perjuicios medioambientales, ya que una planta de acería mediana, que produzca alrededor de 1500 TM de acero por día, estaría generando diariamente 37 TM de este residuo, o lo que es lo mismo, se estarían depositando diariamente, en el medio ambiente, cerca de 2 TM de metales pesados (Zn y Pb).
El difractograma típico de los polvos de acería estudiados en este trabajo se muestra en la figura 1. En dicha figura las letras indican las fases cristalinas identificadas, las cuales son: Espinelas (posiblemente Fe3O4; ZnFe2O4; FeCr2O4 ó MgFe2O4); ZnO, CaCO3; SiO2 y PbO.
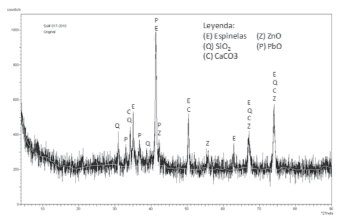
Figura 1. Difractograma de los polvos de acería estudiados
Todas las fases mencionadas, encontradas en polvos de acería venezolanos, son coincidentes con las fases minerales reportadas en la literatura para polvos de EAF generados en otros países [2-9], lo cual indica que, en sentido estricto, los procesos de formación de estas fases mineralógicas son inherentes al propio proceso de fusión en EAF, independientemente de la composición química de las materias primas utilizadas para fabricar el acero.
Continuando con el análisis mineralógico y químico de este residuo, la figura 2 muestra el espectro infrarrojo típico de los polvos de acería estudiados. En primer lugar, se encuentra una banda aguda de intensidad media a 3644 cm-1 , denotada como “A", correspondiente a vibraciones de tensión del grupo O-H libre; estos grupos OH corresponden, probablemente, a aquellos que son adsorbidos por algún grupo higroscópico presente en los polvos, por ejemplo el CaO y son típicos de minerales arcillosos [5].
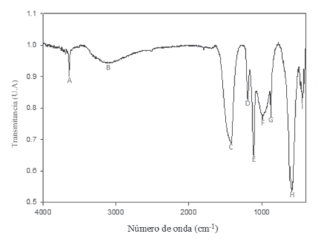
Figura 2. Espectro FT-IR de los de polvos de acería analizados.
También se observa una señal poco intensa, pero amplia (denotada como “B"), a 3102 cm-1 que, se puede asociar con las vibraciones de tensión de los grupos O-H del agua, la cual se puede encontrar como humedad en la muestra o en forma de fases hidratadas o hidróxidos. Por otra parte, se encuentran bandas a 1421 cm-1 y 1193 cm-1 (identificadas, respectivamente, como “C" y “D"), correspondientes, en el primer caso, a vibraciones de grupos carbonatos y, en el segundo caso, a estiramientos de los mismos grupos carbonato.
De acuerdo con estudios previos [5], se pueden encontrar estos grupos funcionales en los polvos de acería como consecuencia de la presencia de carbonatos hidratados de Zn y Pb (hidrocincita e hidrocerusita), sin embargo, los análisis por XRD mostrados en la figura 1 no corroboran la existencia de éstos compuestos en los polvos de acería de origen venezolano estudiados en el presente trabajo. No obstante, de acuerdo con los porcentajes de Zn y Pb, determinados mediante AAS, que se presentan en la tabla 1, dichos elementos se encontrarían formando mayoritariamente ZnO y PbO. Por lo tanto, si se considera que pudiesen existir carbonatos hidratados de Zn y Pb, éstos estarán presentes en muy baja proporción respecto a las otras fases presentes en los polvos de acería estudiados. Lo más probable es que dicha banda se corresponda con la presencia de carbonato de calcio en la muestra. La banda aguda a 1112 cm-1 y la banda de 991 cm-1 (marcadas como “E" y “F", respectivamente) corresponden a las vibraciones del enlace Si-O, posiblemente asociadas con cuarzo o con silicatos presentes en los polvos [5].
La señal que se encuentra a 874 cm-1 (marcada por la letra “G") se atribuye a enlaces S-O, es decir, grupos funcionales de azufre. En este sentido, Bruckard y colaboradores [9], atribuyen la presencia del S en los polvos de acería a los siguientes compuestos: CaSO4, Na2SO4 y K2SO4, sin embargo, dichos compuestos no se detectaron mediante XRD, en los polvos EAF venezolanos, probablemente debido a su baja proporción respecto a las otras fases minerales presentes. Como será explicado más adelante, estos grupos funcionales S-O pudiesen también estar asociados con partículas ricas en carbono, como las mostradas en la figura 3 (I), las cuales pueden provenir del uso de gas natural o de sustancias carbonosas en ciertas etapas del proceso de aceración en el EAF. Finalmente, las señales hacia 585cm-1, 443 cm-1 y 419 cm-1 (bandas “H" e “I") son características del enlace M-O, presente en óxidos simples y espinelas, identificados previamente en los análisis de XRD mostrados en la figura 1.

Figura 3. Imágenes SEM típicas de las partículas que conforman los polvos de acería analizados.
El análisis morfológico SEM realizado a las muestras de polvos de acería venezolanos, mostrado en la figura 3, indica que los mismos presentan una variabilidad importante de tamaños. En (A) se muestra una visión general de los polvos, los cuales son en realidad aglomerados de partículas más pequeñas como se aprecia en la secuencia (B) a (F). En (B), el acercamiento a un agregado de partículas muestra, señalada por flechas numeradas, la coexistencia de partículas aglomeradas (1) y hojuelas de hollín (2). En (C) se aprecia, señalada como (3), otro tipo de partícula esferoidal, de unos 20 µm, que exhibe bordes facetados y partículas más pequeñas adheridas. En (D), (E) y (F), se aprecia a grandes aumentos que los cúmulos están conformados por multitud de partículas esferoidales de entre 0,25 y 2 µm.
La forma esferoidal y alisada de las partículas de menor tamaño, como las mostradas en la imagen F de la figura 3, indica que pudieron haberse formado por condensación de vapores, tal y como lo explican Guézennec y colaboradores [13]. Las partículas esferoidales de mayor tamaño que presentan una superficie irrregular y facetada (Figura 3 C) podrían generarse tras un proceso de aglomeración en caliente y eventual sinterización de partículas más pequeñas durante el arrastre y acopio de los polvos en el proceso de limpieza de los gases del EAF. La superficie facetada, no obstante, también puede atribuirse a un origen de la partícula que ha implicado un proceso de solidificación, en lugar de condensación, como consecuencia del arrastre de gotas de líquidos (escorias o metal) a la corriente gaseosa durante el proceso de aceración [13].
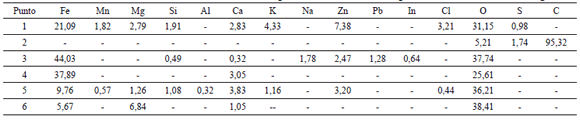
Los análisis químicos semicuantitativos realizados por EDS a cada uno de los puntos señalados y enumerados en la Figura 3, se muestran en la tabla 4. Los mismos indican la alta variabilidad química de las partículas de polvo. La presencia de los diferentes elementos químicos registrados, corroboran las diferentes fases mineralógicas identificadas mediante DRX y FTIR. Se hace la aclaratoria de que en la tabla 4 la señal de carbono está omitida en todos los análisis, salvo en el punto 2.
La práctica totalidad de las partículas analizadas muestra contenidos mayoritarios de hierro, algunas veces asociado a zinc, lo que es indicativo de la presencia de la fase ZnFe2O4, la cual es común de encontrar en polvos de acería [3, 5, 6]. La presencia de azufre en ciertas partículas (puntos 1 y 2 de la figura 3 B), corrobora la presencia de grupos funcionales de azufre en el espectro FTIR de los polvos (figura 2 y tabla 3). Estas regiones que presentan azufre se encuentran asociadas con partículas ricas en carbono (tabla 4, punto 2), que posiblemente corresponden al hollín generado durante la degradación de los electrodos del EAF o producido por la combustión imperfecta del gas natural y de las de adiciones carbonosas empleadas en ciertas etapas del proceso, por ejemplo, los ajustes de carbono o el precalentamiento de materias primas.
Tabla 4. Microanálisis semicuantitativo EDS (% en peso) en los diferentes puntos enumerados en la figura 3.
3.2 Lixiviabilidad de los polvos de acería
En cuanto a la lixiviabilidad de los metales pesados presentes en los polvos de acería cuando se emplean ácidos orgánicos diluidos, los resultados se muestran en la figura 4. La misma se expresa en términos de la masa acumulada (mg) de metal extraído de una columna con 1,6 kg de residuo irrigada durante 28 días. Las sub figuras indican: (I) Control irrigado con agua destilada, (II) columna irrigada con ácido tartárico, (III) columna irrigada con ácido cítrico, (IV) columna irrigada con ácido oxálico. Se hace la acotación de que los volúmenes añadidos hacen referencia a las veces que se irriga la columna con un volumen de lixiviante igual al volumen de la columna ocupado por el residuo, en este caso, 3 litros.
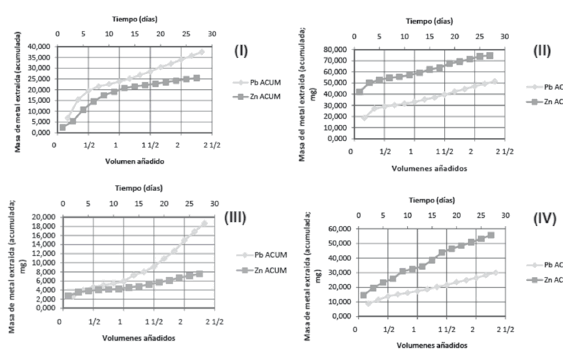
Figura 4. Lixiviabilidad del Zn y del Pb presente en los polvos de acería venezolanos.
Como se aprecia en la sub-figura 4 (I), el agua destilada empleada como control, per se, fue capaz de movilizar cantidades importantes de metales pesados (Zn y Pb) de la columna de residuo, aunque en mayor medida Pb (37,5 mg) que Zn (25 mg), para 28 días de tratamiento. Esto equivale a decir que, bajo las condiciones de riego descritas, se movilizan, mensualmente, 23,4 mg Pb/kg de polvo y 15,6 mg de Zn/kg de polvo, utilizando meramente agua como medio lixiviante (para este cálculo debe tenerse en consideración que la columna de percolación contiene, de manera efectiva, 1,6 kg de polvos de acería). Esta mayor tendencia del agua destilada para lixiviar más fácilmente al Pb frente al Zn ha sido también observada por otros autores [14], durante la lixiviación de polvos provenientes de sistemas de limpieza de los gases de combustión de residuos industriales, constituidos por óxidos multimetálicos, cuya granulometría media varía entre 0,004 y 100 µm, algo similar a la de los polvos de acería estudiados en el presente trabajo. En dicha referencia [14], los autores Wu y Ting atribuyen esta mayor movilidad del Pb como consecuencia de la formación del anión complejo movilizable Pb(OH)3-. Bajo las condiciones experimentales del presente trabajo, éste anión complejo de plomo puede generarse, debido al carácter fuertemente alcalino de los polvos de acería que fueron estudiados, cuyo pH de contacto con el agua destilada se promedia en 12,8 ± 0,1 unidades. Este carácter alcalino surge como consecuencia de la presencia en el mismo de una importante cantidad de óxidos anhidros de calcio, magnesio y hierro, así como carbonato de calcio. Por su parte, el ácido tartárico diluido, sub-figura 4 (II), muestra una tendencia inversa, ya que este ácido favorece la lixiviabilidad del Zn notablemente, alcanzándose movilizaciones del orden de 46,9 mg Zn/kg de polvo y de 31,9 mg Pb/kg de polvo. Este resultado está en concordancia con el trabajo de Golab y Orlowska [12], el cual indica que el ácido tartárico es un excelente agente lixiviante para los óxidos de zinc.
Los resultados que se obtienen con el ácido cítrico - sub-figura 4 (III) - son mucho menores, incluso, que los obtenidos con el agua destilada. En este caso el Pb se moviliza mucho mejor que el Zn, sin embargo, el proceso de lixiviación llevado a cabo solamente es capaz de movilizar, mensualmente, 11,6 mg Pb/kg de polvo y 4,7 mg de Zn/kg de polvo presente en la columna. Anjum y colaboradores [15], utilizaron los ácidos orgánicos producidos por el hongo del suelo Aspergillus niger, encontrando que la movilización del Zn presente en rocas arcillosas se ve afectada negativamente por la presencia de ácido cítrico.
En contraste, la presencia de ácido oxálico o tartárico, mejoraba la lixiviabilidad del Zn. Estos resultados concuerdan con el presente trabajo, como se aprecia en la figura 4 (III), que demuestra la menor eficiencia del ácido cítrico para lixiviar al Zn y al Pb presente en los polvos de acería, al compararse con el agua destilada (control) y los ácidos tartárico y oxálico. Finalmente, para el caso del ácido oxálico diluido - sub-figura 4 (IV) - se tiene una situación similar a la del ácido tartárico, es decir, disuelve mejor al Zn que al Pb, aunque con unos rendimientos un tanto menores. El ácido oxálico movilizó 34,4 mg Zn/kg de polvo y 18,8 mg de Zn/kg de polvo.
En cuanto al potencial de los lixiviantes utilizados en este trabajo, el mismo puede resumirse para el Zn en el siguiente orden: Tartárico > Oxálico > Agua > Cítrico. En tanto, para el Pb el orden es: Tartárico > Agua > Oxálico > Cítrico. Se observa que todos los ácidos estudiados presentan comportamientos diferentes, a pesar de que todas las disoluciones empleadas se prepararon bajo condiciones de isoacidez (pH @ 3). La razón de estas variaciones subyace en el hecho de que cada uno de éstos ácidos es capaz de formar complejos, de distinta estabilidad, con los metales pesados durante la lixiviación de las fases que contienen a dichos metales. Este comportamiento ha sido observado en diversos sistemas de lixiviación heterotrófica empleando hongos [12, 14, 15]. En casos como el del ácido oxálico o del tartárico, la solubilidad de estos complejos pudiese ser elevada en el sistema lixiviante/sólido, haciendo que suba la tasa de percolación de metales pesados. Por otro lado, pueden también generarse sales orgánicas insolubles, las cuales al precipitar se atrapan en la columna, ayudando así a frenar el proceso de lixiviación del metal pesado. Puede ser este el caso del ácido cítrico, cuyos rendimientos de movilización metálica no llegan a superar los del agua destilada. Es posible que se generen citratos parcialmente insolubles de Zn y de Pb que permanezcan adheridos a las partículas del polvo, esto podría verse facilitado por el elevado pH que desarrolla el residuo. No obstante, para dilucidar los mecanismos subyacentes en el proceso de movilización de los metales pesados en este sistema, se hace necesario implementar un estudio termodinámico minucioso, lo cual, por el momento, está fuera de los alcances del presente trabajo. Desde un punto de vista medioambiental, el comportamiento del ácido cítrico resultaría promisorio, ya que, al fomentarse el crecimiento de microrganismos productores de este ácido en la zona en donde se disponen los polvos de EAF, se podría limitar la movilización de metales pesados como el Zn y el Pb a través de las aguas de percolación que se generen en la pila de disposición del residuo.
4. CONSIDERACIONES FINALES
Se concluye que los polvos de acería estudiados (generados en operaciones de hornos de arco eléctrico cuyos patrones de carga se basan en la fusión de DRI), presentan un contenido en metales pesados (específicamente Zn y Pb), puede llegar a ser hasta seis veces menor que el que presentan polvos de acería producidos en operaciones convencionales de fusión de chatarra Sin embargo, en lo referente a la morfología del material y fases mineralógicas presentes, el carácter general de los polvos provenientes de la fusión de DRI no difiere en demasía de los polvos provenientes de la fusión de chatarra, ya que los procesos térmicos, termodinámicos y cinéticos son, en ambos casos, básicamente los mismos. Referente a la lixivia-bilidad del Zn y del Pb presente en los polvos de EAF venezolanos, bajo condiciones similares a las existentes en suelos, se encontró que varía entre 80 y 16 mg de metales pesados por kilogramo de residuo, determinándose que el agua, por sí sola, es capaz de movilizar estos metales durante su percolación a través del residuo. Finalmente, el ácido cítrico, se mostró capaz de frenar la lixiabilidad de estos metales, lo que lo convierte en un agente interesante a adicionar en el sistema de deposición del residuo, para disminuir la velocidad de lixiviación del Zn y del Pb.
AGRADECIMIENTO
Este trabajo fue apoyado financieramente por el DID-USB bajo el proyecto S1-IN-CAI-002-08 y por la Corp. FBK, C. A. bajo el proyecto LOCTI FUNINDES USB 49-2421. Las muestras de polvo fueron suministradas amablemente por J. Tirado y M. Oropeza. Se agradece además la cooperación técnica de J. Herrera, P. Moncada y de L. Ahn.
REFERENCIAS
[1] Castells, X., Reciclaje de residuos industriales, Ediciones Díaz de Santos, Madrid, 2000. [ Links ]
[2] Nyirenda, R. L., The processing of steelmaking flue-dust: a review, Miner. Eng., 4, pp. 1003-1025, 1991. [ Links ]
[3] Sofilic, T., Novosel-Radovi, V., Cerjan-Stefanovic, S. and Rastovcan-Mioc, A., The mineralogical composition of dust from an electric arc furnace, Mater. Tehnol., 39, pp. 149-154, 2005. [ Links ]
[4] Orescanin, V., Mikelic, L., Sofilic, T., Rastovcan-Mioc, A., Uzarevic, K., Medunic, G., Elez, L. and Lulic, S., Leaching properties of electric arc furnace dust prior/following alkaline extraction, J. Environ. Sci. Heal. A, 42, pp. 323 - 329, 2007. [ Links ]
[5] Machado Martins, F., Dos Reis Neto, J. M. and Da Cunha, C., Mineral phases of weathered and recent electric arc furnace dust, J. Hazard. Mater., Vol. 154, pp. 417-425, 2008. [ Links ]
[6] Da Silva Machado, J. G. M., Andrade Brehm, F., Mendes Moraes, C., Dos Santos, C. and Faria Vilela, A., Characterization Study of Electric Arc Furnace Dust Phases, Mater. Res., 9, pp. 41-45, 2006. [ Links ]
[7] Lenz, D. and Martins, F., Lead and zinc selective precipitation from leach electric arc furnace dust solutions, Rev. Matéria, 12, pp. 503 - 509, 2007. [ Links ]
[8] Shawabkeh, R., Hydrometallurgical extraction of zinc from Jordanian electric arc furnace dust, Hydrometallurgy, 104, pp. 61-65, 2010. [ Links ]
[9] Bruckard, W., Davey, K., Rodopoulos, T., Woodcock, J. and Italiano, J., Water leaching and magnetic separation for decreasing the chloride level and upgrading the zinc content of EAF steelmaking baghouse dusts, Int. J. Miner. Process.,75, pp. 1-20, 2005. [ Links ]
[10] Jain, N. and Sharma, D., Bio-hydrometallurgy for nonsulfidic minerals: a review, Geomicrobiol. J., 21, pp. 135-144, 2004. [ Links ]
[11] Groudev, S. N., Biobeneficiation of mineral raw materials, Miner. Metall. Proc., 16, pp. 19-28, 1999. [ Links ]
[12] Golab, Z. and Orlowska, M., The effect of amino and organic acids produced by the selected microorganisms on metal leaching, Acta Microbiol. Pol., 37, pp. 83-93, 1988. [ Links ]
[13] Guézennec, A., Huber, J., Patisson, F., Sessiecq, P., Birat, J. and Ablitzer, D., Dust formation in electric arc furnace: birth of the particles, Powder Technol., 157, pp. 2-11, 2005. [ Links ]
[14] Wu, H. Y. and Ting, Y. P., Metal extraction from municipal solid waste (MSW) incinerator fly ash: Chemical leaching and fungal bioleaching, Enzyme Microb. Tech., 38, pp. 839-847, 2006. [ Links ]
[15] Anjum, F., Bhatti, H., Asgher, M. and Shahid, M., Leaching of metal ions from black shale by organic acids produced by Aspergillus niger, Appl. Clay Sci., 47, pp. 356-36, 2010. [ Links ]













