Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
DYNA
Print version ISSN 0012-7353
Dyna rev.fac.nac.minas vol.82 no.189 Medellín Jan./Feb. 2015
https://doi.org/10.15446/dyna.v82n189.42036
http://dx.doi.org/10.15446/dyna.v82n189.42036
Pechini method used in the obtention of semiconductor nanoparticles based niobium
Uso del método Pechini en la obtención de nanopartículas semiconductoras a base de niobio
Angela Mercedes Raba-Páez a, Diego Nicolás Suarez-Ballesteros b, José Jobanny Martínez-Zambrano c, Hugo Alfonso Rojas-Sarmiento d & Miryam Rincón-Joya e
a Departamento de Física, Universidad Francisco de Paula Santander, Cúcuta, Colombia. amrabap@unal.edu.co
b Grupo de Catálisis, Universidad Pedagógica y Tecnológica de Colombia, Tunja, Colombia. diego.suarez@uptc.edu.co
c Grupo de Catálisis, Universidad Pedagógica y Tecnológica de Colombia, Tunja, Colombia. jose.martinezz@uptc.edu.co
d Grupo de Catálisis, Universidad Pedagógica y Tecnológica de Colombia, Tunja, Colombia. hugo.rojas@uptc.edu.co
e Departamento de Física, Universidad Nacional de Colombia, Bogotá, Colombia. mrinconj@unal.edu.co
Received: February 2th, 2014. Received in revised form: September 10th, 2014. Accepted: September 29th, 2014.
Abstract
The (Nb2O5) niobium pentoxide compound was synthetized by Pechini method. The followed synthesis protocol is promising to obtain Nb2O5 nanoparticles, in orthorhombic phase. This phase was obtained in the samples calcined at 600°C for 2 hours and the submitted at 500°C for 22 hours in gas flow. For the phase determination and crystal structure was performed XRD. The BET method was used to obtain surface area measurements of the obtained oxide. Raman scattering was employed in order to analyze the nanostructures vibrational spectrum and FEG-SEM in order to study the morphology of the obtain oxides.
Keywords: Nb2O5; Nanoparticles; thermal treatment; characterization; Raman.
Resumen
El Pentóxido de niobio (Nb2O5) ha sido sintetizado por el método Pechini. El protocolo de síntesis seguido resulta ser prometedor para obtener nanopartículas de Nb2O5, en la fase ortorrómbica. Esta fase, fue obtenida en la muestra tratada térmicamente a 600°C, durante 2 horas y en la muestra sometida a 500°C durante 22 horas en flujo de gases. Para la determinación de la fase y estructura cristalina se realizó DRX. El método BET se usó con el fin de obtener medidas del área superficial. Se empleó dispersión Raman con el fin de analizar el espectro vibracional de las nanoestructuras y MEB-FEG para estudiar la morfología de los óxidos obtenidos.
Palabras clave: Nb2O5; nanopartículas; tratamiento térmico; caracterización; Raman.
1. Introducción
Recientemente, ha surgido un gran interés en el tratamiento de la contaminación orgánica presente en el agua a través del método fotocatalítico; éste método puede destruir los contaminantes completamente. El uso de fotocatalizadores semiconductores para la oxidación aerobia de moléculas orgánicas tiene ventajas prácticas y eficientes desde el punto de vista económico, ecológico, de reutilización y durabilidad. Además, para una efectiva utilización de energía procedente de radiación solar, es necesario el desarrollo de un material que responda a la luz visible. [1,2]
El agua pierde calidad debido a la contaminación proveniente de urbes e industrias, por lo que se han venido buscando alternativas que aseguren su abastecimiento futuro [3,4], beneficiando así todos los factores que constituyen la sociedad: el ecosistema, la salud, la alimentación, la educación, la economía, etc. La fotocatálisis heterogénea es una de estas alternativas. Básicamente consiste en la aceleración de una reacción química por actuación de un catalizador sólido, activado mediante excitación electrónica al incidir sobre él radiación luminosa. [5]
El niobio y compuestos a base de niobio dan a lugar a diversas aplicaciones [6]. Específicamente el pentóxido de niobio, Nb2O5, debido a sus propiedades físicas y químicas excepcionales puede dar lugar a aplicaciones prometedoras en dispositivos magnéticos, biotecnología, nanotecnología y catálisis [1,7]. Las propiedades físicas y químicas que presenta este material lo hacen promisorio en procesos de fotocatálisis ya que es posible disminuir su energía de gap haciéndolo competitivo frente al óxido de titanio TiO2 [8,9], compuesto comúnmente empleado. El Nb2O5 existe en varias fases cristalinas dependiendo de la presión y la temperatura a la que esté sometido. Algunas de estas fases cristalinas son: fase B (estructura monoclínica), fase Z (estructura monoclínica) y fase T (estructura ortorrómbica) [10]; especialmente en la estructura ortorrómbica, presenta gran absorción de energía en la región del ultravioleta, así que puede ser utilizado en la protección de materiales sensibles a esta radiación. Así, el interés de sintetizar el Nb2O5 radica en que se espera poder estudiar como fotocatalizador en la degradación de pesticidas presentes en el agua, ya que presenta buena respuesta a la fotodegradación de moléculas con grupos fenólicos y el proceso no implica la presencia de reductos adicionales que finalmente actuarían como contaminantes en éste estudio. [11-14].
El polvo cerámico del pentóxido de niobio se puede obtener por diferentes métodos de crecimiento de materiales, entre ellos están: el método de precursor polimérico (Pechini), procesamiento hidrotermal, precipitación controlada y sol-gel, entre otros. Para este estudio se ha elegido el método de precursor polimérico por ser un método accesible, económico y que permite obtener partículas nanométricas con alta pureza química. Además permite obtener una gran variedad de óxidos [15-16] con diferentes dopantes y polvos nanométricos cristalinos y homogéneos. La idea general del proceso es redistribuir los cationes atómicos a través de toda una estructura polimérica y su éxito depende del manejo adecuado de los parámetros de síntesis. En el método se forma un quelato entre los cationes metálicos, (en este caso niobio contenido en sales disueltas) en una solución acuosa con un ácido carboxílico, generalmente ácido cítrico. Al mezclar esta solución con un alcohol polihidroxilado, como el etilenglicol, bajo calentamiento y en agitación constante, se obtiene una solución líquida de color blanco; posteriormente el quelato se poliestérifica al ser sometido a una temperatura entre 300 y 400°C, formando una resina. La resina retiene la homogeneidad de los iones del sistema, a escala atómica, debido a su alta viscosidad. Al calcinar la resina a una temperatura relativamente baja, entre 500 y 650°C, se obtienen óxidos con partículas finas y de adecuada composición química, la cual ha sido controlada de manera precisa durante el proceso. Como etapas posteriores se incluyen otras calcinaciones, la maceración y tratamientos térmicos, encargados de eliminar material orgánico y de facilitar la obtención de mezclas de los óxidos de interés. [17,18].
En este trabajo se sintetizó Nb2O5, fase T (estructura ortorrómbica), utilizando el método Pechini. Se realiza una descripción del proceso de síntesis, garantizando así su control y posterior reproducibilidad. Utilizando técnicas de caracterización como Difracción de Rayos X (DRX), método de Brunnaner - Emmett - Teller (BET), espectroscopía Raman y Microscopía Electrónica de Barrido con Fuente de Emisión de Campo (MEB-FEG), se ha determinado la estructura de los polvos obtenidos, el área superficial específica, el volumen de poro, la respuesta vibracional de los óxidos obtenidos y su morfología. Posterior a este trabajo se espera poder analizar las variables de síntesis y procesamiento del Nb2O5 frente a la respuesta fotocatalítica de las nanopartículas.
2. Procedimiento experimental
2.1. Conformación de la resina
Para la formación del quelato se disuelven 2.0381 g de NbCl5 (Sigma-Aldrich 99%) en 30 ml de agua bajo agitación constante; por separado se disuelven 4.33686 g de ácido cítrico (Sigma-Aldrich 99.5%) en 130 ml de agua bajo agitación constante a 90°C durante media hora. Se mezclan las dos soluciones, con el NbCl5 totalmente solubilizado, manteniendo la temperatura a 90°C durante media hora. Para que se produzca la reacción de poliesterificación se adiciona 40% de etilenglicol (Merck 99.5%) en masa para 60% de ácido cítrico, es decir 2.59537 ml, dejando la solución a una temperatura de 90°C hasta que se reduce el volumen de agua, sin ningún precipitado. Se requiere que la solución que resulta del proceso anterior sea totalmente blanca, condición que indica una mezcla uniforme de los diferentes reactivos lo que favorece la formación del citrato; la temperatura debe permanecer uniforme a 90°C favoreciendo las reacciones de poliesterificación y posteriormente la conformación de la resina. Finalmente se deja enfriar la solución, a temperatura ambiente, hasta que se forma la resina.
2.2. Obtención de los polvos
Con el objetivo de extraer el mayor porcentaje de residuos de agua se realiza la precalcinación de la resina tratándola a una temperatura de 400°C (en un horno Barnstead Thermolyne Furnace - BTF 47900) durante 2 horas, obteniéndose un sólido negro, con gran contenido de carbono, que al macerar resulta en un polvo cerámico marrón oscuro. Los tratamientos térmicos finales se presentan en la Tabla 1.
2.3. Caracterización del Nb2O5
Los polvos sintetizados se caracterizaron con Difracción de Rayos X (DRX), utilizando el equipo Panalytical PW3373, radiación Ka del Cu l=1.540558 Å, con 45 kV y corriente de 40 mA, en el intervalo 2q entre 10° y 90° a una velocidad de barrido de 0.0263°/s. Para obtener medidas del área de superficie específica y de tamaño de poro se utiliza el método de Brunauer Emmett Teller - BET, empleando adsorción de Nitrógeno en un equipo Micromeritics ASAP 2020 a 77 K. Las medidas de dispersión Raman se realizaron usando un equipo monocromador triple Jobin-Yvon modelo T64000 con un detector CCD, empleando luz de longitud de onda 632 nm a temperatura ambiente. El análisis morfológico se realizó a través de un Microscopio Electrónico de Barrido con Fuente de Emisión de Campo (MEB-FEG) JOE modelo JSM 6701F. Esta es una técnica que viene siendo utilizada en el estudio de tamaño, forma y distribución de partículas por medio de la obtención de imágenes con alta resolución. Las muestras fueron preparadas por deposición de una fina capa de material en el porta muestras recubierto de una fina capa de tinta de carbono.
3. Resultados y discusión
3.1. Análisis estructural
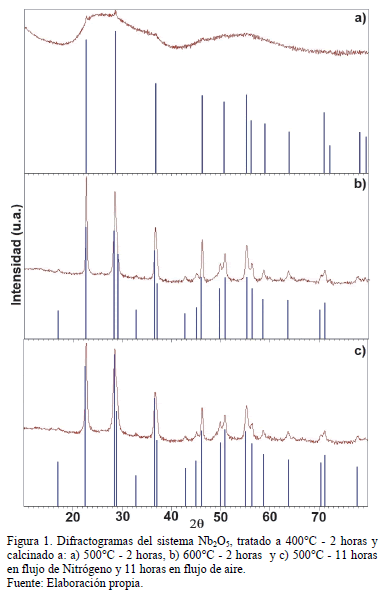
Los difractogramas de la Fig. 1 corresponden a los sólidos obtenidos por el método Pechini, sometidos a los tres tratamientos térmicos registrados en la Tabla 1; difractogramas previos indicaron que la muestra era aún amorfa a 400°C. El difractograma a), muestra 1, indica que a ésta temperatura el sólido presenta cristalización bajo la estructura hexagonal con picos resueltos en 2q = 22.6°, 2q = 28.5°, 2q = 36.7° y 2q =46.2°, lo cual está acorde con lo reportado en la base de datos (JCPDF07-0061). En el caso b), muestra 2, se encuentra que a ésta temperatura el sólido presenta una considerable cristalización en la fase T (ortorrómbica) con picos resueltos en 2q = 22.6°, 2q = 28.3°, 2q = 36.4°, 2q = 46°, 2q = 50.8°, 2q = 54.9°, 2q = 55.3°, 2q = 56.3° y 2q = 58.5°, acorde con lo reportado en la base de datos (JCPDF27-1313).
En el caso c), muestra 3, se evidencia la cristalización en la fase T (ortorrómbica) con picos resueltos en 2q = 22.6°, 2q = 28.4°, 2q = 36.6°, 2q = 46.1°, 2q = 50.8° y 2q = 55°, acorde con lo reportado en la base de datos (JCPDF30-0873). No se logra apreciar una considerable presencia de cloro, hecho que favorece el método de síntesis empleado. A pesar de haber logrado obtener la fase en el caso c) no se elige este proceso de calcinación debido a la complejidad que requiere en la adquisición de elementos adicionales como lo son los gases empleados. En cuanto a los compuestos orgánicos, se evidencia que retardan la fase de cristalización, razón por la cual se emplea una temperatura de 600°C, obteniéndose así en el caso b), muestra 2, las mejores condiciones térmicas de cristalización.
3.2. Análisis morfológico
En la Fig. 2 se observan las imágenes obtenidas con Microscopia Electrónica de Barrido con Fuente de Emisión de Campo (MEB-FEG) de las tres muestras antes analizadas por DRX. La barra guía en las tres muestras es de 100 nm. Analizando la imagen de la Fig. 2-a), se observa la presencia de aglomerados de nanopartículas sin una clara separación. Esto indica que el tratamiento térmico de 500°C por 2 horas no representa la mejor temperatura para obtener nanopartículas bien definidas en muestras empleadas en la degradación de pesticidas. En la Fig. 2-b), se observan nanopartículas bien definidas con un tamaño que oscila entre 50 nm y 90 nm; se presenta una distribución uniforme de las nanopartículas indicando que el tratamiento térmico a 600°C por 2 horas favorece la obtención del tamaño de partícula deseado. En la Fig. 2-c), se observa la muestra sometida a 500°C en flujo de nitrógeno durante11 horas y luego en flujo de aire 11 horas más. Como se aprecia este tratamiento además de costoso no favorece el crecimiento de nanopartículas; en esta imagen solamente se observan aglomerados del material sin ninguna nanopartícula definida.
Comparando las tres microscopias se comprueba que las condiciones que mejor favorecen el crecimiento de partículas son las correspondientes al tratamiento térmico desarrollado a 600°C por 2 horas.
3.3. Análisis superficial
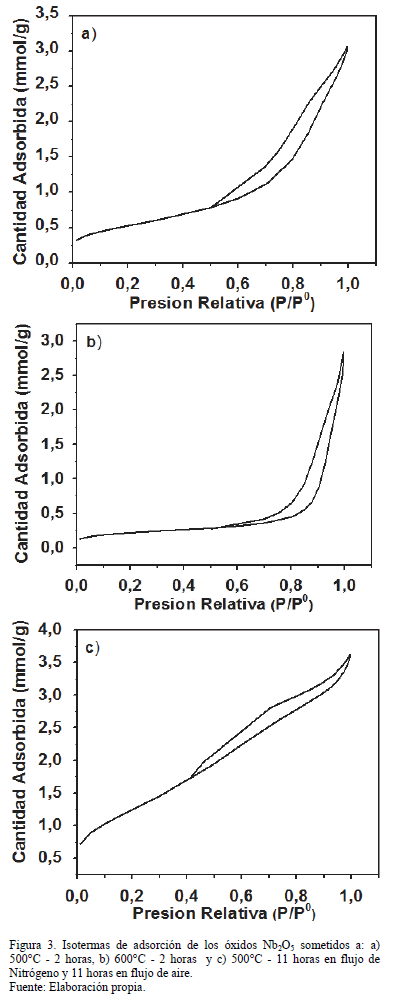
Se presentan las isotermas de adsorción en la Fig. 3, éstas tienen una forma tipo III (baja interacción adsorbato - adsorbente), asociada a sólidos que contienen poros muy grandes (macroporos). En los tres casos se distingue una histéresis a presiones parciales superiores a 0.4, debido a la presencia de mesoporosidad.
El análisis de fisisorción de N2 sobre las tres muestras del óxido semiconductor Nb2O5 revelo que el área superficial específica, SBET, disminuye al aumentar la temperatura de calcinación en procesos térmicos simples, Tabla 2; es posible obtener un valor mayor para esta variable si el proceso de calcinación se realiza bajo la presencia de gases, como en el caso de la muestra 3, proceso que se descarta ya que la idea de sintetizar este óxido es realizarlo bajo las condiciones más sencillas de reproducibilidad, favoreciendo así su posterior uso en aplicaciones catalíticas y finalmente su comercialización.
El óxido calcinado a 600°C presento un valor de SBET = 17m²/g, valor que a pesar de ser pequeño resulta ser útil para la acción catalítica. Debido a que la obtención de óxidos con mayor área superficial específica, diferentes al óxido comercial, mejora su actividad catalítica, por ejemplo en la remoción de cianuro libre [8], a futuro se espera que los óxidos preparados tengan un valor SBET mayor, lo cual puede alcanzarse haciendo el tamaño de partícula muy pequeño, formando así un gran número de poros a través de las partículas [19]. Finalmente se evidencia la obtención del óxido con mayor tamaño de poro, 235 Å para la muestra 2, valor que facilita la acción del óxido con moléculas grandes constituyentes de pesticidas y demás compuestos contaminantes. [20]
3.4. Análisis vibracional
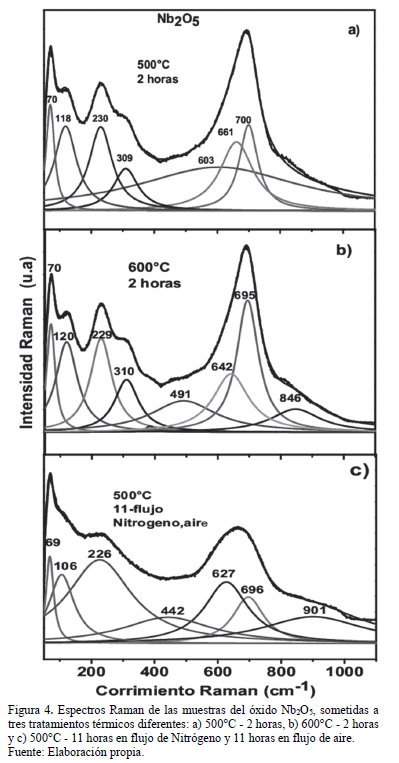
En la Fig. 4 se presentan los espectros Raman de los óxidos semiconductores Nb2O5 sometidos a diferentes tratamientos térmicos. Para el ajuste de los espectros micro Raman se usó del software comercial "Peakfit" una forma lorenzana y de esta forma se encontró la posición central de los diferentes modos vibracionales en el pentóxido de niobio.
En la Fig. 4-a) se observa el espectro para la muestra sometida a 500°C por dos horas; en este espectro tenemos cinco picos sobresalientes con posiciones en torno de 700cm-1, 210 cm-1, 230 cm-1, 118 cm-1 y 70 cm-1. También aparece otro pico de más baja intensidad en torno de 660 cm-1.
Los óxidos de niobio generalmente poseen una estructura octaédrica de coordinación NbO6 que es distorsionada en diferentes extensiones dependiendo si el poliedro posee la deformación en el vértice o en las aristas [21]. La estructura NbO4 es muy rara. Ocasionalmente, las estructuras NbO7 y NbO8 pueden ser encontradas en las fases de otros óxidos. Para el pentóxido de niobio amorfo, las unidades estructurales distorsionadas encontradas son los octaedros NbO6, el pentaedro NbO7 y el hexaedro NbO5 [22].
El espectro Raman del Nb2O5 generalmente presenta un pico entorno de 846 cm-1 hasta 900 cm-1 relacionado con la distorsión de los diferentes grados de los octaedros presentes en la estructura del Nb2O5. La región entre 800 cm-1 - 440 cm-1 se refiere a los estiramientos simétricos del poliedro de Nb2O5 y otros picos entre 360 cm-1 - 200 cm-1 son característicos de los modos de deformación angular de los enlaces Nb-O-Nb. Los picos entre 650 cm-1 - 700 cm-1 y 303 cm-1 son un indicativo de la fase ortorrómbica. Es de recordar también que las estructuras ortorrómbica y hexagonal del Nb2O5 tienen estructuras atómicas muy similares. En otras palabras, como se observa los modos Raman activos en las Fig. 4-a) y 4-b) están muy relacionados con la fase ortorrómbica. Es de resaltar que el espectro de la Fig. 4-b) presenta unos picos más estrechos lo que está bien relacionado con la formación de material cristalino en el crecimiento de la muestra.
En la Fig. 4-c) se presenta el espectro Raman para la muestra tratada a 500°C sometido a flujo de nitrógeno por 11 horas y a flujo de aire por 11 horas más. Se obtiene un espectro Raman con modos más anchos lo que indica una amorfización en el material. Esto nos lleva a pensar que la temperatura ideal de síntesis para las muestras en estas condiciones es de 600°C por dos horas.
Comparando los espectros Raman y las microscopias del material es evidente que hay una clara concordancia entre las bandas anchas de la muestra calcinada a 500°C en flujo de nitrógeno y aire. En las microscopias se puede distinguir la falta de partículas y la muestra se observa como un aglomerado de material. Caso contrario ocurre con la muestra sometida a 600°C por 2 horas. En ésta la formación de nanopartículas es clara y el espectro Raman presenta picos mucho más estrechos.
4. Conclusiones
El método Pechini ayuda a mejorar considerablemente las propiedades estructurales y fisicoquímicas del semiconductor estudiado en este trabajo, ya que se logró obtener el óxido semiconductor Nb2O5 en la fase ortorrómbica, estructura que fue corroborada mediante DRX y al ser analizada por MEB-FEG se verificó que las condiciones que mejor favorecen el crecimiento de partículas son las correspondientes al tratamiento térmico desarrollado a 600°C por 2 horas.
Con el fin de incrementar los valores de área superficial específica y volumen de poro se evidencia la necesidad de optimizar las condiciones de obtención del nanocompuesto; esto facilitaría la interacción del Nb2O5 con moléculas grandes de pesticidas y contaminantes presentes en el agua.
Los modos Raman activos de la muestra tratada a 600°C por dos horas están muy relacionados con la fase ortorrómbica, presentando picos más estrechos bien relacionados con la formación de material cristalino en el crecimiento de la muestra, por lo que se considera a esta temperatura como la ideal de síntesis para las muestras bajo estas condiciones.
Como etapa a seguir se espera poder comprobar que el óxido analizado exhibe un buen desempeño fotocatalítico en las reacciones de degradación de contaminantes orgánicos presentes comúnmente en el agua residual, como la atrazina y la rodamina.
A futuro se tiene la perspectiva de que éste estudio contribuirá en el proceso de manofactura y comercialización de nanocompuestos como este y/o similares.
5. Agradecimientos
Los autores agradecen al Grupo de Catálisis de la UPTC - Tunja; EMBRAPA - SC SP (Brasil); UNAL - Bogotá; UFPS - Cúcuta.
Referencias
[1] Hashemzadeh, F., Rahimi, R. and Gaffarinejad, A., Photocatalytic degradation of methylene blue and rhodamine B dyes by niobium oxide nanoparticles synthesized via hydrothermal method. International Journal of Applied Chemical Sciences Research, 1 (7), pp. 95-102, 2013. [ Links ]
[2] Saupe, G., Zhao, Y., Bang, J., Yesu, N., Carballo, G., Ordonez, R. and Bubphamala, T., Evaluation of a new porous titanium-niobium mixed oxide for photocatalytic water decontamination. Microchemical Journal, (81), pp. 156-162, 2005. http://dx.doi.org/10.1016/j.microc.2005.01.002 [ Links ]
[3] Juárez-Ramírez, I., Torres-Martínez, L.M., Cruz-López, A., Garza-Tovar, L.L. y Meza-de la Rosa, M.E., Nanopartículas semiconductoras: una alternativa para la degradación de contaminantes orgánicos presentes en agua residual y la generación de energía de manera sustentable., Ciencia UANL, 11 (4), pp. 411-422, 2008. [ Links ]
[4] Mahmoud, A.y Renato, S.F., Métodos emergentes para aumentar a eficiência do ozônio no tratamento de águas contaminadas. Química Nova, 30 (1), pp. 198-205, 2007. http://dx.doi.org/10.1590/S0100-40422007000100032 [ Links ]
[5] Fox, M.A. and Dulay, M.T., Heterogeneous photocatalysis. Chemical Reviews, 93 (1), pp. 341-357, 1993. http://dx.doi.org/10.1021/cr00017a016 [ Links ]
[6] Nieto, J., Caicedo, J., Amaya, C., Moreno, H., Aperador, W., Tirado, L. y Bejarano, G., Evaluación de la influencia del voltaje Bias sobre la resistencia a la corrosión de películas delgadas de Al-Nb-N. DYNA, 77 (162), pp. 161-168, 2010. [ Links ]
[7] Santana V.S. and Fernandes-Machado, N.R.C. Photocatalytic degradation of the vinasse under solar radiation. Catalysis Today, 133-135, pp. 606-610, 2008. http://dx.doi.org/10.1016/j.cattod.2007.12.131 [ Links ]
[8] Barbosa-López, A.L. y Castro-Sierra, I.M., Estudio catalítico comparativo de los sistemas TiO2 y Nb2O5.3H2O en la degradación de cianuro en función del tipo de oxidante. Ingeniería y Ciencia, 8 (16), pp. 257-280, 2012. [ Links ]
[9] Osathaphan, K., Chucherdwatanasak, B., Rachdawong, P. and Sharma, V. Photocatalytic oxidation of cyanide in aqueous titanium dioxide suspensions: Effect of ethylenediaminetetraacetate. Solar Energy, 82, pp. 1031-1036, 2008. http://dx.doi.org/10.1016/j.solener.2008.04.007 [ Links ]
[10] Kato, V.K. and Tamura, S., Die kristallstruktur von T- Nb2O5, Acta crystallographics B, 31 (3), pp. 673-677, 1975. [ Links ]
[11] Prado, A.G.S., Bolzon, L.B., Pedroso, C.P., Moura, A.O. and Costa, L.L., Nb2O5 as efficient and recyclable photocatalyst for indigo carmine degradation. Applied Catalysis B, 82, pp. 219-224, 2008. http://dx.doi.org/10.1016/j.apcatb.2008.01.024 [ Links ]
[12] Estéves, et al., New materials based on modified synthetic Nb2O5 as photocatalyst for oxidation of organic contaminants. Catalysis Communications, 10, pp. 330-332, 2008. http://dx.doi.org/10.1016/j.catcom.2008.09.012 [ Links ]
[13] Silva, M.K., Marques, R.G. Machado, N.R.C.F. and Santos O.A.A. Evaluation of Nb2O5 and Ag/Nb2O5 in the photocatalytic degradation of dyes from textile industries. Brazilian Journal of Chemical Engineering, 19 (4), pp. 359-363, 2002. http://dx.doi.org/10.1590/S0104-66322002000400001 [ Links ]
[14] Mills, A. and Le Hunte, S., An overview of semiconductor photocatalysis. Journal of Photochemistry and Photobiology A: Chemistry, 108, pp. 1-35, 1997. http://dx.doi.org/10.1016/S1010-6030(97)00118-4 [ Links ]
[15] Vargas, M.A., Franco, Y., Ochoa, Y., Ortegón, Y. y Rodríguez-Páez, J.E. TiO2 sintetizado por el método de precursor polimérico (Pechini): Estructura de la resina intermedia. Boletín de la Sociedad Española de Cerámica y Vidrio, 50 (5), pp. 267-272, 2011. http://dx.doi.org/10.3989/cyv.352011 [ Links ]
[16] Montenegro, A., Ponce, M., Castro, M.S. yand Rodríguez-Páez, J.E., Uso de métodos químicos en la obtención de SnO2 empleado como sensor de gases. Revista de la Academia Colombiana de Ciencias Exactas, Físicas y Naturales, 31 (120), pp. 405-413, 2007. [ Links ]
[17] Briceño, S.V., Bolaños, G. y Rodríguez Páez J.E. La0.5Ca0.5MnO3 obtenida por el método Pechini. Suplemento de la Revista Latinoamericana de Metalurgia y Materiales, (2), pp. 469-476, 2009. [ Links ]
[18] Lugo, G.C.A., Garcia, M.E.J., Rondón, C.J.J., Melendez, Q.H.J., Pérez, D.P.A. y Del Castillo, H., Preparación y caracterización de óxidos mixtos nanoestructurados soportados sobre MgO. Avances en Química, 5 (1), pp. 37-44, 2010. [ Links ]
[19] Coria, I.D., Variación de las propiedades superficiales a altas temperaturas en óxidos de metales de transición soportados en alúmina, para su utilización en reacciones catalíticas que involucren adsorción de gases. Invenio, 14 (26), pp. 141-154, 2011. [ Links ]
[20] Torres-Martínez, L.M., Juárez-Ramírez, I. y García-Montelongo X.L., Semiconductores tipo perovskita en procesos fotoinducidos para la purificación del agua. Ingenierías, 13 (49), 2010. [ Links ]
[21] Palatnikov, M., Shcherbina, O., Sidorov, N. and Bormanis, K., The structure of niobium and tantalum oxides processed by concentrated light flux. Ukrainian Journal of Physical Optics, 13 (4), 2012. http://dx.doi.org/10.3116/16091833/13/4/207/2012 [ Links ]
[22] Arsova, I., Prusi, A., Grev T. and Arsov, L., Electrochemical characterization of the passive films formed on niobium surfaces in H2SO4 solutions. Journal of the Serbian Chemical Society, 71, pp. 177-187, 2006. http://dx.doi.org/10.2298/JSC0602177A [ Links ]
A.M. Raba-Páez, recibió su título de Físico en 2006 de la Universidad Pedagógica Tecnológica de Colombia, Colombia y su título de MSc. en Ciencias-Física en 2011 de la Universidad Nacional de Colombia. Ha sido profesora de la Universidad Pedagógica Tecnológica de Colombia. Actualmente es profesora de la Universidad Francisco de Paula Santander. Sus áreas de investigación comprenden la síntesis y caracterización de óxidos semiconductores.
D.N. Suárez-Ballesteros, recibió su título de Químico de Alimentos en 2011 y su título de MSc. en Ciencias-Química en 2013, ambos de la Universidad Pedagógica Tecnológica de Colombia. Sus áreas de investigación comprenden la síntesis y caracterización de catalizadores mesoporosos y catálisis heterogénea.
J.J. Martínez-Zambrano, recibió su título de Químico de Alimentos en 2000 de la Universidad Pedagógica Tecnológica de Colombia; su MSc. en 2007 y Dr. en Ciencias-Química en 2013 todos de la Universidad Nacional de Colombia. Ha sido profesor de la Universidad Pedagógica Tecnológica de Colombia. Sus áreas de investigación comprenden la síntesis y caracterización de óxidos semiconductores.
H.A. Rojas-Sarmiento, recibió su título de Licenciado en Química y Biología en 1981 y de Esp. en Bioquímica en 1998, ambos de la Universidad Pedagógica Tecnológica de Colombia; su MSc. en Ciencias Químicas la recibió en 1987 de la Universidad Autónoma Metropolitana, México y su Dr. en Ciencias Químicas en 2003 de la Universidad de Concepción, Chile. Ha sido profesor invitado en las Universidades de Cartagena, Nacional de Colombia y Nacional Autónoma de México. Actualmente es profesor de la Universidad Pedagógica y Tecnológica de Colombia. Sus áreas de investigación comprenden la catálisis heterogénea, por metales y óxidos metálicos y materiales.
M. Rincón-Joya, recibió su título de Licenciado en Física y Matemáticas en 1998 y de Esp. en Física en 2001, ambos de la Universidad Pedagógica Tecnológica de Colombia; su MSc. en Física en 2004 y su Dr. en Física en 2008 ambos de la Universidad Federal de Sao Carlos, Brasil; realizo un PhD. en 2009 en la Universidad Estatal Paulista, Brasil. Es profesora del Departamento de Física de la Universidad Nacional de Colombia. Sus áreas de investigación comprenden propiedades ópticas de materiales y caracterización de materiales.