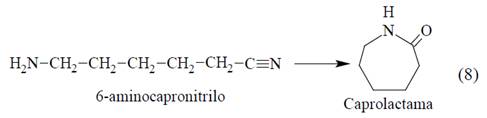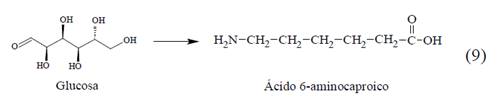1. Introducción
La caprolactama (CPL) es un compuesto orgánico utilizado principalmente para la producción de Nylon 6, tiene un precio cercano a los 1800 USD/t, una demanda de 6500 ktpa y perspectivas de crecimiento de alrededor del 3.0% anual. La CPL es derivada del benceno, siendo el 83 % producido a través del ciclohexano, el 16% del fenol y el resto del tolueno y de polímero reciclado. El proceso de producción dominante de CPL no es sostenible a largo plazo y es dependiente del petróleo. Se basa en la conversión de la ciclohexanona a ciclohexanona oxima. Esta reacción ocurre típicamente en presencia de sulfato de hidroxilamina, bajo condiciones búfer de pH. La oxima es convertida en CPL por medio de la reacción de rearreglo de Beckmann en presencia de ácido sulfúrico fumante. A escala comercial, la separación de la CPL se realiza por la adición de NH3 con un rendimiento del 98%. Este último paso requiere de solventes orgánicos para la purificación y genera como subproducto entre 1.8 y 5.0 kg de sulfato de amonio por cada kilogramo de CPL producida [1].
Se han realizado esfuerzos para reducir la formación de sulfato de amonio [2,3], entre los que resaltan la ruta Montedison, una alternativa de oxidación de la ciclohexanona usando NH3 y un catalizador de TiO2 y SiO2. Otras alternativas son los procesos de DSM/Stamicarbon y su arreglo de Beckmann catalizado; el de Bayer, con un catalizador de B2O3 y Al2O3; el proceso BASF/Inventa, donde la ciclohexanona oxima se forma por una hidrogenación catalítica de óxido nítrico en una solución de sulfonato de amonio seguida por una reacción con ciclohexanona. También se tienen el proceso HPO (hidroxilamina - fosfato - oxima) desarrollado por DSM, la Nitración Fotoquímica de Ciclohexano (PNC) de Toray, el proceso SNIA, entre otros [4]. Sin embargo, sólo la ruta Sumitomo ha probado ser comercialmente competitiva. Esta ruta produce ciclohexanona oxima por una amoximación directa del NH3 y el H2O2 usando un catalizador TS-1 [5]. El uso subsecuente de un catalizador MFI produce CPL, mientras elimina la formación de sulfato de amonio [6].
2. Rutas renovables para la producción de CPL
Aunque no existen actualmente métodos comerciales para la síntesis biobasada directa de la CPL, la combinación de la producción biotecnológica de materias primas básicas o plataformas con subsecuentes modificaciones por procesos físicos y químicos están emergiendo y mostrando resultados prometedores [7]. Estos procesos deben a su vez optimizarse a manera de biorrefinerías para lograr una real viabilidad. Las siguientes son las rutas de producción de CPL a partir de diferentes compuestos intermedios que pueden ser producidos a partir de materias primas renovables.
2.1. Síntesis de CPL por la vía de la Lisina (LYS)
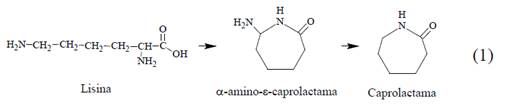
La LYS se produce a escala industrial por fermentación usando Corynebacterium glutamicum, con un rendimiento estimado del 40-50%mol. La investigación para mejorar su producción se centra en el desarrollo de nuevas cepas de bacterias más eficientes. La LYS se puede utilizar como materia prima para la síntesis de CPL debido a su estructura similar. Su modificación química muestra un rendimiento del 75% global. Sin embargo, los altos precios de la LYS limitan la aplicación comercial [1]. La tecnología Draths convierte la glucosa en LYS, luego en aminocaprolactama y finalmente en CPL, con un rendimiento del 60% mol/mol de CPL sublimada a partir de LYS. Draths Corporation fue fundada en diciembre de 2005 para comercializar la tecnología desarrollada en el laboratorio de John Frost y Karen Draths. En 2011 Draths fue comprado por Amyris [8], quienes reportaron la conversión de la LYS a α-amino-ϵ-caprolactama en reflujo con 1,2-propanodiol logrando un 96% de rendimiento. La deaminación siguiente se realiza a -5°C, en presencia de KOH y ácido hidroxilamina-O-sulfónico, con formación de N2 y K2SO4 (Ec.1). La CPL es purificada por sublimación con un rendimiento del 75% [9].
2.2. Síntesis de CPL a partir de Butadieno (BD)
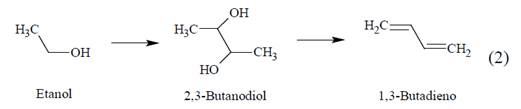
Una ruta convencional para la síntesis de CPL que puede convertirse a biobasada utiliza el BD como materia prima, su reacción con cianuro de hidrógeno produce adiponitrilo y a partir de este proceso se pueden obtener tanto hexametilendiamina, como CPL. Por otra parte, el BD se puede convertir en ácido 6-aminocapróico y posteriormente en CPL en un proceso de varios pasos. Los rendimientos son bajos (34% global), sin embargo, la conversión subsiguiente del 6-ACA a CPL ha demostrado ser eficiente (rendimiento del 95%). El BD puede ser producido a partir de bioetanol, con un rendimiento del 87% (Ec.2) [1].
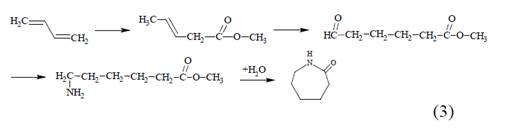
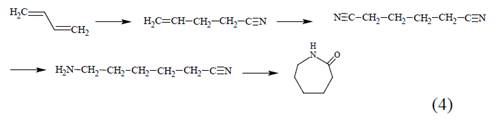
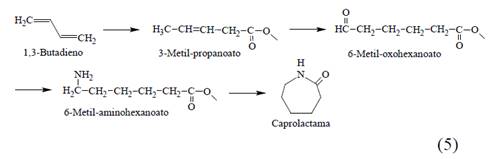
Otro proceso de síntesis de CPL a partir de BD es el de hidroesterificación, desarrollado por BASF [10] y DSM/DuPont [11,12] (Ec.3). Otro proceso similar, implica la hidrocianación como paso clave (Ec.4). El proceso ALTAM de DSM (ALTternativa caprolactAMa) consiste en la carbonilación del BD para obtener 3-metil-pentanoato (Ec.5); su posterior hidroformilación y aminación produce 6-aminocaproato, un precursor de la CPL [13], sin embargo, se han dado a conocer pocos detalles. Estos procesos no se han implementado porque son más costosos que las rutas basadas en benceno.
La dimerización del bioetanol provee una ruta prometedora al BD. Actualmente, se aplican dos métodos biobasados a nivel comercial. El primero, el proceso Lebedev, operado en Brasil y Polonia, usando un catalizador de MgO y SiO2 a 370-390°C para deshidrogenar y dimerizar el bioetanol, dando 70% de selectividad para el BD. El segundo es el proceso Ostromislensky que usa bioetanol, bioacetaldehído y un catalizador, también con rendimientos del 70% para el BD [4]. Una ruta alternativa es la de Ohnishi y otros, esta ruta usa un catalizador de MgO y SiO2 (1:1) y Na2O (0.1%) a 350°C, dando BD con un rendimiento del 87% [14,15].
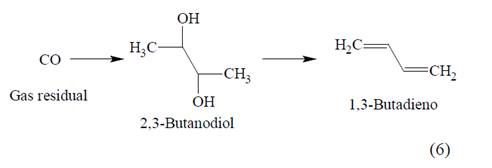
Por otra parte, es posible obtener BD a partir de monóxido de carbono (Ec.6) [16]. Múltiples colaboraciones de empresas biotecnológicas y químicas están combinando ingeniería genética y la tecnología de fermentación con experiencia en catálisis y la ingeniería de procesos. Ejemplos de tales asociaciones son Genomatica y Versalis [17], Global Bioenergies y Synthos [18] e Invista y LanzaTech [19].
Varias empresas han reportado la producción directa de BD a partir de fuentes renovables, entre ellas están Genomatica, Global Bioenergies y Cobalt Technologies [20-23]. Otro interesado es Invista, asociado con Arzeda y colaborando con el Centro para la Innovación de Procesos del Reino Unido para desarrollar una producción directa de BD a partir de la fermentación de gases de síntesis; además de trabajar con LanzaTech para utilizar la fermentación sintética a 2,3-butanodiol con conversión catalítica adicional a BD [24,25]. Finalmente, Michelin tiene un proyecto de producción de BD biobasado llamado "BioButterfly", en conjunto con Axens, IFP Energies Nouvelles y Tereos [26-28].
2.3. Producción de CPL utilizando Adiponitrilo (ADN)
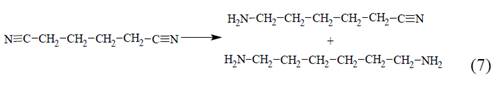
Este proceso fue desarrollado por BASF (en colaboración con DuPont) y Rhodia. El ADN se hidrogena para dar una mezcla de 6-aminocapronitrilo y hexametilendiamina (Ec.7).
El 6-aminocapronitrilo puede usarse para producir CPL mientras que la hexametilendiamina es un precursor para el nylon 6,6 mediante la reacción con ácido adípico. Aunque este proceso ofrece flexibilidad, no se ha implementado debido a los altos costos en comparación con las rutas basadas en el benceno [1]. El proceso depende de una recirculación del ADN para conseguir una conversión completa, con 70% de conversión de ADN por ciclo.
La hidrólisis catalítica consecutiva de 6-aminocapronitrilo produce 79% de CPL (Ec.8), en presencia de agua y etanol, a 70 bar y 220°C [29].
2.4. Síntesis de CPL por la vía del ácido 6-aminocapróico (6-ACA)
La producción biotecnológica directa del 6-ACA ha ganado interés recientemente (Ec.9). Compañías como DSM [30], Genomatica [31], y Celexion LLC [32], reclaman cada una de estas rutas de síntesis, sin embargo, ninguna detalla el proceso. A diferencia del ácido adípico y del ácido succínico, el 6-ACA es un aminoácido no natural, que puede ser potencialmente producido en un proceso de pH neutro, similar a fermentaciones industriales de aminoácidos por bacterias. Escherichia coli mostró mejor tolerancia al 6-ACA en comparación con Bacillus subtilis y Saccharomyces cerevisiae [33]. Zhou et al. demuestran, mediante un diseño experimental y una aproximación estadística, que la eficiencia de la producción de 6-ACA por las cepas de E. Coli es resultado de la covariación entre la regulación génica de diferentes enzimas involucradas y los componentes del medio de cultivo [62]. El 6-ACA producido por fermentación necesita ser ciclado primero a CPL antes de la polimerización. Esta ciclación puede llevarse a cabo directamente usando un caldo de fermentación pretratado, sin necesidad de purificación previa del 6-ACA, como se describe en la patente de Guit [34]. Puede conseguirse una purificación adicional de la CPL mediante destilación [35].
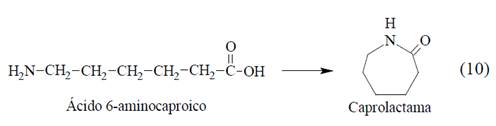
El 6-ACA se puede convertir en CPL en ausencia de un catalizador, como lo demostró BASF [36] y DSM [37]. Una reacción por lotes, utilizando vapor de agua sobrecalentado, generó el 99% de rendimiento. Un proceso continuo en condiciones similares generó el 95% de rendimiento de CPL (Ec.10).
Genomatica prepara 6-ACA a partir del ácido 5-formilvalérico usando un biocatalizador [38] y también tiene una patente donde describe cómo producir una versión de los compuestos intermedios claves usados para la producción de nylon, entre ellos, el 6-ACA, a partir de materias primas renovables como los carbohidratos comercialmente disponibles [39]. Por otro lado, DSM ha demostrado a nivel de laboratorio dos vías sintéticas para la producción fermentativa de 6-ACA mediante ensayos enzimáticos in vitro con un conjunto de proteínas seleccionadas expresadas en la E. coli [33]. Por otra parte, tiene una patente para la transformación del 6-ACA a CPL [40].
2.5. El ácido adípico (ADA) para la producción de CPL
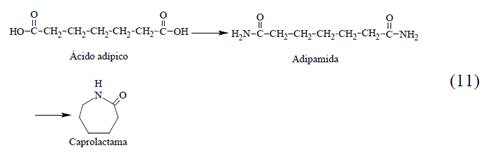
Otra ruta emergente para la producción de CPL, es la del ADA. Recientemente, Coudray y colaboradores demostraron la conversión directa en un solo recipiente del ADA a CPL con un rendimiento del 64% (Ec.11) [41].
El ADA puede convertirse en ADN que a su vez puede convertirse en CPL. En la actualidad, el BD se utiliza para producir ADN, ya que es más económico, sin embargo, el aumento de los precios del BD butadieno han obligado a los participantes del mercado a revisar la ruta de ADA biobasado [42]. Entre las empresas que trabajan para desarrollar el ADA biobasado están DSM, BioAmber, Rennovia, Genomatica, Verdezyne y Biochemtex [43,44]. El proceso de Rennovia, que utiliza la oxidación del aire para convertir la glucosa en ácido glucárico, seguido por la hidrodesoxigenación para convertir el ácido glucárico en ADA, tiene un alto potencial para ser competitivo en costos con el proceso convencional DuPont/Invista de oxidación de ciclohexano, al igual que el proceso de Verdezyne, que utiliza enzimas modificadas genéticamente para fermentar la glucosa a ADA. La ventaja de ambas rutas biológicas es el uso de glucosa como materia prima, en comparación con el proceso convencional que utiliza ciclohexano con un precio mayor en el mercado. Sin embargo, desafíos significativos afectan a estos procesos alternativos como la alta carga, selectividad y productividad del catalizador (en el caso de Rennovia), y la alta tasa de rotación enzimática y cinética satisfactoria para la ruta de fermentación enzimática de Verdezyne [45].
2.5.1. Ruta del Ácido cis,cis-mucónico (MA) para la producción de ADA
La conversión del MA en ADA proporciona un rendimiento del 97%. Sin embargo, la producción del MA a partir de glucosa tiene un bajo rendimiento (24%), combinado con dificultades en su purificación. Por otra parte, convertir el MA directamente en CPL es otra ruta reciente. Se han obtenido rendimientos del 55% y es probable que mejoren rápidamente. Sin embargo, la producción biotecnológica del MA todavía tiene un bajo rendimiento y altos costos de procesamiento [46].
2.5.2. Producción de ADA a partir de Ácido Levulínico (LA)
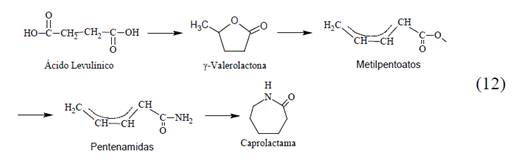
La producción de ADA a través del LA y γ-valerolactona (GVL) da un rendimiento teórico global del 34%, en cuatro pasos. Sin embargo, el bagazo o residuos de alimentos se pueden usar como la materia prima de fermentación para producir el LA con un rendimiento del 83%. Raoufmoghaddam estudia una ruta catalizada desde el LA a la CPL (Ec.12). La transformación de LA en GVL mediante una reacción de hidrogenación tiene un rendimiento alto (>95%). La ruta propuesta procede a través de la destilación reactiva catalizada por ácido de GVL con metanol a una mezcla de metil pentenoatos isoméricos (MP), reacción de MP con amoníaco a las correspondientes pentenamidas, que finalmente se convierten en CPL a través de una reacción de hidroamidometilación intramolecular catalizada con rodio [47].
2.5.3. El Ácido Succínico (SA) para la producción de ADA
La ruta de SA a ADA a través del 1,4-butanodiol (BDO) muestra un 66% de rendimiento teórico, en dos pasos. Del mismo modo, residuos de panadería pueden ser usados como la materia prima de la fermentación para el SA, con un 35% de rendimiento global. Además, se espera que los precios del LA y SA caigan radicalmente a medida que mejoren sus métodos biotecnológicos de producción [1].
2.5.4. Síntesis de ADA a partir de 5-hidroximetilfurfural (HMF)
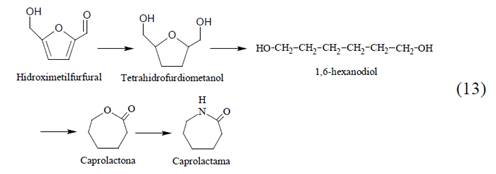
La ruta del HMF al ADA ha sido muy investigada. A partir de fructosa se tiene un rendimiento teórico de ADA hasta del 78%. Sin embargo, estas son materias primas costosas y el margen económico hacia el ADA es pequeño. El HMF obtenido partir de materias primas más baratas proporcionaría márgenes económicos más grandes, promoviendo su viabilidad. Por otro lado, Teddy estudia la conversión catalizada del HMF al 1,6-hexanodiol a través del Tetrahidrofurdiometanol (THFDM), convirtiéndolo luego a caprolactona y finalmente a CPL (Ec.13) [48].
2.5.5. Semialdehído Adípico (SAA) como precursor de ADA
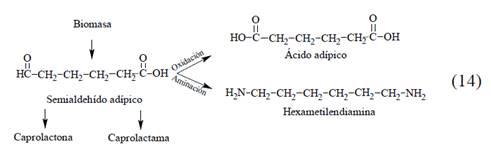
La ruta del SAA es otra combinación de biotecnología y catálisis química. Sin embargo, esta ruta se encuentra en fase inicial. Recientemente, la empresa BioAmber, un pionero en la producción de SA de base biológica, compró la licencia de la ruta de síntesis de Celexion [49] para explorar vías biotecnológicas para producir SAA [50], además, tiene una patente sobre la producción de SAA y otros compuestos orgánicos a partir de microorganismos recombinantes [51]. Este compuesto se puede utilizar como material de partida para producir caprolactona, CPL y HMDA (Ec.14). Por otra parte, su oxidación puede proporcionar una ruta atractiva para ADA [49,50]. Invista también cuenta con una patente sobre la producción de SAA a partir de microorganismos [52].
2.5.6. Reducción de Ácido Glucárico (GA) para la producción de ADA
Un ejemplo prometedor es la oxidación selectiva de la glucosa a GA (66% de rendimiento) y su posterior reducción a ADA (89% de rendimiento). El rendimiento global teórico es del 59%, sin embargo, la desactivación del catalizador es un problema. Un proceso combinado estable y eficiente abriría un camino viable a una ruta del ADA. Rennovia utiliza un proceso químico catalítico patentado para producir ADA, usando glucosa como materia prima. El proceso utiliza catálisis heterogénea, que primero produce ácido glucárico a través de una oxidación aeróbica de glucosa seguida de hidrogenación catalítica a ADA [53,54].
2.5.7. Ruta de la Adipamida
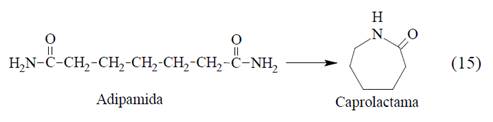
También se observa la valorización de la adipamida, un subproducto común en las reacciones del MA y en la síntesis de CPL. El rendimiento máximo conseguido hasta ahora para la conversión de adipamida a CPL es sólo del 35%. La adipamida se puede obtener del adiponitrilo o a través de la amidificación del ADA. Para convertir directamente adipamida a CPL, Frost y colaboradores utilizan un catalizador 8.6% Pd/Davisil 635 (mol 5.6%) en diglima, a 250 °C (Ec.15) [41].
2.6. Benceno
La producción de BTX (Benceno, Tolueno, Xileno) a partir de biomasa es un enfoque relativamente nuevo, el proceso aún no es comercial, sin embargo, tiene el potencial para serlo. Utilizando biomasa lignocelulósica como materia prima alcanza rendimientos alrededor del 15% [55]. El proceso BioForming® de Virent convierte materias primas derivadas de plantas en un producto BioFormate® que es análogo al reformado del petróleo. Usando procesamiento convencional de aromáticos, Virent ha producido paraxileno renovable, xilenos mixtos, tolueno, benceno y Aromático 100 [56,57]. Por otro lado, Anelloteh, ha desarrollado un proceso de pirolisis catalítica rápida (CFP) en un reactor de lecho fluidizado para la conversión de biomasa no alimentaria en BTX. El producto de salida del reactor requiere solo un hidrotratamiento suave para eliminar las impurezas de trazas utilizando la tecnología de refinado de petróleo existente [58,59].
2.7. Fenol
La producción renovable del fenol se ha enfocado a través de la pirolisis o despolimerización térmica de biomasa lignocelulósica en ausencia de oxígeno añadido, proceso en el que se produce un bioaceite. El espectro de productos obtenidos de este proceso depende de las condiciones de temperatura, presión y tiempo de residencia de los vapores liberados de la pirólisis. Los principales compuestos de valor obtenidos en este proceso son fenoles, ácidos orgánicos, furfural, HMF y levoglucosano. La base para la producción del fenol y los otros compuestos de valor, es el fraccionamiento o separación del bioaceite en varias calidades de aceites y su refinamiento hasta los compuestos finales puros [44,60].
También se ha demostrado la producción del fenol a partir de glucosa, usando tirosina como precursor y con una cepa tolerante a solventes como la Pseudomonas putida S12. Esta cepa produce entre 0.14 y 0.47 g/L de fenol, con un rendimiento 3.5 g/g glucosa en 24 h, incrementándose a 5.5 g/L al extraerse con octanol. Por esta vía, el mantenimiento de la biomasa bacteriana durante períodos prolongados es un factor crítico, así como el mejoramiento de las condiciones óptimas de cultivo que determinan la eficiencia de la ruta metabólica [61].
3. Conclusiones
A pesar de encontrar muchas alternativas para la producción biobasada de CPL, este no es un tema que aparezca frecuentemente en la literatura científica; debido a que la CPL no es uno de los focos de investigación de la biotecnología mundial. Sin embargo, si se logra su producción con éxito mediante la fermentación, puede entrar en la producción industrial muy rápidamente, lo que conduciría a importantes cambios en la industria del nylon y la cadena de suministro de poliamidas. Aunque cada una de las rutas de síntesis planteadas tiene elementos a favor y en contra, la ruta a través de la LYS es la más referenciada en la literatura ya que es la ruta que se observa más prometedora al involucrar pocas etapas de reacción, tener la posibilidad de partir de materias primas económicas y llevarse a cabo bajo condiciones de operación moderadas, que, si se logran mejorar los rendimientos, conduciría a un proceso económicamente viable y de rápida implementación.
En Colombia no se identificaron esfuerzos importantes de investigación y desarrollo de ninguno de los procesos presentados, a pesar de su potencial por la abundancia de materias primas renovables. Sin embargo, la biotecnología debe ser considerada como un sector clave sobre el cual se sustente el avance de la sociedad colombiana y mundial, y debe contribuir a su desarrollo económico, competitividad y calidad de vida. En consecuencia, la Administración Pública, desde su responsabilidad y competencia, debe poner todos los instrumentos a su alcance para permitir, facilitar y promover el adecuado desarrollo de la biotecnología, con actuaciones en diversos ámbitos, entre los que se incluyen la regulación normativa y legislativa, la financiación, la educación y la divulgación.