Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Ciencias Químico - Farmacéuticas
Print version ISSN 0034-7418On-line version ISSN 1909-6356
Rev. colomb. cienc. quim. farm. vol.35 no.2 Bogotá July/Dec. 2006
Artículo de investigación
Estandarización de un modelo basado en monocapas de células Caco-2 con aplicación en estudios de absorción de fármacos
Standardization of a model based on Caco-2 cell monolayers with application on in vitro drug absorption tests
Rocío Castillo, Carlos Chiriboga1 y Marta R. Fontanilla2
1Instituto de Biología Molecular, Universidad El Bosque, Bogotá D. C., Colombia.
2 Departamento de Farmacia, Facultad de Ciencias, Universidad Nacional de Colombia, A. A. 14490, Bogotá D.C., Colombia.
E-mail: mrfontanillad@unal.edu.co
Recibido para evaluación: agosto 15 de 2006 Aceptado para publicación: noviembre 20 de 2006
RESUMEN
La biodisponibilidad de los fármacos administrados oralmente depende de su absorción y de su metabolismo. Entre los factores que determinan la absorción de un compuesto se encuentran la permeabilidad y las características de su transporte a través de la mucosa intestinal. La entidad encargada de la administración de alimentos y drogas norteamericana (Food and Drug Administration / FDA) reconoce que la determinación in vitro de la permeabilidad usando modelos basados en monocapas de células Caco-2 puede ayudar a predecir la absorción in vivo de un fármaco. A pesar de su utilidad, en Colombia no se ha reportado la utilización de este modelo en los análisis de clasificación biofarmacéutica y de predicción de la biodisponibilidad oral. El objetivo de este trabajo fue estandarizar un modelo para el estudio de absorción basado en células Caco-2. Los coeficientes unidireccionales de permeabilidad aparente (Papp) de ranitidina y teofilina fueron establecidos en monocapas celulares en dirección apical-basolateral. Las muestras provenientes de la cámara basolateral fueron analizadas mediante cromatografía líquida de alta eficiencia y los valores de Papp calculados con las concentraciones halladas. Los coeficientes de variación intra e interdías encontrados permitieron establecer la precisión del sistema estandarizado. Con los valores de Papp obtenidos, se hizo la asignación de los compuestos a la clase de permeabilidad que concuerda con la reportada para cada uno. Para que el modelo sea utilizado en la determinación de permeabilidad de compuestos de interés, es necesaria su validación con moléculas de referencia.
Palabras clave: Absorción de fármacos, monocapas celulares, permeabilidad, células. Caco-2.
SUMMARY
The bioavailability of orally administered drugs depends mainly on their transport through the intestinal mucosa. Epithelial cell line cultures have been used as models to asses the intestinal absorption of a drug in vitro. The United States Food and Drug Administration (FDA) acknowledges the epithelial Caco-2 system as part of the in vitro tests used to establish a drug’s bioequivalence. Despite the usefulness of this model, in Colombia it has not been applied to predict oral absorption and the biopharmaceutical classification. In the present work the Caco-2 monolayer unidirectional apparent permeability coefficients (Papp) for ranitidine and theophyline were established. Samples from basolateral and apical chambers were analysed by High Performance Liquid Chromatography (HPLC) and Papp values were calculated based on the concentrations found. The accuracy of this system’s measurements was evaluated intra and inter-day experiments. Ranitidine and theophyline Papp values found allowed the correct assignment of these compounds class permeability. Permeability tests of reference compounds are still required to validate this model.
Key words: Drug absorption, monolayers, permeability, Caco-2 cells.
INTRODUCCIÓN
El desarrollo de moléculas candidatas a fármacos requiere la realización de estudios predictivos de su absorción oral con el fin de evidenciar los problemas de biodisponibilidad que se pueden presentar cuando son administrados por vía oral (1, 2). La permeabilidad de los fármacos a través de la membrana intestinal es el factor más importante en el momento de su clasificación biofarmacéutica, debido a que directamente se relaciona con el proceso de absorción oral (3-5). Se han desarrollado diferentes métodos experimentales para determinar la permeabilidad intestinal de los fármacos (in vivo, in situ e in vitro) con el objetivo fundamental de predecir absorción y definir el mecanismo involucrado en dicho proceso (1, 6 - 7). El fin de estas pruebas es establecer el Coeficiente de Permeabilidad (P) de un fármaco con base en un modelo matemático que relaciona el proceso de permeabilidad con el paso a través de la superficie intestinal (1, 8). El coeficiente de permeabilidad calculado in vitro a partir de medir en una cámara receptora la concentración de un compuesto, que ha pasado de una cámara dadora a través de monocapas celulares, se denomina coeficiente de permeabilidad aparente (Papp) (8-10). Los modelos celulares utilizados para determinar Papp se basan en líneas celulares que al ser cultivadas sobre filtros semipermeables forman monocapas con características que semejan las de la mucosa intestinal, las cuales permiten la cuantificación de Papp en dirección apical-basolateral o viceversa (2, 11). La línea celular Caco-2, inicialmente aislada de carcinoma de colon, es la más empleada en las determinaciones de Papp (12-14). Este modelo aparece en la lista de métodos aceptados por la Food and Drug Administration de Estados Unidos (FDA) para determinar la clase de permeabilidad de un fármaco y predecir su absorción (15).
En Colombia los estudios de absorción de fármacos en desarrollo se llevan a cabo in situ mediante técnicas in vivo y ex vivo con animales de experimentación. En la literatura nacional revisada no encontramos referencias sobre el uso de las monocapas de células Caco-2 para evaluar in vitro la absorción de un fármaco mediante la determinación de su Papp. La regulación colombiana, a través del Decreto 677 del 26 de abril de 1995 del cual se derivaron las resoluciones 1400 del 24 de agosto de 2001 y 1890 del 19 de noviembre del mismo año, establece como requisito para el registro sanitario de un medicamento, la presentación de los resultados de estudios de biodisponibilidad o bioequivalencia (16-18). Todo este proceso está en su fase de implementación y forma parte de la definición de una política farmacéutica nacional (19) acorde con la realidad del país. En este proceso se ha identificado la necesidad de superar limitaciones técnicas graves, como la poca oferta de centros acreditados para desarrollar pruebas de bioequivalencia in vivo o la ausencia de métodos in vitro, implementados siguiendo los nuevos preceptos sobre el Sistema de Clasificación Biofarmacéutica (BCS) y las pruebas de permeabilidad (20-21).
Este trabajo estandarizó un modelo para la determinación de la permeabilidad basado en monocapas de la línea celular Caco-2 y midió valores de permeabilidad de dos fármacos (ranitidina y teofilina) de baja y alta permeabilidad, respectivamente. Estos compuestos fueron escogidos debido a que su permeabilidad ya ha sido evaluada en monocapas de Caco-2 (5-7). En Colombia constituye el primer esfuerzo por implementar pruebas in vitro alternativas o complementarias de los estudios in vivo para el estudio de la absorción intestinal de los fármacos.
MATERIALES Y MÉTODOS
Estandarización del cultivo
En todos los ensayos, se utilizó medio de cultivo compuesto por una mezcla de las siguientes soluciones: penicilina-G/estreptomicina 1% (Invitrogen, Grand Island, N.Y), anfotericina B 1%, (Invitrogen, Grand Island, N.Y), suero bovino fetal (FBS, Invitrogen) 20% y medio Eagle Modificado por Dulbecco con alta concentración en glucosa (DMEM, Invitrogen, número de catálogo 12800017) a pH 7.4. El medio se esterilizó por filtración con membrana con tamaño de poro de 0.22 µm y se guardó a 4 ºC. La expansión de la población celular se realizó siguiendo las técnicas descritas por Yamashita y colaboradores (23-24). Para esto, las células Caco-2 (ATCC, American Type Culture Collection - Rockville, MD, número de Lote 3403757, pasaje N° 20) fueron sembradas a una densidad de 2x105 / mL medio en cajas T-25 (FalconÒ) e incubadas. Los cambios de medio fueron realizados cada tercer día durante el tiempo requerido por las células para alcanzar la confluencia celular.
Para obtener monocapas celulares confluentes, las células Caco-2 provenientes de cultivos confluentes realizados en cajas T-25 se sembraron en insertos de policarbonato (0.4 µm, Falcon) de la siguiente manera: los cultivos confluentes fueron digeridos con tripsina 0.25% - EDTA 0.025% y la suspensión celular obtenida se centrifugó a 2500 g durante 10 min, el precipitado obtenido fue lavado con solución tampón de fosfatos (PBS) y resuspendido en medio fresco. Una alícuota de esta suspensión se tiñó con eritrosina B (Sigma) para determinar el número de células viables. Densidades celulares entre 5 x 104células/cm2 y 60 x 104 células/cm2, con viabilidades mayores al 95%, fueron sembradas en los insertos de policarbonato con el fin de establecer la densidad de siembra requerida para obtener una monocapa celular uniforme en el menor tiempo. Cada tercer día se cambió el medio de cultivo, y a partir del cuarto día se registró diariamente el valor de la resistencia eléctrica transepitelial (TEER). Las células Caco-2 empleadas en la elaboración de la monocapa celular correspondían a los pasajes N° 22-23 del cultivo inicialmente adquirido en la ATCC.
Detección de fosfatasa alcalina
Se realizó la detección de fosfatasa alcalina como indicativo de la diferenciación celular de la monocapa obtenida, debido a que esta enzima se expresa en la cara apical de las células diferenciadas. Para este ensayo se desprendió la monocapa del inserto, se trasladó a una lámina portaobjetos, se adicionó glutaraldehído al 0.5% en PBS por 20 minutos para fijar las células. Luego se hicieron tres lavados con 1 mL de PBS y las células se tiñeron durante 30 minutos en la oscuridad, con una solución tampón (Tris, NaCl, MgCl2) conteniendo NBT (Nitroazul-tetrasodio, Sigma) y BCIP (5-Bromo-4-cloro-3-indocil-fosfato, Sigma) (1:5:94). Las células diferenciadas aparecieron teñidas de azul en el microscopio de luz visible.
Medición de la Resistencia Transepitelial (TEER)
La TEER ohmios.cm2 (Ω.cm2) generada por las capas de epitelio cultivado fue utilizada para evaluar la confluencia e integridad de la monocapa. Estas mediciones se realizaron empleando un voltímetro con electrodos conocido como el sistema Millicell®-ERS (Millipore, USA) siguiendo las recomendaciones del fabricante. Todos los valores, previamente corregidos por la resistencia del filtro y el medio, son reportados por diámetro efectivo de membrana.Determinación de la actividad transportadora
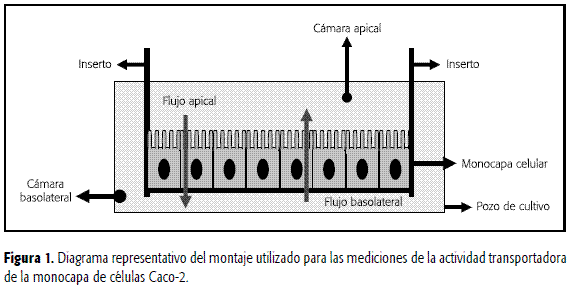
En todos los ensayos de permeabilidad se usaron los pasajes 21 a 23 de las células Caco-2. Para las determinaciones de la actividad transportadora se usaron monocapas con valores de TEER en el rango en que este parámetro se mantuvo constante en los experimentos de medición de resistencia transepitelial ya descritos. La actividad transportadora de la monocapa celular fue determinada en dirección apical-basolateral en función de la permeabilidad aparente exhibida por dos fármacos (ranitidina y teofilina) ya evaluados mediante el sistema de clasificación biofarmacéutica (6-7). En el establecimiento de la actividad transportadora del cultivo epitelial se siguió un procedimiento descrito para la medición de Papp (2, 23-24). Brevemente, se colocaron insertos (0,4µm de tamaño de poro y 1,13 cm2 de área superficial) sembrados con células Caco-2 en cajas de 24 pozos (Falcon), se adicionaron 0.5 mL de PBS en las cámaras apical y basolateral del inserto y se incubó durante 20 minutos a 37°C en 5% de CO2 y 90% de humedad relativa. Transcurrida la incubación 0.5 mL de PBS de las cámaras apical y basolateral fueron removidos y guardados separadamente para ser utilizados como blancos iniciales. En la cámara apical del inserto se inocularon 0.5 mL de las soluciones de los fármacos en estudio (teofilina 400 µM o ranitidina 456 µM en PBS), mientras que en la cámara basolateral o receptora se colocaron 0.5 ml de PBS. Luego, las cajas conteniendo los insertos se colocaron sobre un agitador de Mazzini (20 rpm) y se incubaron en las condiciones anteriormente descritas. Del lado basolateral de la cámara del inserto se tomaron 0.5 mL de muestra y se repuso la cantidad tomada adicionando 0.5 mL de PBS en el lado basolateral (Figura 1). Los tiempos de muestreo fueron diferentes para los dos compuestos evaluados, teofilina (40 minutos) y ranitidina (75 minutos), debido a las respectivas alta y baja permeabilidades que los caracterizan. Las muestras obtenidas a los diferentes tiempos fueron colocadas en viales separados conteniendo agua destilada en cantidad suficiente para completar 1mL. Posteriormente, la cuantificación del fármaco presente en las muestras se realizó por HPLC.
Determinación de la reproducibilidad de la técnica de evaluación de la permeabilidad
Una vez establecida la funcionalidad y la actividad transportadora del cultivo celular epitelial se realizaron las mediciones de Papp por triplicado con los mismos fármacos durante tres días. Este coeficiente fue calculado mediante un análisis de regresión lineal de la cantidad acumulada de un fármaco en el compartimento receptor (dQ) en función del tiempo de toma de muestras (dt). La pendiente resultante dividida entre la concentración en el compartimento dador (C) y la superficie (S) de la membrana absorbente corresponde al valor de Papp (cm.seg-1). Se tomaron 0.5 mL de muestra del lado basolateral (compartimento receptor) de la cámara del inserto, a los siguientes tiempos: teofilina, 10, 20, 30, 40, 50 y 60 min.; ranitidina, 20, 40, 60, 80, 100 y 120 min. Los tiempos de muestreo fueron establecidos considerando la clasificación biofarmacéutica de cada molécula (24). Los experimentos fueron realizados por triplicado. Con base en estos datos, se calculó la precisión intra e interdías del modelo como evidencia de la reproducibilidad de las mediciones llevadas a cabo en este sistema.
Cuantificación de la concentración de los fármacos
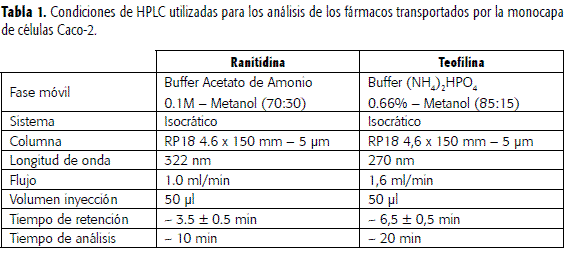
La cuantificación de la concentración de los fármacos transportados a través de la membrana artificial hacia la cámara basolateral se realizó mediante la técnica de Cromatografía Líquida de Alta Eficiencia (HPLC) con detección UV. Se siguieron las metodologías establecidas por la USP vigente (26) que para cada molécula fueron estandarizadas y comprobadas por Quasfar M&F S.A. La Tabla 1 contiene las condiciones empleadas en estos análisis.
Análisis estadístico
Para el análisis de los datos se aplicó un modelo de regresión lineal, a partir del cual se calculó el Papp. El coeficiente de variación de los valores de Papp fue usado para realizar las comparaciones intra e interdías.
RESULTADOS
Estandarización del cultivo y obtención de monocapas
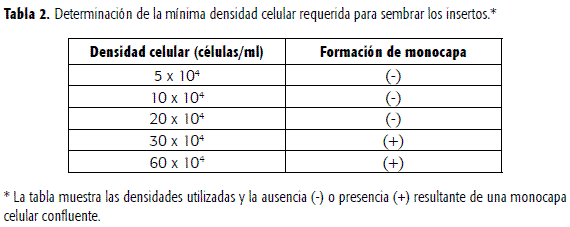
A partir de células Caco-2 obtuvimos monocapas confluentes de células en frascos T-25 en una semana, utilizando una densidad de siembra 1x106 / caja T-25. La disgregación con tripsina de las monocapas proporcionó las células requeridas para sembrar los insertos empleados en la determinación de los coeficientes de permeabilidad aparente (Papp). Al ensayar cinco densidades en el rango de 5.0 x 104 células/ cm2 y 60.0 x 104 células/ cm2, se encontró que 3.0 x 105 células por cm2 es la mínima densidad celular que se debe emplear para sembrar los insertos con el fin de obtener monocapas confluentes (Tabla 2). Estos ensayos fueron repetidos tres veces, cada uno por duplicado.
La detección de la expresión de fosfatasa alcalina en los cultivos fue llevada a cabo para establecer la diferenciación in vitro de las células Caco-2. Cuando los cultivos fueron expuestos al cromógeno nitroazul-tetrasodio (NBT), desarrollaron coloración azul como producto de la defosforilación del BCIP (5-bromo-4-cloro-3-indocil-fosfato) catalizada por la fosfatasa alcalina presente en las células Caco-2 cultivadas (datos no mostrados).
Pruebas de resistencia transepitelial (TEER)
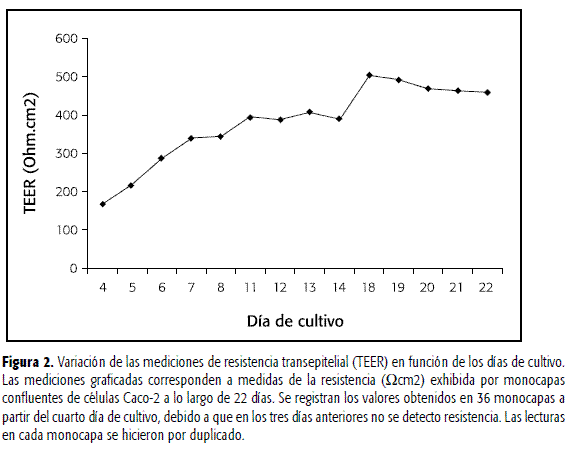
En la Figura 2 se muestran los resultados generales de la medida de la TEER efectuada a cada una de las monocapas que se usaron en las pruebas de funcionalidad y de reproducibilidad. Como se puede observar, antes del cuarto día no se registraron niveles cuantificables de resistencia transepitelial hecho indicativo de la ausencia de monocapa celular. A partir del cuarto día se pudo registrar este parámetro, el cual aumento en función de los días de cultivo hasta llegar en el día 18 a un valor que se mantuvo estable en el rango de 458 a 503 Ω.cm2 hasta el final de la prueba el día 22. La estabilidad observada en las mediciones de TEER en este tiempo se tomó como indicativo de la formación de una capa confluente y semipermeable a partir del día 18 de cultivo.
Actividad transportadora
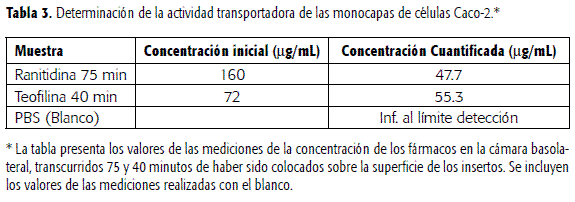
Una vez se estableció el tiempo requerido para obtener cultivos confluentes de células Caco-2 sobre los insertos, se procedió a evaluar la actividad transportadora de la monocapa en dirección apical-basolateral. En estos ensayos se usaron monocapas con valores de TEER en el rango en el que se estabilizaron las mediciones de resistencia (458-503 Ω.cm2). La actividad transportadora de la monocapa fue demostrada ya que 75 y 40 minutos después de colocar sobre la superficie de los insertos las soluciones de ranitidina y teofilina, respectivamente, se detectaron niveles cuantificables de estas sustancias en la cámara receptora. Igualmente, se mostró que el PBS y los insertos Falcon® utilizados en los ensayos no interfieren las mediciones (Tabla 3).
Reproducibilidad de las medidas de la actividad transportadora
Demostrada la actividad transportadora de la monocapa, se procedió a realizar los ensayos de permeabilidad de las dos moléculas empleadas en este estudio. Con tal fin, se determinó su velocidad de aparición en dirección apical-basolateral y se calculó para cada fármaco Papp (s-1cm) en la dirección apical-basolateral, por triplicado y durante tres días diferentes.
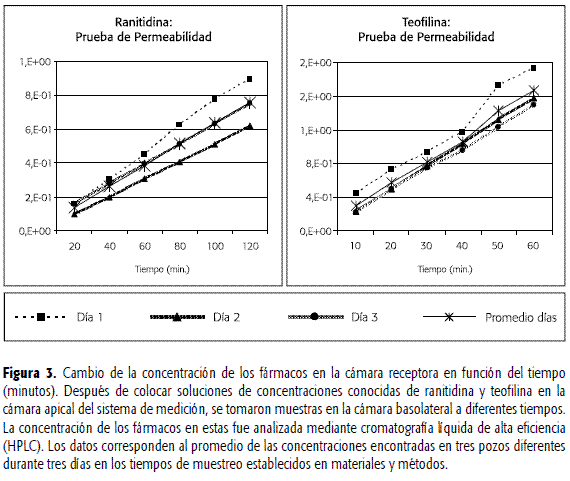
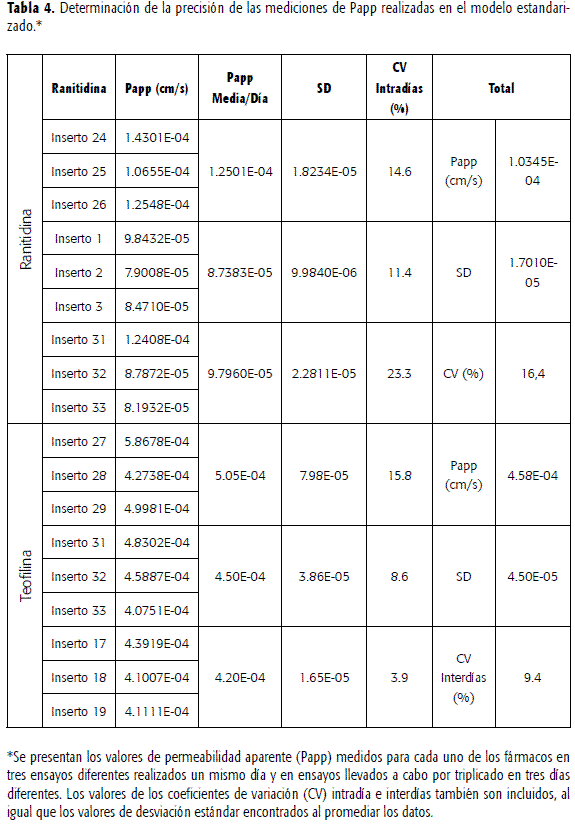
La Figura 3 muestra el resultado de graficar la concentración de los fármacos en la cámara receptora en función del tiempo. Para cada uno de los fármacos, se aprecia la relación de proporcionalidad directa que se establece entre la concentración y el tiempo; la pendiente de cada línea recta obtenida corresponde al valor de Paap. Con la ranitidina los coeficientes de variación intradías obtenidos fueron 14.6; 11.4 y 23.3 % para los días 1, 2 y 3, respectivamente; mientras que el coeficiente de variación total, correspondiente a la variación interdías, fue 16.4 %. Para la teofilina, los coeficientes de los dìas 1, 2 y 3 fueron 15.8; 8.6 y 3.9 %, respectivamente; el coeficiente interdías fue 9.4% (Tabla 4).
DISCUSIÓN
Para el estudio de la absorción de diversos compuestos, incluidos los que exhiben actividad farmacológica, se ha utilizado el modelo de células Caco-2 (27). En el desarrollo de nuevos fármacos, los estudios de absorción realizados en este sistema pueden ser utilizados para solicitar excepción de los estudios de bioequivalencia (15).
La carencia en Colombia de reportes acerca de la utilización de monocapas de células epiteliales para la medición de la permeabilidad de un fármaco, con el fin de predecir su absorción, condujo a estandarizar la metodología de un modelo de cultivo de células Caco-2. Las condiciones de cultivo establecidas permitieron la obtención de monocapas celulares viables, uniformes, diferenciadas y funcionales, es decir con permeabilidad selectiva. Lo anterior es sugerido por los valores de resistencia eléctrica transepitelial (TEER) medidos, mayores a 450 Ω.cm2, que se encuentran dentro del rango utilizado en otros trabajos (24, 28).
En la realización de este trabajo evaluamos la permeabilidad de las monocapas celulares a ranitidina y teofilina, compuestos que se absorben por difusión pasiva y cuyas permeabilidades, efectiva y aparente, han sido reportadas (24, 29). Estos fármacos fueron utilizados debido a que ya fue establecida la categoría en la que se encuentran dentro del sistema de clasificación biofarmacéutica (24, 29). Debido a que los valores de Papp que obtuvimos conducen a la misma clasificación, se puede decir que este modelo permite evaluar la absorción de diferentes sustancias.
La precisión de la metodología estandarizada se estimó mediante los coeficientes de variación de las mediciones. Para esto, se realizaron tres réplicas de un mismo ensayo en el mismo día con el fin de determinar la precisión intradías o repetibilidad. Igualmente, los ensayos se hicieron en tres días diferentes para examinar la precisión inter-días o reproducibilidad. Los coeficientes de variación estimados indican que las medidas de permeabilidad obtenidas en el modelo desarrollado son precisas.
Los dos fármacos empleados en esta estandarización son corrientemente utilizados para evaluar modelos in vivo e in vitro en estudios de permeabilidad (24, 29). Sin embargo, estos son apenas dos de los más de 20 compuestos incluidos en la lista de compuestos sugerida por la FDA en las guías para caracterizar la permeabilidad de fármacos (15). Por esta razón, las únicas conclusiones que podemos sacar del trabajo que presentamos son que el modelo se estandarizó, que las medidas de permeabilidad que con el se efectuaron son precisas y que con base en ellas se estableció correctamente la clasificación de permeabilidad de los fármacos evaluados. De ahí que sea necesario evaluar más moléculas de referencia para determinar completamente la exactitud del modelo y lograr su validación con una muestra de fármacos representativa de las cuatro categorías del sistema de clasificación biofarmacéutica.
Debido a que las monocapas de células Caco-2 han sido utilizadas para estudiar los cuatro tipos de transportes existentes en el epitelio intestinal (10), cuando el modelo in vitro que estandarizamos sea validado en nuestro medio se podrá realizar tamizajes para identificar fármacos en desarrollo con problemas de absorción oral, obtener esquemas de clasificación predictivas de las absorciones en modelos in vivo y ex vivo que justifiquen evaluar la absorción de un compuestos en un modelo animal e identificar moléculas transportadoras relevantes (1,10). Como se mencionó, este modelo puede sustituir o complementar estudios in vivo/ex vivo con animales de experimentación. La consolidación de esta línea de investigación permitirá desarrollar estudios en este campo dirigidos a dar soporte a los entes reguladores en Colombia, en el proceso del registro sanitario de un medicamento.
AGRADECIMIENTOS
Los autores agradecen a la Química Farmacéutica María Mercedes Posada por la lectura crítica del manuscrito, y a la bacterióloga Marcela Buitrago por su asistencia técnica durante la toma de las muestras. Igualmente, declaran no haber incurrido en ningún conflicto de interés durante la realización de este proyecto. El presente trabajo fue realizado con los recursos aportados por la Dirección de Investigaciones-Sede Bogotá de la Universidad Nacional de Colombia, proyecto con código 2030000.
BIBLIOGRAFÍA
1. P. Artursson and J. Karlsson, Correlation between oral drug absorption in humans and apparent drug permeability coefficients in human intestinal (Caco-2) cells, Biochem. Biophys. Res. Commun., 175, 880 (1991). [ Links ]
2. S. Yamashita, Y. Tanaka, Y. Endoh, Y. Taki, T. Sakane, T. Nadai, H. Sezaki, Analysis of drug permeation across Caco-2 monolayer: implication for predicting In vivo drug absorption, Pharm. Research, 14, 486 (1997). [ Links ]
3. H. Lennernas, Human Intestinal Permeability, J. Pharm. Sci., 87, 403 (1998). [ Links ]
4. M.J. Jackson, Drug transport across gastrointestinal epithelia, En: "Physiology of the Gastrointestinal Tract", 2nd Edition. Edited by L.R. Johnson, Ed. Raven Press New York, 1987. p. 1597. [ Links ]
5. G. Trapani, M. Franco, A. Trapani, A. Lopedota, A. Latrofa, E. Gallucci, S. Micelli, G. Liso, Frog intestinal sac: a new in vitro method for the assessment of intestinal permeability, J. Pharm. Sci., 93, 2909 (2004). [ Links ]
6. Y. Tanaka, Y. Taki, Y. Sakane, T. Nadai, H. Sezaki and S. Yamashita, Characterization of drug transport through tight - junctional pathway in Caco-2 monolayer: comparison with isolated rat jejunum and colon, Pharm. Res., 12, 523 (1995). [ Links ]
7. H. Lennernas, K. Palm, U. Fagerholm and P. Artursson, Comparison between active and passive drug transport in human intestinal epithelial (Caco-2) cells in vitro and human jejunum in vivo, Int. J. Pharm., 127, 103 (1996). [ Links ]
8. J.E. Polli and M.J. Ginski, Human drug absorption kinetics and comparison to Caco-2 monolayer permeabilities, Pharm. Res., 15, 47 (1995). [ Links ]
9. G.L. Amidon, H. Lennernas, V.P. Shah and J.R. Crison, A theoretical basis for a biopharmaceutic drug classification: the correlation of in vitro drug product dissolution and in vivo bioavailability, Pharm. Res., 12, 413 (1995). [ Links ]
10. P. Artursson, K. Palm and K. Luthman, Caco-2 monolayers in experimental and theoretical predictions of drug transport, Adv. Drug Deliv. Rev., 46, 27 (2001). [ Links ]
11. P. Artursson, Cell cultures as models for drug absorption across the intestinal mucosa, Crit. Rev. Ther. Drug Carrier Syst., 8, 305 (1991). [ Links ]
12. I.J. Hidalgo, T.J. Raub and R.T. Borchardt, Characterization of the human coloncarcinoma cell line (Caco-2) as a model system for intestinal epithelial permeability, Gastroenterology, 96, 736 (1989). [ Links ]
13. A.R. Hilgers, R.A. Conradi and P.S. Burton, Caco-2 cell monolayers as a model for drug transport across the intestinal mucosa, Pharm. Res., 7, 902 (1990). [ Links ]
14. K.L. Audus, R.L. Bartel, I.J. Hidalgo and R.T Borchardt, The use of cultured epithelial and endothelial cells for drug transport and metabolism studies, Pharm. Res., 7, 435 (1990). [ Links ]
15. U.S. Department of Health and Human Services Food and Drug Administration Guidance for Industry: Waiver of in vivo bioavailability and bioequivalence studies for immediate-release solid oral dosage forms based on a biopharmaceutical classification system. CDER-FDA. Rockville MD, USA 2000, pp. 1-16. [ Links ]
16. Ministerio de Salud, República de Colombia. Decreto 677 del 26 de abril de 1995. [ Links ]
17. Ministerio de Salud, República de Colombia. Resolución 1400 del 24 de agosto de 2001. [ Links ]
18. Ministerio de Salud, República de Colombia. Resolución 1890 del 19 de noviembre de 2001. [ Links ]
19. Ministerio de Protección Social, República de Colombia. Propuesta Documento para una Política Farmacéutica Nacional 2003; p. 11. [ Links ]
20. R. Lobenberg and G.L. Amidon, Modern bioavailability, bioequivalence and biopharmaceutics classification system, Eur. J. Pharm. Biopharm., 50, 3 (2000). [ Links ]
21. L.X. Yu, G.L. Amidon, J.E. Polli, H. Zhao, M.U. Mehta, D.P. Conner, V.P. Shah, L.J. Lesko, M.L. Chen, V.H. Lee and A.S. Hussain, Biopharmaceutics classification system: the scientific basis for biowaiver extensions, Pharm. Res., 19, 921 (2002). [ Links ]
22. Dirección Nacional de Planeación, República de Colombia. Decreto 585 de 1991. [ Links ]
23. S. Yamashita, T. Furubayashi, M. Kataoka, T. Sakane, H. Sezaki, and H. Tozuda, Optimized conditions for prediction of intestinal drug permeability using Caco-2 cells, Eur. J. Pharm. Sci., 10, 95 (2000). [ Links ]
24. S. Yamashita, K. Konishi, Y. Yamasaki, Y. Taki, T. Sakane, H. Sezaki, Y. Furuyama, New and better protocols for a short-term Caco-2 cell culture system, J. Pharm. Sci., 91, 669 (2002). [ Links ]
25. Absorption systems LP. Validation of the Caco-2 epithelial cell cu lture system for permeability evaluation according to the Biopharmaceutics classification system. www.absorption.com/downloads/¿url=AbsorptionSystemsBCSsummary.pdf. [consultado 2005 feb 13]. [ Links ]
26. United States Pharmacopeia. United States Pharmacopeia and National Formulary. USP 27- NF 22. USA, 2003, p. 1624; p. 1811. [ Links ]
27. J. Tallkvist and H. Tjälve, Transport of nickel across monolayers of human intestinal Caco-2 cells, Toxicol. Appl. Pharmacol., 151, 117 (1998). [ Links ]
28. K.A. Lentz, J. Hayashi, L.J. Lucisano, and J.E. Polli, Development of a more rapid, reduced serum culture system for Caco-2 monolayers and application to the biopharmaceutics classification system, Int. J. Pharm., 200, 41 (2000). [ Links ]
29. A. Collet, N.B. Higgs, E. Sims, M. Rowland and G. Warhurtst, Modulation of the permeability of H2 receptor antagonists Cimetidine and Ranitidine by P-glycoprotein in rat intestine and the human colonic cell line Caco-2J, Pharmacol. Exp. Ther., 288, 171 (1999). [ Links ]














