Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Ciencias Químico - Farmacéuticas
Print version ISSN 0034-7418On-line version ISSN 1909-6356
Rev. colomb. cienc. quim. farm. vol.37 no.2 Bogotá July/Dec. 2008
Artículo de Investigación
Avaliação da influência de adjuvantes não-poliméricos solúveis na liberação do nimodipino a partir de formulações matriciais de liberação prolongada
Evaluation of soluble non-polymeric adjuvants in the release of nimodipino from controlled release matrices formulations
Talita Steingräber1, Tatiane Schtoltz1, Patrik Oening Rodrigues*1, 2
1 Departamento de Farmácia, Universidade da Região de Joinville (UNIVILLE), Joinville, Brasil.
2. Departamento de Ciências Farmacêuticas, Universidade Federal de Santa Catarina (UFSC), Florianópolis, Brasil. Departamento de Farmácia, Universidade da Região de Joinville, Bom Retiro, CEP 88040 900, Joinville, Santa Catarina, Brasil. E-mail: patrikoening@gmail.com, fax 55 47 3461 9091.
Recibido para evaluación: mayo 19 de 2008 Aceptado para publicación: agosto 11 de 2008
RESUMEN
Fármacos com características lipofílicas costumam apresentar velocidade de difusão muito baixa a partir de matrizes hidrofílicas de liberação, comprometendo a obtenção de níveis plasmáticos terapeuticamente efetivos. Contudo, a liberação de fármacos lipossolúveis a partir de sistemas matriciais é influenciada pelo pH do meio, que pode facilitar a formação de cargas na molécula, melhorando sua performance. O objetivo deste trabalho foi avaliar a capacidade de adjuvantes não poliméricos em facilitar a solubilização do Nimodipino, "in vitro", através do perfil de dissolução de cápsulas matriciais de idroxipropilmetilcelulose (HPMC). As formulações desenvolvidas apresentaram o mecanismo de liberação do fármaco pela matriz governado pelo processo de erosão de acordo com o modelo cinético de Korsmeyer-Peppas, onde n>1. Entretanto algumas formulações apresentaram 0.5> n < 1 demonstrando ser um sistema anômalo dependente de difusão e erosão. Os perfis de dissolução nos dois meios testados mostraram-se distintos podendo observar diferenças significativas entre eles.
Palabras clave:Hidroxipropilmetilcelulose (HPMC), Nimodipino, Solubilidade, Liberação Prolongada
ABSTRACT
Drugs with slow solubility present very low diffusion from hydrophilic matrices, committing the serum levels therapeutically effectives. However, the liberation of lipophilic drugs starting from matrix systems is influenced by the pH of the medium, that it can facilitate the formation of charges in the molecule, improving your performance. The objective of this work was to evaluate the capacity of non-polymeric excipients in facilitating the solubilization of Nimodipino "in vitro", through the capsules dissolution profiles of hydroxypropylmethylcellulose matrices. The developed formulations presented the release mechanism of drug influenced by erosion process according with the kinetic model of Korsmeyer-Peppas, where n>1. However, some formulations presented 0.5> n <1 demonstrating to be an anomalous system dependent of diffusion and erosion. The dissolution profiles in the two tested mediums showed different, allowing to observe significant differences among them.
Key words: Hydroxypropylmethylcellulose (HPMC), Nimodipine, Solubility, Controlled Drug Release
INTRODUÇÃO
A partir de matrizes hidrofílicas, a solubilidade do fármaco pode ser um fator essencial, capaz de influenciar o comportamento do sistema e os processos de liberação do mesmo. Bettini e colaboradores1 observaram que fármacos com elevada solubilidade tendem a ser liberados por difusão, enquanto fármacos pouco solúveis são liberados, predominantemente, através do fenômeno de erosão. Portanto, a baixa solubilidade do fármaco favorece a presença de partículas sólidas na camada de gel, diminuindo a motilidade e a resistência da mesma, tornando-a mais susceptível ao processo de desestruturação2 Características de pouca solubilidade em água são observadas no vasodilatador Nimodipino, [isopropil (2-metoxietil)1,4-diidro-2,6-dimetil-4-(3-nitrofenil)- 3,5-piridina-dicarboxilada]; antagonista de canais de cálcio pertencente á classe das diidropiridinas. A estrutura química do Nimodipino apresenta duas longas cadeias laterais ligadas ao anel diidropiridínico e um grupo nitro ligado ao anel fenila, que confere ao fármaco características de base fraca, e praticamente insolúvel em água3. A baixa taxa de solubilidade e dissolução de fármacos pouco solúveis em água e nos fluídos gastrintestinais causa, frequentemente, uma insuficiente biodisponibilidade, uma vez que somente os fármacos dissolvidos nos líquidos gastrintestinais podem ser absorvidos, o que requer determinada hidrossolubilidade do fármaco, o que vem a desfavorecer o desenvolvimento de formulações de liberação prolongada4,5. Logo, fármacos lipofílicos costumam apresentar velocidade de difusão muito baixa a partir da matriz hidrofílica de liberação, comprometendo a obtenção de níveis plasmáticos terapeuticamente efetivos6,7. Contudo, a liberação de fármacos lipossolúveis a partir de sistemas matriciais é influenciada pelo pH do meio, que pode facilitar a formação de cargas na molécula, melhorando sua performance. Assim, a solubilidade de bases fracas diminui em função do aumento do pH do solvente8. A presença de um agente ácido ou básico em formulações de medicamentos pode causar a conversão da forma não ionizada do fármaco para formas ionizadas, mais solúveis, e esta conversão, parcial ou total, pode aumentar a solubilidade e, consequentemente, o coeficiente de difusão do fármaco através da matriz, sendo, portanto, um processo dependente tanto do pKa do fármaco quanto do pH do meio de dissolução9,10. A liberação de fármacos a partir de cápsulas, assim como nos comprimidos, está sujeita ao efeito dos excipientes. Portanto, a adição de adjuvantes não-poliméricos com características ácidas ou básicas tem demonstrado alterar não só os perfis de solubilidade do fármaco, como também a estrutura da própria matriz, no que diz respeito á sua porosidade e grau de hidratação11. Cabe ressaltar que, os excipientes utilizados tendem a afetar diretamente os processos de formação dos frentes de intumescimento na liberação de fármacos insolúveis, onde os excipientes e o polímero presentes na formulação possuem as mesmas afinidades pelo meio aquoso podendo haver competição entre excipientes e o polímero pelo meio de dissolução. Este último terá poucas chances de se hidratar, interferindo no intumescimento da matriz no estado gélico12. Deste modo, o presente trabalho tem como objetivo avaliar a capacidade de excipientes não poliméricos em facilitar a solubilização do Nimodipino "in vitro", através do perfil de dissolução de cápsulas matriciais de hidroximetilpropilcelulose (HPMC).
MATERIAIS E MÉTODOS
O fármaco nimodipino e a hidroxipropilmetilcelulose (Methocel® K4M Premium) proveniente da Dow Chemical Company foram doados pela Universidade Federal de Santa Catarina (UFSC). O ácido cítrico proveniente da Vital Especialidades e o carbonato de cálcio, proveniente da Quimidrol, foram gentilmente doados pelo laboratório de Farmacotécnica da Universidade da Região de Joinville (UNIVILLE).
Preparação das cápsulas de liberação prolongada de Nimodipino
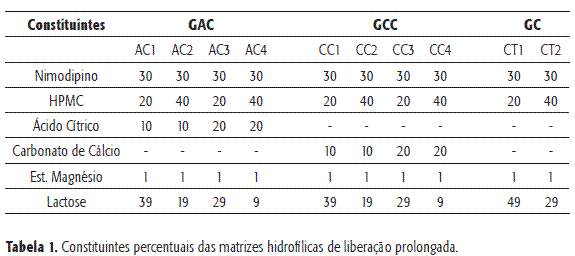
Foram produzidas dez formulações (Tabela 1), considerando uma quantidade fixa de Nimodipino (60 mg), estearato de magnésio (1%) e lactose como diluente. Como fatores de variação foram utilizados a quantidade de HPMC K4M (20% e 40%) e dos adjuvantes ácido Cítrico (AC) e Carbonato de Cálcio (CC), nas concentrações de 10% e 20% do somatório da massa total da formulação. Também foram produzidas formulações controle, contendo as mesmas quantidades dos componentes acima especificados, exceto os adjuvantes AC e CC. As cápsulas de liberação prolongada de Nimodipino foram preparadas misturando os constituintes em grau de porcelana, sem triturar. Procedeu-se com a seguinte seqüência de mistura: (Nimodipino + HPMC + lactose + adjuvante, 5 min) + (estearato de magnésio, 1min).
Avaliação dos perfis de dissolução das cápsulas matriciais de Nimodipino
Um equipamento Nova ética modelo 299 (Brasil) foi utilizado para a avaliação do perfil de dissolução das cápsulas matriciais de Nimodipino. As condições experimentais atenderam o preconizado pela Farmacopéia Britânica (2002)13, utilizando aparato 1 em 100 rpm em dois diferentes meios de dissolução; lauril sulfato de sódio - LSS 0,5% e etanol 15% mantidos na temperatura de 37 °C. O estudo foi realizado com três unidades de cada formulação, sendo retiradas alíquotas de 10 mL, repondo-se o meio de dissolução. Amostras de nimodipino foram retiradas no período compreendido entre 15-900 minutos de análise, sendo as concentrações de fármaco liberado aferidas em espectrofotômetro (UV/VIS Schimadzu 1601PC, Japão) no comprimento de onda de 340 nm com auxílio de uma curva de calibração previamente construída garantindo linearidade no intervalo de 2.4 − 96 µg mL-1 (R2 = 0,9988 em LSS e R2= 0,9995 em etanol). Os resultados dos perfis de dissolução das cápsulas matriciais de Nimodipino foram avaliados através da análise exploratória dos dados, comparação estatística e aplicação da cinética de liberação, segundo o modelo de Korsmeyer e Peppas.
RSULTADOS E DISCUSÃO
O delineamento das formulações visando perfis de liberação prolongada do Nimodipino implicou na seleção de adjuvantes capazes de afetar a liberação do fármaco, sob dois principais aspectos: 1) influência sobre os parâmetros tecnológicos da forma farmacêutica e 2) influência sobre a solubilidade do fármaco. Do ponto de vista tecnológico utilizou-se adjuvante polimérico capaz de intumescer em meio aquoso, favorecendo um comportamento de permeabilidade, típico de sistemas matriciais. O que determina a concentração do polímero na formulação, segundo várias literaturas é a relação direta entre a sua concentração e a liberação do fármaco a partir de sistemas matriciais14, justificando assim, a necessidade de avaliar a influência de diferentes níveis de concentração de HPMC K4M sob o perfil de liberação do nimodipino a partir das formulações produzidas. Considerando a solubilidade do fármaco, foram avaliadas duas substâncias com características de dissociação diferentes: ácido cítrico (AC) e carbonato de cálcio (CC) quanto á capacidade de formação de carga e solubilização do nimodipino.
As formulações matriciais produzidas foram avaliadas quanto ao peso médio e doseamento, mostrandose de acordo com os limites especificados Farmacopéia Britânica (2002)13. As cápsulas matriciais de nimodipino foram avaliadas quanto á liberação do fármaco em dois meios distintos (LSS 0,5% e álcool 15%), já utilizados em estudos anteriores para avaliação da liberação desse fármaco15,16.
As concentrações de Nimodipino liberadas nos tempos pré-determinados foram avaliadas em espectrofotômetro a partir da curva de calibração previamente construída em cada meio de dissolução. A curva de calibração produzida em álcool 15% garantiu linearidade na faixa de 2,4 a 96 µg mL-1 (y = 0,0143x - 0,0018 ; R2 = 0,9995). A curva de calibração produzida em LSS 0,5% garantiu, na mesma faixa de concentração, uma boa linearidade (y = 0,0071x + 0,01 ; R2 = 0,9988).
Através da análise exploratória dos perfis de dissolução (Figura 1) é possível verificar que as formulações contendo AC apresentaram um percentual maior de liberação do nimodipino em comparação ás formulações contendo CC. Sugere-se que esse perfil é resultado da maior capacidade de ionização do nimodipino em meio ácido, uma vez se trata de um fármaco correspondente a uma base fraca. Essa característica da matriz favorece a solubilização do nimodipino e conseqüente permeação desse fármaco pela matriz intumescida10,17.
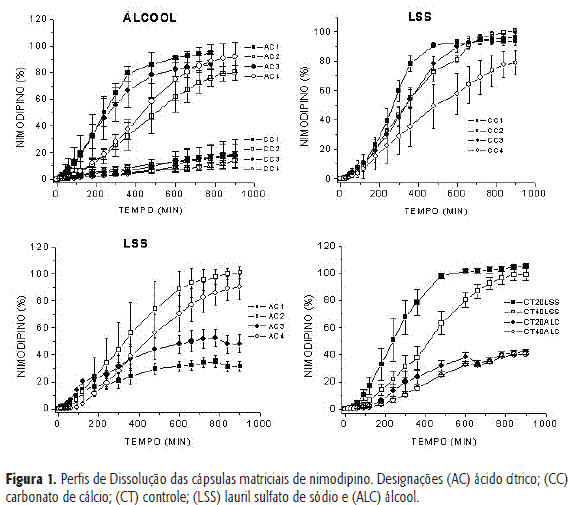
Outro mecanismo proposto para a ação do AC sobre a liberação de fármacos lipofílicos a partir de matrizes poliméricas hidrofílicas, seria o do aumento da formação de poros na matriz, devido justamente, á sua elevada solubilidade10. Este mecanismo explica que no processo de hidratação das cadeias poliméricas e formação da camada de gel na matriz, a presença de excipientes solúveis favorece a formação de canais na estrutura, favorecendo a relaxação polimérica, contribuindo para o mecanismo de liberação do fármaco2,18.
As diferentes concentrações de polímero influenciaram na liberação do fármaco nas formulações contendo AC. Entretanto, essa característica não foi observada naquelas que continham CC. Nas formulações contendo o ácido, os perfis de dissolução mostraram-se também, superiores ás formulações controle (CT). A dissolução do Nimodipino em meio etanólico não se mostrou adequada, dificultando a avaliação da dissolução, muito embora estudo com este meio tenha sido publicado15, afirmando que o adequado perfil de dissolução do fármaco era dependente do etanol do meio. Diferentemente, nas formulações CC analisadas em meio contendo LSS, todas demonstraram uma liberação prolongada do fármaco. Entretanto, aquelas com menor quantidade de polímero, facilitaram a liberação do nimodipino. Com o aumento da concentração de polímero, a matriz mostrou-se mais estável em relação ás formulações com menores teores e também em relação ás formulações testadas no meio etanólico. Esta estabilidade pode estar associada á presença do LSS, que é um forte agente tensoativo.
As formulações AC em meio LSS mostraram perfis diferenciados. Percebe-se que aquelas com maior quantidade de HPMC prolongaram a liberação por um tempo superior, enquanto as que possuíam menor quantidade de polímero apresentaram uma liberação atípica, ou seja, muito inferior. Sugere-se que possa ter ocorrido uma interação entre o LSS e o AC, uma vez que esse tensoativo é uma substância com caráter aniônico.
Nas formulações CT as matrizes demonstraram que a liberação em etanol é menor para ambas as concentrações do polímero. Já em LSS, ocorre uma melhora significativa na liberação nas duas proporções de polímero, sendo que na proporção de 20% de HPMC a liberação ocorre mais rapidamente, como resultado da menor estabilidade da matriz.
Como mencionado anteriormente, a liberação de um fármaco a partir de sistemas matriciais é influenciada pela solubilidade deste em meio aquoso19,20. Considerando que a solubilidade de fármacos com características de base fraca, tal como o Nimodipino, aumenta com a diminuição do pH do solvente8, poderia se esperar que sistemas matriciais contendo tais fármacos, quando tamponados com substâncias com caráter ácido, apresentem perfil de dissolução diferenciado. Não há evidências que permitem afirmar que a presença de carbonato de cálcio nas cápsulas induz ao aumento do pH no micro-ambiente desses sistemas. Pode-se supor, entretanto, que o pH da camada gel formada ao redor das cápsulas contendo CC no decorrer do processo de dissolução seja superior ao formado nas formulações contendo AC, resultando em um efeito tamponante sob as formulações, haja vista as diferenças encontradas nos perfis21.
A cinética de liberação do Nimodipino das cápsulas matriciais foi avaliada pela aplicação da equação proposta por Korsmeyer-Peppas22. O modelo consiste numa derivação da equação proposta por Higuchi, considerando, entretanto, outros mecanismos de liberação não fikianos, como anômalos, caso II e supercaso II. O valor do coeficiente n que pode ser calculado com a equação está relacionado ao tipo de liberação apresentado pela matriz, sendo: difusão fikiana, quando n = 0,5; transporte anômalo quando 0,5 < n <1; transporte caso II quando n = 1; e transporte supercaso II quando n > 1 23-25. Os valores do expoente n encontrados para os perfis de liberação do nimodipino são apresentados na Tabela 2. Em meio etanol 15% verifica-se que o Nimodipino é liberado a partir das cápsulas no grupo CC por um mecanismo do tipo anômalo, com exceção de CC2. Conhecendo-se a característica de matrizes hidrofílicas de HPMC em meio aquoso, pode-se sugerir que o mecanismo anômalo de dissolução ocorre como resultado da ação conjunta dos processos de difusão e erosão da matriz polimérica. As formulações do grupo AC apresentaram valores de n superiores a 1, caracterizando um processo cinético de liberação super caso II, o que implica numa alta velocidade de permeação do meio pela matriz, favorecendo o processo de erosão do sistema. Entretanto, a formulação AC3, de acordo com o coeficiente de linearidade, apresentou o melhor perfil de liberação entre o grupo.
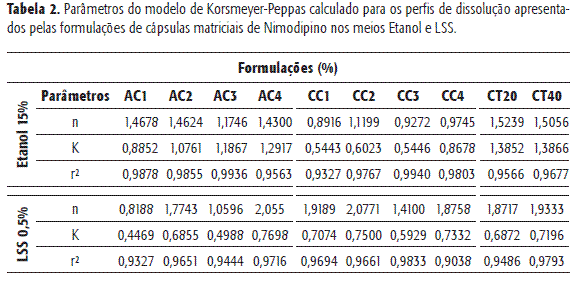
O grupo controle (GC) e a formulação CC2 também apresentaram mecanismo do tipo super caso II, porém o valor da constante de cinética (k) foi maior para o grupo GC, indicando uma maior velocidade de liberação do fármaco em relação a CC2, o que é esperado devido ás características do carbonato de cálcio. Em meio LSS, o valor do expoente n encontrado para o grupo CC e o grupo GC, indica que todas as formulações apresentaram processo de liberação do tipo super caso II (n > 1). Estes dois grupos (CC e GC) demonstraram ter perfis de liberação semelhantes, pois não apresentaram grandes diferenças aos valores da constante de cinética e coeficiente de linearidade. Já a formulação AC1 apresentou um perfil anômalo, caso em que foi notado pela lenta e pouco eficiente liberação do fármaco pela matriz (Tabela 2). Na formulação AC3, o expoente n indica que o nimodipino foi liberado a partir da matriz por um mecanismo do tipo caso II, obtendo-se um maior prolongamento na liberação do fármaco. Já as formulações AC2 e AC4 demonstraram um comportamento semelhante ao grupo CC e GC, mecanismo do tipo super caso II.
O valor do coeficiente n calculado pela equação de Korsmeyer-Peppas sugere que grande parte das formulações apresentou transporte super caso II, ou seja, o mecanismo de liberação do fármaco pela matriz acontece a partir do seu intumescimento e erosão. Todavia, neste caso, a velocidade de difusão do solvente é muito maior que a velocidade de relaxamento do polímero.
Segundo Martin (1993)26 e Netz (2002)27 a presença de eletrólitos em elevada concentração em soluções contendo polímeros hidrofílicos pode resultar, em última instância, em fenômeno de floculação ou salting-out. Desta forma, como a HPMC é um polímero não-iônico e, por esta razão, não é susceptível ao típico efeito salting-out, pode-se esperar que os tensoativos presentes nas formulações, sendo eletrólitos em elevada concentração, poderiam ter competido com a HPMC em relação á captação de água, diminuindo assim, a capacidade de intumescimento da matriz. Portanto, é relevante ressaltar que, os dois meios geraram pH com características diferentes e, estes podem ter influenciado de forma distinta na competição pelo solvente do meio, resultando em diferentes perfis de dissolução.
CONCLUSÃO
A análise exploratória das curvas de dissolução permitiu visualizar a dessemelhança das formulações no prolongamento da liberação do nimodipino em diferentes meios, o que foi confirmado com a análise da cinética de liberação. As formulações AC3, em meio etanol 15%, e CC3, em meio LSS 0,5%, mostraram-se mais eficientes no que tange a um aumento na solubilidade do nimodipino e liberação prolongada. Os grupos de formulações apresentaram mecanismos cinéticos de liberação do fármaco diferenciados, o que confirma a distinção na performance relacionada aos tipos de adjuvantes não-poliméricos utilizados, bem como os diferentes meios de análise. Com base nos resultados, verifica-se que a quantidade e tipo de excipiente nãopolimérico na formulação de cápsulas é dependente do pH do meio de dissolução. Assim, para fármacos pouco solúveis, a otimização de formulações com presença de substâncias tamponantes, torna-se viável, pois o uso de adjuvantes são capazes de promover alteração do micro-ambiente de pH e /ou alterar a porosidade e a tortuosidade do percurso dentro da forma farmacêutica, promovendo modificações na solubilidade ou na velocidade de dissolução do fármaco nas camadas de difusão.
REFERÊNCIA BIBLIOGRáFICAS
1. R. Bettini, P.L. Cattellani, G. Massimo, N.A. Peppas, P. Colombo, Translocation of drug particles in HPMC matrix gel layer: effect of drug solubility and influence on release rate, J. Control. Release 70, 383 (2001). [ Links ]
2. P. Colombo, R. Bettini, P. Santi, N.A. Peppas, Matrices for controlled drug delivery: gel-layer behaviour, mechanisms and optimal performance, PSTT, 3, 198 (2000). [ Links ]
3. A. Grunenberg, B. Keeil, J. Henck, Polymorphism in binary mixtures, as exemplified by nimodipine, Int. J Pharm. 118, 11 (1995). [ Links ]
4. S. Storpirtis, P.G. Oliveira, D. Rodrigues, D. Marinho, Considerações biofarmacotécnicas relevantes na fabricação de medicamentos genéricos: fatores que afetam a dissolução e a absorção de fármacos, Rev. Bras. Ciên. Farmac. 35, 1 (1999). [ Links ]
5. N.A. Urbanetz, B.C. Lippold, Solid dispersions of nimodipine and polyethylene glycol 2000: dissolution properties and physico-chemical characterisation, Eur. J. Pharm. Bio. 59, 107 (2005). [ Links ]
6. T. Salsa, F. Veiga, M.E.O. Pina, Oral controlled-release dosage forms. I. Cellulose ether polymers in hydrophilic matrices, Drug Dev. Ind. Pharm. 23(9), 929 (1997). [ Links ]
7. A.R. Gennaro, "Remington: Ciência y pratica de la Farmácia", 20°ed., Panamericana, Madrid, 2004, 2208 p. [ Links ]
8. C. Van Der Veen, H. Buitendijk, C.F. Lerk, The effect of acidic excipients on the release of weakly basic drugs from the programmed release megaloporous system, Eur. J. Pharm. Biopharm. 37, 238 (1991). [ Links ]
9. A. Steubel, J. Seepmann, A. Dashevsky, R. Bodmeier, pH-independent release of a weakly basic drug from water-insoluble and -soluble matrix tablets, J. Control. Release 67, 101 (2000). [ Links ]
10. R. Espinoza, E. Hong, L. Villafuerte, Influence of admixed citric acid on the release profile of pelanserin hydrochloride from HPMC matrix tablets, Int. J. Pharm. 201(2): 165, (2000). [ Links ]
11. V.O. Consiglieri, S. Storpirtis, H.G. Ferraz, Aspectos farmacotécnicos relacionados á biodisponibilidade e bioequivalência de medicamentos, Rev. Bras. Ciên. Farm. 21 (1), 23 (2000). [ Links ]
12. H.C. Ansel, N.G. Popovich, L.V. Allen, "Farmacotécnica: formas farmacêuticas e sistemas de liberação de fármacos", Premier, São Paulo, 2002, 776 p. [ Links ]
13. Britsh Pharmacopeia, V. II. "The Stationery Office", London, 2002. [ Links ]
14. L.S.C. Wan, P.W.S. Heng, L.F. Wong, Relationship Between Swelling and Drug Release in a Hydrophilic Matrix, Drug Dev. Ind. Pharm. 19(10), 1201 (1993). [ Links ]
15. Z. He, D. Zhong, X. Chen, X. Liu, X. Tang, L. Zhao, Development of a dissolution medium for nimodipine tablets based on bioavailability evaluation, Eur. J. Pharm. Sci. 21, 487 (2004). [ Links ]
16. T.F.M Cardoso, "Caracterização das propriedades físico-químicas do Nimodipino a avaliação da influência do polimorfismo e comprimidos", Dissertação de Mestrado, Universidade Federal de Santa Catarina, Florianópolis, Santa Catarina, Brasil, 2004, 158 p. [ Links ]
17. M.A. Solinís, S. Lugará, B. Alvo, R.M. Hernández, A.R. Gascón, J.L. Pedraz, Release of salbutamol sulfate enantiomers from hydroxypropylmethylcellulose matrices, Int. J. Pharm. 161, 37 (1998). [ Links ]
18. P. Colombo, R. Bettini, P.L. Catellani, P. Santi, N.A. Peppas, Drug volume fraction profile in the gel phase and drug release kinetics in hydroxypropylmethyl cellulose matrices containing a soluble drug, Eur. J. Pharm. Sci. 9: 33-40. [ Links ]
19. L. Yang, R. Fassihi, Examination of drug solubility, polymer types, hydrodynamics and loading dose on drug release behavior from a triple-layer asymmetric configuration delivery system, Int. J. Pharm. 155, 219 (1997). [ Links ]
20. K.V.R. Rao, K.P. Devi, P. Buri, Influence of molecular size and water solubility of the solute on its release from swelling and erosion controlled polymeric matrices, J. Control. Release, 12, 133 (1990). [ Links ]
21. L.H. Andrighetti, "Avaliação tecnológica da concentração de hidroxipropilmetilcelulose e de adjuvantes não-poliméricos solúveis em comprimidos matriciais contendo elevado teor de fármaco solúvel", Dissertação de Mestrado, Universidade Federal do Rio Grande do Sul, Porto Alegre, Santa Catarina - Brasil, 2003, 113 p. [ Links ]
22. N. A. Peppas, Analysis of fickian and non-fickian drug release from polymers, Pharm. Acta Helv. 60, 110 (1985). [ Links ]
23. E.J. Agnes, G.G. Ortega, Modelos matemáticos e físico-química da difusão, Cad. Farm. 19(1), 9 (2003). [ Links ]
24. C.M. Lopes, J.M.S. Lobo, P. Costa, Modified release of drug delivery systems: hydrophilic polymers, Braz. J. Pharm. Sci. 41(2), 143 (2005). [ Links ]
25. P.O. Rodrigues, M.A.S. Silva, Avaliação in vitro de medicamentos de liberação prolongada: aplicação de métodos estatísticos, modelos dependentes e independentes de análise, Rev. Col. Cien. Quím. Farm. 34(1), 13 (2005). [ Links ]
26. A. Martin, "Physical Pharmacy". 4th ed., Willians & Wilkins, Baltimore, 1993, 1328 p. [ Links ]
27. P.A. Netz, G.G. Ortega, "Fundamentos de Físico Química", Artmed, Porto Alegre, 1996, 300 p. [ Links ]














