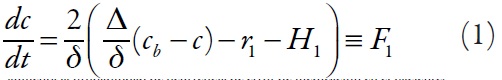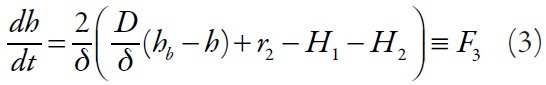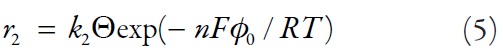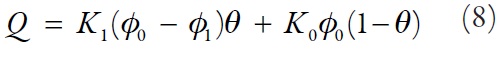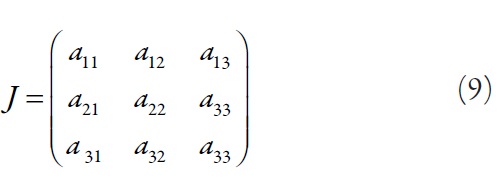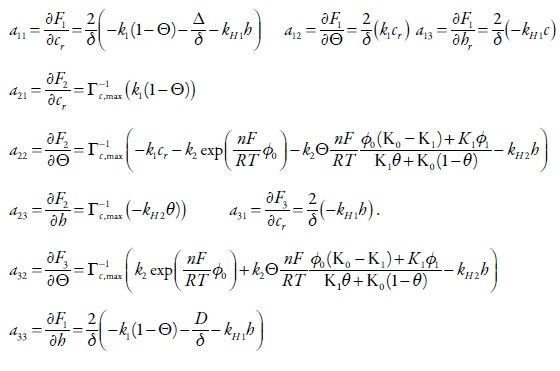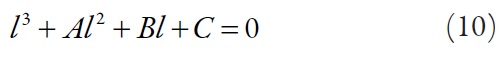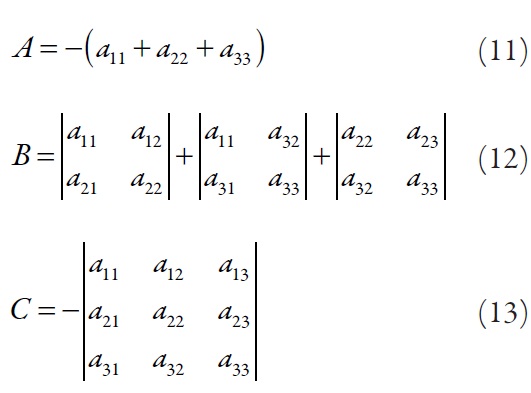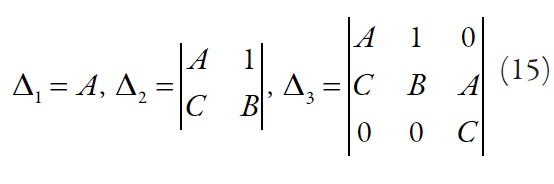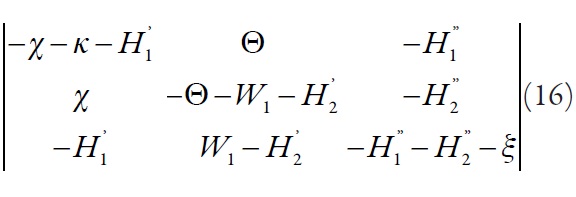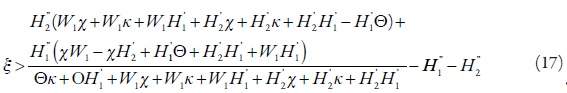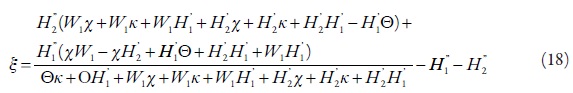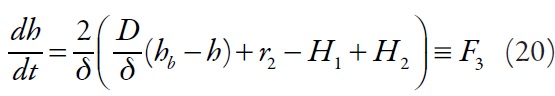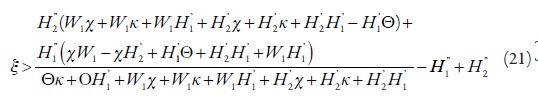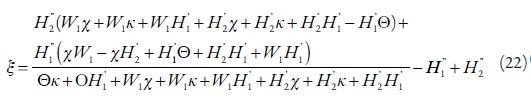Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Ciencias Químico - Farmacéuticas
Print version ISSN 0034-7418
Rev. colomb. cienc. quim. farm. vol.42 no.1 Bogotá Jan./June 2013
Artículo de investigación científica
El estudio de estabilidad en el proceso del desempeño de los sensores y biosensores, basados en los polímeros conductores en medio fuertemente ácido
Stability study in the performance of sensors and biosensors based on conductor polymers in strong acidic media
Volodymyr Valentynovych Tkach•, Vasyl´ Vasyl´ovych Nechyporuk, Petro Ivanonych Yagodynets´
• Universidad Nacional de Chernivtsi, Ucrania. Correo electrónico: nightwatcher2401@gmail.com.
Recibido para evaluación: 17 de marzo de 2013.
Aceptado para publicación: 12 de abril de 2013.
RESUMEN
Por medio del desarrollo del modelo matemático y su análisis (aplicándose la teoría de estabilidad lineal y el análisis de bifurcaciones) se investigó el comportamiento electroquímico, observado en el caso del desempeño de los sensores y biosensores electroquímicos basados en los polímeros conductores en una solución altamente ácida. Fueron derivadas las condiciones de estabilidad del estado estacionario; de las inestabilidades oscilatorias y monotónicas para el desempeño del biosensor en modo de potencia estática. Los resultados del análisis para el caso del medio fuertemente ácido se compararon con los anteriormente obtenidos para el de la solución neutral y básica; por lo cual, así pudo ser inferida la conclusión sobre la influencia del pH al funcionamiento de los sensores y biosensores electroquímicos.
Palabras clave:polímeros conductores, sensores y biosensores electroquímicos, potencial de hidrógeno, oscilaciones electroquímicas, estado estacionario estable.
SUMMARY
Developing and constructing the mathematical model (applying the linear stability theory and bifurcation analysis), the electrochemical behavior, observed during the work of the CP-based electrochemical sensors and biosensors in strongly acid solution, was investigated. The conditions for the steady-state stability and oscillatory and monotonic instabilities were derived for the work of the biosensor in potentiostatic mode. The results of the analysis for the case of strongly acid solution were compared to the previously obtained for the case of neutral and basic solution and in such way it´s possible to make conclusions about the influence of pH on the functioning of sensors and biosensors.
Key words:conducting polymers, electrochemical sensors and biosensors, hydrogen potential, electrochemical oscillations, stable steady-state
INTRODUCCIÓN
La Química Electroanalítica, utilizando los métodos electroquímicos para los fines analíticos, es una de las más importantes ramas de la Química Analítica. Los métodos electroquímicos utilizados para la detección son más precisos que los químicos y, además, hoy son utilizados no solo para la detección de sustancias inorgánicas, sino también para determinar las concentraciones de sustancias orgánicas.
Una de las investigaciones más importantes de la Química Electroanalítica es acerca de la confección de los sensores y biosensores basados en los nuevos materiales y los polímeros conductores (PC) [1-10]; siendo unos de los materiales más estudiados durante las últimas décadas que pueden servir para esta confección.
Esto es posible porque los polímeros conductores son capaces de combinar en sí las propiedades de los plásticos (bajo peso, resistencia a la corrosión, flexibilidad, versatilidad de formación), la conductividad metálica y la facilidad de su propia modificación (modificándose las condiciones de la síntesis es posible modificar las propiedades del polímero, bien como poniéndolo en reacción con otras sustancias). Además, los sensores y biosensores electroquímicos, basados en los PC (neutrales o dopados, normales o sobreoxidados [11]), manifiestan la señal electroquímica, fácilmente interpretable. Además, en la mayoría de los casos es posible regenerar estos sensores.
Sin embargo, como ya se describió en los artículos de revisión [2, 3] y en la tesis [5] (bien como en los trabajos en que habían sido dadas las referencias en los textos), el desempeño de tales sensores en el medio altamente ácido puede ser influenciado por el comportamiento de los protones (o derivados, como iones hidronio). Estos pueden:
- Entrar en la reacción con los sitios de reacción específica entre el polímero conductor y analito (la principal en el proceso de la detección [1-11]) [2, 5] hasta bloquearlos.
- Entrar en la reacción con el propio analito, modificándolo y transformándolo en las sustancias, no capaces de entrar en la reacción específica, en cuyo fondo tiene su base el desempeño del sensor.
- Entrar en la reacción con el polímero conductor (reacción posible, especialmente para el caso de polipirrol sobreoxidado [11-14]).
- Siendo los protones, el analito y unos de los productos de la reacción electroquímica, pueden, por mínimo, dificultar su propia detección.
- Además, el comportamiento de los protones puede generar inestabilidades electroquímicas (oscilatoria y monotónica). Su presencia ya fue confirmada por nuestro grupo [4, 6-10] y experimentalmente observada en [5, 15] para el medio neutral. En el medio altamente ácido, las inestabilidades pueden ser causadas no solo por los factores mencionados en los trabajos anteriores, sino también por los del comportamiento de los protones.
Puesto así, para estimar la influencia del potencial de hidrógeno de la solución al desempeño de sensores y biosensores desde el punto de vista de estabilidad de los estados estacionarios, es preciso desarrollar el modelo matemático, capaz de describir de forma adecuada los procesos en este sistema. Esta investigación es muy importante para la detección del mecanismo de desempeño en el biosensor, por cuanto el comportamiento de los protones tiene una fuerte influencia a este proceso.
LA INFLUENCIA DE LOS PROTONES AL DESEMPEÑO DEL SENSOR O BIOSENSOR EN EL MEDIO ALTAMENTE ÁCIDO CON Y SIN FORMACIÓN AUTOCATALÍTICA DE LOS PROTONES. EL CASO DE LA REACCIÓN ESPECÍFICA DE PROTONES CON EL ANALITO (ACIDOFOBIA)
Para la descripción matemática del proceso de la detección de una sustancia (inerte o no a los protones) con el sensor sin mediador, nosotros introducimos las tres variables:
- c – la concentración del analito en la capa presuperficial.
- Θ – el grado de reducción del revestimiento sensitivo (para los biosensores enzimáticos, de reducción de los fragmentos de la enzima).
- h – la concentración de los protones en la capa presuperficial.
Se supone que el reactor se está agitando intensamente (y entonces podemos menospreciar la influencia de la convección), que el electrolito del soporte (que contiene uno de los dopantes) está en exceso (y por tanto podemos menospreciar la influencia del flujo de la migración y la participación de uno de los dopantes en la reacción) y que los perfiles de las concentraciones del monómero y de la sustancia en la capa presuperficial son lineales y el espesor de la capa es constante e igual a δ.
Se tratará de un modelo general, capaz de estimar la influencia de diferentes posibilidades del comportamiento de los protones en la solución altamente ácida durante el proceso de la detección, descritas arriba.
El analito en la capa presuperficial. Entra en la capa difundiéndose por el interior de la solución y entra en la reacción con el grupo específico. Además, el analito puede entrar en la reacción con los protones. Puesto así, la ecuación de balance será descrita como:
Siendo Δ el coeficiente de la difusión del analito, cb la concentración del analito en el interior de la solución, r1 la velocidad de la reacción específica "analito-polímero conductor" y H1 la velocidad de la posible reacción entre los protones y el analito.
La forma reducida del polímero conductor modificado. Se forma por medio de la reacción "analito-polímero conductor" [2] y desaparece oxidada electroquímicamente. Puede también recibir ataques de los protones de diferentes maneras. Así siendo, la ecuación de su balance será descrita como:
Siendo r2 la velocidad de la reacción electroquímica y H2 la de la reacción provocada por los protones.
Los protones. Entran en la capa presuperficial por medio de su difusión. Además, es posible su formación en la reacción electroquímica, como en el caso del biosensor PQQ-modificado [2, 9]. Ellos pueden entrar en la reacción con el analito (H1) y la forma reducida del polímero conductor modificado (H2) de diferentes maneras. Por eso, la ecuación de su balance
Siendo D el coeficiente de la difusión de los protones, hb la concentración de los protones en el interior de la solución.
El caso de la formación auto catalítica de los protones, el presente modelo sufrirá modificaciones, que se indicarán abajo.
Siendo k1, k2, kH1 y kH2 las constantes de las velocidades de los procesos correspondientes, n la cantidad de los electrones transportados durante el proceso de la detección, F la constante de Faraday (F = NAe), R la constante universal de gases, T la temperatura absoluta, φ0 el salto del potencial en la capa doble relativamente al potencial de la carga cero.
Siendo φ1 el salto del potencial en la CD entre las partes oxidadas y reducidas de ella, K1 y K0 describen las capacitancias integrales de las partes respectivas de la CD.
RESULTADOS Y DISCUSIÓN
Describimos el comportamiento en este sistema usando la teoría de la inestabilidad lineal. La matriz funcional de Jacobi puede ser descrita como
Siendo:
Las condiciones del estado estacionario estable: la ecuación característica para este sistema se describirá como
Siendo:
Para investigar la inestabilidad lineal, usamos el criterio de Routh-Hurwitz.
Él requiere que para un estado estacionario estable los menores de los elementos de la diagonal principal de la matriz de Hurwitz
sean positivos. Los menores de la diagonal principal se ven comoSe puede ver que en Δ3 = CΔ2, la condición de la estabilidad será descrita como C>0. Para simplificar el análisis, vamos a introducir nuevas variables y así el jacobiano será escrito como
Aplicándosele las condiciones de estabilidad de estado estacionario, se obtendrán los valores críticos, correspondientes al margen de estabilidad.
La inecuación (17) puede ser interpretada de la siguiente manera. El estado estacionario es estable cuando la difusión de los protones da más impacto a la concentración de los protones en la capa presuperficial que sus reacciones. El aumento de la concentración de los protones (H1y H2) hace que el estado estacionario sea menos estable. Teniendo en cuenta el hecho de que la región del estado estacionario estable es correspondiente a la de la dependencia lineal entre el parámetro electroquímico y la concentración de analito, puede concluirse que la disminución de pH hace más difícil la interpretación de la señal analítica. Esto está de acuerdo con los datos experimentales, mencionados en los trabajos [1-3, 11, 12, 15].La inestabilidad monotónica, cuya condición es ? = 0, ocurre en la condición de
En esta condición en el sistema existe la "multiplicidad" de los estados estacionarios entre los cuales solo se escoge uno, que se destruye después del cambio de las condiciones.
La inestabilidad oscilatoria se realiza en las condiciones de la bifurcación de Hopf. Para encontrar las condiciones de la inestabilidad del oscilador, se debe resolver la ecuación:
Siendo B1 = -A; B2 = B; B3 = -C, y la condición obligatoria es B2 > 0.
La condición precisa se realiza si la diagonal principal de Jacobi contiene los elementos positivos. Se puede ver que el elemento W1 puede ser negativo (y así –W1 en el elemento a22 será positivo) en el caso de la oxidación anódica de los reductores fuertes. Cuanto más fuerte reductor sea el analito, tanto menor es Φ0.
El caso de la formación autocatalítica de protones. En tal caso, el modelo sufre alteraciones:
- a) La formación autocatalítica de protones es más probable en la reacción con el sitio activo de sensor o biosensor. Siendo así, en esta reacción no habrá la posibilidad de la "salida" de los protones del sistema, sino que su "fuente" y la velocidad correspondiente a este caso aparecerán en la ecuación de balance con la señal positiva:
- b) La condición de la estabilidad del estado estacionario y de la estabilidad monotónica serán alteradas:
- La inecuación (21), comparada con la (17), demuestra que la aparición de la formación autocatalítica de los protones hace que la región topológica de los estados estacionarios estables sea aún más "estrecha". Para la inestabilidad monotónica la condición será alterada:
- c) Será posible una causa más del comportamiento oscilatorio en el caso de H2 > 0, que es la influencia de la formación autocatalítica de los protones.
En el caso de la formación autocatalítica de la forma reducida del polímero conductor. Las diferencias entre el caso principal y este, para el caso de la solución fuertemente ácida, prácticamente no son diferentes de la del caso de la solución neutral, descrita en [9].
Este modelo general puede ser aplicado para los casos particulares de la ausencia de la reacción de los protones con el analito (H1 = 0) y con el polímero conductor (H2 = 0).
Además, este modelo es capaz de describir el proceso de modificación de los polímeros conductores en el medio altamente ácido, usado para la confección de los polímeros conductores.
CONCLUSIONES
- 1. El comportamiento electroquímico, observado durante el proceso del desempeño del sensor o biosensor en el medio altamente ácido, es más complicado que para el medio neutral.
- 2. El aumento de la concentración de los protones no favorece a la estabilidad del estado estacionario y a la precisión del sensor. La formación autocatalítica de los protones lo favorece.
- 3. La inestabilidad monotónica ocurre en los valores marginales entre las regiones topológicas, correspondientes a los estados estacionarios estables e inestables.
- 4. La inestabilidad oscilatoria ocurre, como para el medio neutro, en el caso de la oxidación anódica de los reductores fuertes. Otras causas de este tipo de comportamiento pueden ser las formaciones autocatalíticas de los protones y de la forma reducida del polímero conductor (por ejemplo, modificado por el grupo del factor de una enzima).
- 5. Se trata de una estructura disipativa temporal, cuya existencia es mantenida por la presencia del analito
REFERENCIAS
1. V.M. de Andrade, "Confecção de biossensores através da imobilização de biocomponentes por eletropolimerização de pirrol", Tesis de Maestría en Ingeniería, Universidade Federal do Rio Grande do Sul, Porto Alegre, 2006. [ Links ]
2. A. Ramanavicius, A. Ramanaviciene, A. Malinauskas, Electrochemical sensors, based on conducting polymer polypyrrole, Electrochim. Acta, 51, 6025 (2006). [ Links ]
3. T. McQuade, A. Pullen, T.M. Swager, Conjugated polymer based chemical sensors, Chem. Rev., 100, 2537 (2000). [ Links ]
4. V. Tkach, V. Nechyporuk, P. Yagodynets, The mathematical description of sensor properties of nanocoatings obtained by electropolymerization of heterocyclic compounds, Abstracts 7th Nanoscience and Nanotechnology conference, 26th of June – 1st of July 2011, Istanbul, 2011, p. 173. [ Links ]
5. J.P. Tosar-Rovira, "Estudio de la inmovilización de oligonucleótidos a electrodos modificados de oro: polipirrol, y detección electroquímica de secuencias complementarias", Tesis de Licenciatura en Bioquímica, Universidad de la República, Montevideo, 2008. [ Links ]
6. V.V. Tkach, V.V. Nechyporuk, P.I. Yagodynets, Yu.V. Meslyuk, Mathematical model of the work of the mediated conducting polymer sensors with the use of the polymers of heterocyclic compounds, Rev. Soc. Quím. Perú, 77, 259 (2011). [ Links ]
7. V.V. Tkach, V.V. Nechyporuk, P.I. Yagodynets, Yu.V. Meslyuk, The mathematical modeling of the sensor functions of mediated conductive polymer sensors obtained by electropolymerization of heterocyclic compounds, 2nd International Conference "Advances in Heterocyclic Chemistry", 25-27th of September 2011, Tbilisi, Georgia, 2011, pp. 101-102. [ Links ]
8. V. Tkach, V. Nechyporuk, P. Yagodynets´, I. Rusnak, The CP-based electrochemical biosensors with autocatalytic stage in their function and the mathematical description of their work, Orbital Elec. J. Chem., 4, 136 (2012). [ Links ]
9. V. Tkach, V. Nechyporuk, P. Yagodynets´, A investigação matemática do desempenho de biossensores eletroquímicos enzimáticos baseados nos polímeros condutores, Rev. Colomb. Cienc. Quím. Farm., 41, 203 (2012). [ Links ]
10. V. Tkach, V. Nechyporuk, P. Yagodynets´, A descrição matemática do desempenho de sensores e biossensores eletroquímicos, baseados nos polímeros condutores, no modo potenciodinâmico da voltagem constante, Livro de Resumos do XVIII Encontro Luso-Galego de Química, 28 a 30 de Novembro 2012, Vila Real, Portugal, 2012, p. 29. [ Links ]
11. D. Zane, G.B. Appetecchi, C. Bianchini, An impedimetric glucose biosensor, based on overoxidized polypyrrole, Electroanal., 23, 1134 (2011). [ Links ]
12. A. Ersöz, V. Gavalas, L. Bachas, Potentiometric behavior of electrodes based on overoxidized polypyrrole films, Anal. Bioanal. Chem., 372, 386 (2002). [ Links ]
13. V. Tkach, V. Nechyporuk, P. Yagodynets´, A descrição matemática do comportamento eletroquímico durante o processo da sobreoxidação anódica dos polímeros condutores no meio muito ácido, Orbital Elec. J. Chem., 4, 39 (2012). [ Links ]
14. V.V. Tkach, V.V. Nechyporuk, P.I. Yagodynets´, La investigación matemática de la sobreoxidación electroquímica de polipirrol en el modo potenciostático en el medio fuertemente ácido, XXVI Congreso Peruano de Química "Mariano Eduardo de Rivero y Ustáriz" 17 al 19 de octubre de 2012, Arequipa, Perú, 2012, p. 134. [ Links ]
15. D. Zane, G.B. Appetecchi, C. Bianchini, An impedimetric glucose biosensor, based on overoxidized polypyrrole, Electroanal., 23, 1134 (2011). [ Links ]