Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Colombiana de Ciencias Químico - Farmacéuticas
versión impresa ISSN 0034-7418
Rev. colomb. cienc. quim. farm. vol.42 no.2 Bogotá jul./dic. 2013
Artículo de investigación clínica
Análisis epidemiológico sobre la incidencia y resolución de las infecciones por el virus del papiloma humano en mujeres sometidas a un estudio de seguimiento retrospectivo
Epidemiological analysis of the incidence and resolution of the infection by the Human Papillomavirus in women undergoing a retrospective follow-up study
Erika Gilma Vega Ruiz1,2, Ricardo Sánchez1, José Manuel Lozano1,2*
1Universidad Nacional de Colombia, Bogotá, D. C., Colombia.
2Fundación Instituto de Inmunología de Colombia (fidic), carrera 50 No. 26-20, Bogotá, D. C., Colombia. *Correos electrónicos: jmlozanom@unal.edu.co y jm_lozano@fidic.org.co.
Recibido para evaluación: 17 de diciembre de 2012.
Aceptado para publicación: 23 de octubre de 2013.
RESUMEN
Existen pocos estudios longitudinales en Colombia que abarquen población de distintas zonas del país para el entendimiento de la dinámica de la infección del virus del papiloma humano (VPH). Una muestra representativa de 1.433 mujeres provenientes de tres ciudades de Colombia con edades de 18-60 años y visitas cada 6 ± 2 meses durante dos años, fueron sometidas a la prueba de Papanicolau y reacción en cadena de la polimerasa (pcr). Las mujeres presentaron una tasa de incidencia de 2,49 infecciones/1.000 mujeres/día (IC 95%; 2,25-2,75); la tasa de incidencia para lesiones fue de 0,043 lesiones/1.000 mujeres/día (IC 95%; 0,021-0,086), mientras que para la resolución de la infección la tasa fue de 2,47 infecciones resueltas/1.000 mujeres/día (IC 95%; 2,25-2,71). Un subgrupo de mujeres que presentaron lesiones en la primera visita, tuvo una tasa de 3,92 regresiones de lesión/1.000 mujeres/día (IC 95%; 2,97-5,17). De 619 mujeres con infección, el 27% hizo infección persistente y solo el 10% de 55 mujeres con lesión cervical mantuvo esta condición. Las tasas demuestran que fue frecuente la incidencia y la resolución de las infecciones, mientras que el estudio epidemiológico de las lesiones requiere un mayor número de mujeres y una cohorte de mayor duración.
Palabras clave:VPH, incidencia, resolución de la infección, regresión de la lesión, persistencia, tasa.
SUMMARY
There are few longitudinal studies in Colombia that cover people from different parts of the country to allow understanding the infection dynamics by Human Papilloma Virus (HPV). A representative sample of 1433 women from three Colombian cities aged 18-60 years which were visited every 6 ± 2 months during two years, were submitted to the Papanicolau and reaction Polymerase chain (pcr) tests. Infection incidence was 2.49 /1000 women/day (CI 95%, 2.25-2.75), the incidence rate for lesion was 0.043 lesion/1000 women/day (CI 95%, 0.021-0.086), while for infection clearance the rate was 2.47 infection clearance/1000 women/day (CI 95%, 2.25-2.71). A women´s subgroup who reported having lesions on the first visit, had a rate of 3.92 lesion-regressions/1000 women/day (CI 95%, 2.97-5.17). From a group of 619 women with infection, 27% reported a persistent infection and only 10% of 55 women with cervical lesion kept this condition. Data showed that incidence and infection resolution was frequent, while the epidemiological study of lesions would require a greater number of women and a cohort of longer duration.
Key words: HPV, incidence, infection clearance, lesion regression, persistence, rate.
INTRODUCIÓN
La infección por el virus del papiloma humano (VPH) es un factor obligado para el desarrollo del cáncer cervical [1]; la asociación entre la infección por el vph y el cáncer cervical invasivo es muy estrecha, específica y consistente, y es independiente de otros factores de riesgo conocidos [2]. Se debe tener en cuenta que muchas de las infecciones con anormalidades cervicales o sin ellas son transitorias, aproximadamente el 90% de la población hace una resolución de la infección en 24 meses [3]; por tanto, se han diseñado distintos estudios de seguimiento para ver cómo se relaciona la presencia viral en pacientes con citología sana con el riesgo de padecer cáncer de cuello de útero [4, 5], o miden otras posibles variables involucradas con el estilo de vida de las pacientes, encontrando resultados diversos y en algunos casos contradictorios a lo esperado [6].
Los estudios transversales no permiten determinar la evolución de las infecciones producidas por el VPH; es decir, no se puede establecer incidencia, tiempo de resolución de las lesiones cervicales o persistencia de la infección viral. Por tanto, se ha visto la necesidad de desarrollar estudios longitudinales, también llamados de seguimiento o de cohorte, para evaluar el comportamiento del sistema inmune frente a la infección por el virus a través del tiempo. Estos estudios muestran que la mayoría de las infecciones son transitorias y solo las mujeres que albergan infecciones persistentes logran desarrollar una lesión escamosa intraepitelial cervical [7]; otros factores son probablemente influenciados por la historia natural de las infecciones por el VPH.
En la mayoría de los estudios de cohorte, la incidencia se mide desde el momento en que no se detecta infección por uno o varios tipos virales, que corresponde a la primera visita en el seguimiento, hasta la detección del adn viral que concierne a la última visita. Se ha reportado que la incidencia por el vph en estudios de seguimiento es alta, especialmente por los tipos del vph de alto riesgo (VPHAR) [3].
Determinantes virales, incluyendo el tipo y la carga viral, han sido identificados como marcadores de persistencia o neoplasia cervical [8]. Sin embargo, factores de riesgo medioambientales pueden tener un papel importante en la carcinogénesis cervical, aunque no se sabe con certeza en qué estadio de la infección estos cofactores son influenciables [9]. Además, la definición de persistencia ha variado significativamente entre los estudios y cada estudio de cohorte difiere en cuanto a los métodos de detección y los tiempos del seguimiento [10]. En cuanto a la resolución de las infecciones, algunos estudios han reportado que las infecciones por el vphar se eliminan más lentamente que las producidas por el vph de bajo riesgo (VPHBR), y que la resolución de las infecciones está, a su vez, relacionada con la duración de la infección. Estudios más recientes sugieren que las infecciones por el vph-16 tienen una tendencia más baja a la resolución que otros tipos del VPH [11].
Sin embargo, los estudios de seguimiento que se han llevado a cabo han sido en su mayoría en mujeres jóvenes [12, 13, 14, 15, 16]. En Colombia se han realizado estudios en mujeres jóvenes y adultas [17], aunque todas las mujeres enroladas pertenecían a la ciudad de Bogotá. Este estudio presenta hallazgos sobre la incidencia, resolución y persistencia de la infección por el vph en mujeres jóvenes y adultas con lesión cervical o sin ella, que han sido sometidas a una cohorte en tres zonas geográficas de Colombia.
MATERIALES Y MÉTODOS
Se reclutaron durante el 2007 y 2009, mujeres entre los 18 y 60 años de edad que asistieron al servicio de citología de distintos centros de salud: hospital de Engativá (Bogotá, D. C.), hospital San Rafael de Girardot (Girardot), hospital San Juan Bautista (Chaparral). El seguimiento se realizó cada 6 ± 2 meses; cada participante se sometió a un examen pélvico para la extracción de células cervicales para la citología y detección del vph; además, debía llenar una encuesta con los datos sociodemográficos y firmar el consentimiento informado. Todos los procedimientos realizados en el presente estudio los aprobaron los Comités de Ética de cada uno de los hospitales que participaron en él.
La muestra de células endocervicales para la detección del vph se mantuvo en tubo de vidrio con 2,5 ml de etanol al 95% [18, 19] y se almacenó a 0 oC, para su posterior procesamiento. Cada muestra se centrifugó y se lavó una vez con PBS; después se incubó en 100 µL de buffer de lisis (10 mM Tris-HCL [pH 7,9], 0,45% Nonidet p-40, 0,45% Tween 20 µg/ml y 60 µg/ml de proteinasa K) a 60 oC por 1 h y a continuación a 95 oC durante 10 min [20]. A todas las muestras se les realizó una amplificación usando los iniciadores GH20/PC04 de la β-globina humana, prueba utilizada para garantizar la presencia de adn [21, 22, 23, 24].
A los sobrenadantes obtenidos del tratamiento con buffer de lisis se les practican dos protocolos de pcr; el primero, utilizando los iniciadores consenso GP5+/GP6+ y el segundo con los iniciadores MY09/MY11, para amplificar la región L1 de genoma del vph de alto riesgo [23, 24, 25, 26].
La reacción con los iniciadores GP5+/GP6+ [23], se realizó a un volumen final de 20 µl, con las siguientes condiciones: 2 µl de buffer 10x (Bioline ), 100 µM de cada dNTP (Bioline ), 3 mM MgCl2 (Bioline ), 1 U de Taq polimerasa (Bioline ) y 40 ?mol de cada iniciador. La mezcla de pcr se desnaturalizó a 94 oC por 10 min, seguida de 35 ciclos de amplificación en termociclador Perkin Elmer CETUS-USA; cada ciclo consistió en 94 oC por 30 s, 42 oC por 30 s y 72 oC por 30 s; la elongación final se realizó a 72 oC durante 7 min.
La reacción con los iniciadores MY09/MY011 [25], se efectuó con un volumen final de 20 µl. La mezcla de pcr se desnaturalizó a 94 oC por 5 min, seguida de 40 ciclos de amplificación; cada ciclo consistió en 94 oC por 30 s, 51 oC por 45 s y 72 oC por 45 s; la elongación final se realizó a 72 oC durante 7 min.
Como control negativo para ambas reacciones, se utilizó agua free (GIBCO) [27] y como control positivo, células Sf21 infectadas con adn de la proteína L1 del vph-16 y vph-18, la cual se extrae a partir de epitelios cervicales infectados [28]. Las pcr se analizaron mediante electroforesis en gel de agarosa al 2%, teñido con SYBR safe (Invitrogen), utilizando el escáner molecular imagen Fx BIO RAD® y el software Quantity One®.
Las muestras positivas para uno o ambos protocolos con los iniciadores genéricos se consideraron positivas para el vph; por tanto, se sometieron a pcr con iniciadores
tipo-específicos, para evidenciar el tipo del vph involucrado en la infección. Estos iniciadores se alinean con regiones de las proteínas tempranas E5, E6 y E7 de los vphar 16, 18, 31, 33, 45 y 58, los cuales se encuentran relacionados con el 90% de los casos de cáncer cervical reportados en el ámbito mundial [24, 25, 26, 27, 28, 29].
El análisis estadístico para el presente estudio fue de tipo descriptivo, se utilizó el programa STATA 9.0® para el procesamiento de los datos. La incidencia, resolución y persistencia de las infecciones se expresaron en función de tasas, obtenidas a partir de la tabulación de los resultados de pcr y la información recopilada en la historia clínica del paciente; la curva de Kaplan-Meier permitió representar de forma gráfica los distintos comportamientos de la infección por el vph en la población en estudio, teniendo en cuenta las entradas y salidas de los participantes del seguimiento, en tiempos distintos.
RESULTADOS Y DISCUSIÓN
Para el estudio se reclutaron 1.433 mujeres durante el 2007 y 2009, de las cuales 1.245 contaban con exámenes completos; es decir, poseían un resultado de muestra satisfactoria para la pcr bien sea negativo o positivo, resultado de citología, diligenciamiento y firma de la encuesta para la historia clínica y el consentimiento informado, para cada uno de los seguimientos en los cuales haya participado la paciente. El promedio de edad en las participantes del estudio fue de 42 años, el intervalo y duración de las visitas osciló entre seis meses y un año, las mujeres permanecieron entre un año y dos años en el estudio.
Estas pacientes se agruparon según las características de la línea base en el estudio, para los distintos análisis de incidencia, persistencia y resolución. De esta manera se obtuvo un grupo de 526 mujeres que iniciaron el estudio sin infección (pcr negativa) y sin lesión (citología negativa), y otro grupo de 619 mujeres que en la visita inicial presentaban infección (pcr positiva) con lesión cervical o sin ella.
Con el primer grupo de 526, se pudieron obtener resultados acerca de la incidencia de infección por el vph y de las lesiones; para esto se analizaron dos desenlaces: para infección y para lesión.
Desenlace de la infección
Las 526 mujeres de este subgrupo aportaron para este estudio un momento en riesgo de 150.022 días; esto es, el período durante el cual la participante está en riesgo de desarrollar infección, en este caso, durante el seguimiento.
Para este estudio, la tasa de incidencia fue de 2,49 infecciones/1.000 mujeres/día (IC 95%; 2,25-2,75). El 50% de la población se infectó a los 254 días (mediana de incidencia de la infección) con un total de 373 mujeres que presentaron infección en algún momento de la cohorte.
La curva de Kaplan-Meier, obtenida para este grupo, permite observar que aproximadamente a los 1.000 días del seguimiento es baja la probabilidad de encontrar alguna mujer que no se haya infectado durante la cohorte (figura 1 ).
Al correlacionar los datos obtenidos con otros estudios de cohorte se observan diferencias, ya que las condiciones y características de las poblaciones difieren. Safaeian y col. en el 2010 [30] reportaron una tasa de 0,10 infecciones/1.000 mujeres/día para el vph-16 en 291 mujeres; y una tasa de 0,05 infecciones/1.000 mujeres/día, en 178 mujeres para el vph-18 en una cohorte realizada en Costa Rica.
La curva de Kaplan-Meier, obtenida para este grupo, permite observar que aproximadamente a los 1.000 días del seguimiento es baja la probabilidad de encontrar alguna mujer que no se haya infectado durante la cohorte (figura 1).
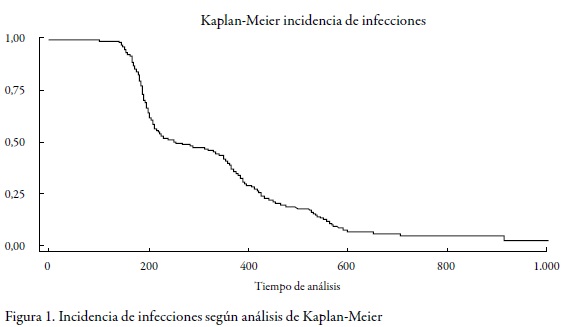
La característica distintiva del análisis con el método de Kaplan-Meier, es que la proporción acumulada que sobrevive se calcula para el tiempo de supervivencia individual de cada paciente y no se agrupan los tiempos de supervivencia en intervalos. Por esta razón, es especialmente útil para estudios que utilizan un número pequeño de pacientes. El método de Kaplan-Meier incorpora la idea del tiempo al que ocurren los eventos.
Desenlace de la lesión
Para este desenlace, las 526 mujeres de este subgrupo aportaron un momento en riesgo de 187.211 días, período durante el cual cada participante está en riesgo de desarrollar lesión, para este caso, durante el seguimiento.
En este estudio, la tasa de incidencia fue de 0,043 lesiones/1.000 mujeres/día (IC 95%; 0,021-0,086). No fue posible determinar una mediana de incidencia de la lesión, solo ocho mujeres desarrollaron lesión en este grupo durante el seguimiento.
La curva de Kaplan-Meier, obtenida para este grupo, permite observar que la mayoría de las participantes de este subgrupo mantienen la condición inicial, siendo muy baja la probabilidad de encontrar mujeres que desarrollen lesión durante el seguimiento (figura 2 ).
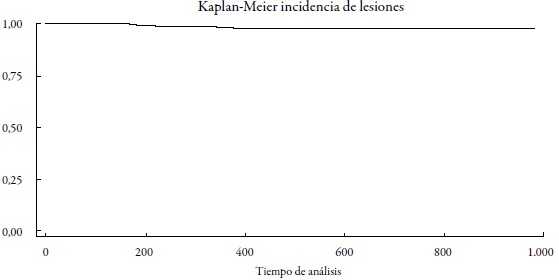
Con el segundo grupo de 619 participantes se pudieron obtener resultados acerca de la resolución y persistencia de la infección.
Los datos obtenidos son comparables con otros estudios de cohorte que determinan incidencia de lesiones, como el estudio de Louvanto y col. en el 2010 [11], quienes reportaron una tasa de 0,0273 lesiones/1.000 mujeres/día en una cohorte de 329 mujeres en Finlandia, donde 14 desarrollaron lesión. Esto se explica por el hecho de que las lesiones premalignas tardan en desarrollarse entre 5 a 10 años, y en un estudio de cohorte de dos años es muy difícil medir la incidencia de las lesiones.
La curva de Kaplan-Meier, obtenida para este grupo, permite observar que la mayoría de las participantes de este subgrupo mantienen la condición inicial, siendo muy baja la probabilidad de encontrar mujeres que desarrollen lesión durante el seguimiento.
Desenlace de resolución de las infecciones
En este desenlace se incluyeron las 619 mujeres de este subgrupo que aportaron un momento en riesgo de 180.930 días, período durante el cual cada participante está en riesgo de desarrollar lesión, para este caso, durante el seguimiento.
En este estudio, la tasa fue de 2,47 infecciones resueltas/1.000 mujeres/día (IC 95%; 2,25-2,71). El 50% de la población hizo resolución a los 260 días (mediana de resolución de la infección). Durante el seguimiento en este grupo, 447 mujeres resolvieron la infección y, por tanto, 172 (27,8%) hicieron una infección persistente.
La curva de Kaplan-Meier, obtenida para este grupo, permite observar que aproximadamente a los 800 días del seguimiento es baja la probabilidad de encontrar alguna mujer que no haya hecho resolución de la infección (figura 3 ).
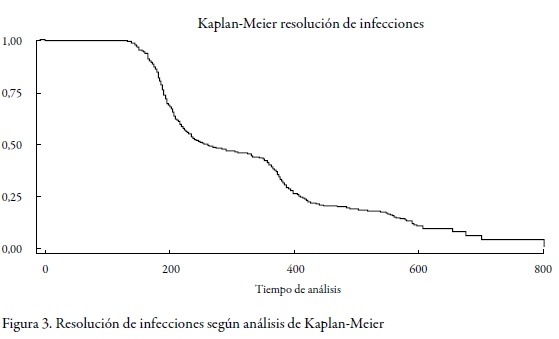
Desenlace de regresión de las lesiones
Dentro de este grupo de mujeres con infección al inicio del seguimiento, se encontró un subgrupo de mujeres que además de presentar infección por el vph, también presentaron lesiones cervicales en sus citologías y aunque fue un grupo pequeño se analizó en ellas la regresión de las lesiones durante el seguimiento.
Este subgrupo correspondió a 55 mujeres que contribuyeron con un momento en riesgo de 12.748 días.
Para este grupo de mujeres, la tasa de regresión para las lesiones fue de 3,92 regresiones/1.000 mujeres/día (IC 95%; 2,97-5,17). El 50% de la población hizo regresión a los 214 días (mediana de regresión de la lesión). 50 mujeres hicieron regresión de las lesiones durante el estudio, solo cinco (10%) tuvieron lesiones cervicales persistentes.
La curva de Kaplan-Meier, obtenida para este grupo, permite observar que aproximadamente a los 600 días del seguimiento es muy bajo el porcentaje de mujeres con lesión (figura 4 ).
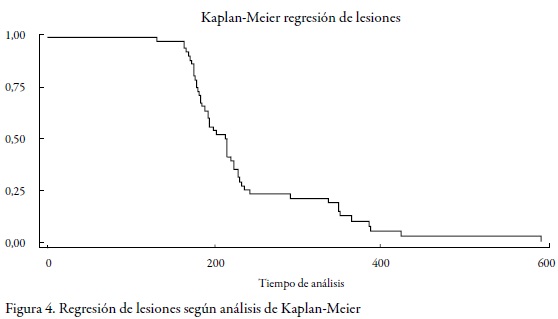
Este tipo de análisis estadístico que se da en función de tasas para las diferentes variables, permite ser aplicado en un estudio donde hay un intervalo considerable entre visita y visita por cada una de las participantes del estudio; eso sumado a las variaciones de la duración en función del tiempo de las mujeres sometidas al seguimiento.
Cabe resaltar que los resultados obtenidos darán la pauta para la realización de otros estudios de cohorte con intervalos más estrictos, mayor duración del estudio y que, además, abarquen la totalidad del territorio colombiano, contribuyendo de esta manera a un conocimiento más aproximado sobre la incidencia y resolución de la enfermedad; pues aunque hasta ahora existen estudios de seguimiento similares a este, ninguno abarca otras zonas del país aparte de la capital (Bogotá), lo cual es muy importante debido a las diferencias socioeconómicas, culturales y climáticas que afectan el comportamiento del virus del papiloma humano en las diferentes poblaciones femeninas y, de igual manera, su aporte para el desarrollo del cáncer de útero.
CONCLUSIONES
Pocos son los estudios de cohorte en Colombia que abarcan poblaciones de distintas zonas del país para el entendimiento de la dinámica de la infección del virus del papiloma humano (vph). Por tanto, el presente estudio no solo abarca la población femenina de diversas zonas del país (Bogotá, Girardot y Chaparral), sino también de diferentes características socioeconómicas y culturales, ya que la problemática de la infección tiene un componente geográfico. Con este estudio se puede vislumbrar un acercamiento en cuanto a la incidencia y resolución de las infecciones por el vph expresado en tasas.
Los resultados reportados tienen semejanzas y diferencias con otros estudios realizados en otros países, lo cual se puede explicar por las diferencias de culturas y costumbres enmarcadas en zonas geográficas del mundo, totalmente distintas.
Este estudio de cohorte puede servir de base a otros estudios que contemplen intervalos estrictos, así como una visita base en donde se pueda partir de mujeres que no han estado en contacto con el virus (mujeres vírgenes) y de esta manera tener una idea más acertada de la incidencia de la infección.
Para los estudios dirigidos hacia la problemática de las lesiones premalignas, malignas y hasta el cáncer cervical, el seguimiento debe abarcar más de cuatro años. De esta manera se podrá observar la aparición y regresión de estas lesiones; de lo contrario, se obtendrán datos como los reportados en este estudio en el grupo de las 55 mujeres, en donde el cambio a través del tiempo no se hizo perceptible.
La implementación de nuevas tecnologías en biología molecular y pruebas diagnósticas estándar y sensibles para detectar la infección de manera temprana, en conjunto con estudios estadísticos, contribuiría a la disminución y tratamiento temprano de esta enfermedad mucho antes de desarrollar el cáncer.
AGRADECIMIENTOS
Expresamos nuestros más sinceros agradecimientos al Grupo Funcional Virología - Biología Molecular de la Fundación Instituto de Inmunología de Colombia (fidic), por el aporte de la información básica necesaria para dar origen a este estudio. Agradecemos a la Asociación de Investigación Solidaria sadar, sin cuyo aporte no hubiese sido posible el desarrollo de la investigación.
REFERENCIAS
1. J.M. Walboomers, M.V. Jacobs, M.M. Manos et al., Human papillomavirus is a necessary cause of invasive cervical cancer worldwide, J. Pathol., 189(1), 12-19 (1999) [ Links ].
2. F. Coutlée, D. Rouleau, A. Ferenczy, E. Franco, The laboratory diagnosis of genital human papillomavirus infections, Can. J. Infect. Dis. Med. Microbiol., 16(2), 83-91 (2005) [ Links ].
3. C. Banura, S. Sandin, L.-J. van Doorn et al., Type-specific incidence, clearance and predictors of cervical human papillomavirus infections (hpv) among young women: A prospective study in Uganda, Infect. Agent Cancer, 5, 7 (2010) [ Links ].
4. G.M. Clifford, S. Gallus, R. Herrero et al., Worldwide distribution of human papillomavirus types in cytologically normal women in the International Agency for Research on Cancer hpv prevalence surveys: A pooled analysis, Lancet, 366(9490), 991-998 (2005) [ Links ].
5. R.C. Gontijo, S.F. Derchain, C. Roteli-Martins et al., Human papillomavirus (hpv) infections as risk factors for cytological and histological abnormalities in baseline PAP smear-negative women followed-up for 2 years in the LAMS study, Eur. J. Obstet. Gynecol. Reprod. Biol., 133(2), 239-246 (2007) [ Links ].
6. H. Richardson, M. Abrahamowicz, P.P. Tellier et al., Modifiable risk factors associated with clearance of type-specific cervical human papillomavirus infections in a cohort of university students, Cancer Epidemiol. Biomarkers Prev., 14(5), 1149-1156 (2005) [ Links ].
7. A.B. Moscicki, J. Palefsky, G. Smith, S. Siboshski, G. Schoolnik, Variability of human papillomavirus dna testing in a longitudinal cohort of young women, Obstet. Gynecol., 82(4 Pt 1), 578-585 (1993) [ Links ].
8. F.X. Bosch, A. Lorincz, N. Muñoz, C.J. Meijer, K.V. Shah, The causal relation between human papillomavirus and cervical cancer, J. Clin. Pathol., 55(4), 244- 265 (2002) [ Links ].
9. Castellsagué, X., F. Bosch, N. Muñoz, Environmental co-factors in hpv carcinogenesis, Virus Res., 89(2), 191-199 (2002) [ Links ].
10. A. Hildesheim, M.H. Schiffman, P.E. Gravitt et al., Persistence of type-specific human papillomavirus infection among cytologically normal women, J. Infect. Dis., 169(2), 235-240 (1994) [ Links ].
11. K. Louvanto, M.A. Rintala, K.J. Syrjänen, S.E. Grénman, S.M. Syrjänen, Genotype- specific persistence of genital human papillomavirus (hpv) infections in women followed for 6 years in the Finnish Family hpv Study, J. Infect. Dis., 202(3), 436-444 (2010) [ Links ].
12. G.Y. Ho, R. Bierman, L. Beardsley, C.J. Chang, R.D. Burk, Natural history of cervicovaginal papillomavirus infection in young women, N. Engl. J. Med., 338(7), 423-428 (1998) [ Links ].
13. A.B. Moscicki, N. Hills, S. Shiboski et al., Risks for incident human papillomavirus infection and low-grade squamous intraepithelial lesion development in young females, jama, 285(23), 2995-3002 (2001) [ Links ].
14. C.B. Woodman, S. Collins, H. Winter et al., Natural history of cervical human papillomavirus infection in young women: A longitudinal cohort study, Lancet, 357(9271), 1831-1836 (2001) [ Links ].
15. D.R. Brown, M.L. Shew, B. Qadadri et al., A longitudinal study of genital human papillomavirus infection in a cohort of closely followed adolescent women, J. Infect. Dis., 191(2), 182-192 (2005) [ Links ].
16. R.L. Winer, N.B. Kiviat, J.P. Hughes et al., Development and duration of human papillomavirus lesions, after initial infection, J. Infect. Dis., 191(5), 731-738 (2005) [ Links ].
17. N. Muñoz, G. Hernández-Suárez, F. Méndez et al., Persistence of hpv infection and risk of high-grade cervical intraepithelial neoplasia in a cohort of Colombian women, Br. J. Cancer, 100(7), 1184-1190 (2009) [ Links ].
18. C.H. Lema, L.V. Hurtado, D. Segurondo et al., Human papillomavirus infection among Bolivian Amazonian women, Asian Pac. J. Cancer Prev., 2(2), 135-141 (2001) [ Links ].
19. J. Cervantes, C. Lema, L. Hurtado et al., Prevalence of human papillomavirus infection in rural villages of the Bolivian Amazon, Rev. Inst. Med. Trop. Sao Paulo, 45(3), 131-135 (2003) [ Links ].
20. Nelson, G.A. Hawkins, K. Edlund et al., A novel and rapid pcr-based method for genotyping human papillomaviruses in clinical samples, J. Clin. Microbiol., 38(2), 688-695 (2000) [ Links ].
21. R.K. Saiki, D.H. Gelfand, S. Stoffel et al., Primer-directed enzymatic amplification of dna with a thermostable dna polymerase, Science, 239(4839), 487-491 (1988) [ Links ].
22. R.K. Saiki, S. Scharf, F. Faloona, K.B. Mullis, G.T. Horn, H.A. Erlich, N. Arnheim, Enzymatic amplification of beta-globin genomic sequences and restriction site analysis for diagnosis of sickle cell anemia, Science, 230(4732), 1350-1354 (1985) [ Links ].
23. A.M. de Roda Husman, J.M. Walboomers, A.J. van den Brule, C.J. Meijer, P.J. Snijders, The use of general primers GP5 and GP6 elongated at their 3´ ends with adjacent highly conserved sequences improves human papillomavirus detection by pcr, J. Gen. Virol., 76(Pt 4), 1057-1062 (1995) [ Links ].
24. M. Camargo, S. Soto-De León, R. Sánchez, A. Pérez-Prados, M.E. Patarroyo, M.A. Patarroyo, Frequency of human papillomavirus infection, coinfection, and association with different risk factors in Colombia, Ann. Epidemiol., 21(3), 204- 213 (2011) [ Links ].
25. W. Qu, G. Jiang, Y. Cruz, C.J. Chang, G.Y. Ho, R.S. Klein, R.D. Burk, pcr detection of human papillomavirus: Comparison between MY09/MY11 and GP5+/GP6+ primer systems, J. Clin. Microbiol., 35(6), 1304-1310 (1997) [ Links ].
26. F. Karlsen, M. Kalantari, A. Jenkins et al., Use of multiple pcr primer sets for optimal detection of human papillomavirus, J. Clin. Microbiol., 34(9), 2095-2100 (1996) [ Links ].
27. S. Soto-De León, M. Camargo, R. Sánchez et al., Distribution patterns of infection with multiple types of human papillomaviruses and their association with risk factors, PLoS One, 6(2), e14705 (2011) [ Links ].
28. S. Soto-De León, R. Sánchez, M.A. Patarroyo, M. Camargo, A. Mejía, M. Urquiza, M.E. Patarroyo, Prevalence of hpv-dna and anti-hpv antibodies in women from Girardot, Colombia, Sex. Transm. Dis., 36(5), 290-296 (2009) [ Links ].
29. D.M. Parkin, M. Almonte, L. Bruni, G. Clifford, M.P. Curado, M. Piñeros, Burden and trends of type-specific human papillomavirus infections and related diseases in the Latin America and Caribbean region, Vaccine, 26(Suppl 11), L1-15 (2008) [ Links ].
30. M. Safaeian, C. Porras, M. Schiffman et al., Epidemiological study of anti-hpv- 16/18 seropositivity and subsequent risk of hpv-16 and -18 infections, J. Natl. Cancer Inst., 102(21), 1653-1662 (2010) [ Links ].













