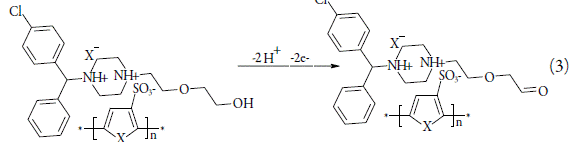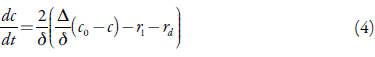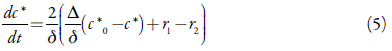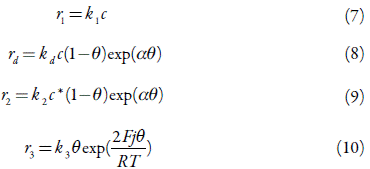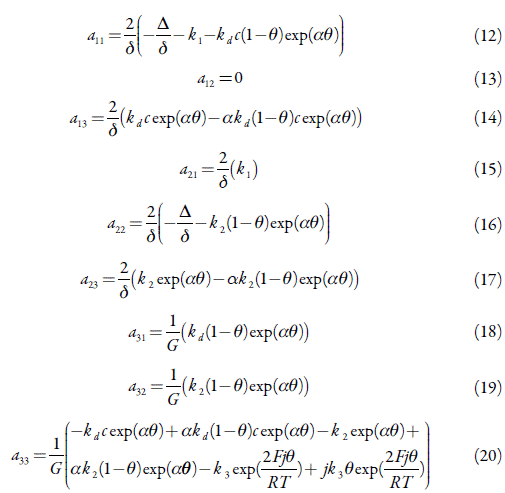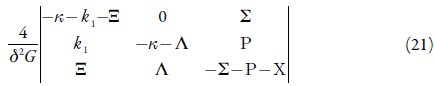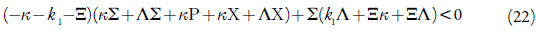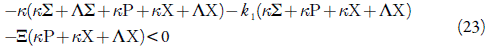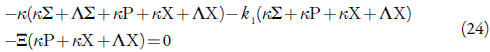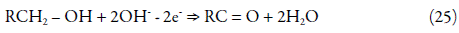INTRODUÇÃO
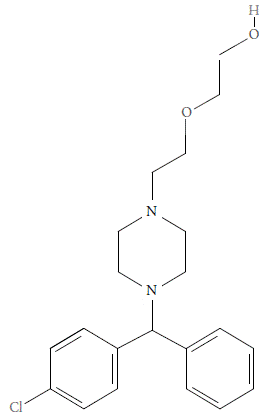
Hidroxizina, isto é, 2-[2-[4-[(4-clorofenil)-fenilmetil]piperazin-1-il]etoxi]etanol, (número CAS: 68-88-2) (Fig. 1) é um fármaco, derivado da piperazina, inibidor dos receptores H1 da histamina [1-4]. É utilizado no tratamento de dermatite atópica ou de contato, urticária e dermografismo [5-8], no entanto, o seu uso também inclui os casos de diversas manifestações alérgicas e cistite [9-10]. Outrossim, ela pode ser usada como hipnótico, ansiolítico, no caso das ansiedades leves e moderadas, e no tratamento de ci-netose (náuseas ou vômitos, induzidas por viagens e movimentos) [11-13].
Sem embargo, a sua ação mantém efeitos colaterais como tontura, sonolência, excitação e prisão de ventre [14-15]. Ademais, durante o seu uso duradouro e excessivo pelas mulheres grávidas pode levar às malformações do feto [16]. Destarte, o desenvolvimento de um método, capaz de detectar a sua concentração de forma mais eficiente, rápida, precisa e exata continua sendo uma tarefa atual [17-20].
Como hidroxizina é uma substância eletroquimicamente ativa, os métodos eletroquímicos podem ser aplicados a ela [21-23], e os polímeros condutores, capazes de combinar as propriedades dos plásticos com a condutividade metálica e de modificar-se facilmente [24-28], também poderiam ser usados na análise deste fármaco.
No entretanto, o uso dos polímeros condutores pode acarretar alguns problemas como:
- o desconhecimento, particularmente, do mecanismo mais provável do desempenho do polímero condutor durante a eletrooxidação do fármaco e, geralmente, do comportamento do polímero na presença do fármaco;
- a possibilidade das instabilidades eletroquímicas, já observadas durante o desempenho dos polímeros condutores experimental [24-28] e teoricamente [29-34].
Ambos os problemas podem ser resolvidos por meio de uma análise mecanística do comportamento eletroquímico da hidroxizina na presença de um polímero condutor especificamente modificado, que se realiza por meio do desenvolvimento e da análise de um modelo matemático, capaz de descrever adequadamente o comportamento do sistema. A modelagem também dá possibilidade de compará-lo com o dos sistemas análogos.
Destarte, o objetivo geral deste trabalho é uma investigação teórica mecanística da eletrooxidação da hidroxizina em meios ácidos sobre um sulfoácido polimérico. Ele se realiza por meio da realização dos objetivos específicos como:
- desenvolvimento do modelo matemático de equações de balanço, que descreve o comportamento no sistema;
- análise do modelo;
- relação entre os resultados da análise do modelo e as observações experimentais;
- comparação do comportamento do sistema com o dos semelhantes [29-34].
O SISTEMA E O MODELO
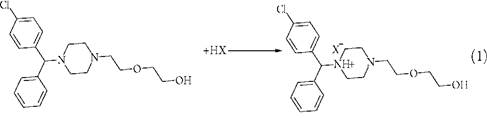
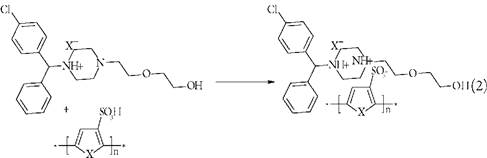
O comportamento da hidroxizina na solução na presença do sulfoácido na superfície e de um outro ácido no eletrólito de suporte merece atenção e, destarte, descrever-se-á agora. Como o fármaco é um derivado de piperazina N,N-disubstituído, ele se comporta como uma diamina ternária, formando o sal duplo com ambos os ácidos. A quaternização na superfície faz com que o fármaco se imobilize com mais eficiência (vide as reações (1 - 2)). Obtém-se, destarte, um caso interessante de dopagem:
A eletrooxidação do fármaco imobilizado realize-se mediante a perda de dois prótons e dois elétrons da hidroxila, conforme a reação:
Em que X é um íon monovalente de um ácido forte, e X- é um fragmento, que faz o polímero condutor aromático ( - CH = CH - , - NH - , - S - , - Se -, em casos mais raros, - O - ).
Haja vista o descrito em cima e o que se descreverá embaixo, introduzimos as três variáveis:
c: a concentração pré-superficial do fármaco não protonizado;
c*: a concentração pré-superficial do fármaco pronizado pelo ácido, presente no ele-trólito de suporte;
θ: o grau de recobrimento da superfície pelo polímero, dopado pelo fragmento do fármaco.
Para simplificar a modelagem, supomos que o reator esteja agitando-se intensamente (para menosprezar o fluxo de convecção), que o eletrólito de suporte esteja em excesso (para menosprezar o fluxo de migração e as despesas do ácido, nele presente). Também é suposto que a distribuição concentracional na camada pré-superficial seja lineal, e a sua espessura, constante, igual a δ. Supõe-se, também, que, no início da reação, o sulfoácido polimérico cubra a superfície inteira.
O fármaco entra na camada pré-superficial mediante a sua difusão e reage tanto com o ácido, presente no eletrólito de suporte, como com o ácido polímero condutor. Destarte, a sua equação de balanço descrever-se-á como:
Em que Δ é o seu coeficiente de difusão, c0 é a concentração do fármaco no interior da solução, r 1 é a velocidade da reação (1) na camada pré-superficial, e r d é a velocidade da reação do sulfoácido com o fármaco não protonizado.
Haja vista a presença do ácido no eletrólito de suporte, as moléculas monoprotonizadas do fármaco estão presentes, não só na camada pré-superficial, mas também no interior da solução. Formando-se durante a reação (1), elas também se difundem do interior da solução, dopando, depois, o polímero conforme a reação (2). Assim sendo, apresentar-se-lhes-á a equação de balanço como:
Em que c0* é a concentração das moléculas do fármaco protonizado no interior da solução, e r2 é a velocidade da reação (2).
A dopagem do polímero pelos fragmentos do fármaco realiza-se tanto pela reação (2), como pela interação dos sulfogrupos com as moléculas não protonizadas da diamina ternária. Dopado, o polímero condutor modificado sofre a oxidação (3). Posto assim, a sua equação de balanço ver-se-á descrita como:
em que G é a concentração máxima do polímero condutor, dopado pelo fármaco, e r3, reação da sua oxidação.
As velocidades das respectivas reações podem descrever-se como:
Em que os parâmetros k são constantes das velocidades das respectivas reações, α e j descrevem as influências dos processos da dopagem e da eletrooxidação nas capacitân-cias da dupla camada elétrica (DCE), Fé o número de Faraday, R é a constante universal de gases e T é a temperatura absoluta.
Apesar de manifestar algumas semelhanças com os sistemas análogos [28-34], este sistema é diferente, haja vista que a dopagem dá influências para a DCE. O efeito destas influências no comportamento do sistema descrever-se-á embaixo.
RESULTADOS Ε DISCUSSÃO
Para investigar o comportamento do sistema com eletrooxidação da hidroxizina em meio ácido sobre um polímero condutor, substituído por um grupo fortemente ácido, analisamos o conjunto de equações diferenciais (4-6) mediante a teoria de estabilidade linear. A matriz funcional de Jacobi, cujos elementos se calculam para o estado estacionário, pode ser descrita como:
Em que:
Observando os elementos (11), (16) e (20), é possível ver que a instabilidade oscilatória, neste caso, é possível. Outrossim, ela é mais provável que no caso comum do desempenho eletroanalítico dos polímeros condutores, haja vista que há dois fatores responsáveis por tal comportamento contra um em [29-35].
O primeiro fator, comum para este sistema e os semelhantes, são as influências da oxidação eletroquímica nas capacitâncias da DCE. O comportamento oscilatório, causado por elas, descreve-se pela positividade do elemento jk
3
θexp 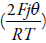
Já o segundo fator, específico para este sistema, são as influências do processo da dopa-gem nas capacitâncias da DCE. O comportamento oscilatório, causado por elas, descreve-se pela positividade dos elementos 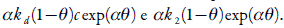
Haja vista a presença dos dois fatores, as oscilações devem ser mais frequentes e de menor amplitude que em [29-35].
Para investigar a estabilidade do estado estacionário, aplicamos ao conjunto de equações diferenciais (4-6) o critério de Routh-Hurwitz. Para simplificar a matriz, evitando a aparição das expressões grandes durante a análise, introduzimos as novas variáveis, de modo que o determinante se descreve como:
Abrindo os parênteses e aplicando a condição Det J<0, saliente do critério, obtemos o requisito de estabilidade do estado estacionário sob a forma de:
Rearranjando a inequação (22) obter-se-á, após se aniquilarem os elementos de módulos iguais com signos diferentes, o requisito, expresso sob a forma de:
Este requisito é garantidamente satisfeito, no caso da positividade dos parâmetros Σ, P e X, que descreve a fraqueza das influências dos processos da dopagem e da reação eletroquímica nas capacitâncias da DCE. Deveras, sendo os mencionados parâmetros positivos, o valor da expressão do lado esquerdo da inequação deslocar-se-á para valores mais negativos, e o estado estacionário será mais estável.
Para efeitos eletroanalíticos, isto corresponde à linearidade da dependência entre o parâmetro eletroquímico e a concentração do analito. Destarte, é possível concluir que o sistema eletroanalítico é eficiente, e esta eficiência é fácil de manter.
O processo, neste sistema, controlar-se-á pela difusão.
No caso da igualdade das influências estabilizadoras às desestabilizadoras, realizar-se-á a instabilidade monotônica, cuja aparição tem condição de
A sua realização é correspondente ao limite de detecção, e, neste ponto, coexistem vários estados estacionários, todos instáveis. Neste sistema, a instabilidade causar-se-á, maioritariamente, pelas influências da dopagem.
As influências do pH, neste sistema são importantes, já que os prótons tomam parte do processo eletroquímico. Geralmente, o pH conveniente para este tipo de reação eletro química é o neutro, ou levemente alcalino. No entanto, as soluções básicas promovem a oxidação direta química da hidroxila alcoólica:
que concorre com a oxidação eletroquímica, e as fortemente ácidas podem reverter a oxidação. Destarte, o pH da solução deve ser escolhido de modo que seja capaz de neutralizar as influências básicas do analito e, assim, na literatura foram usadas as soluções moderadamente ácidas, tendendo a fortemente ácidas, com pH = 2 ou 3.
Algo parecido se realizou no trabalho [35], em que para neutralizar o quitosano, um polímero expressamente básico, usou-se o pH baixo para que se obtivesse o meio neutro, conveniente para a oxidação do composto hidroquinônico sobre o líquido iônico neutro.
Neste sistema, como o polímero condutor é expressamente ácido, podem usar-se as soluções menos ácidas, com o pH=4, ou 5, sem prejuízo para a eficiência eletroanalítica do sistema.
Com mais detalhes a influência do pH nos sistemas como este, ou descrito em [35], descrever-se-á num dos nossos próximos trabalhos.
CONCLUSÕES
A avaliação teórica da possibilidade da detecção eletroquímica da hidroxizina em soluções ácidas sobre um polímero condutor, modificado por grupos expressamente ácidos, deixou concluir que:
- O estado estacionário, neste sistema, é garantidamente estável, sendo fracas as influências dos processos da dopagem e da reação eletroquímica nas capacitâncias da DCE;
- O sistema eletroanalítico é eficiente, e esta eficiência é fácil de manter;
- O processo eletroanalítico é controlado por difusão;
- A instabilidade oscilatória, neste caso, é possível, sendo causada não só pelos fatores das influências eletroquímicas na DCE, mas também pelos fatores das influências da dopagem;
- A instabilidade monotônica realiza-se, no caso da igualdade das influências estabilizadoras às desestabilizadoras, sendo causada, maioritariamente pelas influências da dopagem;
- Haja vista a presença de um ácido forte na superfície, é possível usar soluções menos ácidas que as indicadas na literatura para outros sistemas com a eletrodetecção da hidroxizina, sem prejuízo para o processo eletroanalítico.