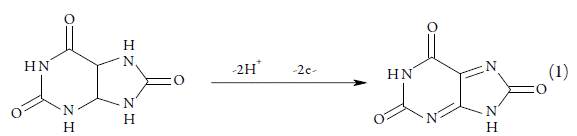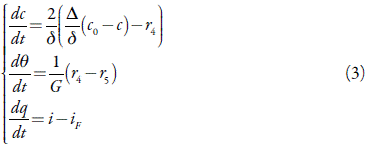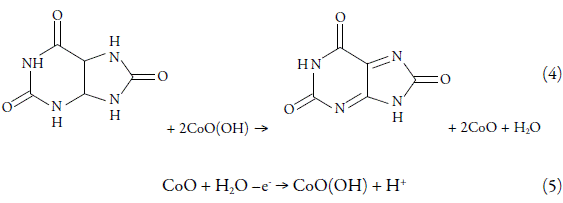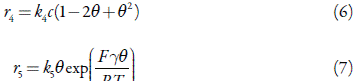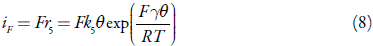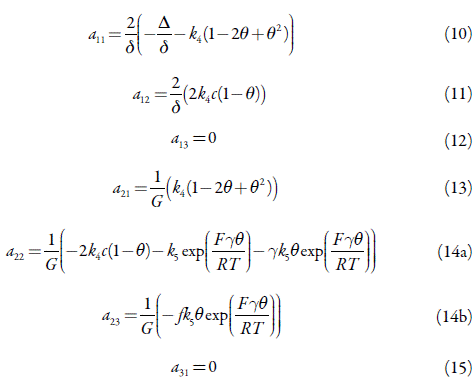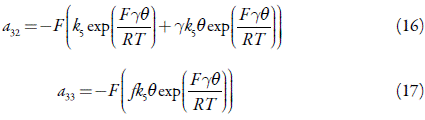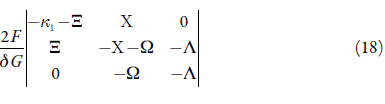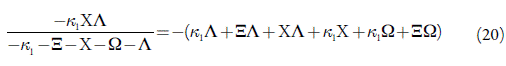INTRODUCCIÓN
El uso de electrodos químicamente modificados se ha convertido en una de las herramientas flexibles, modernas y eficientes del análisis electroquímico [1-6]. Sus ventajas se manifiestan en sensibilidad, precisión, exactitud y, principalmente, en la afinidad de materiales modificadores con el analito.
Por un lado, el ácido úrico (es decir, 2,6,8-trihidroxipurina, CAS: 69-93-2) es el producto final del metabolismo de las purinas, no solo en el organismo humano, sino también en algunos animales, como peces, anfibios y serpientes [7], y su producción en el organismo es un proceso genéticamente determinado [8]. Su ausencia causa síntomas de hiperuricemia, asociada a algunos estados dolosos, como el mal de Wilson [9], de Fanconi [10] u otros [11,12]. Por otro lado, su hiperfunción puede causar otros males, como el de Lesch-Nyhan [13], o la llamada "gota" [14]. Así, el desarrollo de un método de la medición de su concentración en el organismo es un problema de hoy día [15-17].
Se han usado varios modificadores de electrodos para la detección del ácido úrico, como los polímeros conductores [18-21], nanopartículas metálicas y sus compósitos [22-24], derivados ferrocénicos [25,26], y el oxihidróxido de cobalto, un semiconductor del tipo p, visto por algunos investigadores como una alternativa al dióxido de titanio [27,28] y usado para detectar las sustancias, cuya oxidación se da en condiciones semejantes [29,30], también puede ser una buena alternativa.
Sin embargo, las propiedades electroanalíticas de este compuesto recién comenzaron a investigarse, y la tentativa de su aplicación al caso del ácido úrico puede enfrentar problemas como los siguientes:
- la incertidumbre acerca del(los) mecanismo(s) más probable(s) del desempeño de la sustancia modificadora y de la oxidación del analito;
- la posibilidad de inestabilidades electroquímicas, capaces de acompañar la elec-troxidación y la electropolimerización de ciertos compuestos orgánicos [31,32], bien como la electrosíntesis del propio CoO(OH) [33];
- la incertidumbre acerca de la posibilidad de reacciones laterales de la modificadora con otras sustancias, presentes en la solución.
La solución para los mencionados problemas se da mediante el análisis del comportamiento de este sistema desde el punto de vista mecanístico, incluyendo el desarrollo y análisis de un modelo matemático, capaz de describir, de forma adecuada, su comportamiento. El modelo también proporciona la posibilidad de comparar el comportamiento de sistemas análogos sin ensayos experimentales.
Así, el objetivo general de este trabajo es el análisis mecanístico del sistema de la electroxidación del ácido úrico sobre el oxihidróxido de cobalto trivalente. Su realización se da por el alcance de objetivos específicos como:
- la sugerencia de un mecanismo de acción de modificadora;
- el desarrollo de un modelo matemático, basado en los datos del mecanismo;
- el análisis del modelo, con la detección de condiciones de estabilidad del estado estacionario y de inestabilidades electroquímicas;
- comparación del comportamiento del modelo con el de los sistemas semejantes [34,35].
EL SISTEMA Y SU MODELO
Conforme a los datos de literatura [18-26], en la mayoría de los casos, la detección electroquímica del ácido úrico se da en medio neutro, o ligeramente alcalino, según el mecanismo:
Y esta reacción hace que el sistema conjugado en el producto se establezca sin interrupciones.
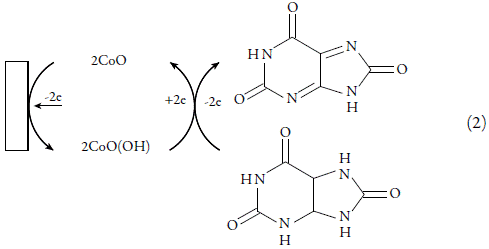
Con la participación del oxihidróxido de cobalto, el mecanismo se describe en el esquema (2):
Para investigar el comportamiento del sistema analítico en medio neutro y en modo galvanostático, introducimos tres variables:
c = la concentración del ácido úrico en la capa presuperficial;
θ = el grado de recubrimiento de la superficie por el óxido de cobalto bivalente;
q = la carga del ánodo.
Para simplificar el modelaje, suponemos que evitando la aparición de ecuaciones diferenciales complejas, la solución se agite intensamente (lo que da posibilidad de menospreciar el flujo de convección), de que el electrólito suporte esté en exceso (lo que da posibilidad de menospreciar el flujo de migración). También es supuesto que el perfil de concentraciones de analito y protones en la capa presuperficial sea lineal y el espesor de la propia capa sea constante e igual a δ. Se cree que la concentración de los protones, que aparecen durante la reacción, no es suficiente para influenciar mucho en el sistema.
Es posible demostrar que el comportamiento de este proceso electroanalítico puede describirse por un modelo clásico de tres ecuaciones de balance:
En que Δ es el coeficiente de difusión, c0 es la concentración del ácido úrico en el interior de la solución, r 4 y r 5 son las velocidades de las reacciones, expuestas en el esquema (2), según lo descrito abajo:
G es la concentración máxima de CoO en la superficie, e i F es la corriente de Faraday.
Las velocidades de las respectivas reacciones pueden presentarse así:
y la corriente de Faraday, como:
Los parámetros k son las constantes de velocidades de las respectivas reacciones, F es el número de Faraday, γ es el coeficiente que describe las relaciones entre la carga del ánodo y el grado de recubrimiento de las respectivas sustancias, suponiéndose que γθ = φ 0 = fq es el salto de potencial, relativo al de carga cero, R es la constante universal de gases y T es la temperatura absoluta.
En el modo galvanostático, el comportamiento será más dinámico que en condiciones potenciostáticas. Sin embargo, aunque haya más factores que colaboran para influenciar el sistema, en el caso del modo potenciostático, el estado estacionario estable también se mantiene con facilidad, lo que será descrito abajo.
RESULTADOS Y DISCUSIÓN
Para investigar el comportamiento electroquímico del sistema con la detección electroquímica del ácido úrico, asistida por el oxihidróxido de cobalto trivalente, analizamos el conjunto de ecuaciones diferenciales (3) mediante la teoría de estabilidad lineal. Los elementos estacionarios de la matriz funcional de Jacobi para este sistema serán descritos como:
en que:
Para investigar la estabilidad del estado estacionario, aplicamos al conjunto de ecuaciones diferenciales (3) el criterio de Routh-Hurwitz. Con fines de simplificar los cálculos, evitando la aparición de ecuaciones grandes, introducimos nuevas variables, y el determinante de la matriz se describe como:
Abriendo los paréntesis y aplicando la condición Det J < 0, saliente del criterio, obtendremos el requisito de estabilidad de estado estacionario, después de eliminar los elementos del módulo igual y signos opuestos, en la forma de:
Esta condición se realiza con mayor probabilidad que en los sistemas semejantes [34,35], ya que los elementos que describían las influencias electroquímicas se eliminan, y, contrariamente a lo observado en [34,35], no dan influencias a la estabilidad del estado estacionario. Para fines electroanalíticos, ella es correspondiente a la linealidad de la dependencia entre la concentración y el parámetro electroquímico. Así, para la detección del ácido úrico sobre el oxihidróxido de cobalto, el modo galvanostático es eficiente.
El proceso será controlado, mayoritariamente, por la difusión, pudiéndose controlar, en el caso de uso de electrodo pequeño, por la reacción. Algunas restricciones aplicadas al requisito (19), relacionadas con el comportamiento oscilatorio, se discutirán abajo.
Como ninguna de las variables mencionadas en la inecuación (19) puede tener valores nulos, la inestabilidad monotónica, cuya condición principal de aparición es Det J = 0, en este sistema, no se realiza.
Observando las ecuaciones (10), (14) y (17), es posible ver que ellas contienen un elemento, que puede tener valores positivos: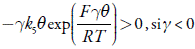 , lo que describe influencias fuertes del proceso de la oxidación electroquímica a la doble capa. Este caso del comportamiento oscilatorio, es el único posible en este sistema y es común para todos los sistemas semejantes [34,35].
, lo que describe influencias fuertes del proceso de la oxidación electroquímica a la doble capa. Este caso del comportamiento oscilatorio, es el único posible en este sistema y es común para todos los sistemas semejantes [34,35].
Todavía existiría, teóricamente, el comportamiento oscilatorio, descrito por la positividad del elemento 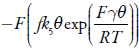 , cuando f < 0. Sin embargo, el parámetro f solo puede llevarse a negatividad, cuando, durante la aplicación del modo galvanostático, el electrodo cambia su polaridad, lo que, en este proceso, no ocurre. Por eso, las influencias del proceso de la oxidación en la doble capa en el modo galvanostático siguen siendo el único factor responsable por el comportamiento oscilatorio. Las oscilaciones se esperan que sean frecuentes y de pequeña amplitud.
, cuando f < 0. Sin embargo, el parámetro f solo puede llevarse a negatividad, cuando, durante la aplicación del modo galvanostático, el electrodo cambia su polaridad, lo que, en este proceso, no ocurre. Por eso, las influencias del proceso de la oxidación en la doble capa en el modo galvanostático siguen siendo el único factor responsable por el comportamiento oscilatorio. Las oscilaciones se esperan que sean frecuentes y de pequeña amplitud.
La condición suficiente del comportamiento oscilatorio para este sistema puede describirse así:
La ecuación (20) puede resolverse, y los significados de los lados derecho e izquierdo solo pueden tener valores opuestos en el caso de la negatividad del parámetro Ω.
Para el caso del modo potenciodinámico con voltaje constante, a la tercera ecuación diferencial del modelo se añade otro elemento, que describe la influencia del cambio de la resistencia del material en el ánodo, en la estabilidad del estado estacionario.
Para el modo potenciostático con decrecimiento de pH, cuando la concentración de protones crece bastante para intervenir en la estabilidad de CoO o CoO(OH), el modelo también es diferente, añadiéndosele una ecuación de balance que describe el comportamiento de protones. Este caso será descrito en uno de nuestros próximos trabajos.
CONCLUSIONES
El análisis del sistema con la detección del ácido úrico sobre el oxihidróxido de cobalto en el modo galvanostático, dejó la siguiente conclusión:
- CoO(OH) puede ser un modificador eficiente de ánodo para la detección del ácido úrico. El estado estacionario estable es electroanalíticamente eficiente y se mantiene fácilmente. Satisface las condiciones del comportamiento oscilatorio, su manutención es garantizada;
- El proceso electroanalítico es controlado, mayoritariamente, por difusión, o, dependiendo del tamaño del electrodo, por la reacción;
- La inestabilidad monotónica para este sistema, contrariamente a lo observado para sistemas semejantes, no es posible, porque no se pueden satisfacer las condiciones necesarias para su realización;
- La inestabilidad oscilatoria, en este sistema, puede realizarse, siendo causada apenas por los factores de las influencias de la reacción electroquímica a la doble capa eléctrica;
- Para el caso del modo potenciodinámico con voltaje constante, a la tercera ecuación diferencial del modelo se añade otro elemento, que describe la influencia del cambio de la resistencia del material en el ánodo, en la estabilidad del estado estacionario.