INTRODUÇÃO
O sucesso dos antibióticos em meados do século XX gerou o falso presságio de que as doenças bacterianas tinham sido eficientemente controladas [1]. Entretanto após quase 50 anos percebemos que esta interpretação estava equivocada. Atualmente existe um aumento alarmante na incidência de doenças infecciosas, tornando-as a primeira causa de mortalidade em países subdesenvolvidos e a terceira em países emergentes [2]. A resistência dos microrganismos as terapias convencionais vêm contribuindo para a intensificação e cronificação deste cenário. Anualmente, morrem 700.000 pessoas por infecções causadas por microrganismos resistentes no mundo [3]. Um estudo recente revelou que caso nenhuma medida efetiva seja tomada pelos órgãos de vigilância sanitária dos diferentes países, em 2050 bactérias multirresistentes matarão 1 pessoa a cada 3 segundos no mundo. Isso totalizará 10 milhões de mortes anuais, superando doenças crônicas como o câncer e o diabetes [4]. No Brasil, o panorama é também preocupante. O Ministério da Saúde estima que das 720.000 infecções hospitalares que ocorrem anualmente no país [5], mais de 70% envolvem bactérias que são resistentes a pelo menos um dos antimicrobianos comumente empregados. O custo hospitalar atribuível à ocorrência dessas infecções é de 651 dólares por dia, passando para 1780 dólares na Unidade de tratamento intensivo (UTI), o que contribui para a elevação expressiva dos custos em saúde pública no país [6].
Na contra mão da reemergência de doenças infecciosas de etiologia bacteriana, observase uma negligência de parte das grandes indústrias farmacêuticas nos investimentos voltados a pesquisa e desenvolvimento (P&D) de novos antibióticos [1,7,8,9]. De 1998 a 2002 a agência americana de controle sanitário Food and Drug Administration (FDA) aprovou apenas 7 fármacos voltados ao tratamento de doenças infecciosas, o que equivale a apenas 3% de todos os 225 novos fármacos licenciados neste período. Se comparado ao período de 1983 a 1987, por exemplo, é observada uma redução de 56% no número de antimicrobianos aprovados [1]. O cenário futuro também é pouco promissor. Dos 315 novos fármacos em fase de pesquisa pelas 15 maiores indústrias farmacêuticas do mundo, apenas 5 (menos de 2%) são novos antibacterianos pertencentes a classes já disponíveis no mercado, e somente 3 estão em fase clínica avançada (fase III) [7,9].
A indústria, no seu modelo de mercado, espera um rápido retorno do capital investido para colocar um novo fármaco na clínica, o qual gira em torno de 400 a 800 milhões de dólares por agente licenciado [10]. Assim sendo, o desinteresse das grandes indústrias do ramo reside no fato de que os exorbitantes custos e a rigorosa legislação aplicada ao desenvolvimento de um novo medicamento não encontram um retorno rápido nos antimicrobianos, devido ao fato de serem utilizados por curtos períodos [11,12]. Recentemente, porém, o conceito de reposicionamento vem ganhando espaço dentro do mercado farmacêutico ao permitir a redução dos gastos, otimização do tempo de liberação pelas agências de regulação sanitária e redução do preço final de novos fármacos [12]. Nesse modelo de desenvolvimento, compostos que já estão em uso clínico são desviados da sua indicação original e é atribuída uma nova aplicação, passando a serem exigidos apenas testes clínicos que comprovem a eficácia do novo uso [11,12].
Nesse contexto, a atividade antibiótica de muitos fármacos não-antibacterianos tem sido reconhecida com destaque a clorpromazina (CPZ) [11]. A CPZ, um neuroléptico típico que age inibindo os receptores dopaminérgicos e alguns outros efeitos dependentes de calmodulina, tem apresentado atividade antibacteriana contra várias espécies Gram-negativas e Gram-positivas de interesse médico [13], bem como contra micobactérias [14]. Este composto tem também mostrado a capacidade de reverter à resistência bacteriana á alguns antibióticos [15,16], inibir bombas de efluxo [15-18], potencializar o efeito antibacteriano dos β-lactâmicos, aminoglicosídeos, clindamicina, tetraciclinas, vancomicina e fluorquinolonas [19, 20], e reduzir a capacidade de formação de biofilmes [21]. O efeito terapêutico da CPZ em humanos com infecções bacterianas em curso tem também sido demostrado, corroborando assim com os estudos básicos [13]. Nessa revisão, foi resumido o conhecimento atual sobre o efeito antibacteriano da CPZ, focando no espectro de atividade e no mecanismo de ação antibiótico desse composto. Em adição, destacase também o efeito da CPZ sobre fatores de virulência e mecanismos de resistências que são associados à patogenicidade bacteriana.
ASPECTOS QUÍMICOS E FARMACOLÓGICOS DA CLORPROMAZINA
A CPZ é um agente neuroléptico derivado das fenotiazinas que originalmente foi desenvolvido em 1952 como um anti-histamínico para ser usado na potencialização da anestesia geral [22,23]. Durante os primeiros ensaios clínicos os pacientes passaram a manifestar um estado psicológico caracterizado por indiferença emocional, sem diminuição importante da vigilância, que ficou conhecido como síndrome neuroléptica. Esta observação casual estimulou, mais tarde, o uso experimental da droga em pacientes com distúrbios mentais. Os efeitos antipsicóticos da CPZ foram bastante relevantes, e a partir da década de 1960 o seu uso na clínica médica passou a reduzir consideravelmente o número de admissões em hospitais psiquiátricos no mundo todo [23,24]. Atualmente a Organização Mundial da Saúde lista a CPZ como um dos 5 medicamentos essenciais no manejo terapêutico da esquizofrenia [25].
Quimicamente, a CPZ é caracterizada pela presença de um anel fenotiazídico clássico, i.e., um sistema de 3 anéis do tipo benzeno com o anel central composto de enxofre e nitrogênio [26]. A presença do átomo de cloro em um dos sistemas de anéis garante uma maior biodisponibilidade do fármaco no sistema nervoso central, e o substituinte amina é importante para a interação com os receptores dopaminérgicos (ver a figura 1) [27]. As fenotiazinas podem ser divididas em: fenotiazinas alifáticas (clorpromazina, promazina, trifluorpromazina), fenotiazinas piperidínicas (tioridazina, mepazina, pipotiazina); fenotiazinas piperazínicas (trifluorperazina, tiopropazato, ilufenazina), e aza-fenotiazinas (protipenclil, isotipendil, oxipendil) [26].
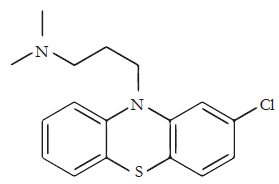
Figura 1 Estrutura química da Clorpromazina. Esse agente neuroléptico é composto por: (i) um anel fenotiazídico, diretamente associado a sua ação farmacológica; (ii) um átomo de cloro, importante na sua biodisponibilidade no sistema nervoso central e (iii) uma amina como substituinte, que está associado a interação com os receptores dopaminérgicos.
Como todo antipsicótico típico, a CPZ exerce sua ação farmacológica ao antagonizar os receptores dopaminérgicos do tipo D2 presentes nos sistemas mesolímbico (efeitos antipsicóticos), mesocortical (efeitos adversos cognitivos e agravamento dos sintomas negativos), nigroestriatal (efeitos extrapiramidais) e túberoinfundibular (efeitos neuroendócrinos) [28]. Em adição, esse fármaco possui a habilidade de inibir, em menor grau, os receptores colinérgicos muscarínicos (M1 e M2), histamínicos (H1) e α-adrenérgicos (α1) [29]. Além dos efeitos neurolépticos induzidos pelo bloqueio dos receptores D2, a CPZ também pode ser útil no tratamento da síndrome serotoninérgica por possuir a habilidade de inibir os receptores 5-hidroxitriptamina (5-HT) [30, 31].
A habilidade que a CPZ tem em inibir múltiplos receptores no sistema nervoso central está diretamente relacionada com os vários efeitos adversos associados ao uso desse fármaco. A via dopaminérgica nigroestriatal participa da regulação da atividade motora, assim, por bloquear receptores dopaminérgicos estriatais, a CPZ pode induzir a síndrome de Parkinson, reações distônicas agudas, discinesia tardia, acatisia, acinesia e síndrome neuroléptica maligna [32]. Outros efeitos adversos também de origem central são os que afetam o sistema neuroendócrino associado à inibição dos receptores dopaminérgicos túberoinfundibulares, os quais podem causar ginecomastia, galactorréia e amenorreia [28, 29].
Os neurolépticos atuam também na periferia do organismo, afetando o sistema nervoso autônomo ao inibir respostas colinérgicas dependentes de M1/M2 e adrenérgicas dependentes de α1, causando sintomas como secura da boca e pele, midríase e dificuldade de acomodação visual, taquicardia, constipação intestinal e retenção urinária [29]. A CPZ pode determinar falso-positivo para gravidez, fenilcetonina e bilirrubina na urina. Aumento nos níveis plasmáticos de colesterol, glicose, prolactina, bilirrubina, iodo, hormônio tireo-estimulante (TSH), cortisol e das enzimas cardíacas e hepáticas têm sido associados ao uso da CPZ nas doses normalmente recomendadas [33]. Em adição, ela costuma deprimir o segmento ST e aumentar os intervalos QT e PR no eletrocardiograma por estar associada a alterações na condução atrioventricular [34].
Somado aos efeitos centrais clássicos produzidos pela inibição de receptores envolvidos na neurotransmissão, a CPZ também modula respostas dependentes de cálcio [35]. Assim como o haloperidol, a CPZ inibe a ligação do cálcio a calmodulina, tendo assim a capacidade de aumentar o tônus imunológico in vivo ao estimular a atividade linfocitária [36], além de ser associada a efeitos citotóxicos antineoplásicos [37]. Como a via de sinalização dependente de cálcio-calmodulina é conservada em diferentes organismos, incluindo patógenos, destacase para a possibilidade desse agente neuroléptico possuir efeitos antimicrobianos e antiparasitários [38].
De fato, a atividade da CPZ já foi determinada contra Plasmodium falciparum [39,40,41], Leishmania spp. [42,43], Candida spp. [44], Aspergillus spp. [45], Scedosporium spp.[45], Zicomicetos [45], Naegleria fowleri [46], Herpes simplex virus (HSV) [47], Virus da Encefalite transmitido por carrapatos (TBEV) [48], Vírus da Hepatite B (HBV) [49], Measles virus [50], Sinbdis Virus [51], Estomatite virus [51], Influenza-virus [52], Poliomavirussímio 40 (SV40) [53], Arenavirus [54], Vírus da Imunodeficiência humana (HIV) e John Cunningham virus (JC vírus) [55]. Em adição, a atividade antibacteriana da CPZ tem sido determinada em vários estudos [15-18,56,57]. Assim, destaca-se o potencial de reposicionamento desse agente farmacológico na terapia de diferentes doenças de etiologia infecciosa.
ATIVIDADE DA CPZ CONTRA PATÓGENOS GRAM-POSITIVOS
O Staphylococcus aureus, um cocus Gram-positivo, é particularmente sensível aos efeitos antibacterianos da CPZ. O crescimento de linhagens referência e de isolados clínicos de S. aureus meticilina-sensível (MSSA) é inibido pela CPZ á concentrações na faixa de 30-64 μg/mL [15,56,57,58]. As linhagens meticilina-resistentes (MRSA) são também susceptíveis a esse fármaco, sendo que as concentrações inibitórias mínimas (CIMs) variam de 40-100 μg/mL contra esses patógenos [15,16,18,58,59].
O efeito bactericida, por sua vez, começa a ser observado a partir de 60 μg/mL [57], sendo que as linhagens MRSA são menos sensíveis. De fato, a concentração bactericida mínima (CBM) da CPZ varia de 70-80 μg/mL para isolados clínicos de MRSA [15], sendo que um estudo reportou ausência de efeito bactericida contra esse microrganismo (CBM >800μg/mL) [16]. Nehme e colaboradores [58], em um estudo recente, mostraram que a CPZ a 128 μg/mL é hábil para reduzir em 2 log o número de unidades formadores de colônias de S. aureus após 3 h de incubação, sendo esse efeito amplificado após 24 h com redução de 4 log. Adicionalmente a atividade antibacteriana direta, a CPZ interage de maneira sinérgica e potencializa a ação de vários antibióticos como a penicilina, clindamicina, ampicilina, amicacina, gentamicina, tobramicina, estreptomicina, tetraciclina, oxacilina e vancomicina contra o S. aureus [19,20,59]. A interação sinérgica entre CPZ e a Vancomicina foi também relatada contra dois isolados clínicos de Enterococcus faecium [60].
O átomo de cloro presente na estrutura da CPZ parece não ser essencial para a atividade antibacteriana, pois a sua remoção promove apenas uma ligeira elevação na CIM contra o MRSA (64-128 μg/mL) in vitro [61]. No entanto, vale destacar que a presença do cloro é importante para elevar a biodisponibilidade da CPZ no sistema nervoso central [62]. Assim sendo, a remoção desse átomo estaria associada à preservação da atividade antibacteriana e, em adição, a redução das reações adversas centrais frequentemente associadas a esse fármaco.
Apesar dos testes in vitro demostrarem o efeito anti-estafilocócico da CPZ, as concentrações necessárias para a atividade antibacteriana são quase 60 vezes mais altas que as usualmente mensuradas no plasma de pacientes (entre 0,1-0,5 μg/mL) [29]. Entretanto, nas concentrações clinicamente disponíveis no plasma (0,1 μg/mL) a CPZ consegue matar células de S. aureus fagocitadas in vitro por macrófagos das linhagens HPBMDM e THP-1 após 6 h de incubação [57]. Isso pode ser justificado pelo fato de o macrófago ser capaz de concentrar a CPZ em até 100-vezes os níveis encontrados no plasma [63]. Em alguns casos as concentrações atingidas no interior dos macrófagos são superiores a necessária para a atividade antimicrobiana [14,64]. Em adição, na faixa de concentração (0,1-0,01 μg/mL) necessária para matar o S. aureus fagocitado, a CPZ não induziu nenhum efeito deletério sobre as células em cultura, como revelado pelas colorações com azul de tripan e naftol azul-negro [57]. Assim sendo, sugere-se que a concentração necessária para induzir o efeito antibacteriano da CPZ contra patógenos intracelulares é associada a uma baixa toxicidade clínica.
Ao contrário da atividade contra S. aureus, já bem demonstrada, o efeito da CPZ sobre outros patógenos Gram-positivos ainda não é bem descrito. Nessa direção, a atividade da CPZ contra o Bacillus anthracis, Enterococcus faecalis, Enterococcus faecium, Listeria monocytogenes, Corynebacterium spp. e Streptococcus spp. têm sido demonstrada [11, 56, 64-67]. Nessa direção, mais estudos devem ser conduzidos para compreendermos melhor o efeito antibacteriano da CPZ contra as demais espécies de bactérias Gram-positivas.
ATIVIDADE DA CPZ CONTRA PATÓGENOS GRAM-NEGATIVOS
Apesar de ainda não estar comprovado o motivo, as bactérias Gram-negativas são mais resistentes ao efeito antibacteriano da CPZ. Estudos in vitro tem revelado que a CPZ é ativa contra as Enterobacteriaceae Escherichia coli (CIM 50-64 μg/mL) [20,58], Klebsiella pneumoniae (CIM 64-128 μg/mL) [58] e Salmonella enterica serovar Typhimurium (CIM 110-512 μg/mL) [21,63], e contra os bastonetes Gram-negativos não-fermentadores Acinetobacter antiratus (CIM 60 μg/mL) [20] e Acinetobacter baumannii (CIM 64 μg/mL) [58]. Em adição a atividade bacteriostática contra A. baumannii, a CPZ (128 μg/mL) possui a habilidade de reduzir em 3 log a densidade celular desse microrganismo após 3 h de incubação, demostrando assim o potencial bactericida desse fármaco também contra espécies de Gram-negativas [58]. O efeito antibacteriano também foi mensurado contra Proteus vulgaris [20] e Pseudomonas aeruginosa [20,58,61], mas em ambos os casos a CPZ foi inativa (CIM >500 μg/mL).
Entretanto, sua interação sinérgica com os antibióticos ceftazidima, ceftriaxona, imipeném, estreptomicina, tetraciclina, canamicina, amicacina e tobramacina foi demostrada contra E. coli [20,68-70]. Adicionalmente, a CPZ na concentração de 200 μg/ mL potencializa os efeitos antibacterianos do ácido nalidíxico, norfloxacino, ciprofloxacino, cloranfenicol, tetraciclina e brometo de etidium contra Salmonella enterica serovar Typhimurium [71]. Os resultados indicam que o sinergismo produzido pela combinação da CPZ com os antibióticos disponíveis na clínica se limita as espécies sensíveis a essa fenotiazina isoladamente [20,71].
Apesar do preciso mecanismo de ação antibacteriano da CPZ ainda não ter sido identificado, alguns trabalhos tem mostrado que essa fenotiazina está relacionada com alterações na parede celular bacteriana (ver figura 2) [56,72]. Esse fato pode, pelo menos em parte, justificar a atividade mais pronunciada contra as espécies Gram-positivas. Kristiansen em 1979 revelou pela primeira vez que a exposição de S. aureus a diferentes concentrações de CPZ (0-200 μg/mL) reduz a liberação de hemolisina no meio de cultura, indicando uma menor permeabilidade celular [56]. Análises posteriores de microscopia eletrônica revelaram que esse efeito é causado pelo aumento na espessura da parede celular induzida pelo composto [72]. Em adição, á altas concentrações (acima de 30 μg/mL) a CPZ é capaz de induzir alterações ultraestruturais na parede de S. aureus, produzindo corpos celulares semelhante a mesossomas, além de divisões celulares assimétricas [72]. Recentemente um estudo mostrou que a concentração de 62,5 μg/mL a CPZ foi capaz de romper a membrana plasmática e parede celular de S. aureus [59]. As alterações observadas foram semelhantes às induzidas por antibióticos β-lactâmicos, o que sugere um mecanismo de ação similar para CPZ [11].
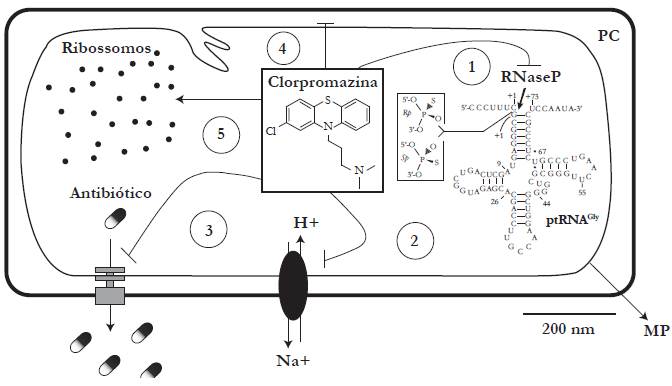
Figura 2 Representação esquemática dos efeitos da CPZ em células bacterianas. Como mostrado a CPZ é capaz de (1) inibir a ribonuclease P, essencial na replicação genética da célula bacteriana; (2) inibir sistemas de transporte de H+ responsáveis pela força próton-motrix que fornece energia para a função das bombas de efluxo; (3) os elétrons π do anel fenotiazídico na CPZ é capaz de interagir diretamente com bombas de efluxo inibindo-as e, em adição, (4) esse fármaco é hábil em agir na parede celular bacterina induzindo divisões assimétricas, a formação de mesossomos e o espessamento dessa estrutura. Análises microscópicas também revelam que esse agente neuroléptico induz distribuição anormal dos ribossomos citosólicos (5). PC: parede celular; MP: membrana plasmática; RNase P: ribonuclease P; Na+: sódio; H+: hidrogênio.
Além disso, as fenotiazinas são conhecidas por alterar a morfologia das bactérias Gram -negativas em concentrações subinibitórias [13]. As alterações estão especificamente relacionadas com a espécie, de tal forma que a CPZ causa a filamentação de E. coli [73] e modificações ribossomais e proteicas em Salmonella enterica serovar Typhimurium [63]. A CPZ (60-40 μg/mL) induz a filamentação de E. coli após 5 h de incubação, entretanto a partir de 8 h a forma bastonete começa a prevalecer novamente, até total reversão para a morfologia normal após 24 h. A determinação das proteínas que formam o envelope celular de E. coli revelou que durante a filamentação existe uma alteração no padrão de expressão. Nesse caso, certas proteínas da parede celular são reguladas positivamente, as quais reduzem a permeabilidade de CPZ e assim, permite a reversão para a morfologia normal [73]. Interessantemente, de maneira semelhante à CPZ, os β-lactâmicos também estimulam a filamentação de E. coli, o que reforça um mecanismo de ação similar entre essas duas substâncias [74].
Alterações morfológicas em Salmonella enterica serovar Typhimurium são também observadas. A CPZ a partir de 75 μg/mL induz uma distribuição citosólica anormal dos ribossomos, além de aumentar a formação de estruturas semelhantes a mesossomas. Na parede celular de S. enterica, a CPZ produz espaços terminais e reduz as granulações. A análise eletroforética dessa estrutura revela que a CPZ promove a completa perda de proteínas com 55 kDa. Em adição, após a exposição para CPZ, a aglutinação de S. enterica pela adição de anticorpos dirigidos ao antígeno O é completamente perdida. Esses resultados confirmam a parede celular como alvo primário da ação antibacteriana desse agente neuroléptico [63]. Entretanto, diferente das espécies Gram-positivas, para acessar os componentes da parede celular de Gram-negativas, a CPZ precisa primeiramente atravessar a membrana externa. As espécies Gram-negativas são particularmente resistentes a uma série de fármacos, pois muitos dos agentes antibacterianos não conseguem vencer essa barreira [75]. Entretanto, o papel da membrana externa na resistência intrínseca das espécies Gram-negativas aos efeitos antibacterianos da CPZ ainda precisa ser determinado.
Em adição aos efeitos da CPZ na estrutura da parede celular bacteriana, um estudo recente tem mostrado que esse fármaco pode também agir em alvos intracelulares. A ribonuclease P (RNase P), uma ribozima essencial para a replicação do material genético de eubactérias, responsável pela 5'-maturação dos precursores de tRNA, é particularmente sensível aos efeitos inibitórios da CPZ (Figura 2) [76,77]. A atividade enzimática da RNase P de M. tuberculosis (Ki 161±16 μM), Mycoplasma hyopneumoniae (Ki 170±9,2 μM) e E. coli (Ki 437±33 μM), medida pela capacidade de clivagem do tRNA, foi eficientemente inibida pela CPZ [77]. Esse fato reflete que a CPZ apresenta mecanismos de ação independente da parede celular bacteriana, a qual inclui alvos conservados entre várias espécies de bactérias, como o caso das ribonucleases. Esse fato justifica o espectro antibacteriano estendido desse composto.
ATIVIDADE CONTRA MICOBACTÉRIAS
Vários estudos demonstram que a CPZ possui atividade in vitro contra M. tuberculosis em concentrações a partir de1 μg/mL, a qual é 10 vezes superior a comumente encontrada no plasma após uma dose usual desse fármaco [78-85]. Entretanto, o M. tuberculosis é um patógeno intracelular com tropismo por macrófagos humanos [86]. Assim sendo, a capacidade que essas células têm de concentrar a CPZ pode favorecer a sua atividade antimicobacteriana.
De fato, vários estudos têm demonstrado que a morte de M. tuberculosis fagocitados por macrófagos é reforçada por concentrações de CPZ a partir de 0,1 μg/mL [14,79,87,88]. É importante notar que enquanto muitos compostos têm demonstrado ter atividade in vitro contra M. tuberculosis, poucos destes penetram no macrófago e retêm a atividade contra as micobactérias intracelulares. Corroborando com esses dados de que as fenotiazinas promovem a morte de micobactérias intracelulares, camundongos infectados com M. tuberculosis foram curados desta infecção quando tratados com análogos estruturais da CPZ [89].
Em adição, estudos têm mostrado que, mesmo em linhagens altamente resistentes a isoniazida e rifamicina, o efeito da CPZ é mantido ao mesmo nível de controles sensíveis as terapias convencionais [78]. Assim sendo, essas evidências apontam que a CPZ deve ser seriamente considerada para a terapêutica da tuberculose, principalmente quando causada por cepas multirresistentes [90-92].
As fenotiazinas inibem o transporte de cálcio (Ca2+), impedindo a sua ligação às proteínas de ligação ao Ca2+, como a calmodulina [35]. Isto significa que os sistemas enzimáticos que são dependentes de Ca2+, tais como os envolvidos na geração de energia celular a partir da hidrólise de ATP, são inibidos [93]. Esses sistemas podem ser muitas vezes associados ao desenvolvimento de resistência aos antibióticos em diferentes espécies de bactérias [38]. Entre os quatro mecanismos gerais de resistência (i.e., inativação do fármaco, alteração do alvo, efluxo do antibiótico e impermeabilização da membrana) a extrusão dos compostos antibacterianos por bombas de efluxo é com certeza um dos mais importantes fatores de resistência para múltiplos antibióticos (MDR). Isso ocorre, pois diferente dos outros mecanismos, as bombas de efluxo apresentam alta eficiência de extrusão dos fármacos e uma ampla especificidade de substratos, podendo assim, conferir resistência a múltiplos agentes [94].
De acordo com a sua composição, número de alças transmembrânicas e fontes de energia e substrato, as bombas de efluxo podem ser classificadas em 5 famílias: família de resistência divisão-nodulação (RND, do inglês resistance-nodulation-division) [95], superfamília facilitadora principal (MFS, do inglês major facilitator superfamily) [96], cassete de ligação ao ATP (ABC, do inglês ATP (adenosine triphosphate)-binding cassette) [97], pequenos efluxos relacionados a multirresistência (SMR, do inglês small multidrug resistance family) [98] e família de extrusão de compostos tóxicos e múltiplas drogas (MATE, do inglês multidrug and toxic compound extrusion family) [99]. A família ABC possui como fonte de energia o ATP, assim sendo, é possível que a CPZ, ao bloquear os sistemas enzimáticos dependentes de Ca2+ que hidrolisam o ATP, possa estar associada à inibição dessas bombas de efluxo [97]. Nessa direção, diversos estudos têm demostrado que CPZ reverte o fenótipo MDR de bactérias por inibir sistemas de efluxo [15-18].
A CPZ em concentrações não antibacterianas (referente a 50% da CIM) é capaz de inibir as bombas de efluxo sensíveis a reserpina em MRSA [15,16]. A utilização dessa fenotizina reduziu a CIM da oxacilina de >800 μg/mL para 100 μg/mL. Em um isolado de MRSA, a CIM da oxacilina reduziu em mais de 40 vezes, e esse β-lactâmico foi efetivo a concentração de 20 μg/mL quando combinada com a CPZ [16]. Adicionalmente, CPZ inibe o transportador NorA em S. aureus.
A exposição de S. aureus que superexpressam NorA, á concentrações subinibitórias (25% da CIM) da CPZ eleva consideravelmente a sensibilidade ao norfloxacino (aumento de 4 vezes) e aos cátions inorgânicos brometo de etídio (EtBr) (aumento de 5 vezes) e brometo de tetrafenilfosfônio (TPP) (aumento de 8 vezes) [18]. NorA é uma proteína com 388 aminoácidos e de 12 alças transmembrânicas pertencentes a família MFS que pode extruir uma variedade de compostos antibacterianos como fluorquino-lonas hidrofílicas (norfloxacino e ciprofloxacino), corantes (como o brometo de etídio) e quartenários de amônio biocidas [17,18]. Semelhante a outros membros da família MFS, a NorA emprega como fonte de energia a força próton-motrix dependente de H+. Em adição ao conhecido efeito sobre os ions Ca2+, outros estudos mostram que CPZ inibe também o transporte do íon H+ em células intestinais de coelhos [100] e em leveduras [101]. Em células de S. aureus, a inibição dos transportadores dependentes de H+ promove uma redução na variação do potencial elétrico transmembrana (Ψ), a qual culmina na queda da força motriz do sistema para 23% do seu total [18]. Assim sendo, tem sido mostrado que a CPZ inibe a NorA por induzir um colapso na fonte energética dessa bomba de efluxo (ver figura 2).
Em adição a NorA, a bomba de efluxo para tetraciclina TetK também é inibida pela CPZ em S. aureus. A exposição de 25 μg/mL por 24 h reduz a CIM da tetraciclina de 6,25 μg/mL para 0,78 μg/mL (redução de 8 vezes) em linhagens de S. aureus TetK-positivas [18]. A inibição de TetK, provavelmente é também devido a inibição da força próton motriz, uma vez que assim como a NorA, esse sistema de efluxo é pertencente a família MFS. No entanto, além dos efeitos sobre a força motrix, parece que os elétrons π do sistema de anéis nas fenotiazinas contribuem para uma inibição direta sobre as bombas de efluxo. Essa região possibilita uma ligação eletrofílica com resíduos importantes para a atividade coordenada dessas proteínas, o que pode comprometer a ligação com o substrato e assim reduzir a sua capacidade de extrusão (ver figura 2) [17].
A CPZ também inibe bombas de efluxo presentes em bactérias Gram-negativas. Nas concentrações a partir de 2 μg/mL essa fenotiazina bloqueia os sistemas de efluxo em S. enterica sorovar Typhimurium. Esse efeito foi similar ao observado pelo tratamento com o Fenil-arginina-|3-naftilamina (PAjEN) e o Carbonil Cianido m-clorofenilhidra-zona (CCCP) inibidores competitivos das bombas de efluxo pertencentes à família RND e da força próton-motriz, respectivamente [21]. A CPZ (200 μg/mL) eleva a concentração intracelular do brometo de etidium em S. enterica sorovar Typhimurium em quase 4-vezes por inibir o sistema de efluxo tripartite AcrAB-TolC, o qual é conhecido pela extrusão desse corante antibacteriano. A inibição desse sistema de efluxo pela CPZ é tão eficiente que em linhagens de S. enterica sorovar Typhimurium com deleção dos genes tolCou acrB, o acúmulo do brometo de etidium ocorreu em um nível inferior ao induzido pelo uso do agente neuroléptico [71].
As fenotiazinas também afetam a expressão de genes que codificam determinantes de resistência. Um estudo tem revelado, por exemplo, que a prometazina é capaz de eliminar plasmídeos que carreiam genes codificadores de bombas de efluxo em E. coli, reduzindo a CIM para tetraciclinas [17]. A CPZ reduz também a expressão dos genes mecA e blaZ induzidos pela oxacilina em S. aureus, os quais são envolvidos na codificação da proteína de ligação a penicilina do tipo 2a (PBP2a) e β-lactamases, respectivamente [59]. Na S. enterica sorovar Typhimurium a CPZ reduz a expressão do gene acrB o qual codifica uma bomba de efluxo envolvida na extrusão do cloranfenicol, tetraciclina, ácido nalidíxico, triclosano e solventes orgânicos [71].
Outros mecanismos de resistência, como as enzimas aminoglicosídeo fosforilases [102], são também dependentes de ATP. Além disso, diversas outras bombas de efluxo são dependentes da força próton-motrix [96,98,99]. Entretanto, até a presente revisão, não existem evidências sobre o papel da CPZ nesses sistemas relacionados à resistência aos antibióticos. Assim sendo, mais estudos devem ser conduzidos nesse sentido, objetivando alcançar uma compreensão mais ampla sobre o papel da CPZ nesses diferentes determinantes de resistência.
EFEITO DA CPZ SOBRE FATORES DE VIRULÊNCIA
Os patógenos bacterianos são direcionados para a necessidade de assimilarem nutrientes, sobreviverem e se reproduzirem dentro de um hospedeiro [103]. Em um curto espaço de tempo, eles requerem a flexibilidade para se adaptarem às mudanças ambientais as quais foram expostos de maneira a viabilizar a sua colonização [104]. A adaptação necessária que garante o estabelecimento do processo infeccioso é dependente dos fatores de virulência [103, 104]. A principal característica biológica das bactérias que afeta a saúde humana reside na capacidade desses microrganismos em formar biofilmes [58,105]. Essas estruturas são caracterizadas por um conjunto de células aderentes com propriedades que as distinguem daqueles livres (planctônicas), como a grande resistência a agentes antimicrobianos químicos e físicos [105].
Um estudo tem demostrado que a CPZ inibe a formação de biofilme por S. enterica sorovar Typhimurium [21]. A revelação do biofilme pelo ensaio do cristal violeta mostrou que o uso de concentrações subinibitórias da CPZ (a partir de 2 μg/mL) foi capaz de reduzir a formação do biofilme de maneira dose-dependente. O efeito parece ser associado à capacidade que a CPZ tem de inibir os sistemas de efluxo. A inibição da formação de biofilme pelo composto foi similar ao induzido pela remoção experimental dos genes tolC e acrB, os quais codificam para proteínas de efluxo homólogas pertencentes a família RND [21].
Além da formação de biofilmes, existe uma série de outros fatores relacionados à pato-genicidade de bactérias [103,104]. Esses incluem a produção de toxinas, invasinas (proteases, lipases e sacaridases), enzimas antioxidantes (catalase, superóxido dismutase), adesinas e cápsulas. Tem sido demonstrado que a fenotiazina prometazina reduz a adesão de E. coli nas células epiteliais HEp-2 em cultura, sugerindo uma inibição na produção de adesinas [58, 105]. Entretanto, apesar da evidência que as fenotiazinas inibem a produção de certos fatores de virulência, nenhum estudo tem descrito o efeito da CPZ além do biofilme.
CONCLUSÃO
Em resumo, a CPZ apresenta uma potente atividade antibacteriana contra micobactérias e patógenos Gram-positivos intracelulares. A capacidade que as células monofagocitárias têm de concentrar esse agente neuroléptico está relacionado a uma importante vantagem farmacocinética, uma vez que M. tuberculosis e S. aureus apresentam forte tropismo para monócitos e macrófagos. Em adição, a CPZ é capaz de inibir bombas de efluxo e promover a reversão fenotípica de bactérias resistentes, tornando-as altamente susceptíveis para as terapias convencionais. Assim sendo, conclui-se com essa revisão que a CPZ pode eventualmente ser direcionada para o arsenal terapêutico antimicrobiano contra patógenos intracelulares, especialmente no que se refere ao manejo das infecções causadas por cepas resistentes as terapias convencionais.
Entretanto, embora existam fortes evidências sobre o potencial terapêutico da CPZ em infecções bacterianas o seu uso não é recomendado nesse momento, a menos que exista a necessidade da terapia compassiva, ou seja, caso tenha exaurido todas as medidas terapêuticas tradicionais disponíveis. Para introduzir a CPZ, como monoterapia ou terapia combinada, no entanto, são necessários estudos in vivo que busquem descrever o perfil de eficácia e segurança desse composto em um contexto de infecções sistêmicas. Além disso, mais estudos clínicos controlados devem ser conduzidos para avaliar o risco-benefício associado á inclusão da CPZ no protocolo terapêutico das doenças infecciosas.















