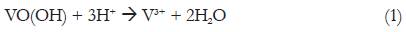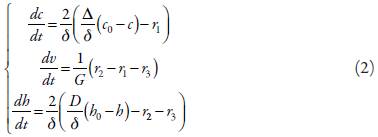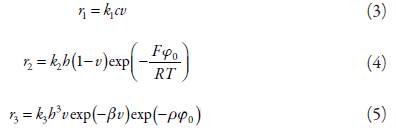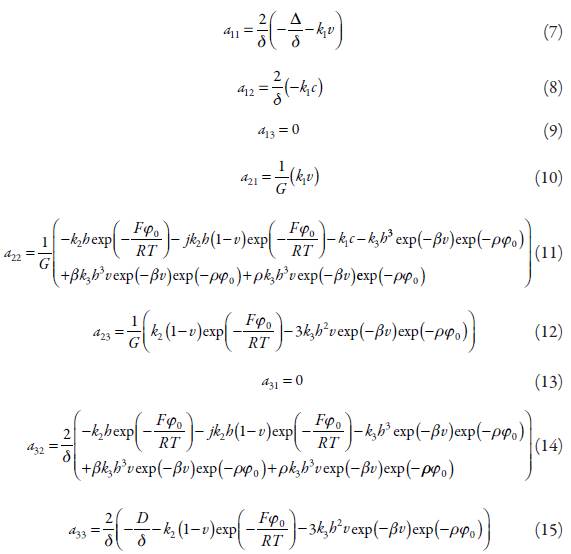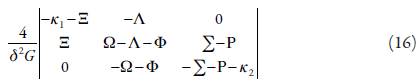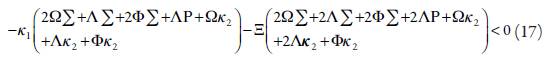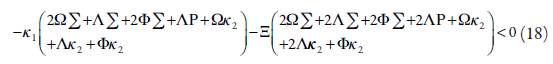INTRODUCCIÓN
La sacarina (E954, 2H-H6,2-benzotiazol-1,1,3-triona, número CAS 81-07-2) es un edulcorante artificial, que suele utilizarse con frecuencia, tanto en la industria alimentar, como en formulaciones farmacéuticas [1-3]. Ella es considerada 500 veces más dulce que el azúcar y 1,5 más dulce que el aspartamo. Pasando por el organismo humano con pequeño grado de metabolismo, se usa en alimentación especial para diabéticos [4]. Ella tiene potencial de ser antídoto para casos de envenenamiento por compuestos de metales pesados [5].
Sin embargo, como la sacarina contiene un conjunto con potencial tóxico (CO - NH - SO2, o CO - NNa - SO2, en su forma soluble) su uso es conjugado con varios efectos colaterales [6-10], por ejemplo, reacciones alérgicas y alteración de microbiota intestinal, puede provocar cáncer. Así, el desarrollo de un método eficiente, barato y rápido para su detección y cuantificación es una tarea actual [11-13], y los métodos electroquímicos pueden servirle de respuesta interesante.
Varios métodos electroanalíticos han sido desarrollados [14-16] o previstos [17-18] para la sacarina, en los que varios modificadores han sido usados. Un material interesante con potencial para ser modificador de cátodo para la reducción electroanalítica de la sacarina podría ser el oxihidróxido de vanadio (VO(OH)), un material análogo al oxihidróxido de cobalto, estable en la banda de pH entre 3 y 14, pero con un comportamiento electroquímico más inclinado para catódico, pudiendo ser sustancia activa o mediador.
Por otro lado, por ahora, ningún método electroanalítico, que use el oxihidróxido de vanadio con sacarina o cualquier otro analito ha sido desarrollado. Solamente un trabajo [19], en que VO (OH) es usado como modificador de electrodo en condensadores, ha sido publicado. De otra parte, el desarrollo y uso práctico de nuevos métodos electroanalíticos puede implicar la resolución de ciertos problemas como:
- La necesidad de combinar los parámetros de estabilidad de sustancias, que participan en el acto electroanalítico, con los de la mayor eficiencia del proceso electroanalítico.
- La posibilidad de la aparición de inestabilidades electroquímicas, que ya han sido observadas durante el desempeño del oxihidróxido de cobalto [20-21], que es un compuesto semejante.
Teniendo en cuenta lo citado, el análisis teórico a priori es necesario para describir un sistema con potencial electroquímico. Así, el objetivo general de este trabajo es el análisis aplicado para el sistema con la detección electroquímica de sacarina en el cátodo y modificado por VO(OH). El modelo matemático, capaz de describir adecuadamente el comportamiento del sistema, se desarrolla y analiza mediante la teoría de estabilidad lineal y análisis de bifurcaciones. Del análisis se concluye acerca de la eficiencia del proceso en la detección electroanalítica de la sacarina y, también se compara el comportamiento de este proceso con otros procesos los semejantes [17, 18, 22, 23].
EL SISTEMA Y SU MODELO
El esquema del proceso electroanalítico, en el que la reducción electroquímica de la sacarina es asistida por el oxihidróxido de vanadio, puede ser descrita como:
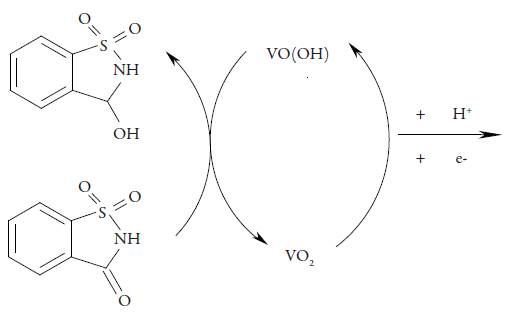
Figura 1 El esquema del desempeño de VO(OH) como modificador del cátodo en la reducción electroquímica de la sacarina.
Como se puede ver, el medio ácido es necesario para la realización del proceso electroanalítico. Entretanto, mantener el pH en valores muy bajos, inferiores a 3 llevará a la disolución de VO(OH):
Esta reacción se realiza sin oxidación o reducción, pero causa alteración en las capacitancias de la doble capa eléctrica (DCE), fuerza iónica y composición de la superficie. Si el oxihidróxido de vanado está presente en la superficie de un material polimérico o carbónico como componente de la matriz, la disolución puede ser parcial o hasta no ocurrir, solo haciendo que el ion del vanadio trivalente permanezca en la matriz.
Así, para describir el comportamiento de este sistema introducimos tres variables:
c: la concentración de la sacarina en la capa presuperficial.
v: el grado de recubrimiento de la superficie por el oxihidróxido de vanadio.
h: concentración de los protones en la capa presuperficial.
Para simplificar el modelo, suponemos que el reactor se agite intensamente, lo que nos deja menospreciar el flujo de convexión. Consecuentemente, suponemos que el electrólito de soporte esté presente en su exceso, dejándonos menospreciar el flujo de migración. Suponemos, también, que el perfil concentracional de las sustancias en la capa presuperficial sea lineal, y su espesor, constante e igual a δ.
Es posible mostrar que, considerando lo citado, el comportamiento del sistema será descrito por un conjunto de ecuaciones diferenciales conforme:
En que D y Δ son los coeficientes de difusión de los protones y de la sacarina, c0 y h0, sus concentraciones en la capa presuperficial, G es la concentración superficial máxima del oxihidróxido de vanadio en la superficie del cátodo y los parámetros r son las velocidades de las reacciones de la reducción de sacarina, regeneración y disolución del oxihidróxido de vanadio, que se pueden calcular como:
En que los parámetros k son constantes de velocidades de las respectivas reacciones, F es el número de Faraday, (0 es el salto de potencial en la doble capa eléctrica (DCE), relacionado al potencial de carga cero, las variables β y ρ describen las influencias superficiales y electroquímicas de la disolución VO(OH) a las capacitancias de la DCE, R es la constante universal de gases y T es la temperatura absoluta.
Como se ve, la presencia de un medio ácido es necesaria para mantener el proceso electroanalítico "en el aire". Sin embargo, las soluciones fuertemente ácidas llevan a la disolución del oxihidróxido e inestabilidades vinculadas a esta disolución, lo que será descrito abajo.
RESULTADOS Y DISCUSIÓN
Para investigar el comportamiento del sistema con la detección electroquímica de sacarina en soluciones ácidas, mediante un proceso de reducción, asistida por el oxihidróxido de vanadio, analizamos el conjunto de ecuaciones diferenciales (2), mediante la teoría de estabilidad linear. Los elementos estacionarios de la matriz funcional de Jacobi se presentan así:
en que:
Es posible ver que el comportamiento oscilatorio en este sistema es más probable que en los semejantes. Hay tres factores responsables por este tipo de comportamiento, contra uno o dos en los sistemas semejantes [17, 18, 22, 23].
Para que la condición principal de la bifurcación de Hopf (que describe el comportamiento oscilatorio) se satisfaga, es preciso que los elementos de la diagonal principal de la matriz (7), (11) y (15) contengan elementos positivos, correspondientes a la positiva conexión del retorno. No solo el elemento
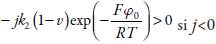 , que describe las influencias a la DCE de la electroreducción de VO2 típicas para sistemas semejantes [17, 20, 21], sino el elemento
, que describe las influencias a la DCE de la electroreducción de VO2 típicas para sistemas semejantes [17, 20, 21], sino el elemento
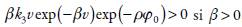 , que describe la atracción de las partículas durante la disolución de VO(OH) y el pk
3
vexp (־βν)exp (־ρφ0 ) si ρ > 0, que describe las influencias en la CDE, causadas por la formación de los iones V3+ cerca del cátodo. Las oscilaciones se esperan frecuentes y de poca amplitud.
, que describe la atracción de las partículas durante la disolución de VO(OH) y el pk
3
vexp (־βν)exp (־ρφ0 ) si ρ > 0, que describe las influencias en la CDE, causadas por la formación de los iones V3+ cerca del cátodo. Las oscilaciones se esperan frecuentes y de poca amplitud.
Para investigar la estabilidad de estado estacionario aplicamos al conjunto de ecuaciones diferenciales (2) el criterio Routh-Hurwitz. Evitando las expresiones grandes introducimos nuevas variables para que el determinante del Jacobiano se describa como:
Abriendo los paréntesis y aplicando el requisito Det J<0, según el criterio, se obtiene la condición de estabilidad del estado estacionario descrita como:
Este requisito se satisfice de forma garantizada, no habiendo influencias fuertes en la DCE y en la superficie, y, así, manteniéndose positivos los valores de los parámetros Ω y Φ. Consecuentemente, teniendo los dichos parámetros valores positivos, lo que se obtiene, cuando las variables β y ρ mantienen valores nulos o negativos, el estado estacionario se hará estable.
Entretanto, en este sistema, al contrario de la mayor parte de los semejantes [17, 18, 22, 23] la estabilidad de estado estacionario, en el aspecto más general no garantiza la eficiencia electroanalítica. De veras, siendo los valores de los parámetros Φ y P superiores a los de los demás parámetros del sistema (lo que ocurre, cuando el oxihidróxido de vanadio se disuelve de la superficie formando los cationes V+), el proceso electroanalítico no se realizará, es decir, no tendrá el sentido estipulado, aunque el estado estacionario permanezca estable.
Así, con el pH bajo, la probabilidad de la realización de inestabilidades electroquímicas en el sistema electroanalítico se hará mayor. Por eso, a pesar de la manutención muy probable de la estabilidad del estado estacionario en los valores bajos de pH, para que se realice la eficiencia electroanalítica del sistema es preciso usar las soluciones frágil o moderadamente ácidas, pudiendo hasta llegar a valores neutros (3<pH<7).
Satisfechas las condiciones de eficiencia electroanalítica del estado estacionario, la curva de la dependencia entre el parámetro electroanalítico y la concentración del analito se mantendrá lineal. Es decir, la señal electroanalítica se hará fácil de interpretar.
El proceso electroanalítico se hará controlado por la difusión, o por la reacción, dependiendo de la concentración de la sacarina, del pH, del tamaño del cátodo y de la dispersión del VO(OH) en su superficie).
La inestabilidad monotónica en este sistema también es posible. Su condición principal es Det J =0, lo que, para este sistema corresponde a:
En términos electroanalíticos, esta inestabilidad es correspondente al límite de detección, y en este punto coexisten varios estados estacionarios, todos inestables. El sistema escoge apenas uno, y este se autodestruye, cuando las condiciones del sistema se alteran.
En el caso de la nulidad de los parámetros β y ρ, las exponentes incluidas en la velocidad de la disolución se harán iguales a 1, y el comportamiento del sistema se hará más estable y menos dinámico. Aún, si la disolución de VO(OH) no ocurre o sea menospreciablemente lenta, lo que deja anular el elemento r3 y todos los elementos de la matriz, que son derivados de él. Eso también hará el comportamiento del sistema más próximo de los semejantes [17, 18, 22, 23]
CONCLUSIONES
El análisis teórico de la posibilidad de la detección electroquímica de la sacarina, asistida por el oxihidróxido de vanadio trivalente, se concluye que:
- Para la mayor eficiencia de reducción electroanalítica, es preferible usar los valores de pH, suficientes para mantener la reducción electroanalítica, pero insuficientes para disolver el modificador del cátodo, es decir, satisfaciendo el pH la condición 3<pH≤7.
- Dependiendo de varios factores del sistema, el proceso electroanalítico se controlará por la difusión o por la reacción.
- El comportamiento oscilatorio en este sistema se hará más probable, visto que hay más factores superficiales y electroquímicos, capaces de causarlo.
- La probabilidad de este tipo de comportamiento aumenta cuando hay valores relativamente bajos de pH, las oscilaciones se esperan frecuentes y de pequeña amplitud, que, mismo así, se mantendrá dependiente del pH.