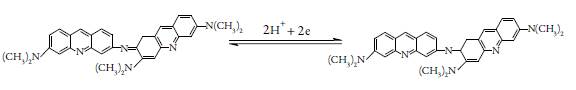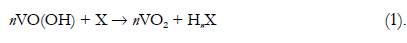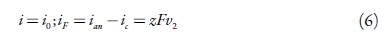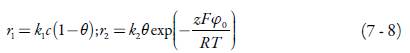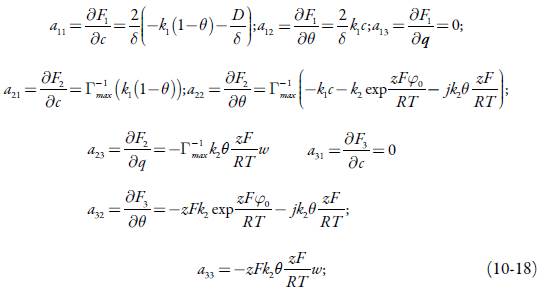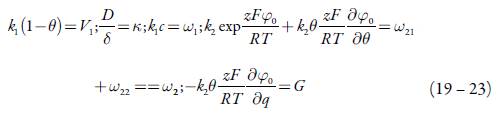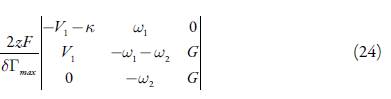INTRODUÇÃO
Entacapona (ou seja, (E)-2-ciano-3-(3,4-dihidroxi-5-nitrofenil)-N,N-dietilprop-2-e-namida, registro CAS: 130929-57-6) é um fármaco, comummente utilizado como parte da terapia complexa do tratamento da doença de Parkinson [1-4], relacionada com a baixa produção da dopamina no cérebro. O uso deste fármaco junto com o car-bidopa e levodopa consegue prolongar o efeito dos mencionados fármacos no cérebro e é mais eficaz na redução dos sintomas da doença, comparado com o uso de carbidopa e levodopa cada um só. No entretanto, esses efeitos são relacionados com a dose. Outrossim, o seu uso duradouro e excessivo pode levar aos efeitos colaterais, como náusea, vômito, dores nas costas, mudança da cor da ureia [5-8]. Destarte, o desenvolvimento de um método analítico, capaz de detectar a presença e a concentração da entacapona, rápida e eficientemente, faz-se, deveras, um problema atual [9-12].
Tanto a dopamina, como os fármacos em questão, possui uma unidade hidroquinônica, cuja atividade eletroquímica é muito conhecida [13-16]. Mas, ao contrário dos mais compostos mencionados, a entacapona possui dois grupos aceptores, comooni-trogrupo e o cianogrupo, fáceis de serem reduzidos em meio ácido, o que nos deixa realizar a sua quantificação seletiva catodicamente, usando os potenciais catódicos relativamente maiores (ou seja, mais próximos do zero). A depender do pH da solução, o potencial do elétrodo, ele pode ser reduzido conforme o processo, análogo à reação de Zínin, ou reduzindo-se o grupo nitrila, ou carbonila, ou todos. Neste caso, o cátodo poder-se-ia modificar, de forma eficiente, por um polímero condutor específico, materiais de carbono e compostos metálicos, estáveis em meio da reação [17-20] e capazes de desempenhar função de substância ativa e(ou) mediador na transferência de elétrons e prótons do cátodo para o sistema analítico, o que se manifestaria no sinal analítico.
Um desses modificadores poderia ser um material híbrido, que se obteria pela intercalação do oxihidróxido de vanádio (VO(OH)) sobre o polímero do corante alaranjado da acridina. Contendo as ligações de Schiff, capazes de transmitir prótons com facilidade, ele pode ser mediador eficiente durante o processo eletroquímico. Já o oxihidróxido poderia ser uma substância ativa, capaz de reduzir a entacapona.
No entretanto, por ora, nenhum trabalho tem sido publicado acerca do uso do oxihi-dróxido de vanádio como modificador de ânodo ou cátodo em processos eletroana-líticos (à exceção de alguns trabalhos teóricos do nosso grupo [20, 21], em que tal comportamento era previsto). E, destarte, a introdução eficiente dos novos métodos eletreoanalíticos não é possível sem uma avaliação a priori do comportamento do sistema, realizada por via teórica. Esta avaliação comportamental pretende resolver, ou, ao menos, aproximar a resolução dos problemas da:
Assim sendo, o desiderato deste trabalho é avaliar, do ponto de vista mecanístico teórico, a possibilidade da detecção eletroquímica da entacapona por meio da sua redução eletroquímica sobre o compósito poli(alaranjado da acridina) - oxihidróxido de vanádio. A realização deste objetivo inclui o alcance das seguintes metas:
- A sugestão do mecanismo da reação, incluindo o desempenho de VO(OH) no processo.
- O desenvolvimento de modelo, na base deste mecanismo.
- Análise de estabilidade do estado estacionário neste sistema (na base do modelo).
- Verificação da possibilidade das instabilidades eletroquímicas nele.
- Comparação do seu comportamento com o dos sistemas semelhantes [27, 28].
O SISTEMA E SEU MODELO
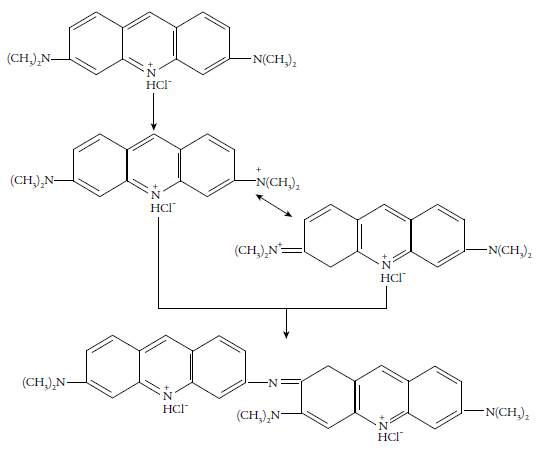
O uso do processo catódico, em vez do anódico, na determinação da entacapona, providencia uma análise eletroquímica da concentração desta mais seletiva, haja vista a menor capacidade da dopamina, da carbidopa e da levodopa de reduzir-se. Neste caso, o poli(alaranjado da acridina), cujo processo de formação é descrito na figura 1 atua como mediador, conforme o exposto na figura 2.
Já o comportamento eletroquímico do oxihidróxido de vanádio, em meio moderadamente ácido com analitos, que se reduzem recebendo o número igual de prótons e elétrons, pode ser descrito como:
A reversibilidade do elétrodo obtém-se, mediante a reação (2):
Destarte, o processo eletroanalítico da deteminação eletroquímica da entacapona pode ser descrito conforme na figura 3:
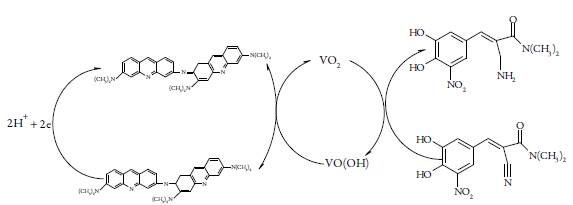
Figura 3 O esquema do funcionamento do mecanismo eletroanalítico do compósito poli(laranja da acridina) - oxihidróxido de vanádio durante a detecção eletroquímica da entacapona.
Para a modelagem matemática do comportamento deste tipo de sistemas existem dois modos de interpretação - considerar o compósito como material único (que é o mais simples) ou considerar as duas partes, que o compõem, em separado.
Em se tratando do primeiro tipo de interpretação comportamental deste tipo de sistema e em se lhe aplicando o modo galvanostático, introduzir-se-ão as três variáveis:
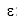 : a concentração da entacapona na camada pré-superficial.
: a concentração da entacapona na camada pré-superficial.
θ: o grau de recobrimento da superfície pelo compósito VO(OH), polímero condutor na sua forma oxidada.
q: a carga do elétrodo.
Para simplificar a modelagem, supomos que o reator esteja agitando-se intensamente (para menosprezar o fluxo de convecção), que o eletrólito de suporte esteja em excesso (para menosprezar o fluxo de migração). Também é suposto que a distribuição concentracional na camada pré-superficial seja lineal, e a sua espessura, constante, igual a S.
A entacapona entra na camada pré-superficial, por meio da sua difusão, e é reduzida pelo compósito híbrido. Destarte, a sua equação de balanço será descrita como:
Sendo
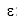 0
a concentração do analito no interior da solução, D o seu coeficiente de difusão e r1 a velocidade da reação entre a entacapona e o compósito.
0
a concentração do analito no interior da solução, D o seu coeficiente de difusão e r1 a velocidade da reação entre a entacapona e o compósito.
O compósito é oxidado após reagir com o analito e, posteriormente, reduzido eletroquimicamente, ressarcindo a sua forma inicial. Posto assim, a equação de balanço da sua forma oxidada descrever-se-á conforme:
Em que Γ max é a concentração máxima do compósito na sua forma oxidada, e r2 a velocidade da sua eletrorredução.
A carga aplicada ao elétrogo diminui, mediante a reação eletroquímica. Assim sendo, a equação de balanço da carga do cátodo será descrita como:
Sendo i a densidade da corrente, aplicada ao elétrodo, iF a corrente de Faraday.
No modo galvanostático,
Nesta equação z é o número de elétrons transferidos (que, conforme o mecanismo supracitado, é igual ao número de prótons transferidos), F = N A * e é o número de Faraday.
Em que
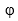 0
é o salto de potencial, comparado ao da carga zero.
0
é o salto de potencial, comparado ao da carga zero.
Neste sistema, trata-se de um caso particular do uso dos compósitos de polímeros condutores conjugados em meio galvanostático, cujas características comportamentais se descreverão abaixo.
RESULTADQS E DISCUSSÃO
O comportamento deste sistema será analisado mediante a teoria de estabilidade linear. Os elementos estacionários da matriz funcional de Jacobi veem-se conforme:
em que:
A instabilidade oscilatória, cuja realização é característica para sistemas semelhantes [27, 28], é realizada nas condições da bifurcação de Hopf, para a qual é preciso haver elementos positivos na diagonal principal da matriz de Jacobi. O único elemento, capaz de ser positivo, é a22, que pode obter valores acima do zero, no caso da negatividade de p0. O parâmetro p0 pode ser negativo, se a forma oxidada do compósito é um oxidante bastante forte, o que leva a mudanças significantes nas capacitâncias da dupla camada elétrica. Contrariamente a alguns casos, mencionados em [27, 28], em que tal comportamento podia ser causado não só por fatores eletroquímicos da DCE, mas também pelos superficiais, neste sistema é a única causa do comportamento oscilatório.
A investigação de estabilidade do estado estacionário dá-se mediante aplicação do critério de Routh-Hurwitz ao conjunto de equações diferenciais (3 - 5). Para evitar a aparição de expressões grandes, introduzimos as novas variáveis, conforme:
Destarte, o determinante do jacobiano descrever-se-á conforme:
Abrindo os parênteses e aplicando a condição de Det J<0, saliente do critério, obtemos o requisito de estabilidade do estado estacionário, expresso sob a forma de:
Como o parâmetro G é sempre negativo, e os wi sempre têm valores positivos, o sistema (não se satisfazendo os requisitos da instabilidade oscilatória) sempre existe no estado estacionário estável, correspondente ao trecho linear da dependência "parâmetro ele-troquímico-concentração" e, destarte, é confortável para a eletroanálise. Durante a detecção, a instabilidade monotônica, cuja condição é Det J=0 e que é possível para os modos potenciostático e potenciodinâmico [27,28], não se realiza. Destarte, o limite de detecção definir-se-á, neste sistema, pela composição das soluções e tamanho de elé-trodo de trabalho. Já o processo eletroanalítico será controlado pela difusão do analito.
No caso do uso do modo potenciodinâmico de voltagem constante, a resistência do compósito terá influência definitiva no comportamento do sistema, e as suas mudanças serão responsáveis pelo comportamento oscilatório. Assim, a terceira equação de balanço descrever-se-á conforme
E este caso será abordado num dos nossos próximos trabalhos.
CONCLUSÕES
A investigação mecanística teórica do sistema da eletrorredução da entacapona, assistida pelo compósito de VO(OH) com o polímero do corante alaranjado da acridina deixou concluir que:
- O oxihidróxido de vanádio trivalente pode ser usado como um perfeito modificador de elétrodo para a quantificação de metanol em meios neutro, leve e moderadamente ácido.
- O estado estacionário no sistema é fácil de obter e manter. A estabilidade do estado estacionário só pode ser atrapalhada por impactos da reação eletroquímica na DCE, que causam o comportamento oscilatório.
- A zona topológica da estabilidade do estado estacionário é muito vasta e a dependência linear entre o parâmetro eletroquímico e a concentração mantém-se facilmente.
- O limite de detecção, neste sistema, é definido apenas por medidas construtivas.
- O comportamento oscilatório neste sistema é possível, mas menos provável que nos semelhantes, haja vista a ausência das instabilidades superficiais. Ele pode ter como única causa as influências da reação eletroquímica nas capacitâncias da DCE.