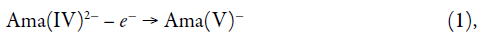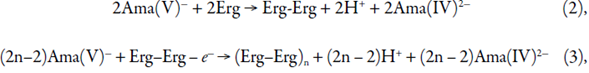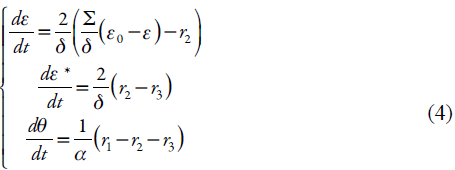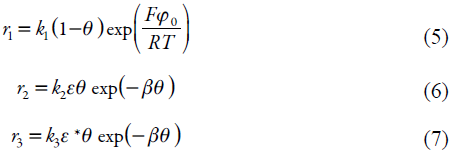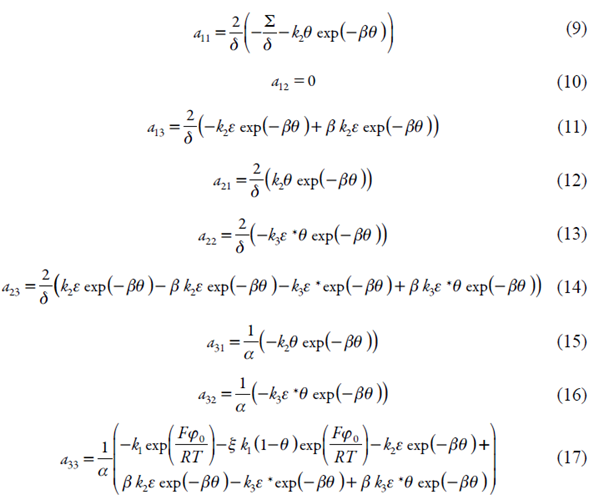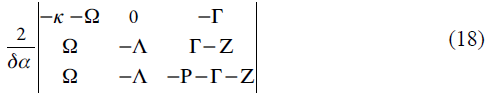INTRODUÇÃO
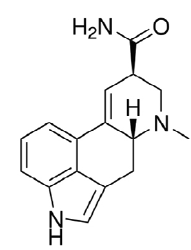
A ergina (LSA, amida do ácido lisérgico, (8β)-9,10-dideídro-6-metilo-ergolino-8-carboxamida, número CAS 478-94-4) (figura 1) é um composto psicotrópico de caráter sedativo [1-4]. Os primeiros registros do seu uso vão desde os estados mesoamericanos, que usavam as plantas, que continham a ergina, para ritos religiosos, em que com a sonolência indicada, alegadamente, vinha a perdão de todos os pecados e(ou) esquecimento total. A ergina tem composição bastante semelhante à da droga conhecida LSD.
A sua atividade biológica é dependente de dose. Já 50 μg da substância causam cansaço, falhas de memória e faltas nas funções cognitivas. Por outro lado, o seu excesso levará à manifestação de euforia descontrolável e alucinações. Malgrado o uso da ergina não cause a dependência, a maioria dos países considera a ergina como droga, com as consequências do seu tráfico, previstas por lei [3, 4]. O uso medicinal da substância é, destarte, condicionado a receita médica. Outrossim, o seu uso pelos desportistas é banido por regulamento da federação desportiva correspondente e por lei (quando aplicável). Destarte, a elaboração de um método da detecção da ergina é, sem dúvida, atual [5-8], e o uso dos métodos eletroanalíticos poderia dar bom serviço [9, 10].
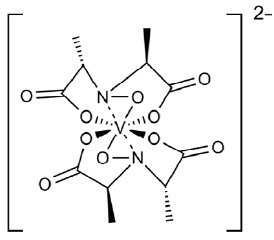
Sendo a ergina um derivado de indol, substituído por um grupo doador, ela é eletroquimicamente ativa. Ademais, a sua composição deixa pressupor que o íon amavadina (figura 2), isolado do cogumelo mata-moscas, onde desempenha função de oxidante natural [11, 12], pode ser um modificador eficiente para a detecção da ergina:
A modificação do elétrodo pela amavadina é realizada por meio da sua inserção numa matriz, porque o cátodo está coberto. A matriz pode ser baseada nos compostos com nitrogênio piridínico, como os triazóis [13, 14], capazes de estabilizar a amavadina, formando um sal com ela.
Malgrado o supracitado, o desenvolvimento prático de um processo eletroanalítico, requer, a priori, uma investigação teórica comportamental do sistema, com a análise do modelo matemático correspondente. Esta análise poderá fornecer-nos resposta a perguntas, que surgem da indecisão acerca do mecanismo mais provável do desempenho eletroanalítico do sistema, da possibilidade das instabilidades eletroquímicas, não necessariamente desejáveis para o desempenho eletroanalíticos [15, 16] e, ademais, da mera comparação entre este processo eletroanalítico e os já descritos [17, 18].
Destarte, o objetivo geral do nosso trabalho é avaliar, do ponto de vista teórico o processo da detecção eletroanalítica da ergina por um ânodo, modificado por um composto triazólico dopado pelo íon amavadina. A sua realização far-se-á mediante o desenvolvimento e a análise comportamental de estabilidade do modelo matemático, correspondente ao sistema. Ademais, comparar-se-ão este sistema e os análogos, com ênfase às diferenças mecanísticas e do desempenho [19-21].
O SISTEMA E O SEU MODELO
Na primeira etapa, o átomo de vanádio, que fica no centro do íon amavadina, é oxidado, rendendo a amavadina(V), conforme (1):
Sendo Ama(IV) e Ama(V) as amavadinas inicial e oxidada. Esta entra na reação com o analito (ergina) oxidando-o até formar o radicalcátion (e, por conseguinte, o dímero) e recuperando aquela (2-3). O cenário da polimerização da ergina não é descartável não só por causa de o potencial da oxidação do dímero ser inferior do potencial da dime-rização do monômer, mas também por serem os íons amavadina intercalados numa superfície orgânica, que promove a adesão da camada polimérica sobre o ânodo, assim como se observou durante a determinação da pesticida isoproturona sobre o polipirrol [19], o que foi observado não só experimental [19], mas também teoricamente para a determinação direta [20] e indireta [21].
Destarte, para descrever o comportamento do sistema eletroanalítico da determinação eletroanalítica da ergina, assistida pelo composto triazólico, dopado pela amavadina, introduzimos as três variáveis:
Ε: a concentração da ergina na camada pré-superficial;
Ε: * a concentração do dímero da ergina na camada pré-superficial;
θ: o grau de recobrimento da superfície do ânodo pela amavadina na sua forma oxidada.
Para simplificar a modelagem, supomos que o reator esteja agitando-se intensamente, o que nos deixa menosprezar o fluxo de convecção e as suas influências. Outrossim, supomos que o eletrólito de suporte esteja em excesso, o que nos permite menosprezar o fluxo de migração e as suas influências. Ademais, supomos que o perfil da distribuição de concentrações das substâncias na camada pré-superficial seja lineal, e a espessura da camada, estável, igual a $. Além disso, para simplificar a modelagem, a priori, não incluimos no modelo a participação do monômero da eletropolimerização do dímero (esta será incluída no modelo para um analito análogo num dos nossos próximos trabalhos).
Destarte, o comportamento do sistema será descrito pelo conjunto de equações diferenciais de balanço (CEDB), conforme (4):
Sendo Σ o coeficiente de difusão da ergina, ε 0 a concentração da ergina no interior da solução, α é a concentração superficial máxima da amavadina na superfície do ânodo modificado e os parâmetros r são as velocidades das reações correspondentes, que se podem calcular conforme:
em que os parâmetros k são as constantes de velocidade das respectivas reações, β é uma variável, que descreve as influências entre a capacitância da dupla camada elétrica (DCE) e o grau de recobrimento da superfície pela forma oxidada da amavadina, F é o número de Faraday, R é a constante universal de gases e T, a temperatura absoluta.
Em princípio, temos um sistema, em que há, de fato, a eletrooxidação gradual assistida do analito. Sem embargo, o serem os processos eletroanalíticos assistidos pelos compostos iónicos faz com que se influencia fortemente a DCE aquando do processo. Essas influências têm valor importante para o comportamento do sistema, o que será descrito abaixo.
RESULTADOS E DISCUSSÃO
Para descrever o comportamento do sistema com a detecção eletroanalítica da ergina, assistida pela amavadina, analisamos, mediante a teoria de estabilidade linear e da análise de bifurcações o CEDB (4), havendo vista as relações algébricas (5-7). Os elementos estacionários da matriz funcional de Jacobi podem ser descritos conforme:
Sendo:
Tendo em conta os elementos da diagonal principal (9), (13) e (17), é possível confirmar que o comportamento oscilatório, neste caso, é possível. É mais provável que no caso da detecção, assistida por um óxido ou oxihidróxido de metal [19, 0], por haver mais fatores, que influenciam o comportamento da DCE, mas menos provável que no caso da eletrodetecção e eletropolimerização direta [21], por não haver instabilidades superficiais
Além do elemento ξ K
1 (1-θ) exp
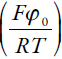 >0, caso ξ<0, que descreve as influências da etapa eletroquímica na capacitância da DCE, responsáveis pela aparição da positiva conexão de retorno (e, por conseguinte, o comportamento oscilatório), existe, também o par de elementos β(r2 + r3), que descreve a influência das mudanças periódicas do valor da capacitância da DCE, que se observam aquando da transformação mútua das formas iónicas da amavadina. As oscilações se preveem mais frequentes e menos amplas que e [20], mas menos frequentes e mais amplas que em [21].
>0, caso ξ<0, que descreve as influências da etapa eletroquímica na capacitância da DCE, responsáveis pela aparição da positiva conexão de retorno (e, por conseguinte, o comportamento oscilatório), existe, também o par de elementos β(r2 + r3), que descreve a influência das mudanças periódicas do valor da capacitância da DCE, que se observam aquando da transformação mútua das formas iónicas da amavadina. As oscilações se preveem mais frequentes e menos amplas que e [20], mas menos frequentes e mais amplas que em [21].
Para investigar a estabilidade do estado estacionario, aplicamos ao CEDB (4) o critério Routh-Hurwitz. Evitando a aparição de expressões grandes, introduzimos as novas variáveis, fazendo que o determinante da matriz se descreva conforme:
Abrindo os parênteses e aplicando a condição Det /<0, saliente do critério, obtemos o requisito de estabilidade do estado estacionário, expresso conforme:
O primeiro multiplicador só pode ter (do ponto de vista do senso físico dos fatores, a que se referem) valores negativos. Destarte, a expressão inteira do lado esquerdo da inequação (19) só pode ter valores negativos, sendo positivo o outro multiplicador. Isto se realiza, quando as influências da DCE dos processos eletroquímico e químico da dimerização têm menos efeito que o efeito estabilizador da transformação equirrítmica das substâncias.
Vale a pena mencionar que o elemento, que é correspondente à polimerização do dímero, é excluído da inequação final. Assim, a estabilidade do estado estacionário, bem como a inestabilidade monotônica, ficam indiferentes às influências da eletropolimerização do dímero.
Havendo vista o supracitado, poder-se-á concluir que se trata de um sistema eletroanalí-tico eficiente, controlado pela difusão da ergina. Não havendo reações laterais, capazes de comprometer a estabilidade do analito e(ou) modificadores (o que se realiza neste caso), do ponto de vista eletroanalítico, a estabilidade do estado estacionário é correspondente à dependência linear entre o parâmetro eletroquímico e a concentração do analito.
A condição da instabilidade monotônica, relativa ao limite de detecção, para este sistema descreve-se conforme:
que, devido à não nulidade do primeiro multiplicador, será simplificada até (21):
Neste ponto, realiza-se a igualdade das influências estabilizadoras a desestabilizadoras.
Este modelo é útil para descrever o caso geral da eletropolimerização assistida de um monômero, obtido pela eletrossíntese assistida pelo mesmo íon. Porém, no caso mais geral dos derivados de indol, substituídos pelos grupos doadores, a participação do monômero inicial da polimerização do dímero não é descartada. Este caso vai ser descrito num dos nossos próximos trabalhos.
O produto da polimerização é, de fato, um compósito polimérico, em que a amavadina será intercalada entre as duas camadas orgânicas. Este material por si só pode ser usado em sistemas eletroanalíticos.tanto como substância ativa como mediador. O seu uso também será descrito posteriormente pelo nosso grupo.
CONCLUSÕES
Da análise teórica do processo da determinação eletroanalítica da ergina (LSA), assistida pelo sal de um derivado triazólico com a amavadina foi possível concluir que:
- Em se tratando da determinação da ergina, o íon amavadina é um modificador eficiente para a sua detecção e eletropolimerização;
- O processo eletroanalítico é controlado pela difusão do analito;
- O estado estacionário estável mantém-se facilmente, sendo correspondente à linearidade da dependência entre o parâmetro eletroquímico e a concentração;
- O comportamento oscilatório, neste caso, é mais provável que no sistema da detecção e polimerização, assistida por um óxido de metal, mas menos provável que no caso da eletrooxidação direta.