Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Obstetricia y Ginecología
Print version ISSN 0034-7434
Rev Colomb Obstet Ginecol vol.64 no.4 Bogotá Oct./Dec. 2013
Recibido: agosto 20/13 - Aceptado: noviembre 8/13
1 Médico cirujano. Especialista en Obstetricia y Ginecología. Magíster en Epidemiología. Director Centro NACER. Docente, Universidad de Antioquia. Medellín, Colombia.
2 Coordinador Epidemiología Clínica de la subguía. Enfermero. Especialista en Gerencia de IPS. Magíster en Epidemiología. Medellín, Colombia.
3 Médica cirujana. Especialista en Obstetricia y Ginecología. Magíster en Salud Pública. Coordinadora Área Salud Sexual y Reproductiva, NACER-Universidad de Antioquia. Medellín, Colombia.
4 Médico cirujano. Especialista en Obstetricia y Ginecología. Magíster en Epidemiología. Docente, Universidad de Antioquia, NACER. Medellín, Colombia.
5 Médico cirujano. Especialista en Obstetricia y Ginecología. Coordinador del Área de Educación, NACER-Universidad de Antioquia. Medellín, Colombia.
6 Jesús Arnulfo Velásquez Penagos, MD. Médico cirujano. Especialista en Obstetricia y Ginecología. Fellow en Cuidado Crítico Obstétrico. Coordinador de Mortalidad Materna-NACER. Docente, Universidad de Antioquia. Medellín, Colombia.
* Representantes Grupo Desarrollador de la Guía - Universidad Nacional de Colombia - Alianza CINETS. Lista completa al final del documento.
RESUMEN
Objetivo: formular recomendaciones basadas en la mejor evidencia disponible que sirvan como guía para los profesionales de salud en la prevención, detección y el manejo de la hemorragia posparto y de las complicaciones asociadas a la misma con el fin de homogeneizar las conductas clínicas y contribuir a la reducción de la morbi-mortalidad materna.
Materiales y métodos: el grupo desarrollador de la Guía (GDG) elaboró esta GPC durante 2011-2012 acorde con la Guía Metodológica para la elaboración de Guías de Atención Integral en el Sistema Generalde Seguridad Social en Salud colombiano, basándose en la evidencia científica disponible y sumando la participación activa de grupos de pacientes, sociedades científicas y grupos de interés. En particular, la evidencia de esta Guía fue adaptada de las GPC del Royal College of Obstetricians and Gynaecologists (RCOG) “Prevention and management of postpartum haemorrhage” (2009) y de la Organización Mundial de la Salud (OMS), “WHO guidelines for the management of postpartum haemorrhage and retained placenta” (2009), y actualizada por medio de procedimientos sistemáticos, tanto para la búsqueda y la valoración de la evidencia, como para la generación de recomendaciones. El nivel de evidencia y la fuerza de las recomendaciones fueron expresadas por medio del sistema del Scottish Intercollegiate Guidelines Network (SIGN).
Resultados: se presentan recomendaciones para la prevención, detección y el tratamiento de la hemorragia posparto a partir de 17 preguntas clínicas.
Conclusión: se presenta una versión resumida de las recomendaciones y evidencia de esta Guía, que se espera sea adoptada por los profesionales de la salud encargados de la atención del embarazo en el país para disminuir la morbilidad y mortalidad asociada a la gestación.
Palabras clave: hemorragia posparto, choque hemorrágico, guías de práctica clínica, práctica clínica basada en la evidencia, Colombia.
ABSTRACT
Objective: To make recommendations based on the best available evidence designed to guide healthcare professionals in the prevention, detection and management of post-partum bleeding and complications associated with it, in order to arrive at uniform clinical practices and contribute to the reduction of maternal morbidity and mortality.
Materials and methods: The Guideline Developer Group (GDG) prepared this CPG during 2011-2012, in accordance with the Methodology Guideline for the development of Comprehensive Care Guidelines of the Colombian General System of Social Security, based on the available scientific evidence, and with the active participation of patient groups, scientific societies and stakeholders. In particular, the evidence for these Guidelines was adapted from the CPG of the Royal College of Obstetricians and Gynaecologists (RCOG) “Prevention and management of postpartum haemorrhage” (2009) and of the World Health Organization (WHO), “WHO guidelines for the management of postpartum haemorrhage and retained placenta” (2009) and updated through systematic procedures for the search and assessment of the evidence as well as for the generation of recommendations. The level of evidence and the power of the recommendations were expressed using the Scottish Intercollegiate Guidelines Network (SIGN) system.
Results: Recommendations are presented for the prevention, detection and treatment of postpartum haemorrhage based on 17 clinical questions.
Conclusion: We present a summarized version of the recommendations and the evidence for these guidelines, which are expected to be adopted by healthcare practitioners in charge of pregnancy care in Colombia, in order to reduce pregnancy-associated morbidity and mortality.
Key words: Postpartum haemorrhage, hemorragic shock, evidence-based clinical practice, Colombia.
INTRODUCCIÓN
Las complicaciones hemorrágicas asociadas el embarazo continúan como una de las principales causas de muerte materna en el mundo y en Colombia (1). La principal causa de hemorragia obstétrica es la hemorragia posparto. Según la Organización Mundial de la Salud (OMS), la incidencia promedio de la hemorragia posparto en el mundo es de 6,09% (IC 95%: 6,06-6,11); esta cifra varía con la metodología objetiva o subjetiva empleada para la medición del sangrado (10,55 y 7,23%, respectivamente). La hemorragia posparto masiva es un evento que se presenta en 1,86% de los partos (IC 95%: 1,821,9) y es la primera causa de muerte materna en el mundo. La incidencia en América Latina y el Caribe se estima en 8,9% según una revisión sistemática que evaluó este evento en diferentes regiones del mundo (IC 95%: 8,03-9,86) (2). Estos mismos estudios no confirmaron la influencia de los factores de riesgo asociados tradicionalmente a la hemorragia posparto como la multiparidad o el embarazo múltiple (3) y, por el contrario, en dos tercios de las mujeres que la sufren no se logra identificar ningún factor de riesgo asociado (4). En los países en vías de desarrollo el riesgo de morir a causa de una hemorragia posparto es de 1 por cada 1000 nacimientos en un periodo determinado, mientras que en países desarrollados como el Reino Unido, el riesgo es 100 veces menor. Cada año en el mundo aproximadamente 14 millones de mujeres sufren de hemorragia posparto y de ellas, 125.000 fallecen debido a la falta de reconocimiento de las causas y a deficiencias con el tratamiento oportuno y adecuado (2). La hemorragia obstétrica no es solo la primera causa de muerte materna, sino que es también la primera causa de morbilidad obstétrica extrema (5). Las principales complicaciones derivadas de la hemorragia obstétrica incluyen el choque hipovolémico, la coagulación intravascular diseminada, y la disfunción o falla de órganos como el riñón, el hígado y el pulmón. Las mujeres, además, se ven expuestas a los riesgos derivados de transfusiones masivas y a consecuencias como la realización de cirugías radicales como la histerectomía.
La disponibilidad de una Guía de Práctica Clínica (GPC) para la prevención, detección temprana y tratamiento de hemorragia posparto implica estandarizar para Colombia el cuidado de la mujer gestante, con énfasis en la necesidad de la prevención, la detección temprana y el tratamiento oportuno en todos los niveles de atención, a fin de reducir la morbimortalidad materna asociada y promover la optimización de la salud materna y la calidad de la atención médica en todos los niveles de atención obstétrica.
En el presente artículo se presenta una versión abreviada de la información contenida en la GPC de Embarazo y Parto referente a la sección de manejo de las complicaciones hemorrágicas asociadas al embarazo, en la que se muestra la evidencia relacionada para cada tema y se presentan las recomendaciones elaboradas por el GDG durante el proceso de desarrollo de esta GPC. El grupo desarrollador de la Guía (GDG) elaboró esta GPC durante 2011-2012 acorde con la Guía Metodológica para la elaboración de Guías de Atención Integral en el Sistema General de Seguridad Social en Salud colombiano, basándose en la evidencia científica disponible y sumando la participación activa de grupos de pacientes, sociedades científicas y grupos de interés. En particular, la evidencia de esta sección fue adaptada de las GPC del Royal College of Obstetricians and Gynaecologists (RCOG), “Prevention and management of postpartum haemorrhage” (2009) (6) y de OMS, “WHO guidelines for the management of postpartum haemorrhage and retained placenta” (2009) (7), y actualizada por medio de procedimientos sistemáticos, tanto para la búsqueda y valoración de la evidencia como para la generación de recomendaciones. El nivel de evidencia y la fuerza de las recomendaciones fueron expresadas por medio del sistema del Scottish Intercollegiate Guidelines Network (SIGN). La versión completa de esta GPC (incluida la búsqueda sistemática de información científica y la presentación detallada de la evidencia científica), así como la versión para pacientes y sus anexos, están disponibles para la consulta de los interesados por diferentes medios (físicos y electrónicos) (8, 9).
1. ¿Cuáles son las intervenciones efectivas para prevenir la hemorragia posparto al finalizar el segundo periodo del parto?


La evidencia indica que el manejo activo del alumbramiento disminuye la pérdida de sangre materna y reduce el riesgo de hemorragia pos-parto de más de 1.000 mL. El agente de elección para el manejo activo del alumbramiento debe ser la oxitocina en una dosis de 5 UI o 10 UI; aunque la vía de administración más frecuentemente usada es la intramuscular, el GDG consideró importante sugerir la posibilidad de administrar la profilaxis con oxitocina por vía intravenosa cuando exista un acceso venoso permeable, dado que no hay evidencia que favorezca la vía intramuscular (IM) sobre la intravenosa (IV).
La consideración del uso de otros agentes oxitócicos diferentes a la oxitocina requiere de mayor evidencia que soporte su uso en la práctica diaria. Aunque el misoprostol no es tan efectivo como la oxitocina para la prevención de la hemorragia pos-parto, puede ser usado cuando la oxitocina no esté disponible. El efecto específico del masaje uterino con uterotónicos o sin estos en la prevención de la hemorragia posparto requiere más ensayos con mayor número de participantes para evaluar su eficacia en estos casos. Por otra parte, retrasar el corte del cordón umbilical por al menos 2 o 3 min parece no incrementar el riesgo de hemorragia posparto.
2. ¿Cuál es la intervención más efectiva para prevenir la hemorragia posparto en una paciente sometida a cesárea?


La evidencia indica que la oxitocina es el agente de elección para la prevención de la hemorragia posparto en mujeres sometidas a cesárea. Algunos estudios han subrayado que la dosis actualmente utilizada puede ser más alta que la necesaria para lograr el efecto deseado y, por tanto, estas dosis podrían producir cambios hemodinámicos importantes en la mujer. De igual forma, la evidencia demuestra que la infusión de una dosis baja de oxitocina después de una dosis inicial reduce la necesidad de uterotónicos adicionales en cesárea, pero no afecta la ocurrencia general de hemorragia obstétrica mayor. Lo que es claro con la evidencia actual es que la adición de una infusión de oxitocina en pacientes sometidas a cesárea electiva no afecta los parámetros hemodinámicos maternos, ni durante, ni después de la cirugía. Al parecer, la carbetocina puede ser tan efectiva como la oxitocina en la reducción del sangrado después de parto por cesárea y en el uso de uterotónicos adicionales, no así para la hemorragia mayor de 500 mL. La ventaja que ofrece la carbetocina es la dosis única y no tener que utilizar infusiones adicionales. Recientemente, la Comisión de Regulación en Salud publicó un estudio de efectividad, seguridad y análisis económico de la carbetocina frente a la oxitocina en la prevención de la atonía uterina y hemorragia posparto de mujeres sometidas a cesárea. La conclusión del análisis económico indica que el uso de carbetocina resulta 70 veces más costoso en comparación con la oxitocina. Por tanto, no se puede emitir un concepto de favorabilidad o no favorabilidad para el uso de carbetocina en la prevención de la hemorragia posparto en mujeres sometidas a cesárea (40).
3. ¿Cuáles son las intervenciones necesarias para disminuir el riesgo de hemorragia grave y complicaciones en mujeres con diagnóstico antenatal de acretismo placentario?


La técnica del ultrasonido resulta importante para realizar el diagnóstico antenatal de inserción anormal de la placenta y la planeación de la atención del parto. El GDG consideró que el ultrasonido con Doppler debe ser realizado por personal calificado, buscando identificar al máximo la localización y el grado de inserción de la placenta. Así mismo, se consideró importante que estas ecografías se realicen en una edad gestacional donde haya viabilidad fetal para mejorar los desenlaces maternos y fetales.
Dejar la placenta acreta en su sitio parece ser una alternativa más segura que removerla. El tratamiento conservador para la placenta acreta puede ayudar a las mujeres a evitar una histerectomía y presenta bajas tasas de morbilidad materna cuando se realiza en instituciones con los equipos y los recursos adecuados.
4. ¿Cuál es la intervención más efectiva para tratar la retención placentaria sin sangrado, después de manejo activo del alumbramiento?


La inyección por la vena umbilical de prostaglandinas requiere de investigaciones adicionales, aunque los resultados de dos ensayos clínicos evidencian un impacto en la disminución de remoción manual de la placenta.
El consenso de expertos de la “Guía de práctica clínica para el manejo de la hemorragia posparto y placenta retenida” publicada por la OMS (7), no halló evidencia que soportara el uso de uterotónicos para el manejo de la placenta retenida sin sangrado. Sin embargo, este grupo recomendó la administración de una nueva dosis de oxitocina y realizar un nuevo intento de extracción por tracción controlada. Ante esto el GDG junto, con el grupo de expertos consultados, consideró importante subrayar que no se debe mantener de forma persistente la tracción controlada del cordón y que es suficiente una sola tracción para procurar la extracción de la placenta retenida como coadyuvante a la administración de la oxitocina.
Así mismo, dadas las condiciones geográficas y la atención por niveles establecida en el sistema de salud, es aconsejable diferenciar el manejo por niveles de atención. Para el primer nivel resulta importante no intentar más de una sola tracción y una dosis adicional de oxitocina. En su defecto, es recomendable iniciar una infusión de oxitocina y remitir la paciente a un nivel superior, donde se pueda garantizar un manejo adecuado. El GDG también consideró que la extracción manual debe realizarse en una institución que cuente con los recursos necesarios para atender cualquier complicación derivada de un posible acretismo placentario.
5. ¿Se recomienda el uso profiláctico de antibióticos cuando se realiza revisión manual de la cavidad uterina?


El consenso de expertos de la guía de práctica clínica para el manejo de la hemorragia posparto y placenta retenida de la OMS (7) recomendó el uso de cefalosporina de primera generación basados en evidencia indirecta de estudios realizados en mujeres sometidas a cesárea y de mujeres con aborto. El GDG consideró la necesidad de incluir otra posibilidad antibiótica en los casos de alergia documentada, así como la importancia de contar con un perfil microbiológico que apoye de forma más segura la elección del antibiótico que se va a utilizar.
6. ¿Cuáles son los criterios que determinan el inicio del manejo del choque hipovolémico?


La evidencia narrativa retoma los signos de choque hipovolémico de la clasificación de Baskett (54), enfatizando dos aspectos importantes: en primer lugar, debido al aumento del volumen plasmático que ocurre en la mujer durante el embarazo, cualquier porcentaje de pérdida representa para la gestante un volumen mayor que en la mujer no embarazada. En segundo lugar, se debe tener en cuenta que las alteraciones del pulso y la presión arterial son tardías en la mujer embarazada, por tanto, el estado de conciencia y la perfusión deben ser evaluados inicialmente. El GDG consideró que el estado de choque lo establece el peor parámetro encontrado después de evaluar a la mujer con hemorragia posparto.
7. ¿Cuáles son las intervenciones más efectivas para el manejo de la hemorragia posparto con signos de choque?


No se encontró evidencia relacionada con la eficacia de las intervenciones o los procedimientos complementarios necesarios para el manejo de la hemorragia posparto. Para la atención se deben considerar al menos cuatro componentes: la comunicación con todos los profesionales relevantes, la resucitación, el monitoreo e investigación de la causa del sangrado y las medidas para contrarrestar el sangrado. Estos componentes deben ser iniciados simultáneamente para brindar un cuidado óptimo. Es fundamental alertar tempranamente al grupo de profesionales pertinente para el manejo de la hemorragia posparto.
El GDG consideró importante definir una forma estandarizada de activar el protocolo de atención y adoptar el nombre de código rojo obstétrico para nombrarlo. Así mismo, es importante reorganizar las acciones de intervención ante una mujer con hemorragia posparto, teniendo en cuenta las consideraciones de la GPC del RCOG (6). Es indispensable estructurar un enfoque de ABC que permita, además de la resucitación, la identificación de otros problemas. La urgencia y las medidas instauradas para la resucitación y el control de la hemorragia necesitan estar en la medida del grado del choque. Debe administrarse oxígeno en altas concentraciones sin tener en cuenta la concentración del oxígeno materno. Usualmente, los niveles de conciencia y el control de la oxigenación mejoran rápidamente una vez el volumen de circulación es restaurado.
Es indispensable establecer dos accesos venosos de buen calibre y tomar muestras de sangre para optimizar el manejo y la necesidad de terapia transfusional. Los componentes principales de la resucitación durante la hemorragia posparto son la restauración del volumen de sangre y la capacidad de transportar oxígeno. El reemplazo de volumen debe ser llevado a cabo sobre la base de que la pérdida de sangre es, a menudo, subestimada (55, 56). El cuadro clínico debe ser el principal determinante de la necesidad y urgencia de la transfusión de hemoderivados y no se debe perder el tiempo esperando los resultados de laboratorio (57, 58).
Una vez que el sangrado está bajo control, se debe considerar transferir a la mujer a una unidad de cuidados intensivos o a una unidad de cuidados intermedios, dependiendo de la severidad del sangrado. Es necesario el monitoreo médico continuo y el registro de los parámetros en el tiempo sugerido en formatos preestablecidos, los cuales darán a los profesionales que intervienen en el manejo de la mujer señales visuales adecuadas sobre su evolución clínica.
8. ¿Cuáles son las medidas más efectivas para la recuperación del volumen sanguíneo en el manejo del choque hipovolémico por hemorragia obstétrica?


El uso de la albúmina y de coloides para el manejo de la hemorragia posparto no se recomienda porque aunque no se encuentra evidencia directa en la obstetricia, se considera que el manejo del choque hipovolémico puede no diferir entre pacientes con condiciones específicas y variadas. Según esto, el riesgo de muerte de una mujer en el posparto con la administración de coloides puede ser similar al reportado en otro tipo de pacientes.
Aunque no existe evidencia de la cantidad de volumen por transfundir, la GPC del RCOG (6) propone un volumen total de 3,5 litros. El GDG y el grupo de expertos consultados consideró que iniciar con volúmenes altos sin hacer una medición frecuente de los cambios en los parámetros clínicos puede acarrear consecuencias en la recuperación de la mujer con choque hipovolémico; por este motivo, se sugirió la evaluación cada 5 min de la respuesta a la infusión de cristaloides para determinar la continuidad en la infusión de los mismos.
Probablemente, la elección de un vasopresor en pacientes con choque no influye sobre el resultado más allá del efecto mismo del vasopresor. Ante esta evidencia, el GDG consideró que se pueden utilizar vasopresores una vez se halla verificado una adecuada reposición de volumen y un control adecuado del sitio del sangrado, pero sin que su uso retrase la implementación de otras medidas o una remisión a un nivel de mayor complejidad. Seleccionar uno u otro vasopresor dependerá de la disponibilidad de los mismos, de la vía de acceso disponible para su administración y del entrenamiento del personal que lo vaya a utilizar.
9. ¿Cuáles son las intervenciones más efectivas para el control de la hemorragia por atonía uterina?


El tratamiento debe estar acompañado por un examen clínico cuidadoso para comprobar que el útero en efecto está atónico y que las otras fuentes de sangrado, tales como traumas y laceraciones genitales o inversión uterina, han sido excluidas.
La compresión uterina bimanual y el vaciamiento de la vejiga para estimular la contracción uterina representan la primera línea de manejo de la hemorragia posparto, así como la compresión de la aorta que, como medida temporal pero efectiva, permite lograr tiempo en la resucitación con la reposición de volumen y en la elección del soporte quirúrgico apropiado. Aunque no existen estudios publicados que provean evidencia para estas intervenciones, el consenso de expertos de la guía del RCOG (6) y de la guía de la OMS (7), soportan la continuidad de su uso.
La evidencia no muestra que la adición de misoprostol sea superior a la combinación de oxitocina y ergometrina sola para el tratamiento de la hemorragia posparto primaria. La oxitocina es preferida especialmente en mujeres con hipertensión previa o preeclampsia. Los resultados de ensayos clínicos muestran que el uso de una dosis de 800 mcg de misoprostol parece ser tan efectivo como la oxitocina cuando se usa para detener el 1++ sangrado posparto por sospecha de atonía uterina en mujeres que han recibido oxitocina profiláctica.
El consenso de expertos de la guía del RCOG (6) sugiere una dosis no mayor a 5 UI de oxitocina por vía intravenosa lenta, ya que tal recomendación está en concordancia con las guías de otras organizaciones. El GDG consideró importante adicionar una infusión de oxitocina que permita mejorar las contracciones uterinas y así lograr disminuir la hemorragia posparto. Por otra parte, no consideró útil la inclusión de una recomendación para apoyar el uso del carboprost como medicamento en el manejo de la hemorragia posparto por atonía uterina debido a la ausencia de evidencia más consistente y de mejor calidad, y por ser un medicamento que no se consigue en el país.
El GDG consideró importante incluir el ácido tranexámico dentro de las recomendaciones, pero ajustando la dosis y aclarando que solo se debe usar cuando los demás agentes como la oxitocina, la ergometrina y el misoprostol no hayan sido efectivos. Así mismo, por la ausencia de evidencia disponible, no se recomienda una segunda dosis de ácido tranexámico. Se requieren más estudios para aclarar la efectividad del masaje en el escenario de la hemorragia posparto.
10. ¿Cuáles son las intervenciones más efectivas para el control de la hemorragia posparto por atonía uterina sin respuesta al manejo médico?


El uso de agentes farmacológicos no debe retrasar el recurso quirúrgico en los casos de hemorragia por atonía uterina. Una vez se toma la decisión, la elección del procedimiento depende de la experiencia y la experticia del equipo de profesionales disponibles. Es importante tener en cuenta las aspiraciones reproductivas futuras de la mujer en la decisión de la secuencia apropiada de intervenciones. Las técnicas quirúrgicas tales como el taponamiento uterino y las suturas hemostáticas pueden detener el sangrado de forma inmediata y facilitar una pronta decisión con respecto a la necesidad de la histerectomía. La técnica B-Lynch como alternativa al manejo de la hemorragia pos-parto es invaluable y puede proveer un primer paso quirúrgico para detener la hemorragia cuando las medidas con oxitócicos han fallado.
El GDG consideró importante incluir el manejo antibiótico cuando se utiliza el taponamiento uterino con balón para el control de la hemorragia posparto bajo los mismos preceptos formulados en la revisión de la cavidad uterina y la extracción manual de la placenta. En relación con el tiempo durante el cual se debe dejar el balón, se consideró que un máximo de 24 horas puede ser adecuado en ausencia de evidencia clara sobre este tópico. La histerectomía no se debe retrasar hasta que la mujer esté in extremis o mientras se intentan procedimientos menos definitivos si el obstetra tiene menos experiencia en ellos.
11. ¿Cuál es el mejor tipo de histerectomía indicada para el manejo de la hemorragia posparto?


La técnica subtotal de histerectomía es la cirugía de elección en muchos casos; hay menos trauma en el cérvix y en el segmento inferior. Aunque no se encuentra diferencia en la morbilidad materna entre la histerectomía total y subtotal, el daño del tracto urinario fue la complicación reportada con más frecuencia cuando se realizó histerectomía total comparada con la subtotal. Se considera que la experticia del clínico cobra relevancia en esta intervención, ya que ante una hemorragia y un útero aumentado de tamaño, la probabilidad de que una histerectomía sea total o subtotal dependerá de otros factores adicionales.
12. ¿Cuáles son las intervenciones más efectivas para el control de la hemorragia posparto por acretismo placentario?


El GDG consideró importante la opción de realizar ligadura bilateral de la arteria uterina, seguida de una sutura de B-Lynch en mujeres con acretismo placentario que desean preservar su fertilidad. De igual forma, la opción de realizar oclusión perioperatoria de la arteria iliaca interna, si se cuenta con el recurso para realizarla, puede ser adecuada. Como punto importante, no se debe intentar tratar a estas pacientes en instituciones que no cuenten con recurso humano y tecnológico suficiente para manejar las complicaciones.
Así mismo, se consideró como punto fundamental no intentar separar la placenta en lugares o instituciones donde no se cuente con personal y equipos necesarios y suficientes para atender el caso. Por tanto, una remisión oportuna a una institución de mayor complejidad donde se pueda realizar la extracción de la placenta y al mismo tiempo el manejo de la hemorragia, es vital para disminuir los riesgos de morbilidad y mortalidad.
13. ¿Cuál es la intervención más efectiva para el manejo de la hemorragia obstétrica por abrupcio de placenta?


La escasa evidencia actualizada y de calidad sobre el manejo de la hemorragia por abrupcio de placenta lleva a considerar intervenciones muy generales y que indiscutiblemente van a estar supeditadas a la situación específica de cada mujer que presente el evento. El GDG consideró que en mujeres con abrupcio y feto muerto se debe evitar al máximo realizar una cesárea y se debe insistir en parto vaginal, simultáneamente con el manejo integral de la situación.
14. ¿Cuáles son las recomendaciones generales para el uso de hemoderivados en el tratamiento de la mujer con hemorragia obstétrica?
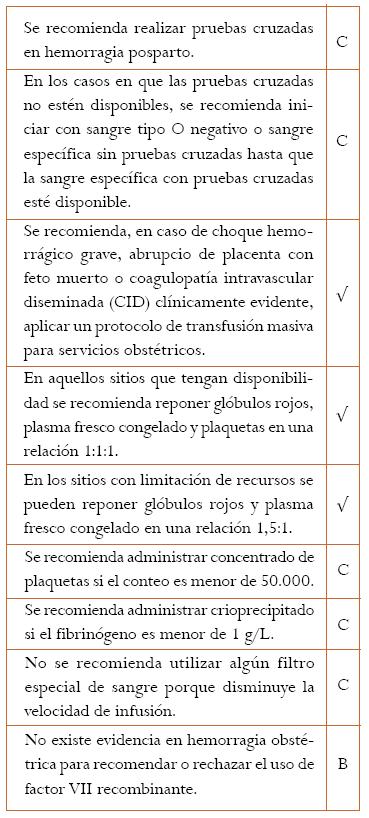

Si las pruebas cruzadas no están disponibles se debe brindar la mejor alternativa para restaurar la capacidad de transporte de oxígeno. La sangre tipo O negativo puede ser el camino más seguro para evitar una incompatibilidad transfusional. Cuando la pérdida de sangre alcance alrededor de los 4,5 litros y se hayan administrado grandes volúmenes de cristaloides, habrá defectos en los factores de coagulación de la sangre y se tendrán que administrar algunos hemoderivados.
El GDG consideró que la reposición de volumen con hemoderivados para mejorar la capacidad de transporte de oxígeno y corregir los problemas de coagulación debe hacerse en una relación 1:1:1. En instituciones donde la disponibilidad de hemoderivados no es muy amplia puede hacerse una reposición en una relación de 1,5 a 1.
15. ¿Cuál es la indicación más efectiva para transfundir en ausencia de sangre O negativo?


Aunque no todos los estudios relacionan las unidades transfundidas con los desenlaces presentados, parece claro que a pesar de brindar una seguridad relativa, la transfusión de glóbulos rojos sin pruebas cruzadas y de sangre tipo “O” positivo en ausencia de sangre tipo “O” negativo se debe limitar y considerar en cada caso específico.
16. ¿Cuáles son los aspectos logísticos para tener en cuenta en el manejo del choque hipovolémico por causa obstétrica?


El consenso de expertos de la Guía para el manejo de la hemorragia posparto y la placenta retenida de la OMS (53) considera que la implementación de un protocolo formal es un proceso complejo que requiere adaptaciones locales.
17. ¿Cuál es la estrategia más efectiva para mejorar las habilidades del personal de salud en el manejo de la hemorragia obstétrica?


Aunque se requieren más estudios que permitan mostrar cambios positivos en la incidencia de complicaciones y de mortalidad a través del mejoramiento de habilidades técnicas, comunicacionales y del conocimiento, es claro que el camino hacia este propósito es el entrenamiento en escenarios de simulación y un acompañamiento continuo para el mantenimiento de las habilidades adquiridas.
DECLARACIÓN DE CONFLICTOS DE INTERÉS
El trabajo científico de investigación, así como la elaboración de las recomendaciones incluidas en el presente documento, fueron realizados de manera independiente por el Grupo Desarrollador de Guías (GDG) de la Universidad Nacional de Colombia. Todos los miembros del GDG, así como las personas que han participado tanto en la colaboración experta como en la revisión externa, realizaron declaración de conflictos de interés previo a su participación. Esta Guía se publica con el permiso del Ministerio de Salud y Protección Social y el Departamento de Ciencia, Tecnología e Innovación (Colciencias). ISBN 978-958-57937-4-3.
ACTUALIZACIÓN DE LA GUÍA
Las recomendaciones de esta Guía deben actualizarse en los próximos tres años a partir de su expedición, o previamente en caso de disponer de nuevas evidencias que modifiquen de manera significativa las recomendaciones aquí anotadas.
FUENTES DE FINANCIACIÓN
Ministerio de Salud y Protección Social de Colombia - Departamento de Ciencia, Tecnología e Innovación (Colciencias).
REPRESENTANTES DEL GRUPO DESARROLLADOR DE LA GUÍA - UNIVERSIDAD NACIONAL DE COLOMBIA - ALIANZA CINETS
Joaquín Guillermo Gómez Dávila MD, MSc. Médico cirujano. Especialista en Obstetricia y Ginecología. Magíster en Epidemiología. Director Centro NACER. Docente, Universidad de Antioquia. Medellín, Colombia.
Jhon Henry Osorio Castaño, Enf. MSc. Coordinador Epidemiología Clínica de la subguía. Enfermero. Especialista en Gerencia de IPS. Magíster en Epidemiología. Medellín, Colombia.
Gladis Adriana Vélez Álvarez, MD, MSP. Médica cirujana. Especialista en Obstetricia y Ginecología. Magíster en Salud Pública. Coordinadora Área Salud Sexual y Reproductiva, NACER-Universidad de Antioquia.
John Jairo Zuleta Tobón MD, MSc. Médico cirujano. Especialista en Obstetricia y Ginecología. Magíster en Epidemiología. Docente, Universidad de Antioquia, NACER.
Juan Guillermo Londoño Cardona, MD. Médico cirujano. Especialista en Obstetricia y Ginecología. Coordinador del Área de Educación, NACER-Universidad de Antioquia.
Jesús Arnulfo Velásquez Penagos, MD. Médico cirujano. Especialista en Obstetricia y Ginecología. Fellow en Cuidado Crítico Obstétrico. Coordinador de Mortalidad Materna-NACER. Docente, Universidad de Antioquia.
Ingrid Arévalo-Rodríguez MSc, PhD (c). Epidemióloga clínica, Universidad Nacional de Colombia. PhD (c) en Pediatría, Obstetricia y Ginecología, Medicina Preventiva y Salud Pública, Universidad Autónoma de Barcelona. Coordinadora General de Epidemiología Clínica de la Guía. Instructor asociado División de Investigaciones, Fundación Universitaria de Ciencias de la Salud, Hospital de San José-Hospital Infantil de San José.
Pío Iván Gómez-Sánchez, MD, MSc, FACOG. Médico cirujano. Especialista en Obstetricia y Ginecología, y Epidemiología. Magíster en Salud Sexual y Reproductiva. Profesor Titular y Director del Grupo de Investigación en Salud Sexual y Reproductiva de la Facultad de Medicina, Universidad Nacional de Colombia. Líder general de la GPC.
RECONOCIMIENTO A INSTITUCIONES PARTICIPANTES
Las siguientes instituciones participaron en los consensos de expertos o reuniones de socialización de la GPC para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto o puerperio: Federación Colombiana de Obstetricia y Ginecología (FECOLSOG), Sociedad Colombiana de Anestesiología y Reanimación (SCARE), Asociación Colombiana de Facultades de Medicina (ascoFame), Asociación Colombiana de Facultades de Enfermería (ACOFAEN), Asociación Colombiana de Empresas de Medicina Integral (ACEMI), Academia Nacional de Medicina, Colegio Médico Colombiano, Asociación Colombiana de Hospitales y Clínicas, Instituto Nacional de Salud, Cafam IPS, Centro Médico Imbanaco, Clínica de Occidente, Clínica de la Mujer, Clínica del Norte, Clínica Materno Infantil Farallones, Clínica el Rosario, Clínica El Prado, Fundación Cardioinfantil, Fundación Valle de Lili, Fundación Santafé de Bogotá, Hospital Militar, Hospital San José, Hospital Simón Bolívar, Fundación Universitaria de Ciencias de la Salud, Universidad de Antioquia, Universidad del Quindío, Universidad Libre, Universidad Surcolombiana, Comfama, Metrosalud.
NOTAS AL PIE DE PÁGINA
1Esta guía y sus secciones hacen parte de un grupo de 25 GAI basadas en la evidencia que incorporan consideraciones económicas y de implementabilidad en el contexto del Sistema General de Seguridad Social en Salud colombiano, y que se desarrollaron por iniciativa del Ministerio de Salud y Protección Social y el Departamento de Ciencia, Tecnología e Innovación (Colciencias) en temas prioritarios y de alta prevalencia en el país mediante contrato otorgado a la Universidad Nacional de Colombia en el año 2010.
REFERENCIAS
1. WHO, UNFPA, Bank. W. Trends in Maternal Mortality: 1990-2008: WHO Library Cataloguing-in-Publication Data; [2010 Jan 2012]. Disponible: http://whqlibdoc.who.int/publications/2010/9789241500265_eng.pdf. [ Links ]
2. Carroli G, Cuesta C, Abalos E, Gulmezoglu AM. Epidemiology of postpartum haemorrhage: a systematic review. Best Pract Res Clin Obstet Gynaecol. 2008;22:999-1012. Epub 2008/09/30. [ Links ]
3. Alcaldía de Medellín. Salud sexual y reproductiva, Universidad de Antioquia. Informe final de la vigilancia epidemiológica de la Morbilidad Obstétrica Severa en la ciudad de Medellín. Medellín: Secretaría de Salud, Dirección de Salud Pública. Nacer Salud sexual y reproductiva, Universidad de Antioquia; 2008. [ Links ]
4. Lalonde A, Daviss BA, Acosta A, Herschderfer K. Postpartum hemorrhage today: ICM/FIGO initiative 2004-2006. Int J Gynaecol Obstet. 2006;94:243-53. Epub 2006/07/18. [ Links ]
5. Waterstone M, Bewley S, Wolfe C. Incidence and predictors of severe obstetric morbidity: case-control study. BMJ. 2001;322:1089-93. Epub 2001/05/05. [ Links ]
6.Royal College of Obstetricians and Gynaecologists. Prevention and Management of Postpartum Haemorrhage. London; 2009 [Visitado 2011 Jun 1]. Disponible en: http://www.rcog.org.uk/womens-health/clinical-guidance/prevention-andmanagement-postpartum-haemorrhage-greentop-52. [ Links ]
7. World Health Organization. WHO guidelines for the management of postpartum haemorrhage and retained placenta. Geneve: WHO Press; 2009 [Visitado 2011 Jun 1]. Disponible en: http://whqlibdoc.who.int/publications/2009/9789241598514_eng.pdf. [ Links ]
8. Ministerio de Salud y Protección Social, Colciencias. Guía de práctica clínica para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto o puerperio. Versión completa. Bogotá: Alianza CINETS; 2013. ISBN: 978-95857937-4-3. Disponible en: http://www.guiascolcienciasminproteccionsocialalianzacinets.org/index.php?option=com_wrapper&view=wrapper&Itemid=552. [ Links ]
9. Ministerio de Salud y Protección Social, Colciencias. Guía de práctica clínica para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto o puerperio. Version para pacientes. Bogotá: Alianza Cinets; 2013. ISBN: 978-958-8838-07-6. Disponible en: http://www.guiascolcienciasminproteccionsocialalianzacinets.org/index.php?option=com_wrapper&view=wrapper&Itemid=552. [ Links ]
10. Prendiville WJ, Elbourne D, McDonald S. Active versus expectant management in the third stage of labour. Cochrane Database Syst Rev. 2000(3):CD000007. Epub 2000/07/25. [ Links ]
11. Begley CM, Gyte GM, Devane D, McGuire W, Weeks A. Active versus expectant management for women in the third stage of labour. Cochrane Database Syst Rev. 2011(11):CD007412. Epub 2011/11/11. [ Links ]
12. Elbourne DR, Prendiville WJ, Carroli G, Wood J, McDonald S. Prophylactic use of oxytocin in the third stage of labour. Cochrane Database Syst Rev. 2001(4):CD001808. Epub 2001/11/01. [ Links ]
13. Soltani H, Hutchon DR, Poulose TA. Timing of prophylactic uterotonics for the third stage of labour after vaginal birth. Cochrane Database Syst Rev. 2010(8):CD006173. Epub 2010/08/06. [ Links ]
14. McDonald S, Abbott JM, Higgins SP. Prophylactic ergometrine-oxytocin versus oxytocin for the third stage of labour. Cochrane Database Syst Rev. 2004(1):CD000201. Epub 2004/02/20. [ Links ]
15. Gulmezoglu AM, Forna F, Villar J, Hofmeyr GJ. Prostaglandins for preventing postpartum haemorrhage. Cochrane Database Syst Rev. 2007(3): CD000494. Epub 2007/07/20. [ Links ]
16. Alfirevic Z, Blum J, Walraven G, Weeks A, Winikoff B. Prevention of postpartum hemorrhage with misoprostol. Int J Gynaecol Obstet. 2007;99 Suppl 2:S198-201. Epub 2007/10/27. [ Links ]
17. Liabsuetrakul T, Choobun T, Peeyananjarassri K, Islam QM. Prophylactic use of ergot alkaloids in the third stage of labour. Cochrane Database Syst Rev. 2007(2):CD005456. Epub 2007/04/20. [ Links ]
18. Novikova N, Hofmeyr GJ. Tranexamic acid for preventing postpartum haemorrhage. Cochrane Database Syst Rev. 2010(7):CD007872. Epub 2010/07/09. [ Links ]
19. Peters NC, Duvekot JJ. Carbetocin for the prevention of postpartum hemorrhage: a systematic review. Obstet Gynecol Surv. 2009;64:129-35. Epub 2009/01/23. [ Links ]
20. Mathew JL. Timing of umbilical cord clamping in term and preterm deliveries and infant and maternal outcomes: a systematic review of randomized controlled trials. Indian Pediatr. 2011;48:123-9. Epub 2011/03/08. [ Links ]
21. McDonald SJ, Middleton P. Effect of timing of umbilical cord clamping of term infants on maternal and neonatal outcomes. Cochrane Database Syst Rev. 2008(2):CD004074. Epub 2008/04/22. [ Links ]
22. Hofmeyr GJ, Abdel-Aleem H, Abdel-Aleem MA. Uterine massage for preventing postpartum haemorrhage. Cochrane Database Syst Rev. 2008(3): CD006431. Epub 2008/07/23. [ Links ]
23. Dennehy KC, Rosaeg OP, Cicutti NJ, Krepski B, Sylvain JP. Oxytocin injection after caesarean delivery: intravenous or intramyometrial? Can J Anaesth. 1998;45:635-9. Epub 1998/08/26. [ Links ]
24. Munn MB, Owen J, Vincent R, Wakefield M, Chestnut DH, Hauth JC. Comparison of two oxytocin regimens to prevent uterine atony at cesarean delivery: a randomized controlled trial. Obstet Gynecol. 2001;98:386-90. Epub 2001/09/01. [ Links ]
25. Lokugamage AU, Paine M, Bassaw-Balroop K, Sullivan KR, Refaey HE, Rodeck CH. Active management of the third stage at caesarean section: a randomised controlled trial of misoprostol versus syntocinon. Aust N Z J Obstet Gynaecol. 2001;41:411-4. Epub 2002/01/15. [ Links ]
26. Chou MM, MacKenzie IZ. A prospective, doubleblind, randomized comparison of prophylactic intramyometrial 15-methyl prostaglandin F2 alpha, 125 micrograms, and intravenous oxytocin, 20 units, for the control of blood loss at elective cesarean section. Am J Obstet Gynecol. 1994;171:1356-60. Epub 1994/11/01. [ Links ]
27. George RB, McKeen D, Chaplin AC, McLeod L. Up-down determination of the ED(90) of oxytocin infusions for the prevention of postpartum uterine atony in parturients undergoing Cesarean delivery. Can J Anaesth. 2010;57:578-82. Epub 2010/03/20. [ Links ]
28. Svanstrom MC, Biber B, Hanes M, Johansson G, Naslund U, Balfors EM. Signs of myocardial ischaemia after injection of oxytocin: a randomized double-blind comparison of oxytocin and methylergometrine during Caesarean section. Br J Anaesth. 2008;100:683-9. Epub 2008/04/04. [ Links ]
29. Butwick AJ, Coleman L, Cohen SE, Riley ET, Carvalho B. Minimum effective bolus dose of oxytocin during elective Caesarean delivery. Br J Anaesth. 2010;104:338-43. Epub 2010/02/13. [ Links ]
30. Sheehan SR, Montgomery AA, Carey M, McAuliffe FM, Eogan M, Gleeson R, et al. Oxytocin bolus versus oxytocin bolus and infusion for control of blood loss at elective caesarean section: double blind, placebo controlled, randomised trial. BMJ. 2011;343:d4661. Epub 2011/08/03. [ Links ]
31. King KJ, Douglas MJ, Unger W, Wong A, King RA. Five unit bolus oxytocin at cesarean delivery in women at risk of atony: a randomized, double-blind, controlled trial. Anesth Analg. 2010;111:1460-6. Epub 2010/10/05. [ Links ]
32. Gungorduk K, Asicioglu O, Celikkol O, Olgac Y, Ark C. Use of additional oxytocin to reduce blood loss at elective caesarean section: A randomised control trial. Aust N Z J Obstet Gynaecol. 2010;50:36-9. Epub 2010/03/12. [ Links ]
33. McLeod G, Munishankar B, MacGregor H, Murphy DJ. Maternal haemodynamics at elective caesarean section: a randomised comparison of oxytocin 5-unit bolus and placebo infusion with oxytocin 5-unit bolus and 30-unit infusion. Int J Obstet Anesth. 2010;19:155-60. Epub 2010/03/03. [ Links ]
34. Quiroga R, Cantu R, Tello HE, Puente M, Montemayor R, Martinez A. [Intrauterine misoprostol for the prevention of bleeding cesarean]. Ginecol Obstet Mex. 2009;77:469-74. Epub 2009/11/12. [ Links ]
35. Chaudhuri P, Banerjee GB, Mandal A. Rectally administered misoprostol versus intravenous oxytocin infusion during cesarean delivery to reduce intraoperative and postoperative blood loss. Int J Gynaecol Obstet. 2010;109:25-9. Epub 2010/01/15. [ Links ]
36. Eftekhari N, Doroodian M, Lashkarizadeh R. The effect of sublingual misoprostol versus intravenous oxytocin in reducing bleeding after caesarean section. J Obstet Gynaecol. 2009;29:633-6. Epub 2009/09/17. [ Links ]
37. Sekhavat L, Tabatabaii A, Dalili M, Farajkhoda T, Tafti AD. Efficacy of tranexamic acid in reducing blood loss after cesarean section. J Matern Fetal Neonatal Med. 2009;22:72-5. Epub 2009/01/24. [ Links ]
38. Attilakos G, Psaroudakis D, Ash J, Buchanan R, Winter C, Donald F, et al. Carbetocin versus oxytocin for the prevention of postpartum haemorrhage following caesarean section: the results of a double-blind randomised trial. BJOG. 2010;117(8):929-36. [ Links ] Epub 2010/05/21.
39. Borruto F, Treisser A, Comparetto C. Utilization of carbetocin for prevention of postpartum hemorrhage after cesarean section: a randomized clinical trial. Arch Gynecol Obstet. 2009;280:707-12. Epub 2009/02/21. [ Links ]
40. CRES. Informe Técnico 125: Efectividad, seguridad y análisis económico de la carbetocina versus la oxitocina para la prevención de la atonía uterina y hemorragia posparto; 2011. [ Links ]
41. Levine AB, Kuhlman K, Bonn J. Placenta accreta: comparison of cases managed with and without pelvic artery balloon catheters. J Matern Fetal Med. 1999;8:173-6. Epub 1999/07/16. [ Links ]
42. Alvarez M, Lockwood CJ, Ghidini A, Dottino P, Mitty HA, Berkowitz RL. Prophylactic and emergent arterial catheterization for selective embolization in obstetric hemorrhage. Am J Perinatol. 1992;9:441-4. Epub 1992/09/01. [ Links ]
43. Mitty HA, Sterling KM, Alvarez M, Gendler R. Obstetric hemorrhage: prophylactic and emergency arterial catheterization and embolotherapy. Radiology. 1993;188:183-7. Epub 1993/07/01. [ Links ]
44. Dubois J, Garel L, Grignon A, Lemay M, Leduc L. Placenta percreta: balloon occlusion and embolization of the internal iliac arteries to reduce intraoperative blood losses. Am J Obstet Gynecol. 1997;176:723-6. Epub 1997/03/01. [ Links ]
45. Hansch E, Chitkara U, McAlpine J, El-Sayed Y, Dake MD, Razavi MK. Pelvic arterial embolization for control of obstetric hemorrhage: a five-year experience. Am J Obstet Gynecol. 1999;180(6 Pt 1):1454-60. Epub 1999/06/16. [ Links ]
46. Ojala K, Perala J, Kariniemi J, Ranta P, Raudaskoski T, Tekay A. Arterial embolization and prophylactic catheterization for the treatment for severe obstetric hemorrhage. Acta Obstet Gynecol Scand. 2005;84:1075-80. Epub 2005/10/20. [ Links ]
47. Bodner LJ, Nosher JL, Gribbin C, Siegel RL, Beale S, Scorza W. Balloon-assisted occlusion of the internal iliac arteries in patients with placenta accreta/percreta. Cardiovasc Intervent Radiol. 2006;29:354-61. Epub 2006/02/28. [ Links ]
48. Tan CH, Tay KH, Sheah K, Kwek K, Wong K, Tan HK, et al. Perioperative endovascular internal iliac artery occlusion balloon placement in management of placenta accreta. AJR Am J Roentgenol. 2007;189:1158-63. Epub 2007/10/24. [ Links ]
49. Sentilhes L, Ambroselli C, Kayem G, Provansal M, Fernandez H, Perrotin F, et al. Maternal outcome after conservative treatment of placenta accreta. Obstet Gynecol. 2010;115:526-34. Epub 2010/02/24. [ Links ]
50. van Beekhuizen HJ, de Groot AN, De Boo T, Burger D, Jansen N, Lotgering FK. Sulprostone reduces the need for the manual removal of the placenta in patients with retained placenta: a randomized controlled trial. Am J Obstet Gynecol. 2006;194:446-50. Epub 2006/02/07. [ Links ]
51. Nardin JM, Weeks A, Carroli G. Umbilical vein injection for management of retained placenta. Cochrane Database Syst Rev. 2011(5):CD001337. Epub 2011/05/13. [ Links ]
52. Abdel-Aleem H, Abdel-Aleem MA, Shaaban OM. Tocolysis for management of retained placenta. Cochrane Database Syst Rev. 2011(1):CD007708. Epub 2011/01/21. [ Links ]
53. Chongsomchai C, Lumbiganon P, Laopaiboon M. Prophylactic antibiotics for manual removal of retained placenta in vaginal birth. Cochrane Database Syst Rev. 2006(2):CD004904. Epub 2006/04/21. [ Links ]
54. Baskett PJ. ABC of major trauma. Management of hypovolaemic shock. BMJ. 1990;300:1453-7. Epub 1990/06/02. [ Links ]
55. Bose P, Regan F, Paterson-Brown S. Improving the accuracy of estimated blood loss at obstetric haemorrhage using clinical reconstructions. BJOG. 2006;113:919-24. Epub 2006/08/16. [ Links ]
56. Duthie SJ, Ven D, Yung GL, Guang DZ, Chan SY, Ma HK. Discrepancy between laborator y determination and visual estimation of blood loss during normal delivery. Eur J Obstet Gynecol Reprod Biol. 1991;38:119-24. Epub 1991/01/30. [ Links ]
57. Ho AM, Karmakar MK, Dion PW. Are we giving enough coagulation factors during major trauma resuscitation? Am J Surg. 2005;190:479-84. Epub 2005/08/18. [ Links ]
58. Hirshberg A, Dugas M, Banez EI, Scott BG, Wall MJ, Jr., Mattox KL. Minimizing dilutional coagulopathy in exsanguinating hemorrhage: a computer simulation. J Trauma. 2003;54:454-63. Epub 2003/03/14. [ Links ]
59. Human albumin administration in critically ill patients: systematic review of randomised controlled trials. Cochrane Injuries Group Albumin Reviewers. BMJ. 1998;317:235-40. Epub 1998/07/24. [ Links ]
60. Roberts I, Blackhall K, Alderson P, Bunn F, Schierhout G. Human albumin solution for resuscitation and volume expansion in critically ill patients. Cochrane Database Syst Rev. 2011(11):CD001208. Epub 2011/11/11. [ Links ]
61. Perel P, Roberts I. Colloids versus crystalloids for fluid resuscitation in critically ill patients. Cochrane Database Syst Rev. 2011(3):CD000567. Epub 2011/03/18. [ Links ]
62. Havel C, Arrich J, Losert H, Gamper G, Mullner M, Herkner H. Vasopressors for hypotensive shock. Cochrane Database Syst Rev. 2011(5):CD003709. Epub 2011/05/13. [ Links ]
63. Mousa HA, Alfirevic Z. Treatment for primary postpartum haemorrhage. Cochrane Database Syst Rev. 2007(1):CD003249. Epub 2007/01/27. [ Links ]
64. Buttino L, Jr., Garite TJ. The use of 15 methyl F2 alpha prostaglandin (Prostin 15M) for the control of postpartum hemorrhage. Am J Perinatol. 1986;3:241-3. Epub 1986/07/01. [ Links ]
65. Oleen MA, Mariano JP. Controlling refractory atonic postpartum hemorrhage with Hemabate sterile solution. Am J Obstet Gynecol. 1990;162:205-8. Epub 1990/01/01. [ Links ]
66. Hofmeyr GJ, Walraven G, Gulmezoglu AM, Maholwana B, Alfirevic Z, Villar J. Misoprostol to treat postpartum haemorrhage: a systematic review. BJOG. 2005;112:547-53. Epub 2005/04/22. [ Links ]
67. Widmer M, Blum J, Hofmeyr GJ, Carroli G, Abdel-Aleem H, Lumbiganon P, et al. Misoprostol as an adjunct to standard uterotonics for treatment of postpartum haemorrhage: a multicentre, double-blind randomised trial. Lancet. 2010;375:1808-13. Epub 2010/05/25. [ Links ]
68. Blum J, Winikoff B, Raghavan S, Dabash R, Ramadan MC, Dilbaz B, et al. Treatment of post-partum haemorrhage with sublingual misoprostol versus oxytocin in women receiving prophylactic oxytocin: a double-blind, randomised, non-inferiority trial. Lancet. 2010;375:217-23. [ Links ] Epub 2010/01/12.
69. Winikoff B, Dabash R, Durocher J, Darwish E, Nguyen TN, Leon W, et al. Treatment of post-partum haemorrhage with sublingual misoprostol versus oxytocin in women not exposed to oxytocin during labour: a double-blind, randomised, non-inferiority trial. Lancet. 2010;375:210-6. Epub 2010/01/12. [ Links ]
70. Ducloy-Bouthors AS, Jude B, Duhamel A, Broisin F, Huissoud C, Keita-Meyer H, et al. High-dose tranexamic acid reduces blood loss in postpartum haemorrhage. Crit Care. 2011;15:R117. Epub 2011/04/19. [ Links ]
71. Abdel-Aleem H, Singata M, Abdel-Aleem M, Mshweshwe N, Williams X, Hofmeyr GJ. Uterine massage to reduce postpartum hemorrhage after vaginal delivery. Int J Gynaecol Obstet. 2010;111:32-6. Epub 2010/07/06. [ Links ]
72. Ikechebelu JI, Obi RA, Joe-Ikechebelu NN. The control of postpartum haemorrhage with intrauterine Foley catheter. J Obstet Gynaecol. 2005;25:70-2. Epub 2005/09/09. [ Links ]
73. Bakri YN, Amri A, Abdul Jabbar F. Tamponadeballoon for obstetrical bleeding. Int J Gynaecol Obstet. 2001;74:139-42. Epub 2001/08/15. [ Links ]
74. Chan C, Razvi K, Tham KF, Arulkumaran S. The use of a Sengstaken-Blakemore tube to control post-partum hemorrhage. Int J Gynaecol Obstet. 1997;58:251-2. Epub 1997/08/01. [ Links ]
75. Condous GS, Arulkumaran S, Symonds I, Chapman R, Sinha A, Razvi K. The "tamponade test" in the management of massive postpartum hemorrhage. Obstet Gynecol. 2003;101:767-72. Epub 2003/04/12. [ Links ]
76. Akhter S, Begum MR, Kabir Z, Rashid M, Laila TR, Zabeen F. Use of a condom to control massive postpartum hemorrhage. Med Gen Med. 2003;5:38. Epub 2003/11/06. [ Links ]
77. B-Lynch C, Coker A, Lawal AH, Abu J, Cowen MJ. The B-Lynch surgical technique for the control of massive postpartum haemorrhage: an alternative to hysterectomy? Five cases reported. Br J Obstet Gynaecol. 1997;104:372-5. Epub 1997/03/01. [ Links ]
78. Hayman RG, Arulkumaran S, Steer PJ. Uterine compression sutures: surgical management of postpartum hemorrhage. Obstet Gynecol. 2002;99:502-6. Epub 2002/02/28. [ Links ]
79. Ghezzi F, Cromi A, Uccella S, Raio L, Bolis P, Surbek D. The Hayman technique: a simple method to treat postpartum haemorrhage. BJOG. 2007;114:362-5. Epub 2007/01/16. [ Links ]
80. Hwu YM, Chen CP, Chen HS, Su TH. Parallel vertical compression sutures: a technique to control bleeding from placenta praevia or accreta during caesarean section. BJOG. 2005;112:1420-3. Epub 2005/09/20. [ Links ]
81. Kafali H, Demir N, Soylemez F, Yurtseven S. Hemostatic cervical suturing technique for management of uncontrollable postpartum haemorrhage originating from the cervical canal. Eur J Obstet Gynecol Reprod Biol. 2003;110:35-8. Epub 2003/08/23. [ Links ]
82. Joshi VM, Otiv SR, Majumder R, Nikam YA, Shrivastava M. Internal iliac artery ligation for arresting postpartum haemorrhage. BJOG. 2007;114:356-61. Epub 2007/01/31. [ Links ]
83. Dildy GA, 3rd. Postpartum hemorrhage: new management options. Clin Obstet Gynecol. 2002;45:330-44. Epub 2002/06/06. [ Links ]
84. Hong TM, Tseng HS, Lee RC, Wang JH, Chang CY. Uterine artery embolization: an effective treatment for intractable obstetric haemorrhage. Clin Radiol. 2004;59:96-101. Epub 2003/12/31. [ Links ]
85. Bloom AI, Verstandig A, Gielchinsky Y, Nadiari M, Elchalal U. Arterial embolisation for persistent primary postpartum haemorrhage: before or after hysterectomy? BJOG. 2004;111:880-4. Epub 2004/07/24. [ Links ]
86. Yong SP, Cheung KB. Management of primary postpartum haemorrhage with arterial embolisation in Hong Kong public hospitals. Hong Kong Med J. 2006;12:437-41. Epub 2006/12/07. [ Links ]
87. Doumouchtsis SK, Papageorghiou AT, Arulkumaran S. Systematic review of conservative management of postpartum hemorrhage: what to do when medical treatment fails. Obstet Gynecol Surv. 2007;62:540-7. Epub 2007/07/20. [ Links ]
88. Rossi AC, Lee RH, Chmait RH. Emergency postpartum hysterectomy for uncontrolled postpartum bleeding: a systematic review. Obstet Gynecol. 2010;115:637-44. Epub 2010/02/24. [ Links ]
89. Shahin AY, Farghaly TA, Mohamed SA, Shokry M, Abd-El-Aal DE, Youssef MA. Bilateral uterine artery ligation plus B-Lynch procedure for atonic postpartum hemorrhage with placenta accreta. Int J Gynaecol Obstet. 2010;108:187-90. Epub 2009/12/01. [ Links ]
90. Neilson JP. Interventions for treating placental abruption. Cochrane Database Syst Rev. 2003(1): CD003247. Epub 2003/01/22. [ Links ]
91. Hurd WW, Miodovnik M, Hertzberg V, Lavin JP. Selective management of abruptio placentae: a prospective study. Obstet Gynecol. 1983;61:467-73. Epub 1983/04/01. [ Links ]
92. Catling SJ, Williams S, Fielding AM. Cell salvage in obstetrics: an evaluation of the ability of cell salvage combined with leucocyte depletion filtration to remove amniotic fluid from operative blood loss at caesarean section. Int J Obstet Anesth. 1999;8:79-84. Epub 2004/08/24. [ Links ]
93. Marik PE, Corwin HL. Efficacy of red blood cell transfusion in the critically ill: a systematic review of the literature. Crit Care Med. 2008;36:2667-74. Epub 2008/08/06. [ Links ]
94. Simpson E, Lin Y, Stanworth S, Birchall J, Doree C, Hyde C. Recombinant factor VIIa for the prevention and treatment of bleeding in patients without haemophilia. Cochrane Database Syst Rev. 2012;3:CD005011. Epub 2012/03/16. [ Links ]
95. Marti-Carvajal AJ, Comunian-Carrasco G, Pena-Marti GE. Haematological interventions for treating disseminated intravascular coagulation during pregnancy and postpartum. Cochrane Database Syst Rev. 2011(3):CD008577. Epub 2011/03/18. [ Links ]
96. Inaba K, Teixeira PG, Shulman I, Nelson J, Lee J, Salim A, et al. The impact of uncross-matched blood transfusion on the need for massive transfusion and mortality: analysis of 5,166 uncross-matched units. J Trauma. 2008;65:1222-6. Epub 2008/12/17. [ Links ]
97. Cortés A, Bolaños F. Reanimación con glóbulos rojos Rh positivo y sin prueba cruzada en emergencias médicas. Colomb Med. 2004;35:185-90. [ Links ]
98. Ball CG, Salomone JP, Shaz B, Dente CJ, Tallah C, Anderson K, et al. Uncrossmatched blood transfusions for trauma patients in the emergency department: incidence, outcomes and recommendations. Can J Surg. 2011;54:111-5. Epub 2011/01/22. [ Links ]
99. Kongnyuy EJ, Mlava G, van den Broek N. Using criteria-based audit to improve the management of postpartum haemorrhage in resource limited countries: a case study of Malawi. Matern Child Health J. 2009;13:873-8. Epub 2008/09/10. [ Links ]
100. Deneux-Tharaux C, Dupont C, Colin C, Rabilloud M, Touzet S, Lansac J, et al. Multifaceted intervention to decrease the rate of severe postpartum haemorrhage: the PITHAGORE6 cluster-randomised controlled trial. BJOG. 2010;117:1278-87. Epub 2010/06/25. [ Links ]
101. Birch L, Jones N, Doyle PM, Green P, McLaughlin A, Champney C, et al. Obstetric skills drills: evaluation of teaching methods. Nurse Educ Today. 2007;27:915-22. Epub 2007/03/23. [ Links ]
102. Cook DA, Hatala R, Brydges R, Zendejas B, Szostek JH, Wang AT, et al. Technology-enhanced simulation for health professions education: a systematic review and meta-analysis. JAMA. 2011;306:978-88. Epub 2011/09/09. [ Links ]













