Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Obstetricia y Ginecología
Print version ISSN 0034-7434
Rev Colomb Obstet Ginecol vol.65 no.3 Bogotá July/Sept. 2014
https://doi.org/10.18597/rcog.50
DOI: http://dx.doi.org/10.18597/rcog.50
Mauricio Vasco-Ramírez, MD1
Recibido: septiembre 19/13 - Aceptado: septiembre 12/14
1 Especialista en Anestesiología, Cuidados Intensivos y Reanimación, Universidad Pontificia Bolivariana, Medellín (Colombia). Coordinador del Comité de Anestesia Obstétrica, Sociedad Colombiana de Anestesiología y Reanimación (SCARE). Coordinador para América Latina de la Comisión de Anestesia Obstétrica, Confederación Latinoamericana de Sociedades de Anestesia (CLASA) y Federación Mundial de Sociedades de Anestesia (WFSA). Miembro Honorario de la Federación Colombiana de Obstetricia y Ginecología (FECOLSOG), Bogotá (Colombia). machuchovasco@yahoo.com
RESUMEN
Objetivo: proporcionar a los profesionales de la salud involucrados en el manejo de gestantes con complicaciones (obstetras, enfermeras, médicos generales y de emergencias, anestesiólogos, intensivistas, entre otros) los principios fundamentales de prevención y manejo de paro cardiorrespiratorio (PCR) en este grupo poblacional con el fin de mejorar los resultados del binomio madre-hijo.
Materiales y métodos: el documento se basa en una búsqueda de publicaciones en las bases de datos Medline, SciELO y Embase utilizando los términos "Cardiopulmonary Resuscitation, Pregnancy, Perimortem Cesarean, Maternal Cardiac Arrest, Cardiac arrest in pregnancy", y restringida a los siguientes tipos de publicación: "Meta Analysis, Systematic Reviews, Practice Guideline, Randomized Controlled Trial, Review, Case Report, Chapter, Editorial, Survey".
Resultados: se encontraron 78 títulos de los cuales se incluyeron 63; de estos, 22 corresponden a revisiones narrativas, 20 a reportes y series de caso, 8 a guías de práctica clínica, 5 a ensayos clínicos, 4 editoriales, 2 corresponden a revisiones sistemáticas o metaanálisis, 1 capítulo de libro y 1 encuesta o survey.
Conclusiones: el paro cardiaco en gestantes impone un reto al grupo interdisciplinario que lo enfrenta, por ser una entidad de baja frecuencia que se puede asociar a un alto grado de morbimortalidad materna y perinatal. Las principales acciones por realizar son: activación del código azul obstétrico con respuesta adecuada para realización de histerotomía de emergencia oportuna, compresiones torácicas de buena calidad, desviación manual uterina 15º a la izquierda cuando el útero grávido se palpe por encima del ombligo materno, manejo avanzado farmacológico y de vía aérea, y cuidado óptimo luego de la resucitación para la madre y el neonato.
Palabras clave: embarazo, resucitación cardiopulmonar.
ABSTRACT
Objective: To provide healthcare professionals involved in the management of complications in pregnancy (including obstetricians, nurses, general and emergency practitioners, anaesthetists, critical care physicians) with the fundamental principles for the prevention and management of cardiopulmonary arrest in this population group in order to improve outcomes for both the mother and the newborn.
Materials and methods: A search was conducted in the Medline, SciELO and Embase databases using the terms "Cardiopulmonary Resuscitation, Pregnancy, Perimortem Caesarean, Maternal Cardiac Arrest, Cardiac arrest in pregnancy", restricted to the following types of publications: "Meta-analysis, Systematic Reviews, Practice Guideline, Randomized Controlled Trial, Review, Case Report, Chapter, Editorial, Survey".
Results: Of 78 titles found overall, 63 were included. Of these, 22 were narrative reviews, 20 case reports and case series, 8 practice guidelines, 5 clinical trials, 4 editorials, 2 systematic reviews or meta-analyses, 1 book chapter and 1 survey. Conclusions: Cardiac arrest in pregnant women poses a challenge to the interdisciplinary team managing the case because it may be associated with a high degree of maternal and perinatal morbidity and mortality. The main steps required are: obstetric blue code activation with appropriate response for performing timely emergent hysterotomy; good-quality chest compressions; manual uterine displacement 15º to the left when the pregnant uterus is palpated above the maternal umbilicus; advanced pharmacological and airway management; and optimal care after resuscitation for both the mother and the neonate.
Key words: Pregnancy, cardiopulmonary resuscitation.
INTRODUCCIÓN
El paro cardiorrespiratorio (PCR) se define como la cesación abrupta de la función cardiaca. El desarrollo de PCR desencadena una serie de maniobras encaminadas a restablecer las funciones vitales de la víctima, estas maniobras se agrupan bajo la expresión reanimación cerebro-cardio-pulmonar (RCPP). La RCCP tiene cinco eslabones: 1) Llamada, 2) RCP básica precoz, 3) desfibrilación precoz, 4) RCP avanzada, y 5) cuidados posresucitación (figura 1). La activación de un protocolo que permita aplicar de manera organizada estos cinco eslabones en medicina de emergencia y reanimación se denomina código azul (1, 2).
En gestantes, el paro cardiaco ocurre en uno de cada 30.000 embarazos a término (3-5). Las causas más frecuentes de PCR en embarazo están dadas por: trastornos hipertensivos del embarazo (preeclampsia-eclampsia / síndrome HELLP), hemorragia obstétrica masiva, complicaciones tromboembólicas e infecciones severas (1). La mortalidad materna y perinatal posterior al PCR es superior que en la paciente no embarazada (6). Series reportan tasas de sobrevida materna de solo un 7 %, debido a cambios fisiológicos que dificultan el éxito de las maniobras de reanimación básica y avanzadas (tabla 1).

Se ha descrito que hasta un 84 % de las pacientes obstétricas hospitalizadas que desarrollan colapso materno presentaba signos de deterioro en las 8 horas previas al PCR (7) De esta manera, el manejo adecuado de las entidades que conducen al colapso materno es primordial, así como la existencia de criterios de activación de los sistemas de alarma y el apoyo de equipos de respuesta rápida en obstetricia (8).
Hoy en día se dispone del Sistema de Alerta Temprana Modificado para Obstetricia (Modified Early Obstetric Warning System - MEOWS), herramienta que permite detectar precozmente gestantes con deterioro de parámetros fisiológicos y disfunción orgánica que podrían desarrollar colapso materno con el fin de manejarlas de manera oportuna y en los sitios adecuados tales como: las unidades de cuidados especiales, alta dependencia obstétrica o cuidados intensivos (9). Dicho sistema es actualmente recomendado por el Consenso Colombiano para la definición de los criterios de ingreso a unidades de cuidados intensivos en la paciente embarazada críticamente enferma (ver anexos 1 y 2) (10). En el año 2010, se publica el International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science With Treatment Recommendations que enuncia los cambios más recientes en reanimación cardiopulmonar; a su vez, se presentan las recomendaciones para grupos especiales, incluyendo la paciente obstétrica (3, 4). Estas recomendaciones han sido adoptadas por los grupos especializados en reanimación y medicina de emergencias en todo el mundo (11-20). En el 2014 se publica el Consenso de la Sociedad de Anestesia Obstétrica y Perinatología (SOAP) que adopta estas recomendaciones y las complementa con nuevas recomendaciones de estudios realizados luego del 2010 (21). Recientemente se publicaron los resultados del análisis de PCR en gestantes hospitalizadas en los Estados Unidos reportando un episodio de PCR por cada 12.000 hospitalizaciones para atención del parto y una sobrevida al alta hospitalaria del 58,9 %, la más alta reportada hasta ahora en esta población. Estos resultados probablemente son atribuibles a mejores competencias, infraestructura y adherencia a los protocolos de manejo del PCR en la gestante (21-27).
Es muy importante que los profesionales de la salud involucrados en el manejo de gestantes (obstetras, enfermeras, médicos generales y de emergencias, anestesiólogos, intensivistas, entre otros) conozcan los principios fundamentales y más actualizados en el manejo de PCR en estas pacientes, entiendan que su tratamiento debe ser abordado de manera interdisciplinaria y que deben prepararse en escenarios de simulación para el personal de salud que labora en salas de trabajo de parto así como en salas de cirugía con el fin de obtener competencias técnicas y no técnicas orientadas a mejorar los desenlaces en el binomio madre-hijo (21-28).
El objetivo de este artículo de educación médica es proporcionar información actualizada sobre los aspectos más relevantes en el manejo de la RCP en mujeres gestantes con el fin de mejorar los resultados del binomio madre-hijo.
MATERIALES Y MÉTODOS
El trabajo se aborda con base en las siguientes preguntas: ¿Cómo responder inicialmente al colapso materno? ¿Cuáles son las modificaciones de los cinco eslabones de la RCP para aplicar en la gestante? ¿Cuál es el papel de la histerotomía de emergencia en la gestante que no responde a las manobras de RCP?
Se hizo una búsqueda de publicaciones en las bases de datos Medline, SciELO y Embase, utilizando los términos "Cardiopulmonary Resuscitation, Pregnancy, Perimortem Cesarean, Maternal Cardiac Arrest, Cardiac arrest in pregnancy", restringida a los siguientes tipos de publicación: "Meta Analysis, Systematic Reviews, Practice Guideline, Randomized Controlled Trial, Review, Case Report, Chapter, Editorial, Survey".
RESULTADOS
Se encontraron 78 títulos de los cuales se incluyeron 63; de estos, 22 corresponden a revisiones narrativas, 20 a reportes y series de caso, 8 a guías de práctica clínica, 5 a ensayos clínicos, 4 editoriales, 2 corresponden a revisiones sistemáticas o metaanálisis, 1 capítulo de libro y 1 encuesta o survey.
RESPUESTA INICIAL AL COLAPSO MATERNO
Luego de la aplicación de los criterios de detección temprana de gestantes críticamente enfermas se procede al inicio de las maniobras iniciales para la prevención del PCR, que son (21): posicionar a la gestante en decúbito lateral izquierdo al menos 15º, administrar oxígeno al 100 %, acceso venoso permeable y evaluación de los medicamentos que está recibiendo o recientemente recibió. De manera simultánea, se trata de hacer un diagnóstico de la condición que tiene comprometida a la madre, posteriormente se deben considerar uno a uno los diagnósticos diferenciales de las causas de colapso materno, proceso que debe ser continuo durante todo el desarrollo de la RCCP en la gestante (tabla 2).
Con este fin se han utilizado varias mnemotecnias, la más utilizada en población gestante es la sugerida por el International Liaison Committee on Resuscitation-American Heart Association (ILCOR-AHA) (4, 6), constituida por las iniciales en inglés de las principales causas de colapso materno y paro cardiaco en las gestantes: BEAU CHOPS (Bleeding, Embolism, Anesthetic complications, Uterine Atony, Cardiac, Hypertension, Others, Placenta, Sepsis), mnemotecnia que permite evaluar los diagnósticos diferenciales del paro cardiaco en la embarazada (3). El Consenso de la Sociedad de Anestesia Obstétrica y Perinatología (SOAP) propone otra mnemotecnia en orden alfabético de la letra A hasta la H, donde se enuncian las principales causas de PCR, y sugiere que se apliquen listas de chequeo para no omitir pasos críticos (21).
Por último, es importante recordar que al establecer contacto inicial con la gestante críticamente enferma se deben tener las medidas completas de bioseguridad (guantes, tapabocas, gafas) antes de iniciar las maniobras básicas de reanimación (1).
MODIFICACIONES DE LOS CINCO ESLABONES DE LA REANIMACIÓN CARDIOPULMONAR Y CEREBRAL (RCCP) EN LA GESTANTE
Primer eslabón: llamada
Si al establecer contacto con la paciente esta no responde, se activa el código azul obstétrico con un componente propio de este grupo poblacional; se debe llamar de manera urgente al equipo quirúrgico compuesto por obstetra, anestesiólogo, neonatólogo, instrumentadora y personal de enfermería, dado que si a los cuatro minutos de reanimacion no se ha logrado el retorno a la circulación espontánea con las maniobras básicas y avanzadas de resucitación, se deberá realizar la histerotomía de emergencia para extracción fetal (anteriormente denominada cesárea perimortem) (21). La prioridad es la realización de maniobras básicas de reanimación cerebro-cardio-pulmonar (RCCP) que permitan la circulación materna a órganos vitales, evitando al máximo secuelas por hipoxemia. La mejor maniobra de reanimación fetal es reanimar efectivamente a la madre (22-28).
Segundo eslabón: RCCP precoz con énfasis en compresiones torácicas de buena calidad
Luego de la activación del código azul obstétrico se posiciona a la paciente realizando desviación manual del útero a la izquierda al menos 15º para aliviar la compresión aorto-cava ocasionada por el útero grávido luego de la semana 20 de embarazo, ya que el útero grávido palpable por encima del ombligo produce esta compresión (29), y se inician maniobras básicas de RCCP con la nueva secuencia CAB (Circulación, Abrir vía aérea, Buena ventilación) (6). En caso de no palpar pulso carotideo durante 10 segundos se inicia la secuencia de compresiones cardiacas-ventilaciones en una relación 30 compresiones: 2 ventilaciones, durante 2 minutos, y al disponer del cardiodesfibrilador se identifica el ritmo de paro y se desfibrila si está indicado (30). (ver tercer eslabón).
Adicional a la desviación manual uterina se debe colocar una tabla rígida entre la paciente y la cama, proporcionando una superficie dura para aumentar la efectividad de las compresiones torácicas (21). Se debe tener en cuenta que las pacientes con alteraciones de la coagulación (trombocitopenia en preeclampsia severa, CID en embolismo de líquido amniótico, abrupcio de placenta o hemorragia posparto mayor) que reciban compresiones torácicas inadecuadas podrían desarrollar hemorragias intratorácicas por fracturas costales (1).
En el tercer trimestre del embarazo se recomienda realizar las compresiones torácicas 2 pulgadas más arriba del punto esternal habitual (1), porque debido a los cambios torácicos inducidos por el útero grávido hay desplazamiento de los contenidos pélvicos y abdominales hacia arriba. En cuanto al manejo de la vía aérea, esta se permeabiliza luego de un adecuado posicionamiento materno, soportando la ventilación con dispositivo (BVM) y oxígeno suplementario al 100 % (figura 2); se debe disponer siempre de dispositivos de succión y recordar que en las gestantes las mucosas son muy friables y los dispositivos nasofaríngeos no se deben usar porque pueden llevar a trauma local y hemorragia significativa (28).
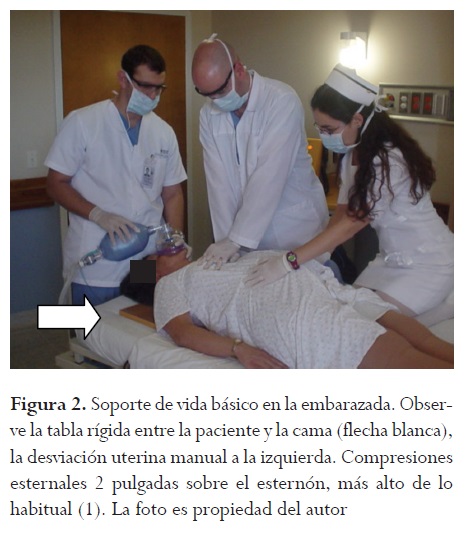
En ocasiones, la gestante no desarrolla PCR sino una apnea que mejora con las maniobras básicas de permeabilización de la vía aérea; si luego de abrir la vía aérea la paciente respira adecuadamente, se puede dejar en posición de seguridad (decúbito lateral) con oxígeno suplementario mientras se identifica y trata la causa de la activación del código azul obstétrico (por ejemplo, apnea por toxicidad asociada a sulfato de magnesio) (18).
Tercer eslabón: identifique ritmo de paro, desfibrile si está indicado
Luego se debe realizar la monitorización electrocardiográfica de la paciente en paro. Los cuatro probables ritmos de paro son: dos desfibrilables (la fibrilación ventricular, la taquicardia ventricular sin pulso) y dos no desfibrilables (asistolia y la actividad eléctrica sin pulso); los ritmos de paro no desfibrilables son más frecuentes en gestantes, aunque existen reportes de alteraciones de las enzimas cardiacas sugestivas de lesión miocárdica en gestantes con hemorragia obstétrica mayor que pudieran desencadenar ritmos de paro desfibrilables (31). La desfibrilación no está contraindicada en el embarazo, aunque sí se debe tener la precaución de retirar los dispositivos de monitorización fetal externa o interna antes de realizarla (3, 4, 11, 14, 21). En caso de ritmos desfibrilables se realiza descarga única de 360 Joules en corriente monofásica o de 200 Joules en corriente bifásica (21).
Cuarto eslabón: soporte de vida avanzado efectivo
a) Aseguramiento de la vía aérea, consideración de intubación endotraqueal. Las gestantes se consideran una vía aérea difícil, tienen mayor riesgo de broncoaspiración y si se dispone de las competencias se debe tener un umbral muy bajo para realizar intubación traqueal precoz (32, 33).
La probabilidad de vía aérea difícil en gestantes es 10 veces mayor que en población no obstétrica; las mamas hipertróficas en el embarazo interfieren con las maniobras de laringoscopia e intubación, por lo que se recomienda utilizar mangos de laringoscopio cortos ya que estos no chocan con las mamas ni las manos del reanimador que está realizando maniobras de manipulación laríngea externa (figura 3) (1). De las maniobras de manipulación laríngea externa la que mejora la visualización de cuerdas vocales facilitando la intubación endotraqueal es la maniobra BURP (Back-Up-Right-Pressure, hacia atrás, arriba y a la derecha) (34). Se deben utilizar tubos endotraqueales de al menos 7 French y, en caso de entidades como preeclampsia-eclampsia asociada a edema de glotis y presencia de estridor materno, se deben utilizar tubos endotraqueales de diámetros aún menores. Es necesario aplicar los algoritmos para manejo de vía aérea difícil en gestantes ya que intentos repetitivos no exitosos de intubación generan edema y trauma con posible pérdida completa de esta vía. En servicios obstétricos se debe disponer de carro de vía aérea difícil con dispositivos extraglóticos y bujías de intubación (Eschman® o Frova®) (32, 33).
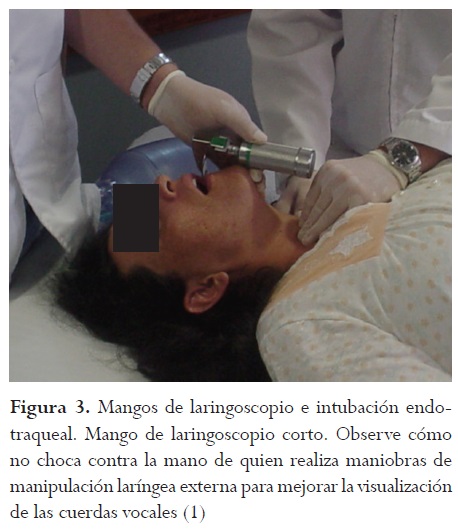
b) Verificación de intubación, aseguramiento del tubo endotraqueal y conexión a una fuente de oxígeno. Luego de intubar se verifica visualmente la excursión torácica simétrica, se auscultan los campos pulmonares y la cámara gástrica, y se instala el dispositivo para la medición del CO2 (capnografía-capnometría), al comprobar la adecuada posición del tubo endotraqueal o dipositivo extraglótico se inmoviliza el dispositivo de vía aérea y se conecta a un sistema BVM con O2 al 100 % (32, 33). Luego de colocado un dispositivo para permeabilizar la vía aérea (intubación orotraqueal o extraglóticos), la secuencia de compresión torácica-ventilación es asincrónica, esto quiere decir que ya no es en una relación 30 compresiones: 2 ventilaciones, sino que se suministran 100 compresiones torácicas por minuto y se ventila cada 6 segundos (3, 4, 11, 14, 21).
Se debe evitar la hiperventilacion, la frecuencia de ventilacion recomendada es una ventilacion cada 6 segundos, ya que la hiperventilacion disminuye el flujo sanguíneo cerebral, aumenta el volumen intratorácico, reduce el retorno venoso y el flujo sanguíneo placentario, y dificulta el retorno a la circulación espontánea empeorando los desenlaces materno-fetales (3, 4, 11, 14, 21). La monitorización de CO2 espirado cuantitativa (capnometría) tiene valor pronóstico ya que pacientes con valores mayores a 10 mm/Hg durante las compresiones torácicas tienen mayor probabilidad de retornar a circulación espontánea, valores inferiores deben llevar a mejorar la calidad en las compresiones (3, 4).
c) Establecimiento y verificación de accesos venosos, monitorización del ritmo cardiaco, uso de fármacos y continuación de compresiones torácicas de buena calidad. La mayoría de gestantes hospitalizadas tienen un acceso venoso periférico, en caso de no tenerlo se debe considerar su inserción vía periférica o vía intraósea (3, 4, 11, 14, 21).
La reanimación cerebro-cardio-pulmonar es un proceso dinámico y siempre debemos evaluar sistemáticamente las condiciones que perpetúan el PCR, la mnemotecnia de las 6H y 6T nos ayuda a cumplir este objetivo (tabla 3).
Quinto eslabón: cuidado posresucitación
Luego del retorno a la circulación espontanea las metas para el periodo posresucitación son (9):
1. Tratar la causa del paro cardiaco.
2. Evitar la recurrencia de la situacion causante del paro cardiaco.
3. Optimizar la perfusión a órganos, principalmente el cerebro.
4. Instaurar medidas que modifiquen los desenlaces neurológicos adversos.
Se recomienda instaurar la hipotermia moderada, definida como el logro de una temperatura central de 33 a 35 ºC en pacientes comatosos, luego del regreso a la circulación espontánea y de manera conjunta con el tratamiento de la causa del paro cardiaco (35-37).
La inducción de hipotermia se puede iniciar desde el retorno a la circulación espontánea hasta 6 horas después, manteniéndose durante 24 horas, y posteriormente se permite el calentamiento espontáneo. La manera más práctica para inducir hipotermia es la infusión de cristaloides: 30 cc/kg en 30 minutos a 4 ºC en pacientes con adecuada sedoanalgesia y relajación neuromuscular para evitar escalofrío durante la inducción de la hipotermia y el posterior calentamiento. La monitorización de la temperatura se realiza mediante catéter de arteria pulmonar, medición timpánica o vesical, estas reflejan adecuadamente la temperatura central de la paciente (35-37). Si se utiliza hipotermia moderada en pacientes aún embarazadas la monitorización fetal continua es obligada, en conjunto con las otras medidas del cuidado posresucitación (35-37).
CONSIDERACIONES ESPECIALES EN EL MANEJO DE LA GESTANTE CON PCR
Terapia eléctrica durante el soporte de vida avanzado (3, 4, 11, 14, 21).
Ritmos desfibrilables: fibrilación ventricular y taquicardia ventricular sin pulso.
Las dosis y los fármacos utilizados para RCCP obstétrica son iguales a las de pacientes adultas no obstétricas. La terapia eléctrica depende del ritmo de paro y su causa.
Los ritmos desfibrilables se desfibrilan con una descarga de 360 J en corriente monofásica, o de 200 J corriente bifásica, si el paciente no responde a esta descarga de debe continuar con maniobras de RCCP y con soporte farmacológico de la siguiente manera:
• Adrenalina 1 mg IV c/3 min o vasopresina 40 U IV dosis única.
• La amiodarona, considerada como medicamento categoría D de la FDA en el embarazo, no está contraindicada en el contexto de paro por ritmos desfibrilables recurrentes resistentes a la desfibrilación, su dosis inicial es de 300 mg IV en bolo y se debe aplicar otro bolo de 150 mg IV a los 5 minutos si persisten los ritmos desfibrilables; cuando la paciente presente ritmo de perfusión se inicia una infusión de 1 mg/min por 6 horas y luego 0,5 mg/min por 18 horas sin sobrepasar 2,2 g en 24 horas.
Tratamiento de los ritmos no desfibrilables
Asistolia y actividad eléctrica sin pulso.
Continuar con maniobras de RCCP y con soporte farmacológico de la siguiente manera:
• Adrenalina, 1 mg IV c/3 min. Considerar el uso de vasopresina 40 U IV dosis única en reemplazo de la adrenalina. No está indicado el uso de marcapaso transcutáneo o transvenoso en asistolia.
• Siempre en ritmos de paro no desfibrilables se debe considerar la carga de volumen con cristaloides, suero salino 0,9 %, 250 cc en bolo intravenoso, puesto que estos ritmos de paro se acompañan frecuentemente de hipovolemia.
Consideraciones farmacológicas especiales
Gluconato de calcio: medicamento de elección en toxicidad por sulfato de magnesio, el cual es utilizado de manera rutinaria en preeclampsia-eclampsia, neuroprotección neonatal y en casos seleccionados para tocolísis. Su dosis intravenosa es de 30 cc de gluconato de calcio al 10 %; en caso de disponer de cloruro de calcio se recomienda utilizar por vía IV 2-4 mg/kg de una solución al 10 %; la utilización de calcio también está indicada en los casos de hiperpotasemia. Durante su aplicación se debe vigilar que este agente no se extravase porque produciría necrosis cutánea (3, 4, 11, 14, 21).Emulsión de lípidos (intralipid 20 %®): está indicado en casos de toxicidad por anestésicos locales, se debe iniciar de manera precoz y como adyuvante a las medidas básicas y avanzadas de RCCP (algunos autores promulgan disminuir la dosis de adrenalina en este escenario, entre 10-100 mcg IV); esta terapia se utiliza en dosis de 1 ml/kg vía IV a intervalos de 5 minutos por dos dosis, y se continúa con una infusión parenteral a 0,25 ml/kg/min hasta regresar a la circulación espontánea sin sobrepasar los 840 ml de emulsión lipídica al 20 % (38-40). Desde el punto de vista anestésico prevenir, detectar y tratar la toxicidad por anestésicos locales, en especial la bupivacaina utilizada para técnicas analgésicas-anestésicas por vía epidural, es fundamental. Actualmente, con el uso casi rutinario de técnicas espinales (raquídeas) para cesárea, la utilización de concentraciones bajas de anestésico local (bupivacaína < 0,125 % en la analgesia epidural), o técnicas combinadas espinal-epidural, la incidencia de toxicidad por anestésicos locales es baja pero latente en los anestesiólogos que no han adoptado estas prácticas seguras neuroaxiales (41).
En situaciones como paro cardiaco materno prolongado luego de cesárea perimortem, embolia de líquido amniótico o toxicidad por anestésicos locales, la realización de ecocardiografía transesofágica, soporte con circulación extracorpórea y toracotomía de resucitación con masaje cardiaco directo han sido reportados en la literatura (1); estas conductas requieren del trabajo interdisciplinario con los equipos de cardiología, cuidados intensivos y cirugía cardiovascular, y la disponibilidad de equipos de toracotomía disponibles en los servicios obstétricos.
Reportes recientes de necesidad de reanimación cardiopulmonar avanzada por depresión respiratoria asociada a remifentanilo, cuando este es usado como agente analgésico para trabajo de parto en pacientes con contraindicaciones a los abordajes neuroaxiales, muestran otra causa anestésica potencialmente prevenible de paro cardiaco en las gestantes (42, 43).
Histerotomía de emergencia (cesárea perimortem)
Katz propone un cambio en la terminología para el término "cesárea perimortem" por "histerotomía de emergencia"; este término, actualmente acogido por la Asociación Americana del Corazón (AHA), reemplaza el de cesárea perimortem en la literatura (44).
La realización de histerotomía de emergencia, así el feto no sea viable, está indicada en embarazos por encima de las 20 semanas (útero grávido palpable por encima del ombligo). La evacuación uterina y el resultante alivio de la compresión aorto-cava producida por el útero grávido mejora los desenlaces maternos al optimizar la hemodinámica y la probabilidad de regreso a circulación espontánea (45-49). Cuando hay viabilidad fetal los desenlaces neonatales son mejores si la histerotomía de emergencia se realiza antes de los 4 minutos de presentado el PCR; Katz et al., en una búsqueda sistemática en la literatura, describen 38 casos de histerotomía de emergencia entre 1986 y 2004, soportando el concepto de que su realización a los 4 minutos del paro cardiaco, si las medidas de reanimación son inefectivas, aumenta la probabilidad materna de retorno a la circulación espontánea (45). Otro estudio mostró que de 45 neonatos que nacieron en los primeros 5 minutos el 98 % sobrevivió sin secuelas neurológicas (46).
Otra medida que mejora los desenlaces neona tales es la inducción de hipotermia terapéutica neonatal, entre 33,5 a 34,5 ºC. Esta estrategia estaría indicada en recién nacidos mayores de 36 semanas con encefalopatía hipóxico-isquémica moderada a severa; se debe instaurar en las primeras 6 horas de vida y mantenerla por 72 horas para luego permitir el recalentamiento; los neonatos sometidos a este protocolo de hipotermia terapéutica presentan menor mortalidad y mejor neurodesarrollo a los 18 meses comparados con los que no reciben dicho protocolo (50).
Ante la activación del código azul obstétrico todo el equipo debe asistir al sitio donde se presenta el evento, la histerotomía de emergencia se realiza en el sitio de ocurrencia del paro cardiaco, tratar de trasportar la paciente a otro lugar retrasa su realización en el estándar de tiempo determinado (minuto 5) y evita que se realice RCCP básica de buena calidad (51-57).
En las áreas de riesgo para la ocurrencia de PCR en la embarazada, como los servicios de urgencias, las áreas de trabajo de parto, salas de hospitalización y unidades de cuidado intensivo se debe disponer de un kit para la realización de este procedimiento que incluya soluciones asépticas, guantes y apósitos estériles, hoja de bisturí, retractores abdominales, pinza y tijeras quirúrgicas, así como insumos para la reanimación neonatal (21, 58).
Si luego de 4 minutos de RCCP básica y avanzada no se obtiene retorno a la circulación espontánea materna el abdomen se lava con un jabón quirúrgico de acción rápida (idealmente clorhexidina con alcohol), no hay tiempo de colocar una sonda vesical, se realiza incisión mediana infraumbilical, se hace la extracción fetal, el alumbramiento manual y se cierran rápidamente útero y fascia para que las compresiones torácicas no pierdan efectividad al estar el abdomen abierto (51-55).
Luego del regreso a la circulación espontánea y estabilización hemodinámica se deben establecer medidas para la prevención, detección y tratamiento de hemorragia posparto, tomar medidas para la identificación de sangrado intraperitoneal o de tejidos blandos por hemostasia inadecuada (individualizar traslado a quirófano), e iniciar tratamientos farmacológicos, antibióticos y orientados a la causa del PCR (53-55). Luego de esto, la paciente y el recién nacido, si es viable, deben ser trasladados a una Unidad de Cuidados Intensivos (10).
La disponibilidad de medidas avanzadas de RCCP, como ecocardiografía transesofágica, soporte con membrana extracorpórea (ECMO) y toracotomía de resucitación han sido descritas en este grupo poblacional y se deben protocolizar cuando estén indicadas (53-55).
Dado que el paro cardiaco en la embarazada es un evento de baja frecuencia y con alto potencial de morbimortalidad materna y perinatal, es importante que los trabajadores de la salud involucrados en el cuidado del binomio madre-hijo se puedan entrenar en escenarios de simulación para mejorar las competencias tanto técnicas como no técnicas y facilitar el trabajo en equipo durante las crisis, además de los simulacros (59-64). El uso de ayudas cognitivas como las listas de chequeo durante el paro cardiaco en la embarazada, que minimizan la posibilidad de omitir pasos críticos durante la reanimación cardiopulmonar, es ahora recomendado por las sociedades científicas de anestesia obstétrica y perinatología (21).
CONCLUSIONES
El paro cardiaco en gestantes impone un reto al grupo interdisciplinario que lo enfrenta por ser una entidad de baja frecuencia y asociada a un alto grado de morbimortalidad materna y perinatal.
Las principales acciones por realizar son:
• Activación del código azul obstétrico con respuesta adecuada para realización de histerotomía de emergencia oportuna.
• Compresiones torácicas de buena calidad, 2 pulgadas por encima del punto esternal habitual.
• Desviación manual uterina 15º a la izquierda.
• Medicamentos y desfibrilación igual que en población no obstétrica.
• Manejo avanzado de vía aérea.
• Cuidados posresucitación óptimos para madre y neonato.
• Realización de simulacros y uso de ayudas cognitivas como las listas de chequeo para minimizar la posibilidad de omisión de pasos críticos durante la reanimación cardiopulmonar.
Datos recientes muestran que con la optimización de estas medidas las tasas de sobrevida al alta hospitalaria en gestantes que presentan paro cardiaco hospitalario pueden estar alrededor de un 60 %.
REFERENCIAS
1. Vasco M. Resucitación cardiopulmonar en la embarazada. Rev Col Anest. 2004; 32:243-51. [ Links ]
2. Navarro Vargas R. Manual de reanimación básica. Guía para el entrenamiento del estudiante. Bogotá: Sociedad Colombiana de Anestesiología y Reanimación; 2011. [ Links ]
3. Vanden Hoek TL, Morrison LJ, Shuster M, Donnino M, Sinz E, Lavonas EJ et al. Part 12: Cardiac arrest in special situations: 2010 American Heart Association Guidelines for Cardiopulmonar y Resuscitation and Emergency Cardiovascular Care. Circulation. 2010;122(18 Suppl. 3):S829-861. [ Links ]
4. Soar J, Perkins GD, Abbas G, Alfonzo A, Barelli A, Bierens JJ, et al. European Resuscitation Council Guidelines for Resuscitation 2010: Section 8. Cardiac arrest in special circumstances: electrolyte abnormalities, poisoning, drowning, accidental hypothermia, hyperthermia, asthma, anaphylaxis, cardiac surgery, trauma, pregnancy, electrocution. Resuscitation. 2010;81:1400-33. [ Links ]
5. ACLS for experienced providers. Cardiac Arrest associated with pregnancy. American Heart Association; 2003. p. 143-149. [ Links ]
6. Morrison LJ, Deakin CD, Morley PT, Callaway CW, Kerber RE, Kronick SL, et al. Part 8: advanced life support: 2010 International Consensus on Cardiopulmonar y Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Circulation. 2010;122(16 Suppl. 2): S345-421. [ Links ]
7. Gosman GG, Baldisseri MR, Stein KL, Nelson TA, Pedaline SH, Waters JH, et al. Introduction of an obstetric specific medical emergency team for obstetric crises: implementation and experience. Am J Obstet Gynecol. 2008;198:367. [ Links ]
8. Maternal Collapse in Pregnancy and the Puerperium. [Visitado 2013 Ene 15]. Disponible en: https://www.rcog.org.uk/en/guidelines-research-services/guidelines/gtg56/ [ Links ]
9. Singh S, McGlennan A, England A, Simons R. A validation study of the CEMACH recommended modified early obstetric warning system (MEOWS). Anaesthesia. 2012;67:12-8. [ Links ]
10. Rojas JA, González M, Monsalve G, Escobar MF, Vasco M. Consenso colombiano para la definición de los criterios de ingreso a unidades de cuidados intensivos en la paciente embarazada críticamente enferma. Rev Colomb Obstet Ginecol. 2014;65:47-74. [ Links ]
11. Ezri T, Lurie S, Weiniger CF, Golan A, Evron S. Cardiopulmonar y resuscitation in the pregnant patient--an update. Isr Med Assoc J. 2011;13:306-10. [ Links ]
12. Farinelli CK, Hameed AB. Cardiopulmonar y resuscitation in pregnancy. Cardiol Clin. 2012;30: 453-61. [ Links ]
13. Sommerkamp SK, Gibson A. Cardiovascular disasters in pregnancy. Emerg Med Clin North Am. 2012;30:949-59. [ Links ]
14. Hui D, Morrison LJ, Windrim R, Lausman AY, Hawryluck L, Dorian P, et al. The American Heart Association 2010 guidelines for the management of cardiac arrest in pregnancy: consensus recommendations on implementation strategies. J Obstet Gynaecol Can. 2011;33:858-63. [ Links ]
15. Schimmelpfennig K, Stanfill TJ. Advanced cardiovascular life support for the obstetric population: bridging the gap. J Perinat Neonatal Nurs. 2012;26:136-46. [ Links ]
16. Puck AL, Oakeson AM, Morales-Clark A, Druzin M. Obstetric life support. J Perinat Neonatal Nurs. 2012;26:126-35. [ Links ]
17. Jones R, Baird SM, Thurman S, Gaskin IM. Maternal cardiac arrest: an overview. J Perinat Neonatal Nurs. 2012;26:117-23 [ Links ]
18. van Waning VH, van der Weiden RM, de Feiter PW, Brouwers AJ. Cardiac arrest in pregnancy: lessons to be learned! Intensive Care Med. 2012;38:721. [ Links ]
19. Ramsay G, Paglia M, Bourjeily G. When the Heart Stops: A Review of Cardiac Arrest in Pregnancy. J Intensive Care Med. 2013;28:204-14. [ Links ]
20. Campbell TA, Sanson TG. Cardiac arrest and pregnancy. J Emerg Trauma Shock. 2009;2:34-42. [ Links ]
21. Lipman S, Cohen S, Einav S, Jeejeebhoy F, Mhyre JM, Morrison LJ, et al. The Society for Obstetric Anesthesia and Perinatology consensus statement on the management of cardiac arrest in pregnancy. Anesth Analg. 2014;118:1003-16. [ Links ]
22. Mhyre JM, Tsen LC, Einav S, Kuklina EV, Leffert LR, Bateman BT. Cardiac Arrest during Hospitalization for Deliver y in the United States, 1998-2011. Anesthesiology. 2014;120:810-8. [ Links ]
23. Morrison LJ, Jeejeebhoy FM. Estimating Maternal Card iac Ar rest In c id en c e an d Out c omes . Anesthesiology 2014;120:790-1. [ Links ]
24. Jeejeebhoy FM, Zelop CM, Windrim R, Carvalho JC, Dorian P, Morrison LJ. Management of cardiac arrest in pregnancy: a systematic review. Resuscitation. 2011;82:801-9. [ Links ]
25. King SE, Gabbott DA. Maternal cardiac arrest rarely occurs, rarely researched. Resuscitation. 2011;82: 795-6. [ Links ]
26. Morris S, Stacey M. Resuscitation in pregnancy. BMJ.2003;327:1277-79. [ Links ]
27. Whitty JE. Maternal Cardiac Arrest in Pregnancy. Clin Obstet Ginecol. 2002;45:377-92. [ Links ]
28. Suresh MS, LaToya Mason C, Munnur U. Cardiopulmonary resuscitation and the parturient. Best Pract Res Clin Obstet Gynaecol. 2010;24:383-400. [ Links ]
29. Kinsella SM. Lateral tilt for pregnant women: why 15 degrees? Anaesthesia. 2003;58:835-6. [ Links ]
30. Nanson JD, Elcock D, Williams M, et al. Do physiological changes in pregnancy change defibrillation energy requirements? Br J Anaesth 2001;87:237-9. [ Links ]
31. Karpati P, Rossignol M, Pirot M, Cholley B, Vicaut E, Henry P, et al. High Incidence of Myocardial Ischemia during postpartum Hemorrhage. Anesthesiology. 2004;100:30-6. [ Links ]
32. Borrás R, Perinan R, Fernández C, Plaza A, Andreud E, Schmucker E, et al. Airway management algorithm in the obstetrics patient. Rev Esp Anestesiol Reanim. 2012;59:436-43. [ Links ]
33. Mhyre JM, Healy D. The Unanticipated Difficult Intubation in Obstetrics. Anesth Analg. 2011;112: 648-52. [ Links ]
34. Knill RL. Difficult laryngoscopy made easy with a "BURP". Can J Anaesth. 1993;40:279-82. [ Links ]
35. Wenk M, Pöpping DM, Hillyard S, Albers H, Möllmann M. Intraoperative thrombolysis in a patient with cardiopulmonary arrest undergoing caesarean delivery. Anaesth Intensive Care. 2011;39:671-4. [ Links ]
36. Chauhan A, Musunuru H, Donnino M, McCurdy MT, Chauhan V, Walsh M. The use of therapeutic hypothermia after cardiac arrest in a pregnant patient. Ann Emerg Med. 2012;60:786-9. [ Links ]
37. Rittenberger JC, Kelly E, Jang D, Greer K, Heffner A. Successful outcome utilizing hypothermia after cardiac arrest in pregnancy: a case report. Crit Care Med. 2008;36:1354-6. [ Links ]
38. Bern S, Weinberg G. Local anesthetic toxicity and lipid resuscitation in pregnancy. Curr Opin Anaesthesiol. 2011;24:262-7. [ Links ]
39. Toledo P. The role of lipid emulsion during advanced cardiac life support for local anesthetic toxicity. Int J Obstet Anesth. 2011;20:60-3. [ Links ]
40. Williamson RM, Haines J. Availability of lipid emulsion in obstetric anaesthesia in the UK: a national questionnaire survey. Anaesthesia. 2008;63:385-8. [ Links ]
41. Comparative Obstetric Mobile Epidural Trial (COMET) Study Group UK Randomized Controlled Trial Comparing Traditional with two "Mobile" Epidural techniques Anesthetic and Analgesic Efficacy. Anesthesiology 2002;97:1567-75. [ Links ]
42. Bonner JC, McClymont W. Respiratory arrest in an obstetric patient using remifentanil patient-controlled analgesia. Anaesthesia. 2012;67:538-40. [ Links ]
43. Marr R, Hyams J, Bythell V. Cardiac arrest in an obstetric patient using remifentanil patient-controlled analgesia. Anaesthesia. 2013;68: 283-7. [ Links ]
44. Katz V. Cesarean deliver y: a reconsideration of terminology. Obstet Gynecol. 1995;86:152-3. [ Links ]
45. Katz V, Balderston K, DeFreest M. Perimorten caesarean delivery: Were our assumptions correct? Am J Obstet Gynecol. 2005;192:1916-21. [ Links ]
46. Katz VL, Dotters DJ, Droegemueller W. Perimortem cesarean delivery. Obstet Gynecol. 1986;68:571-6. [ Links ]
47. Vencken PM, van Hooff MH, van der Weiden RM. Cardiac arrest in pregnancy: increasing use of perimortem caesarean section due to emergency skills training? BJOG. 2010;117:1664-5. [ Links ]
48. Engels PT, Caddy SC, Jiwa G, Douglas Matheson J. Cardiac arrest in pregnancy and perimortem cesarean delivery: case report and discussion. CJEM. 2011;13:399-403. [ Links ]
49. Whitty JE. Maternal cardiac arrest in pregnancy. Clin Obstet Gynecol. 2002;45:377-92. [ Links ]
50. Perlman JM, Wyllie J, Kattwinkel J, Atkins DL, Chameides L, Goldsmith JP. Part 11: Neonatal resuscitation: 2010 International Consensus on Cardiopulmonar y Resuscitation and Emergency Cardiovascular Care Science With Treatment Recommendations. Circulation. 2010;122(16 Suppl 2):S516-38. [ Links ]
51. Katz VL. Perimortem cesarean delivery: its role in maternal mortality. Semin Perinatol. 2012; 36:68-72. [ Links ]
52. Jeejeebhoy F, Windrim R. Management of cardiac arrest in pregnancy. Best Pract Res Clin Obstet Gynaecol. 2014;28:607-18. [ Links ]
53. McDonnell NJ. Cardiopulmonary arrest in pregnancy: two case reports of successful outcomes in association with perimortem caesarean delivery. Br J Anaesth. 2009;103:406-9. [ Links ]
54. Zdolsek HJ, Holmgren S, Wedenberg K, Lennmarken C. Circulatory arrest in late pregnancy: caesarean section a vital decision for both mother and child. Acta Anaesthesiol Scand. 2009;53:828-9. [ Links ]
55. Ecker JL, Solt K, Fitzsimons MG, MacGillivray TE. Case records of the Massachusetts General Hospital. Case 40-2012. A 43-year-old woman with cardiorespiratory arrest after a cesarean section. N Engl J Med. 2012;367:2528-36. [ Links ]
56. Kim S, You JS, Lee HS, Lee JH, Park YS, Chung SP. Park I. Quality of chest compressions performed by inexperienced rescuers in simulated cardiac arrest associated with pregnancy. Resuscitation. 2013;84: 98-102. [ Links ]
57. Lipman SS, Wong JY, Arafeh J, Cohen SE, Carvalho B. Transport decreases the quality of cardiopulmonary resuscitation during simulated maternal cardiac arrest. Anesth Analg. 2013;116:162-7. [ Links ]
58. Lipman S, Daniels K, Cohen SE, Carvalho B. Labor room setting compared with the operating room for simulated perimortem cesarean delivery: a randomized controlled trial. Obstet Gynecol. 2011;118:1090-4. [ Links ]
59. Hards A, Davies S, Salman A, Erik-Soussi M, Balki M. Management of simulated maternal cardiac arrest by residents: didactic teaching versus electronic learning. Can J Anaesth. 2012;59:852-60. [ Links ]
60. Berkenstadt H, Ben-Menachem E, Dach R, Ezri T, Ziv A, Rubin O, et al. Deficits in the provision of cardiopulmonar y resuscitation during simulated obstetric crises: results from the Israeli Board of Anesthesiologists. Anesth Analg. 2012;115:1122-6. [ Links ]
61. Fisher N, Eisen LA, Bayya JV, Dulu A, Bernstein PS, Merkatz IR, Goffman D. Improved performance of maternal-fetal medicine staff after maternal cardiac arrest simulation-based training. Am J Obstet Gynecol. 2011;205:239.e1-5. [ Links ]
62. Lipman SS, Daniels KI, Arafeh J, Halamek LP. The case for OBLS: a simulation-based obstetric life support program. Semin Perinatol. 2011;35:74-9. [ Links ]
63. Lipman SS, Daniels KI, Car valho B, Arafeh J, Harney K, Puck A, et al. Deficits in the provision of cardiopulmonary resuscitation during simulated obstetric crises. Am J Obstet Gynecol. 2010;203: 179.e1-5. [ Links ]
64. Vasco M. Estrategias de manejo mediante competencias no técnicas para la disminución de la morbimortalidad materna y perinatal. Rev colomb anestesiol. 2013; 41:20-3. [ Links ]
Conflicto de intereses: ninguno declarado.













