Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Obstetricia y Ginecología
Print version ISSN 0034-7434
Rev Colomb Obstet Ginecol vol.66 no.4 Bogotá Oct./Dec. 2015
https://doi.org/10.18597/rcog.293
DOI: http://dx.doi.org/10.18597/rcog.293
Jairo Amaya-Guío, MD1. Jorge Andrés Rubio-Romero, MD, MSc, FACOG2, Leonardo Arévalo-Mora, MD, MSc3, John Henry Osorio Castaño, Enfermero, MSc4, Francisco Edna- Estrada, MD5, Martha Patricia Ospino-Guzmán, MD, MSc6, Grupo Desarrollador de la Guía - Universidad Nacional de Colombia - Alianza CINETS*
Recibido: mayo 27/15 - Aceptado: octubre 6/15
1 Médico cirujano; Especialista en Obstetricia y Ginecología. Profesor Asociado, Departamento de Obstetricia y Ginecología, Universidad Nacional de Colombia y Profesor asistente, Fundación Universitaria San Martín. Bogotá (Colombia). jaamayagu@ unal.edu.co
2 Médico cirujano; Especialista en Obstetricia y Ginecología. Profesor Asociado, Departamento de Obstetricia y Ginecología, Universidad Nacional de Colombia. Bogotá (Colombia).
3 Médico Cirujano; médico experto en VIH, Servicios de Salud Suramericana. Estudiante de Maestría en Salud Sexual y Reproductiva. Bogotá (Colombia).
4 Especialista en Gerencia de IPS; Magíster en Epidemiología. Bogotá (Colombia).
5 Médico Cirujano; Especialista en Obstetricia y Ginecología. Vocal Zona Norte de la Junta Directiva de la Federación Colombiana de Obstetricia y Ginecología. Bogotá (Colombia).
6 Médica Cirujana; Especialista en Epidemiología. Estudiante de Maestría en Salud Sexual y Reproductiva. Integrante del grupo de investigación de Salud Sexual y Reproductiva de la Universidad Nacional de Colombia. Bogotá (Colombia).
* Representantes del Grupo Desarrollador de la Guía - Universidad Nacional de Colombia - Alianza CINETS. Lista completa al final del documento.
RESUMEN
Objetivo: realizar recomendaciones para la atención del embarazo con ruptura prematura de membranas como parte integral de la Guía de Práctica Clínica (GPC) para la prevención, detección temprana y tratamiento de las complicaciones del embarazo en Colombia.
Materiales y métodos: el grupo desarrollador de la Guía (GDG) elaboró esta GPC durante 2011-2012, acorde con la Guía Metodológica para la elaboración de Guías de Atención Integral en el Sistema General de Seguridad Social en Salud Colombiano, basándose en la evidencia científica disponible y sumando la participación activa de grupos de pacientes, sociedades científicas y grupos de interés. En particular, la evidencia de esta sección fue adaptada de la GPC "Preterm prelabour rupture of membranes" (Royal College of Obstetricians and Gynaecologists-2006) y actualizada por medio de procedimientos sistemáticos, tanto para la búsqueda y valoración de la evidencia como para la generación de recomendaciones. El nivel de evidencia y la fuerza de las recomendaciones fueron expresadas por medio del sistema del Scottish Intercollegiate Guidelines Network (SIGN).
Resultados: se presentan las recomendaciones para la atención de los embarazos con ruptura prematura de membranas. Estas incluyen cambios en la conducta del personal de salud y las instituciones para aumentar la probabilidad de obtener un resultado materno fetal exitoso en las gestaciones con esta complicación.
Conclusiones: se presenta una versión resumida de las recomendaciones y evidencia de esta sección, que se espera sea adoptada por los profesionales de salud encargados de la atención del embarazo en el país para disminuir la morbilidad y mortalidad asociada a la gestación.
Palabras clave: guía de práctica clínica, práctica clínica basada en la evidencia, embarazo, rotura prematura de membranas fetales, Colombia.
ABSTRACT
Objective: To make recommendations for care in pregnancies with Premature Rupture of Membranes, as an integral part of the Clinical Practice Guidelines (CPG) for the prevention, early detection and treatment of pregnancy-associated complications in Colombia.
Materials and methods: The developer group worked on these CPG during 2011-2012 following the Methodological Guidelines for the development of Comprehensive Care Guidelines under the Colombian General Social Security System. The work was based on the scientific evidence available, and was conducted with the active participation of patient groups, scientific societies and stakeholders. In particular, the evidence for this section was adapted from the CPG on "Preterm prelabour rupture of membranes"(Royal College of Obstetricians and Gynaecologists-2006) and updated using systematic procedures both for the search and assessment of the evidence as well as for developing the recommendations. The level of evidence and the power of the recommendations were expressed using the Scottish Intercollegiate Guidelines Network system (SIGN).
Results: Recommendations for care of pregnancies with Premature Rupture of Membranes are presented. They include behavioural changes for the healthcare institutions and staff in order to increase the odds of achieving a successful outcome for the mother and the neonate in pregnancies with this complication.
Conclusions: A summarized version of the recommendations and the evidence for this section is presented. These recommendations are expected to be adopted by the healthcare professionals in charge pregnancy care, in order to reduce pregnancy-related morbidity and mortality in this country.
Key words: Clinical practice guideline, evidence-based clinical practice, pregnancy, Premature Rupture of Foetal Membranes, Colombia.
INTRODUCCIÓN
Entre las infecciones en el embarazo, la ruptura prematura de membranas (RPM) ocupa un lugar relevante. Esta patología complica aproximadamente entre el 8 y el 10 % de todos los embarazos, generando una alta tasa de morbilidad materna y perinatal (1). En la mayoría de los casos, la RPM ocurre en embarazos a término; cuando sucede antes de las 37 semanas de gestación se denomina ruptura prematura de membranas pretérmino, que complica aproximadamente entre 1 a 3 % de todos los embarazos únicos y entre 7 y 20 % de los embarazos gemelares. La RPM es la causa directa de aproximadamente 40 % de todos los partos pretérmino en el mundo, lo cual genera complicaciones y secuelas graves en el neonato (2). El periodo de latencia, el cual es definido como el intervalo de tiempo comprendido entre la ruptura de las membranas y el parto, determina el tipo de complicaciones que se pueden presentar en esta patología, dependiendo de la edad gestacional en que ocurre la ruptura y del manejo instaurado en la gestante (3). Entre las complicaciones maternas se destaca un mayor riesgo de corioamnionitis, el cual predispone a infecciones secundarias y a complicaciones asociadas a la hospitalización, como el tiempo de estancia y la inmovilización, entre otras. En la mayoría de los casos, el diagnóstico correcto de la RPM está basado en una historia clínica bien elaborada, sumada a los hallazgos concordantes del examen físico (2). Aunque es una patología muy frecuente en los servicios obstétricos, el manejo médico aún se basa en un balance entre el riesgo de infección amniótica o fetal y las complicaciones asociadas a la prematurez. Por tanto, existen controversias respecto a su diagnóstico y al abordaje terapéutico, lo cual genera a su vez disparidades en los beneficios a los pacientes respecto al incremento en la tasa de corioamnionitis, sepsis neonatal e ingreso a la unidad de cuidados intensivos, entre otros (2-4).
La disponibilidad de una GPC para la prevención, detección temprana y tratamiento de las alteraciones del embarazo, parto y puerperio busca estandarizar el cuidado de la mujer gestante en Colombia, enfatizando la necesidad de la prevención, la detección temprana y el tratamiento oportuno de las alteraciones que afectan la gestación en todos los niveles de atención, con el fin de reducir la morbimortalidad materna asociada y promoviendo la optimización de la salud y la calidad de la atención médica en todos los niveles de atención obstétrica.
En el presente artículo se presenta una versión abreviada de la información contenida en la GPC de Embarazo y Parto referente a la sección de ruptura prematura de membranas (RPM), mostrando la evidencia relacionada para cada tópico y presentando las recomendaciones elaboradas por el GDG durante el proceso de desarrollo de esta GPC. El grupo desarrollador de la Guía (GDG) elaboró esta GPC durante 2011-2012, acorde con la Guía Metodológica para la elaboración de Guías de Atención Integral en el Sistema General de Seguridad Social en Salud Colombiano, basándose en la evidencia científica disponible y sumando la participación activa de grupos de pacientes, sociedades científicas y grupos de interés. En particular, la evidencia de esta sección fue adaptada de la GPC "Preterm prelabour rupture of membranes"(Royal College of Obstetricians and Gynaecologists-2006) (5) y actualizada por medio de procedimientos sistemáticos, tanto para la búsqueda y valoración de la evidencia como para la generación de recomendaciones. El nivel de evidencia y la fuerza de las recomendaciones fueron expresadas por medio del sistema del Scottish Intercollegiate Guidelines Network (SIGN). La versión completa de esta GPC (incluida la búsqueda sistemática de información científica y la presentación detallada de la evidencia científica), así como la versión para pacientes y sus anexos, estín disponibles para la consulta de los interesados por diferentes medios (físicos y electrónicos) (6, 7).
RECOMENDACIONES
La nomenclatura para la calificación de las recomendaciones y la calidad de la evidencia está contenida en las "Guías de príctica clínica para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto o puerperio: introducción y metodología" (6, 7).
1. ¿Cuál es la definición de la ruptura prematura de membranas (RPM)?
La ruptura prematura de membranas (RPM) se define como la pérdida de continuidad de las membranas corioamnióticas que sobreviene con salida de líquido amniótico de más de una hora, previo al inicio del trabajo de parto. La ruptura de las membranas amnióticas ocurre en 10 % de las gestaciones y es responsable del 25 al 30 % de los nacimientos pretérmino (8, 9).
La gestante con RPM requiere de un adecuado manejo y para ello es necesario tener en cuenta el periodo de latencia, entendido como el intervalo entre la ruptura de las membranas y el inicio del trabajo de parto. En la presente guía se denomina RPM prolongada a aquella con un periodo de latencia mayor a 24 horas (10).
El GDG recomienda que la ruptura de membranas se subdivida en dos categorías:
a. Ruptura prematura de membranas a término: después de la semana 37 de gestación.
b. Ruptura prematura de membranas prermino: previo a la semana 37 de gestación. Esta se divide en tres categorías (11):
1. RPM previable: corresponde a la ruptura prematura de membranas pretérmino en gestaciones menores a 24 0/7 semanas.
2. RPM lejos del término: corresponde a la ruptura prematura de membranas pretérmino en gestaciones entre 24 0/7 y 32 6/7 semanas.
3. RPM cerca del término: corresponde a la ruptura prematura de membranas pretérmino en gestaciones de 33 0/7 a 36 6/7 semanas (12).
2. ¿Cómo se realiza el diagnóstico clínico de ruptura prematura de membranas?


El diagnóstico de RPM debe ser realizado mediante la combinación de la anamnesis con el examen físico (historia clínica). El tacto vaginal debe evitarse hasta que el diagnóstico de RPM se haya descartado, a menos que haya una fuerte sospecha de que la gestante está en trabajo de parto. El primer paso para hacer el diagnóstico de RPM es realizar una especuloscopia con el fin de evidenciar la salida de líquido a través del orificio cervical o lagos de líquido amniótico en el fondo del saco posterior de la vagina.
3. ¿Qué ayudas diagnósticas están recomendadas para el diagnóstico de ruptura prematura de membranas?


La evidencia es de baja calidad e indica pocos avances en pruebas de diagnóstico para la RPM. Las nuevas técnicas que involucran marcadores placentarios como la microglobulina-1 alfa placentaria pueden ser herramientas útiles para el diagnóstico de casos no claros de RPM.
4. ¿Cuáles son los criterios clínicos recomendados para el diagnóstico de corioamnionitis?
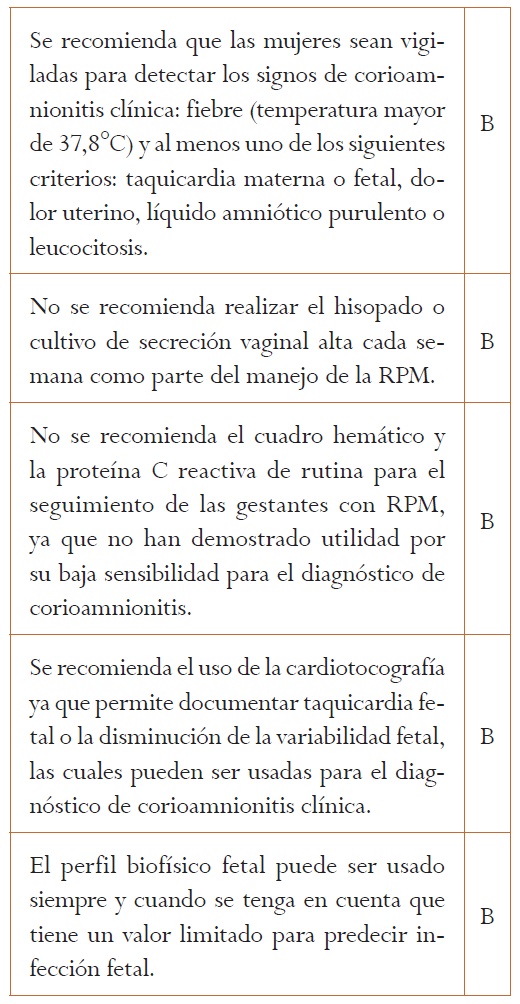

La evidencia no apoya el uso de la PCR para el diagnóstico de corioamnionitis en casos de RPM. Con la ayuda de otras pruebas diagnósticas, su valor predictivo puede ser usado en el contexto de situaciones clínicas especiales. Si se desea usar una única muestra de PCR para el diagnóstico de corioamnionitis, lo apropiado sería utilizar puntos corte de al menos 30 mg/l. Para estimaciones seriadas, niveles > 20 mg/l parecen ser predictores de infección. No hay evidencia de buena calidad que soporte que el uso frecuente del perfil biofísico y del Doppler mejore el resultado del embarazo.
5. ¿Está recomendado el uso de la amniocentesis en gestantes con ruptura prematura de membranas?


El consenso de expertos consideró que la amniocentesis tiene el potencial de detectar infecciones subclínicas antes de que aparezcan los signos maternos de corioamnionitis y antes de que se desencadene la sepsis fetal, permitiendo intervenciones apropiadas, entre ellas, la administración de antibióticos en casos de infección y la inducción del parto dependiendo de la edad gestacional, el manejo expectante en pacientes con cultivo de líquido amniótico negativo y la realización de pruebas diagnósticas que indiquen infección. La amniocentesis está indicada en casos de RPM entre 32 a 34 semanas de gestación para documentar si hay madurez pulmonar.
6. ¿Cuáles son los criterios recomendados para el diagnóstico de infección intraamniótica en una muestra de líquido amniótico?


La evidencia encontrada es de baja calidad y no permite recomendar la MMP-8, la interleucina 6 o la PCR para el diagnóstico de infección intraamniótica. El GDG y el grupo de expertos, recomendó el uso de pruebas en paralelo para el análisis de la muestra de líquido amniótico a fin de establecer el diagnóstico de infección intraamniótica.
7. ¿En qué grupo de pacientes está recomendada la utilización de corticoides en RPM?


La evidencia identificada es de buena calidad, consistente y apunta en la misma dirección a las recomendaciones originales de la guía adaptada que indican el uso de corticosteroides en mujeres con RPM. El uso de un ciclo único de corticosteroides prenatales para acelerar la maduración de los pulmones del feto en las mujeres con riesgo de parto prematuro por ruptura de membranas, debe considerarse de rutina para fetos prematuros desde la viabilidad fetal hasta la semana 34 6/7, con pocas excepciones.
8. ¿En qué casos se encuentra indicada la dosis de corticoide de rescate en RPM?


Existe evidencia directa de que una dosis simple de rescate con betametasona en mujeres que persistan con riesgo de parto pretérmino siete días o más después de la dosis inicial se asocia con una reducción de la dificultad respiratoria sin incrementar aparentemente la enfermedad infecciosa perinatal. El GDG y el consenso de expertos recogieron estas consideraciones y recomendaron el uso de una dosis de rescate de corticoides en las condiciones señaladas.
9. ¿Cuál es el esquema antibiótico y el tiempo de duración recomendado para profilaxis de infección intraamniótica en RPM?


La evidencia es de buena calidad, mantiene la dirección de la recomendación de la guía original del RCOG y muestra que en pacientes con RPM pretérmino, se encuentran beneficios del uso de antibióticos sobre la morbilidad materna y neonatal,se retarda el inicio del trabajo de parto y permite el tiempo para la acción de los corticosteroides.
10. ¿Cuál es el esquema antibiótico recomendado para tratamiento de corioamnionitis en el escenario de una RPM?


La evidencia demuestra de forma indirecta que el tratamiento antibiótico de la corioamnionitis clínica iniciado antes del parto redujo las complicaciones maternas y neonatales. El cubrimiento con esquemas antibióticos para anaerobios parece disminuir el riesgo de endometritis posparto comparado con otros esquemas de amplio espectro. La evidencia apoya el uso de dosis únicas por día de gentamicina para el tratamiento de la infección materna y fetal.
11. ¿Qué medicamento están recomendados para la inducción del parto en manejo no expectante de paciente con RPM sin trabajo de parto?


La evidencia es consistente en los resultados de la efectividad del misoprostol como agente para la maduración cervical y la inducción del parto en las mujeres en general. Para la inducción del parto en las pacientes con RPM, el GDG y el consenso de expertos consideró que el misoprostol es efectivo para la maduración cervical y la inducción del parto. En las diferentes revisiones, los análisis del subgrupo de mujeres con RPM muestran que el misoprostol es superior a la mayoría de métodos de inducción excepto cuando se compara con la oxitocina. Finalmente, la administración de misoprostol por vía oral parece tener más seguridad que la vía vaginal con dosis menores de 50 mcg.
12. ¿En qué grupo de pacientes se encuentra recomendada la amnioinfusión?


El GDG y el grupo de expertos en consenso, consideró que se requiere mayor evidencia para recomendar la amnioinfusión rutinaria en la práctica clínica en gestantes con RPM.
13. ¿Cuál debe ser el manejo recomendado de la RPM acorde con la edad gestacional?


La evidencia, de moderada calidad, muestra que el manejo expectante por encima de la semana 34, parece disminuir la aparición de complicaciones neonatales. Durante el manejo expectante, las pacientes deben ser vigiladas para identificar complicaciones como desprendimiento de la placenta, infección, el inicio del trabajo de parto o el deterioro del bienestar fetal. Un manejo expectante puede asociarse con un incremento en la tasa de corioamnionitis clínica y puede ser más benéfico para los neonatos debido a que se disminuyen los riesgos de morbilidad asociados a la prematurez. La edad gestacional específica cuando los beneficios superan los riesgos, tanto para la madre como para el bebé, parece estar después de la semana 34 de gestación. Hasta la fecha, todos los ensayos clínicos han tenido debilidades metodológicas y poco poder para detectar medidas con mejoras significativas de la morbilidad materna e infantil. No hay suficiente evidencia para soportar la terapia tocolítica en mujeres con ruptura prematura de membranas, pues hubo un incremento en la corioamnionitis materna sin beneficios significativos para el bebé. Por estas razones, el GDG, en conjunto con el consenso de expertos, sugirió el manejo individualizado de cada caso, en especial en las gestaciones menores a 26 semanas.
14. ¿Cuáles son las recomendaciones para la profilaxis de estreptococo del grupo B?


El GDG, junto al grupo de expertos en consenso, mantuvo las recomendaciones de la guía original del RCOG para la prevención de la sepsis neonatal temprana asociada al EGB, basada en profilaxis antibiótica intraparto, en paciente con RPM y estado de colonización vaginal o rectal desconocido.
15. ¿Está recomendado el esquema de sulfato de magnesio para neuroprotección en parto pretérmino asociado a RPM?


Evidencia de buena calidad permite recomendar el uso de sulfato de magnesio para la neuroprotección fetal en mujeres con amenaza o riesgo inminente de parto pretérmino, antes de las 32 semanas de gestación. Dicha evidencia se sustenta en una reducción observada del riesgo de parálisiscerebral en los dos años siguientes al nacimiento, de alrededor de un 30 %.
DECLARACIÓN DE CONFLICTOS DE INTERÃS
El trabajo científico de investigación, así como la elaboración de las recomendaciones incluidas en el presente documento, fueron realizados de manera independiente por el Grupo Desarrollador de Guías (GDG) de la Universidad Nacional de Colombia. Todos los miembros del GDG, así como las personas que han participado tanto en la colaboración experta como en la revisión externa, realizaron declaración de conflictos de interés previo a su participación.
Este artículo hace parte de un grupo de 25 GPC basadas en la evidencia que incorporan consideraciones económicas y de implementabilidad en el contexto del Sistema General de Seguridad Social en Salud Colombiano (SGSSS), y que se desarrollaron por iniciativa del Ministerio de Salud y Protección Social y el Departamento de Ciencia, Tecnología e Innovación â COLCIENCIAS, en temas prioritarios y de alta prevalencia en el país, mediante contrato otorgado a la Universidad Nacional de Colombia en el año 2010. Código ISBN 978-958-8858-29-8.
La nomenclatura para la calificación de las recomendaciones y la calidad de la evidencia está contenida en las "Guías de práctica clínica para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto o puerperio: introducción y metodologíaâ. Publicado en el año 2013, en esta revista, (84).
ACTUALIZACIÓN DE LA GUÃA
Las recomendaciones de esta Guía deben actualizarse en los próximos tres años a partir de su expedición o previamente en caso de disponer de nuevas evidencias que modifiquen de manera significativa las recomendaciones aquí anotadas.
FUENTES DE FINANCIACIÓN
Ministerio de Salud y Protección Social de Colombia â Departamento de Ciencia, Tecnología e Innovación (COLCIENCIAS).
REPRESENTANTES DEL GRUPO DESARROLLADOR DE LA GUÍA - UNIVERSIDAD NACIONAL DE COLOMBIA - ALIANZA Cinets*
Jairo Amaya-Guío, MD. Médico cirujano; Especialista en Obstetricia y Ginecología. Profesor Asociado, Departamento de Obstetricia y Ginecología, Universidad Nacional de Colombia y Profesor asistente, Fundación Universitaria San Martín. Bogotá (Colombia). jaamayagu@ unal.edu.co
Jorge Andrés Rubio-Romero, MD, MSc, FACOG. Médico cirujano; Especialista en Obstetricia y Ginecología. Profesor Asociado, Departamento de Obstetricia y Ginecología, Universidad Nacional de Colombia. Bogotá (Colombia).
Leonardo Arévalo-Mora, MD, MSc. Médico Cirujano; médico experto en VIH, Servicios de Salud Suramericana. Estudiante de Maestría en Salud Sexual y Reproductiva. Bogotá (Colombia).
John Henry Osorio-Castaño, Enfermero, MSc. Especialista en Gerencia de IPS; Magíster en Epidemiología. Bogotá (Colombia).
Francisco Edna-Estrada, MD. Médico Cirujano; Especialista en Obstetricia y Ginecología. Vocal Zona Norte de la Junta Directiva de la Federación Colombiana de Obstetricia y Ginecología. Bogotá (Colombia).
Martha Patricia Ospino-Guzmán, MD, MSc. Médica Cirujana; Especialista en Epidemiología. Estudiante de Maestría en Salud Sexual y Reproductiva. Integrante del grupo de investigación de Salud Sexual y Reproductiva de la Universidad Nacional de Colombia. Bogotá (Colombia).
Mónica Ballesteros-Silva, MD, MSc, PhD(c). Médica Cirujana; Especialista en Epidemiología; Máster en Epidemiología Clínica; Máster en Salud Pública, PhD (c) en Pediatría, Obstetricia y Ginecología, Medicina Preventiva y Salud Pública, Universidad Autónoma de Barcelona (España).
Ingrid Arévalo-Rodríguez, MSc, PhD(c). Epidemióloga Clínica, Universidad Nacional de Colombia; PhD (c) en Pediatría, Obstetricia y Ginecología, Medicina Preventiva y Salud Pública, Universidad Autónoma de Barcelona (España). Coordinadora General de Epidemiología Clínica de la Guía; instructor asociado, División de Investigaciones,Fundación Universitaria de Ciencias de la Salud, Hospital de San José-Hospital Infantil de San José. Bogotá (Colombia).
Pio Iván Gómez-Sánchez MD, MSc, FACOG. Médico Cirujano; Especialista en Obstetricia y Ginecología, y Epidemiología; Magíster en Salud Sexual y Reproductiva. Feedback Editor del Grupo Cochrane de Infecciones de Transmisión Sexual; Director del Grupo de Investigación en Salud Sexual y Reproductiva de la Facultad de Medicina; Profesor Titular, Universidad Nacional de Colombia. Líder general de la GPC. Bogotá (Colombia).
RECONOCIMIENTO A INSTITUCIONES PARTICIPANTES
Las siguientes instituciones participaron en los consensos de expertos o reuniones de socialización de la GPC para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto o puerperio: Federación Colombiana de Obstetricia y Ginecología (FECOLSOG), Sociedad Colombiana de Anestesiología y Reanimación (SCARE), Asociación Colombiana de Facultades de Medicina (ASCOFAME), Asociación Colombiana de Facultades de Enfermería (ACOFAEN), Asociación Colombiana de Empresas de Medicina Integral (ACEMI), Academia Nacional de Medicina, Colegio Médico Colombiano, Asociación Colombiana de Hospitales y Clínicas, Instituto Nacional de Salud, CAFAM IPS, Centro Médico Imbanaco, Clínica de Occidente, Clínica de la Mujer, Clínica del Norte, Clínica Materno Infantil Farallones, Clínica el Rosario, Clínica el Prado, Fundación Cardioinfantil, Fundación Valle de Lili, Fundación Santafé de Bogotá, Hospital Militar Central, Hospital de San José, Hospital Simón Bolívar, Fundación Universitaria de Ciencias de la Salud, Universidad de Antioquia, Universidad del Quindío, Universidad Libre, Universidad Sur colombiana.
REFERENCIAS
1. Merenstein GB, Weisman LE. Premature rupture of the membranes: neonatal consequences. Semin Perinatol. 1996;20:375-80. Epub 1996/10/01. [ Links ]
2. Di Renzo GC, Facchinetti F, Antsaklis A, Breborowicz G, Gratacos E, Cabero Roura L, et al. Guidelines for the management of spontaneous preterm labor: identification of spontaneous preterm labor, diagnosis of preterm premature rupture of membranes, and preventive tools for preterm birth. The journal of maternal-fetal & neonatal medicine: the official journal of the European Association of Perinatal Medicine, the Federation of Asia and Oceania Perinatal Societies, the International Society of Perinatal Obstet. 2011;24:659-67. [ Links ]
3. Mercer BM. Preterm premature rupture of the membranes: current approaches to evaluation and management. Obstet Gynecol Clin North Am. 2005;32:411-28. Epub 2005/08/30. [ Links ]
4. ACOG Practice Bulletin No. 80: premature rupture of membranes. Clinical management guidelines for obstetrician-gynecologists. Obstet Gynecol. 2007;109:1007-19. Epub 2007/04/03. [ Links ]
5. Royal College of Obstetricians and Gynaecologists. Preterm Prelabour Rupture of Membranes. Dublin, Ireland; 2006 [Visitado 2011 Jun 1]. Disponible en: http://www.rcog.org.uk/womens-health/clinical-guidance/preterm-prelabour-rupture-membranes-green-top-44. [ Links ]
6. Ministerio de Salud y Protección Social, Colciencias. Guía de práctica clínica para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto o puerperio. Versión completa. Bogotá: Alianza CINETS; 2013. Disponible en: http://www.guiascolcienciasminproteccionsocialalianzacinets.org/index.php?option=com_wrapper&view=wrapper&Itemid=552. [ Links ]
7. Ministerio de Salud y Protección Social, Colciencias. Guía de práctica clínica para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto o puerperio. Versión para pacientes. Bogotá: Alianza CINETS; 2013. Disponible en: http://www.guiascolcienciasminproteccionsocialalianzacinets.org/index.php?option=com_wrapper&view=wrapper&Itemid=552. [ Links ]
8. DeFranco E AK, Heyl PS. Preterm Labor, Premature Rupture of Membranes, and Cervical Insufficiency. En: Evans, AT. Manual of Obstetrics. 7a. ed. Lippincott Williams & Wilkins; 2007. p. 141-5. [ Links ]
9. Mercer BM. Preterm premature rupture of the membranes. Obstet Gynecol. 2003;101:178-93. Epub 2003/01/09. [ Links ]
10. Amaya J, Gaitan MA. Ruptura prematura de membranas. En: Parra M, Angel E, editores. Obstetricia Integral Siglo XXI. Bogotá: Universidad Nacional de Colombia; 2011. p. 122-46. [ Links ]
11. Canavan TP, Simhan HN, Caritis S. An evidence-based approach to the evaluation and treatment of premature rupture of membranes: Part I. Obstet Gynecol Surv. 2004;59:669-77. Epub 2004/08/27. [ Links ]
12. Santolaya-Forgas J, Espinoza J, Erez O, Friel LA , Kusanovic JP, et al. Prelabor Rupture of the Membranes. En: Clinical Obstetrics: The Fetus & Mother. 3a ed. Blackwell Publishing; 2007. p. 1130-88. [ Links ]
13. Friedman ML, McElin TW. Diagnosis of ruptured fetal membranes. Clinical study and review of the literature. Am J Obstet Gynecol. 1969;104:544-50. Epub 1969/06/15. [ Links ]
14. El-Messidi A, Cameron A. Diagnosis of premature rupture of membranes: inspiration from the past and insights for the future. J Obstet Gynaecol Can. 2010;32:561-9. Epub 2010/06/24. [ Links ]
15. Lewis DF, Major CA, Towers CV, Asrat T, Harding JA, Garite TJ. Effects of digital vaginal examinations on latency period in preterm premature rupture of membranes. Obstet Gynecol. 1992;80:630-4. Epub 1992/10/01. [ Links ]
16. Mulhair L, Carter J, Poston L, Seed P, Briley A. Prospective cohort study investigating the reliability of the AmnioSense method for detection of spontaneous rupture of membranes. BJOG. 2009;116:313-8. Epub 2008/07/26. [ Links ]
17. van der Ham DP, van Melick MJ, Smits L, Nijhuis JG, Weiner CP, van Beek JH, et al. Methods for the diagnosis of rupture of the fetal membranes in equivocal cases: a systematic review. Eur J Obstet Gynecol Reprod Biol. 2011;157:123-7. Epub 2011/04/13. [ Links ]
18. Carroll SG, Papaioannou S, Ntumazah IL, Philpott-Howard J, Nicolaides KH. Lower genital tract swabs in the prediction of intrauterine infection in preterm prelabour rupture of the membranes. Br J Obstet Gynaecol. 1996;103:54-9. Epub 1996/01/01. [ Links ]
19. Yucel N, Yucel O, Yekeler H. The relationship between umbilical artery Doppler findings, fetal biophysical score and placental inflammation in cases of premature rupture of membranes. Acta Obstet Gynecol Scand. 1997;76:532-5. Epub 1997/07/01. [ Links ]
20. Vintzileos AM, Campbell WA, Nochimson DJ, Weinbaum PJ, Mirochnick MH, Escoto DT. Fetal biophysical profile versus amniocentesis in predicting infection in preterm premature rupture of the membranes. Obstet Gynecol. 1986;68:488-94. Epub 1986/10/01. [ Links ]
21. Goldstein I, Romero R, Merrill S, Wan M, O'Connor TZ, Mazor M, et al. Fetal body and breathing movements as predictors of intraamniotic infection in preterm premature rupture of membranes. Am J Obstet Gynecol. 1988;159:363-8. Epub 1988/08/01. [ Links ]
22. Roussis P, Rosemond RL, Glass C, Boehm FH. Preterm premature rupture of membranes: detection of infection. Am J Obstet Gynecol. 1991;165(4 Pt 1):1099-104. Epub 1991/10/01. [ Links ]
23. Carroll SG, Papaioannou S, Nicolaides KH. Assessment of fetal activity and amniotic fluid volume in the prediction of intrauterine infection in preterm prelabor amniorrhexis. Am J Obstet Gynecol. 1995; 172:1427-35. Epub 1995/05/01. [ Links ]
24. Carroll SG, Papaioannou S, Nicolaides KH. Doppler studies of the placental and fetal circulation in pregnancies with preterm prelabor amniorrhexis. Ultrasound Obstet Gynecol. 1995;5:184-8. Epub 1995/03/01. [ Links ]
25. Ismail MA, Zinaman MJ, Lowensohn RI, Moawad AH. The significance of C-reactive protein levels in women with premature rupture of membranes. Am J Obstet Gynecol. 1985;151:541-4. Epub 1985/02/15. [ Links ]
26. Ferguson MG, Rhodes PG, Morrison JC, Puckett CM. Clinical amniotic fluid infection and its effect on the neonate. Am J Obstet Gynecol. 1985;151:1058-61. Epub 1985/04/15. [ Links ]
27. van de Laar R, van der Ham DP, Oei SG, Willekes C, Weiner CP, Mol BW. Accuracy of C-reactive protein determination in predicting chorioamnionitis and neonatal infection in pregnant women with premature rupture of membranes: a systematic review. Eur J Obstet Gynecol Reprod Biol. 2009;147:124-9. Epub 2009/10/13. [ Links ]
28. Popowski T, Goffinet F, Maillard F, Schmitz T, Leroy S, Kayem G. Maternal markers for detecting early-onset neonatal infection and chorioamnionitis in cases of premature rupture of membranes at or after 34 weeks of gestation: a two-center prospective study. BMC Pregnancy Childbirth. 2011;11:26. Epub 2011/04/08. [ Links ]
29. Wiwanitkit V. Maternal C-reactive protein for detection of chorioamnionitis: an appraisal. Infect Dis Obstet Gynecol. 2005;13:179-81. Epub 2005/08/30. [ Links ]
30. Trochez-Martinez RD, Smith P, Lamont RF. Use of C-reactive protein as a predictor of chorioamnionitis in preterm prelabour rupture of membranes: a systematic review. BJOG. 2007;114:796-801. Epub 2007/06/15. [ Links ]
31. Carroll SG, Ville Y, Greenough A, Gamsu H, Patel B, Philpott-Howard J, et al. Preterm prelabour amniorrhexis: intrauterine infection and inter val between membrane rupture and delivery. Arch Dis Child Fetal Neonatal Ed. 1995;72:F43-6. Epub 1995/01/01. [ Links ]
32. Jacobsson B, Holst RM, Mattsby-Baltzer I, Nikolaitchouk N, Wennerholm UB, Hagberg H. Interleukin-18 in cervical mucus and amniotic fluid: relationship to microbial invasion of the amniotic fluid, intra-amniotic inflammation and preterm delivery. BJOG. 2003;110:598-603. Epub 2003/06/12. [ Links ]
33. Cotton DB, Gonik B, Bottoms SF. Conser vative versus aggressive management of preterm rupture of membranes. A randomized trial of amniocentesis. Am J Perinatol. 1984;1:322-4. Epub 1984/07/01. [ Links ]
34. Porreco RP, Heyborne KD, Shapiro H. Amniocentesis in the management of preterm premature rupture of the membranes: a retrospective cohort analysis. J Matern Fetal Neonatal Med. 2008;21:573-9. Epub 2008/07/09. [ Links ]
35. Di Naro E, Raio L, Romano F, Mueller M, Mcdougall J, Cicinelli E. C-reactive protein in vaginal fluid of patients with preterm premature rupture of membranes. Acta Obstet Gynecol Scand. 2003;82:1072-9. [ Links ]
36. Trochez-Martinez R, Lamont R. Use of C-reactive protein as a predictor of chorioamnionitis in preterm prelabour rupture of membranes: a systematic review. BJOG. 2007;114:796-801. [ Links ]
37. van de Laar R, Oei SG, Willekes C, Weiner P, Mol B. Accuracy of C-reactive protein determination in predicting chorioamnionitis and neonatal infection in pregnant women with premature r upture of membranes: A systematic review. Eur J Obstet Gynecol Reprod Biol. 2009;147:124-9. [ Links ]
38. Pettker M, Magloire L, Sfakianaki A, Hamar B, Buhimschi, C. Value of Placental Microbial Evaluation in Diagnosing Intra-amniotic Infection. Obstet Gynecol. 2007;109:739-49. [ Links ]
39. Kim KW, Romero R, Park HS, Park CW, Shim SS, Jun JK, et al. A rapid matrix metalloproteinase-8 bedside test for the detection of intraamniotic inflammation in women with preterm premature r upture of membranes. Am J Obstet Gynecol. 2007;197:292 e1-5. Epub 2007/09/11. [ Links ]
40. Harding JE, Pang J, Knight DB, Liggins GC. Do antenatal corticosteroids help in the setting of preterm r upture of membranes? Am J Obstet Gynecol. 2001;184:131-9. Epub 2001/02/15. [ Links ]
41. Roberts D, Dalziel S. Antenatal corticosteroids for accelerating fetal lung maturation for women at risk of preterm birth. Cochrane Database Syst Rev. 2006(3):CD004454. Epub 2006/07/21. [ Links ]
42. Been JV, Degraeuwe PL, Kramer BW, Zimmermann LJ. Antenatal steroids and neonatal outcome after chorioamnionitis: a meta-analysis. BJOG. 2011;118:113-22. Epub 2010/11/09. [ Links ]
43. Vermillion ST, Bland ML, Soper DE. Effectiveness of a rescue dose of antenatal betamethasone after an initial single course. Am J Obstet Gynecol. 2001;185:1086-9. Epub 2001/11/22. [ Links ]
44. Crowther CA, McKinlay CJ, Middleton P, Harding JE. Repeat doses of prenatal corticosteroids for women at risk of preterm birth for improving neonatal health outcomes. Cochrane Database Syst Rev. 2011(6):CD003935. Epub 2011/06/17. [ Links ]
45. Kenyon S, Boulvain M, Neilson JP. Antibiotics for preterm rupture of membranes. Cochrane Database Syst Rev. 2010;(8):CD001058. [ Links ]
46. Yudin MH, van Schalkwyk J, van Eyk N, Boucher M, Castillo E, Cormier B, et al. Antibiotic therapy in preterm premature rupture of the membranes. J Obstet Gynaecol Can. 2009;31:863-7, 8-74. Epub 2009/11/28. [ Links ]
47. Flenady V, King JF. Antibiotics for prelabour rupture of membranes at or near term. Cochrane. 2011(2). DOI: 10.1002/14651858.CD001807.pub2 [ Links ]
48. Hopkins L, Smaill F. Antibiotic regimens for management of intraamniotic infection. Cochrane Database Syst Rev. 2002(3):CD003254. Epub 2002/07/26. [ Links ]
49. Locksmith GJ, Chin A, Vu T, Shattuck KE, Hankins GD. High compared with standard gentamicin dosing for chorioamnionitis: a comparison of maternal and fetal ser um dr ug levels. Obstet Gynecol. 2005;105:473-9. Epub 2005/03/02. [ Links ]
50. Lyell DJ, Pullen K, Fuh K, Zamah AM, Caughey AB, Benitz W, et al. Daily compared with 8-hour gentamicin for the treatment of intrapartum chorioamnionitis: a randomized controlled trial. Obstet Gynecol. 2010;115(2 Pt 1):344-9. Epub 2010/01/23. [ Links ]
51. Fox NS, Saltzman DH, Roman AS, Klauser CK, Moshier E, Rebarber A. Intravaginal misoprostol versus Foley catheter for labour induction: a meta-analysis. BJOG. 2011;118:647-54. Epub 2011/02/22. [ Links ]
52. Dare MR, Middleton P, Crowther CA, Flenady VJ, Varatharaju B. Planned early birth versus expectant management (waiting) for prelabour rupture of membranes at term (37 weeks or more). Cochrane Database Syst Rev. 2006(1):CD005302. Epub 2006/01/27. [ Links ]
53. Lin MG, Nuthalapaty FS, Carver AR, Case AS, Ramsey PS. Misoprostol for labor induction in women with term premature rupture of membranes: a meta-analysis. Obstet Gynecol. 2005;106:593-601. Epub 2005/09/02. [ Links ]
54. Alfirevic Z, Weeks A. Oral misoprostol for induction of labour. Cochrane Database Syst Rev. 2006(2):CD001338. Epub 2006/04/21. [ Links ]
55. Hofmeyr GJ, Gulmezoglu AM, P ileggi C. Vaginal misoprostol for cer vical ripening and induction of labour. Cochrane Database Syst Rev. 2010(10):CD000941. Epub 2010/10/12. [ Links ]
56. Hofmeyr GJ. Prophylactic versus therapeutic amnioinfusion for oligohydramnios in labour. Cochrane Database Syst Rev. 2010(2):CD000176. [ Links ]
57. Hofmeyr GJ. Amnioinfusion for umbilical cord compression in labour. Cochrane Database Syst Rev. 2012(2):CD000013. Epub 2000/05/05. [ Links ]
58. Hofmeyr GJ. Amnioinfusion for preterm rupture of membranes. Cochrane Database Syst Rev. 2011(2):CD000942. Epub 2000/05/05. [ Links ]
59. Pristauz G, Bauer M, Maurer-Fellbaum U, Rotky-Fast C, Bader AA, Haas J, et al. Neonatal outcome and two-year follow-up after expectant management of second trimester rupture of membranes. Int J Gynaecol Obstet. 2008;101:264-8. doi: 10.1016/j. ijgo.2007.12.007. Epub 2008 Mar 4. [ Links ]
60. Manuck T, Esplin S, Stoddard G, Varner M, Silver R. Outcomes of Expectantly Managed Preterm Premature Rupture of Membranes Occurring Before 24 Weeks of Gestation. Obstet Gynecol. 2009;114: 29-37. [ Links ]
61. Melamed N, Pardo J, Chen R, Hadar E, Hod M, Yogev Y. Expectant management of preterm premature rupture of membranes: is it all about gestational age? Am J Obstet Gynecol. 2011;204:48.e1-8. [ Links ]
62. Borna S, Khazardoost S, Hantoushzadeh S. Perinatal outcome in preterm premature rupture of membranes with Amniotic fluid index < 5 (AFI < 5). BMC Pregnancy and Childbirth. 2004:4:15. [ Links ]
63. Kayem G, Goffinet F, Cabrol D, Haddad B. Active versus expectant management for preterm prelabor rupture of membranes at 34-36 weeks of completed gestation: comparison of maternal and neonatal outcomes. Acta Obstet Gynecol Scand. 2010;89:776-81. [ Links ]
64. Lieman J, Carlo W, Ramsey P. Preterm Premature Rupture of Membranes: Is There an Optimal Gestational Age for Deliver y? Obstet Gynecol. 2005;105:12-7. [ Links ]
65. Shrivastava V, Ehsanipoor R, Lee RM, Chan K, Gaylean A, Garite T, et al. 165: Randomized double-blinded trial of indomethacin tocolysis versus expectant management in patients with premature rupture of membranes at 24-32 weeks of gestation. Am J Obstet Gynecol. 2008;199:S59. [ Links ]
66. Javaid MK, Hassan S, Tahira T. Management prelabour rupture of the membranes at term; induction of labor compared with expectant. Professional Medical Journal. 2008;15:216-9. [ Links ]
67. Kayem G, Bernier-Dupreelle A, Goffinet F, Cabrol D, Haddad B. Active versus expectant management for preterm prelabor rupture of membranes at 34-36 weeks of completed gestation: comparison of maternal and neonatal outcomes. Acta Obstet Gynecol Scand. 2010;89:776-81. Epub 2010/03/17. [ Links ]
68. Canavan TP, Simhan HN, Caritis S. An evidence-based approach to the evaluation and treatment of premature rupture of membranes: Part II. Obstet Gynecol Surv. 2004;59:678-89. Epub 2004/08/27. [ Links ]
69. Mackeen AD, Seibel-Seamon J, Grimes-Dennis J, Baxter JK, Berghella V. Tocolytics for preterm premature rupture of membranes. Cochrane Database Syst Rev. 2011(10):CD007062. Epub 2011/10/07. [ Links ]
70. Neerhof MG, Cravello C, Haney EI, Silver RK. Timing of labor induction after premature rupture of membranes between 32 and 36 weeks' gestation. Am J Obstet Gynecol. 1999;180(2 Pt 1):349-52. Epub 1999/02/13. [ Links ]
71. Buchanan SL, Crowther CA, Levett KM, Middleton P, Morris J. Planned early birth versus expectant management for women with preterm prelabour rupture of membranes prior to 37 weeks' gestation for improving pregnancy outcome. Cochrane Database Syst Rev. 2010(3):CD004735. Epub 2010/03/20. [ Links ]
72. Gardner SE, Yow MD, Leeds LJ, Thompson PK, Mason EO, Clark DJ. Failure of penicillin to eradicate group B streptococcal colonization in the pregnant woman. A couple study. Am J Obstet Gynecol. 1979;135:1062-5. Epub 1979/12/15. [ Links ]
73. Wood EG, Dillon HC, Jr. A prospective study of group B streptococcal bacteriuria in pregnancy. Am J Obstet Gynecol. 1981;140:515-20. Epub 1981/07/01. [ Links ]
74. de Cueto M, Sanchez MJ, Sampedro A, Miranda JA, Herruzo AJ, Rosa-Fraile M. Timing of intrapartum ampicillin and prevention of vertical transmission of group B streptococcus. Obstet Gynecol. 1998;91:112-4. Epub 1998/02/17. [ Links ]
75. Lin FYC, Brenner RA, Johnson YR, Azimi PH, Philips JB 3rd, Regan JA, et al. The effectiveness of risk-based intrapartum chemoprophylaxis for the prevention of early-onset neonatal group B streptococcal disease. Am J Obstet Gynecol. 2001;184:1204-10. [ Links ]
76. Valkenburg-van den Berg AW, Houtman-Roelofsen RL, Oostvogel PM, Dekker FW, Dorr PJ, Sprij AJ. Timing of group B streptococcus screening in pregnancy: a systematic review. Gynecol Obstet Invest. 2010;69:174-83. Epub 2009/12/18. [ Links ]
77. Ohlsson A, Shah VS. Intrapartum antibiotics for known maternal Group B streptococcal colonization. Cochrane Database Syst Rev. 2009(3):CD007467. Epub 2009/07/10. [ Links ]
78. Stade B, Shah V, Ohlsson A. Vaginal chlorhexidine during labour to prevent early-onset neonatal group B streptococcal infection. Cochrane Database Syst Rev. 2004(3):CD003520. Epub 2004/07/22. [ Links ]
79. Fiore Mitchell T, Pearlman MD, Chapman RL, Bhatt-Mehta V, Faix RG. Maternal and transplacental pharmacokinetics of cefazolin. Obstet Gynecol. 2001;98:1075-9. Epub 2002/01/05. [ Links ]
80. Laiprasert J, Klein K, Mueller BA, Pearlman MD. Transplacental passage of vancomycin in nonin- fected term pregnant women. Obstet Gynecol. 2007;109:1105-10. Epub 2007/05/02. [ Links ]
81. Muller AE, Mouton JW, Oostvogel PM, Dorr PJ, Voskuyl RA, DeJongh J, et al. Pharmacokinetics of clindamycin in pregnant women in the peripartum period. Antimicrob Agents Chemother. 2010;54:2175- 81. Epub 2010/02/24. [ Links ]
82. Verani JR, McGee L, Schrag SJ. Prevention of perinatal group B streptococcal disease-revised guidelines from CDC, 2010. MMWR Recomm Rep. 2010;59:1-36.Epub 2010/11/23. [ Links ]
83. Doyle LW, Crowther CA, Middleton P, Marret S, Rouse D. Magnesium sulphate for women at risk of preterm birth for neuroprotection of the fetus. Cochrane Database Syst Rev. 2009(1):CD004661. Epub 2009/01/23. [ Links ]
84. Gómez-Sánchez PI, Arévalo-Rodríguez I, Rubio-Romero JA, Amaya-Guío J, Osorio-Castaño JH, Buitrago-Gutiérrez G. Guías de Práctica Clínica para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto o puerperio: introducción y metodología. Rev Colomb Obstet Ginecol [serial on the Internet]. 2013 Sep [Visitado 2015 Oct 1]; 64(3): 234-244. Disponible en: http://www.scielo.org.co/scielo.php?script=sci_arttext&pid=S0034-74342013000300004&lng=en. [ Links ]













