Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Obstetricia y Ginecología
Print version ISSN 0034-7434On-line version ISSN 2463-0225
Rev Colomb Obstet Ginecol vol.69 no.3 Bogotá July/Sept. 2018
https://doi.org/10.18597/rcog.3149
Investigaciones originales
Evaluación de la utilidad de un dispositivo para toma y preservación del ADN del virus del papiloma humano de muestras cérvico-vaginales autorrecolectadas y almacenadas en seco en mujeres con displasia cervical, Bogotá, Colombia
1 Gynaecologist. Professor of the Colposcopy Diploma Course. Fundación Universitaria Ciencias de la Salud - Hospital de San José, Bogotá (Colombia). ginejairo@yahoo.es
2 Gynaecologist. Tenured Professor, Universidad Nacional de Colombia, Subred Norte de servicios de Salud, Bogotá (Colombia).
3 Bacteriologist; Microbiologist, Pontificia Universidad Javeriana. Scientific Director, Molecular Analysis Centre, Bogotá (Colombia).
4 Gynaecology Resident, FUCS - Hospital de San José, Bogotá (Colombia).
Objetivo:
Evaluar la utilidad de un dispositivo para toma y preservación del DNA del virus del papiloma humano (VPH) de muestras vaginales recolectadas por autotoma y almacenadas en seco durante 14 días.
Materiales y métodos:
Estudio piloto de concordancia diagnóstica. Se incluyeron mujeres mayores de 24 años no gestantes con un resultado de neoplasia intraepitelial cervical (NIC) grado 1 o más, confirmado por biopsia en dos instituciones de referencia en Bogotá, Colombia. Se excluyeron mujeres con antecedente de histerectomía total. Se realizó un muestreo por conveniencia. El dispositivo utiliza PCR (reacción en cadena de la polimerasa) en tiempo real para detección del ADN. Se midieron variables sociodemográficas y clínicas, así como el resultado de la prueba por autotoma y tomada por el médico, y la cantidad de ADN de las muestras tomadas el día 1 procesadas ese día, y el día 14, por medio del Ct umbral. Se realizó estadística descriptiva. Se calculó la concordancia global por medio del índice de kappa ponderado y la diferencia de medias de la cantidad de ADN.
Resultados:
La concordancia en la detección de VPH de alto riesgo mostró un kappa = 0,84 (IC 95 %: 0,71-0,96) entre la muestra cervicovaginal recolectada por autotoma frente a la muestra cervical recolectada por el médico. No hubo diferencias en la cantidad de ADN viral entre el día 1 y el 14 (DM -0,34 ciclos; IC 95 %: -2,29 a 1,61).
Conclusión:
Las muestras vaginales recolectadas por autotoma usando el dispositivo de almacenamiento son confiables para la detección de VPH de alto riesgo en pacientes con displasia cervical, y preservan el ADN viral por 14 días si se almacenan en seco a temperatura ambiente. Se requieren estudios en población general para poder confirmar.
Palabras clave: pruebas de ADN del papilomavirus humano; cribado; frotis vaginal; autoexamen; manejo de especímenes.
Objective:
To evaluate the usefulness of a device for collecting and preserving human papilloma virus (HPV) DNA in self-collected vaginal samples stored dry during 14 days.
Materials and methods:
Diagnostic concordance pilot study that included non-pregnant women over 25 years of age with a biopsy-confirmed result of cervical intraepithelial neoplasia (CIN) grade 1 or more, coming to two referral centres in Bogotá, Colombia. Women with a history of total hysterectomy were excluded. Convenience sampling was used. The device uses real-time PCR (polymerase chain reaction) for DNA detection. Sociodemographic and clinical variables were measured, as well as the results of the test when the sample was collected by the patient and when it was collected by the physician, and the amount of DNA in the samples taken and processed on day 1, and in those processed on day 14, using Ct thresholds. Descriptive statistics were applied. Overall concordance was estimated by means of the kappa coefficient and mean differences in DNA amount.
Materials and methods:
Diagnostic concordance pilot study that included non-pregnant women over 25 years of age with a biopsy-confirmed result of cervical intraepithelial neoplasia (CIN) grade 1 or more, coming to two referral centres in Bogotá, Colombia. Women with a history of total hysterectomy were excluded. Convenience sampling was used. The device uses real-time PCR (polymerase chain reaction) for DNA detection. Sociodemographic and clinical variables were measured, as well as the results of the test when the sample was collected by the patient and when it was collected by the physician, and the amount of DNA in the samples taken and processed on day 1, and in those processed on day 14, using Ct thresholds. Descriptive statistics were applied. Overall concordance was estimated by means of the kappa coefficient and mean differences in DNA amount.
Results:
A kappa coefficient of 0.84 (95% CI: 0.71-0.96) was found for concordance in high-risk HPV detection between the self-collected cervicovaginal sample and the sample taken by the clinician. There were no differences in terms of the amount of viral DNA between day 1 and day 14 (DM -0.34 cycles; 95% CI: - 2.29 to 1.61).
Conclusion:
Self-collected vaginal samples using the storage device are reliable for high-risk HPV detection in patients with cervical dysplasia, and preserve viral DNA for 14 days if stored dry at room temperature. Confirmation studies in the general population are required.
Key words: human papilloma virus DNA testing; vaginal smear; self-testing; specimen handling.
INTRODUCCIÓN
El cáncer de cuello uterino es el cuarto cáncer más frecuente en las mujeres y el séptimo en la población general en el mundo. En Colombia, en el año 2012 se registraron 4.661 casos nuevos de cáncer de cuello uterino y 1.986 mujeres murieron por esta enfermedad, lo que constituyó la segunda causa de mortalidad por cáncer en la mujer1. Esta patología genera una gran carga social, especialmente porque en Colombia, en el 40 % de los hogares la mujer tiene el soporte económico y el mantenimiento de los hijos2. Desde el punto de vista etiológico se ha demostrado que la enfermedad es precedida por la infección con alguno de los 14 tipos oncogénicos de virus del papiloma humano (VPH) definidos de “alto riesgo” (VPH-ar) por el Centro Internacional de Investigaciones sobre el Cáncer (IARC, por sus siglas en inglés) en el 20093.
Luego de una infección con VPH-ar, un pequeño porcentaje de mujeres desarrollan anormalidades del epitelio cervical (denominadas en citología “lesiones intraepiteliales” también llamadas “neoplasias intraepiteliales”). Las neoplasias intraepiteliales de bajo grado (NIC1) tienen una alta probabilidad de regresión (60 al 80 %), dentro de los 2 primeros años luego de su detección, y no ameritan tratamiento4. Sin embargo, un 10 % de ellas puede persistir y transitar a neoplasias de alto grado (NIC2 o NIC3), las cuales progresan a carcinoma en un 20 a 30 % y, por tanto, ameritan tratamiento4.
A diferencia de otros tipos de cáncer, con el de cuello uterino existe la posibilidad de realizar un diagnóstico temprano, 10 a 15 años antes de manifestarse, mediante la identificación de lesiones intraepiteliales precancerosas (LIE), ya sea por medio de la citología cervical o, más recientemente, con la detección del VPH. Los programas de tamización a partir de la citología se iniciaron en los años sesenta con muy buenos resultados en países desarrollados donde se han implementado este tipo de programas de una manera organizada y garantizando coberturas superiores al 70 %, allí las tasas de mortalidad por cáncer cervical se han reducido en un 50-90 %5. Sin embargo, en países de medios y bajos ingresos los resultados en cuanto a incidencia y mortalidad no han sido los mismos, debido a que la citología tiene limitaciones importantes por problemas de cobertura y barreras de acceso a los servicios de salud, mal procesamiento de la muestra, baja sensibilidad, pobre seguimiento de las positivas y los altos costos de infraestructura y recurso humano5. En el caso de Colombia, el 9 % de las mujeres en edad de tamización nunca se han realizado una citología, el 12 % solo se la ha tomado una vez en la vida, y el 30 % de las mujeres no reclaman el resultado2. Se ha descrito que las mujeres no asisten a los programas de tamización por razones culturales o subjetivas como dolor, miedo, vergüenza a la toma de muestras por personal masculino o por desconocimiento de la enfermedad6.
Con la implementación de programas de tamización basados en VPH, se ha logrado reducir la mortalidad por cáncer de cuello uterino3,5. Una revisión sistemática que incluyó 40 estudios (144.000 mujeres) reportó que la sensibilidad relativa de la prueba de VPH comparada con la citología tradicional para detectar NIC 3+ es de 1,46 (IC 95 %: 1,12-1,91) y la especificidad relativa 0,95 (IC 95 %: 0,93-0,97)7. Por otra parte, Ronco et al., con base en los datos de cuatro ensayos clínicos controlados europeos concluyen que, dada su mayor sensibilidad para la detección de neoplasia intraepitelial cervical, las pruebas de VPH proporcionan un 60-70 % más de protección contra el cáncer invasivo en comparación con la citología8. La identificación del VPH se puede hacer con pruebas que detectan directamente el ADN del VPH-ar, con pruebas que amplifican un fragmento del ADN del virus o con pruebas que identifican el ARNm viral. Las primeras detectan el ADN de cualquier tipo de VPH-ar sin realizar amplificación previa del ADN. Una segunda opción utiliza la reacción en cadena de polimerasa (PCR) convencional o en tiempo real, amplifican un fragmento del ADN para obtener millones de copias de este, y las pruebas de ARNm identifican la sobreexpresión de las oncoproteínas E6 y E7 del VPH-ar7. Colombia está en el proceso de cambiar gradualmente la citología por las pruebas de VPH en su programa de tamización4.
La prueba del VPH tiene la ventaja de permitir que la muestra sea recolectada por la paciente (autotoma) y entregada en los programas de tamización. Se ha descrito que esta autotoma podría aumentar la cobertura en un 10 a 15 % y reducir las tasas de cáncer cervical9-11. La autotoma ofrece una alternativa atractiva por su facilidad y privacidad en países donde las barreras culturales y la estructura de los programas limitan el acceso a los programas de tamización12-15. Se han diseñado diferentes tipos de dispositivos para la recolección de la muestra por autotoma como: hisopos, cepillos, tampones o dispositivos de lavado16-18.
Un metaanálisis concluye que independientemente del tipo de dispositivo usado (hisopo, cepillo, tampón) para la recolección de la muestra, la sensibilidad y la especificidad de las muestras recolectadas por autotoma son similares a las muestras tomadas por el clínico para la detección de infección por VPH19. El lavado cervicovaginal es la técnica de automuestreo más estudiada, su principal desventaja es el manejo adecuado de los especímenes líquidos que hacen difícil su transporte. Por eso es importante tener alternativas para que el ADN del VPH extraído pueda almacenarse y transportarse en seco11,17. Lo que tendrá un impacto favorable en el incremento de la cobertura y oportunidad de la tamización del cáncer de cérvix en la atención primaria20,21.
Debido a la heterogeneidad de su territorio, la presencia de poblaciones indígenas y áreas con difícil acceso a los servicios de salud, en la región latinoamericana la implementación de la autotoma es una estrategia de detección del cáncer cervical basado en VPH que se debe evaluar. Se requiere valorar si hay concordancia entre la muestra obtenida por autotoma con la muestra obtenida por el médico, como también si la muestra almacenada mantiene la cantidad de ADN viral durante el tiempo hasta el análisis. Aunque a la fecha se han publicado algunos estudios que reportan la estabilidad del ADN de VPH en una muestra recolectada hasta un mes(22, 23), en Colombia no encontramos estudios que evalúen este tema y es importante valorar si la prueba se comporta de manera similar en diferentes contextos.
Este estudio tiene como objetivo evaluar la utilidad de un nuevo dispositivo de recolección para identificar y preservar el ADN de VPH de alto riesgo de muestras cervicovaginales recolectadas por autotoma y almacenadas en seco durante 14 días a temperatura ambiente.
MATERIALES Y MÉTODOS
Diseño y población. Estudio piloto de concordancia diagnóstica. Se incluyeron mujeres mayores de 25 años, no gestantes, que consultaron a las unidades de patología cervical y colposcopia, con un resultado de neoplasia intraepitelial cervical (NIC) grado 1 o más, confirmado por biopsia. Se excluyeron mujeres con antecedente de histerectomía total, que estuvieran menstruando o que se hubieran aplicado medicamentos tópicos vaginales 15 días previos a la consulta. El estudio se realizó entre el 1 de agosto y el 30 noviembre de 2016 en dos instituciones de la ciudad de Bogotá: Clínica ESIMED, institución privada que atiende población perteneciente al régimen de aseguramiento contributivo en el sistema de seguridad social en Colombia, y el Hospital de Engativá, institución pública que pertenece a la Subred Integrada de Servicios de Salud Norte ESE, y atiende población adscrita al régimen de aseguramiento subsidiado por el Estado. Se realizó un muestreo por conveniencia a partir del universo de pacientes con displasia cervical atendidas en las instituciones participantes durante el periodo de estudio.
Procedimiento. El estudio se diseñó en dos fases: la primera se realizó con el objetivo de evaluar la concordancia en el resultado de las muestras vaginales recolectadas en seco por la paciente (autotoma) (utilizando el dispositivo HerSwab®, Eve Medical, Toronto, ON) con el resultado de muestras cervicales tomadas en medio líquido por el médico para la detección de ADN de VPH en mujeres con displasia cervical. La segunda fase se diseñó para evaluar la utilidad de este dispositivo para preservar ADN de VPH de las muestras vaginales recolectadas por autotoma y almacenadas en seco a temperatura ambiente durante 14 días, comparado con una segunda muestra autocolectada el día inicial con el mismo dispositivo de autocolección y procesada el mismo día de la toma.
Fase 1: las mujeres candidatas a participar recibieron información verbal sobre el objetivo del estudio, aquellas que aceptaron participar firmaron el consentimiento informado y se procedió a aplicar una encuesta para determinar sus características sociodemográficas. Posteriormente, por parte de la enfermera de la unidad de patología cervical, recibieron instrucciones verbales sobre la técnica de automuestreo utilizando un folleto con instrucciones ilustradas. El médico entregó un dispositivo HerSwab® para que la paciente recolectara por autotoma, en el baño del consultorio, una muestra vaginal de acuerdo con las siguientes instrucciones del fabricante: “introducir el dispositivo en vagina, girar el extremo distal del dispositivo 5 veces en el sentido del reloj para exponer el cepillo y, sin retirar de la vagina, girar en sentido contrario 5 veces para retraer el cepillo, luego retirar el dispositivo de la vagina y entregar a la enfermera”. A continuación, la paciente era llevada al consultorio donde el médico recolectaba una segunda muestra mediante la inserción del cepillo Cervicollect ® de Abbott en el endocérvix girándolo 5 veces y después enjuagándolo en el medio líquido de transporte siguiendo las indicaciones del fabricante. La muestra recolectada por el médico siempre se obtuvo después de la recolectada por autotoma para evitar que el espéculo lesionara la mucosa vaginal y contaminara la muestra. Una vez recibidas las muestras en el laboratorio, fueron procesadas y analizadas el mismo día por una bacterióloga entrenada, de acuerdo con las indicaciones del fabricante.
Fase 2: un segundo grupo de mujeres recibió información verbal sobre el objetivo del estudio, y aquellas que aceptaron participar firmaron el consentimiento informado y se procedió a aplicar una encuesta para determinar las características sociodemográficas. Posteriormente, recibieron de la enfermera de la unidad instrucciones verbales sobre la técnica de automuestreo utilizando un folleto con instrucciones ilustradas. El médico entregó dos dispositivos HerSwab® para que la paciente recolectara por autotoma dos muestras vaginales, de acuerdo con las instrucciones del fabricante, de la misma manera como se entregaron a las mujeres que participaron en la fase 1 de este estudio. Las dos muestras fueron recibidas por la enfermera, conservadas en seco y transportadas a temperatura ambiente hasta el laboratorio. Una vez recibidas las muestras en el laboratorio, una de ellas se procesó y analizó inmediatamente (tiempo 0) y la segunda muestra se almacenó en el mismo dispositivo de recolección a temperatura ambiente y fue analizada 14 días después. La bacterióloga que procesó la muestra el día 14 desconocía el resultado de la primera.
Procesamiento de las muestras: para identificar ADN de VPH en las muestras se usó la técnica de PCR en tiempo real (Real Time de Abbott®), de acuerdo con las instrucciones del fabricante y el procedimiento estándar del laboratorio. Esta prueba fue diseñada para la detección de los 14 tipos de VPH de alto riesgo con genotipado para VPH16 y 18. Para la extracción del ADN cada una de las muestras colectadas se preparó utilizando el Sistema m2000sp de Abbott (Abbott, Wiesbaden, Germany). Se definió como positiva la detección de ADN viral cuando se logró un ciclo umbral (CT) menor o igual a 32.
Se midieron las variables basales (sociodemográficas y clínicas), y de desenlace (resultado de la prueba por autotoma y de la prueba tomada por el médico, cantidad de ADN de las muestras tomadas el día 1 (tiempo 0), procesadas ese día, y la cantidad de ADN viral de la procesada el día 14).
Análisis estadístico. Se realizó estadística descriptiva para las características clínicas y sociodemográficas. Se calculó la media y la desviación estándar (DE) o las medianas y el rango según el tipo de variable, y se calculó la prevalencia de VPH por medio de la PCR. Además, se calculó la proporción de muestras con un resultado positivo para infección por VPH con base en las muestras por autotoma procesadas en el día 0 de las dos fases del estudio y las tomadas por el médico.
Se calculó la concordancia global para la detección de ADN de VPH entre las muestras tomadas por la paciente (autotoma) y la muestra tomada por el médico, y el índice de kappa ponderado de Cohen (K). Valores de K < 0.40 indican pobre acuerdo, valores de 0,41 a 0,75 indican buen acuerdo, y valores de > 0,75 indican excelente acuerdo. Para determinar la capacidad de preservación del ADN viral en la muestra por autotoma almacenada en seco se calculó la diferencia de medias para muestras relacionadas del Ct umbral (número de ciclos necesarios para que cada curva alcance un umbral en la señal de fluorescencia) de las muestras secas procesadas en tiempo 0 y a los 14 días. El Ct umbral es un valor directamente proporcional a la cantidad de ADN presente en cada muestra: a mayor cantidad de ADN, menor número de ciclos (Ct) se requieren para alcanzar este umbral. Los datos se analizaron con el programa SPSS versión 19. Se presentan las proporciones de la escala de preferencias de pacientes.
Aspectos éticos. El estudio fue aprobado por el Comité de Ética y por el Comité de Investigaciones de la USS Engativá (julio 22 de 2016). A las mujeres que participaron se les solicitó la firma del consentimiento informado. Se garantizó confidencialidad de la información.
RESULTADOS
Se incluyeron 93 mujeres, con informe histopatológico de biopsia: NIC 1 en 22, NIC 2 en 36, NIC 3 en 31 y carcinoma invasivo en 4; las pacientes habían sido remitidas a colposcopia por citología anormal: ASCUS (n = 22), ASC-H (n = 11), LIE-BG (n = 35), LIE-AG (n = 21) AGC-NOS (n = 2) y negativa (n = 2). La edad promedio fue de 35,1 años (DE ± 9,16), provenían de estrato bajo el 63,4 % (59/93) y medio 36,6 %, (34/93); primera relación sexual con una mediana de 17 (rango: 13-28) y mediana del primer parto a los 19 (rango 3-32), mediana de número de partos: 2 (rango 0-6), mediana de tres compañeros sexuales (rango 1-50).
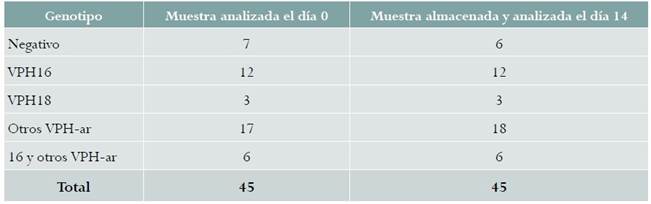
En la fase 1 se incluyeron las muestras de 48 mujeres. La infección por VPH-ar en muestras tomadas por el médico se detectó en 35/48 (72,9 %) mujeres, en comparación con 34/48 (70,8 %) de las muestras por autotoma, con una kappa ponderado de 0,84 (IC 95 %: 0,71-0,96). Los diferentes genotipos de VPH identificados mediante esta técnica se presentan en la tabla 1.
Tabla 1 Genotipo de VPH identificado por autotoma y muestra recolectada por el médico en mujeres con displasia cervical en Bogotá, Colombia, 2016
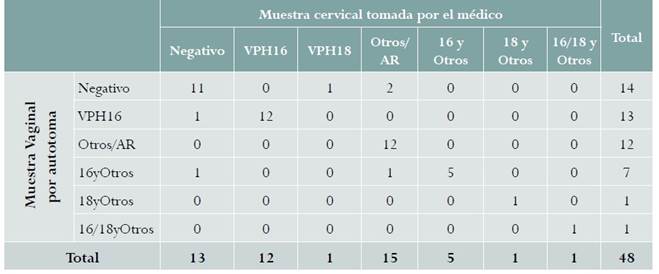
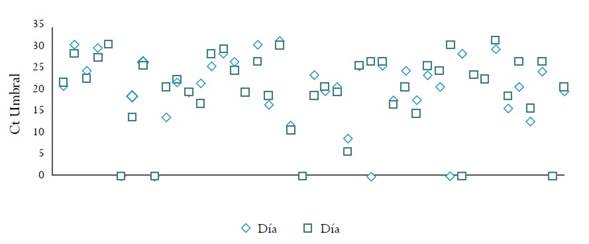
En la fase 2 se incluyeron las muestras de 45 mujeres. Los datos de las 45 muestras analizadas en los días 0 y 14 se presentan en la figura 1. La cantidad de ADN viral detectada en la muestra seca procesada al día 0: Media 20,11 Ct (DE ± 9,10), fue similar a la encontrada en la muestra procesada al día 14: Media 20,45 Ct (DE ± 8,79). Diferencia de Medias = -0,34 (IC 95 %: -2,29 a 1,61). No hubo diferencias en el porcentaje de positividad de VPH-ar entre los especímenes que se analizaron el mismo día de la recolección, 38/45 (84,4 %), y las muestras que se analizaron 14 días después, 39/45 (86,6 %) (tabla 2). Una muestra que fue negativas en el día 0, fue positiva para otros VPH-ar al día 14 (tabla 2).
DISCUSIÓN
Nuestros resultados señalan que muestras vaginales recolectadas en seco por autotoma arrojan una alta concordancia para la detección de ADN de VPH comparado con muestras cervicales que se toman en medio líquido por el médico.
Se encontró una prevalencia de infección por VPH del 72,9 % en mujeres con displasia cervical, esta es ligeramente superior a la reportada por autotoma, que fue del 70,8 %. Esta frecuencia es mayor a la informada por van Baars et al. (53 %) en muestras recolectadas por autotoma con el mismo cepillo. La diferencia se podría explicar porque en nuestro estudio las muestras se analizaron con PCR y van Baars lo hizo con el sistema SPF10-DEIALiPA 2520. Nuestros resultados difieren con lo reportado en la revisión sistemática de Stewart et al., que encontró pobre concordancia para la detección de infección por VPH entre las muestras recolectadas por el paciente y el clínico (kappa < 0,6) en tres estudios recuperados que utilizaron el cepillo vaginal para la autotoma21.
En nuestro estudio, la cantidad de ADN de VPH detectado en una muestra recolectada por autotoma en seco con el dispositivo HerSwab y almacenada a temperatura ambiente durante 2 semanas fue igual a la de una muestra tomada en las mismas condiciones y procesada el mismo día. Estos hallazgos coinciden con otros estudios que reportan que la estabilidad del ADN en una muestra autorrecolectada en seco se preserva hasta por dos semanas22. Baay et al. reportó que la cantidad y calidad del ADN de VPH permanece estable hasta un mes (concentración media de ADN de las muestras almacenadas: 45,1 ng /μl, vs. 50,9 ng /μl para las muestras procesada el mismo día), sin perder su capacidad para detectar lesiones intraepiteliales de alto grado23.
El estudio tiene limitaciones por el tamaño de muestra pequeño y porque se realizó en dos centros de referencia en mujeres con lesiones displásicas, lo que genera dudas en la posibilidad de extrapolar nuestros resultados a población general donde se tienen prevalencias menores ya que se incluyen mujeres sin lesiones preneoplásicas. Como fortalezas del estudio se encuentra que los resultados de las pruebas iniciales por autotoma día 0 y la tomada por el médico no fueron divulgados al personal del laboratorio que procesó las muestras de autotoma del día 14 para la detección del ADN de VPH.
CONCLUSIONES
Nuestros resultados indican que las muestras vaginales recolectadas por autotoma usando el cepillo HerSwab® son similares a las obtenidas por el médico para la identificación de ADN de VPH-ar, y que este dispositivo preserva el ADN de VPH durante 14 días si se almacena en seco a temperatura ambiente. Se requieren estudios en población general para poder confirmar la utilidad de la prueba en programas de tamización.
REFERENCIAS
1. Ferlay J, Soerjomataram I, Ervik M, Dikshit R, Eser S, Mathers C, et al. GLOBOCAN 2012 v1.0, Cancer Incidence and Mortality Worldwide: IARC CancerBase No. 11. Lyon, France: International Agency for Research on Cancer; 2013. https://doi.org/10.1002/ijc.29210. [ Links ]
2. Profamilia, Colombia. Encuesta nacional de demografía y salud ENDS 2010 Colombia. Bogotá D.C.: Profamilia. 2010 [visitado 2018 sep 1]. Disponible en: http://profamilia.org.co/docs/ENDS %202010.pdf. [ Links ]
3. IARC Human papillomaviruses. IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. Lyon, France; 1995. [ Links ]
4. Ministerio de Salud y Protección Social, Instituto Nacional de Cancerología ESE. Guía de Práctica Clínica para la detección y manejo de lesiones precancerosas de cuello uterino. Colombia 2014 [visitado 2018 sep 1]. Disponible en: http://gpc.minsalud.gov.co/gpc_sites/Repositorio/Otros_conv/GPC_cuello_uterino_inv/CCU_Guia_profesionales_julio_2016.pdf. [ Links ]
5. Castle PE, de Sanjosé S, Qiao Y-L, Belinson JL, Lazcano-Ponce E, Kinney W. Introduction of human papillomavirus DNA screening in the world: 15 years of experience. Vaccine. 2012;30:F117-22. https://doi.org/10.1016/j.vaccine.2012.05.071. [ Links ]
6. Gupta S, Palmer C, Bik EM, Cardenas JP, Nuñez H, Kraal L, et al. Self-sampling for human papillomavirus testing: Increased cervical cancer screening participation and incorporation in international screening programs. Frontiers in Public Health. 2018;6:77. https://doi.org/10.3389/fpubh.2018.00077. [ Links ]
7. Koliopoulos G, Nyaga VN, Santesso N, Bryant A, Martin-Hirsch PPL, Mustafa RA, et al. Cytology versus HPV testing for cervical cancer screening in the general population. Cochrane Database of Systematic Reviews 2017, Issue 8. CD008587. https://doi.org/10.1002/14651858.CD008587.pub2. [ Links ]
8. Ronco G, Dillner J, Elfstrom KM, Tunesi S, Snijders PJF, Arbyn M, et al. Efficacy of HPV-based screening for prevention of invasive cervical cancer: Follow-up of four European randomised controlled trials. Lancet. 2014;383:524-32. https://doi.org/10.1016/S0140-6736(13)62218-7. [ Links ]
9. Arrossi S, Thouyaret L, Herrero R, Campanera A, Magdaleno A, Cuberli M, et al. Effect of self-collection of HPV DNA offered by community health workers at home visits on uptake of screening for cervical cancer (the EMA study): A population-based cluster-randomised trial. Lancet Glob Health. 2015;3:e85-94. https://doi.org/ 10.1016/S2214-109X (14)70354-7. [ Links ]
10. Racey CS, Withrow DR, Gesink D. Self-collected HPV testing improves participation in cervical cancer screening: A systematic review and meta-analysis. Can J Public Health. 2013;104:e159-66. [ Links ]
11. Gok M, Heideman DAM, van Kemenade FJ, Berkhof J, Rozendaal L, Spruyt JWM, et al. HPV testing on self-collected cervicovaginal lavage specimens as screening method for women who do not attend cervical screening: Cohort study. BMJ. 2010;340:c1040-c1040. https://doi.org/10.1136/bmj.c1040. [ Links ]
12. Catarino R, Vassilakos P, Stadali-Ullrich H, Royannez-Drevard I, Guillot C, Petignat P. Feasibility of at-home self-sampling for HPV testing as an appropriate screening strategy for nonparticipants in Switzerland. J Low Genit Tract Dis. 2015;19:27-34. https://doi.org/10.1097/LGT.0000000000000051 [ Links ]
13. Mandigo M, Frett B, Laurent JR, Bishop I, Raymondville M, Marsh S, et al. Pairing community health workers with HPV self-sampling for cervical cancer prevention in rural Haiti. Int J Gynecol Obstet. 2015;128:206-10. https://doi.org/10.1016/j.ijgo.2014.09.016. [ Links ]
14. Curotto M, Barletta P, Paolino M, Arrossi S. La perspectiva de los agentes sanitarios sobre la incorporación programática de la autotoma del test de VPH. Cad Saúde Pública. 2017;33:1-13. https://doi.org/10.1590/0102-311x00138515. [ Links ]
15. Nelson EJ, Maynard BR, Loux T, Fatla J, Gordon R, Arnold LD. The acceptability of self-sampled screening for HPV DNA: A systematic review and meta-analysis. Sex Transm Infect. 2017;93:56-61. https://doi.org/10.1136/sextrans-2016-052609. [ Links ]
16. Fairley CK, Chen S, Tabrizi SN, Quinn MA, McNeil JJ, Garland SM. Tampons: A novel patient-administered method for the assessment of genital human papillomavirus infection. J Infect Dis. 1992;165:1103-6. https://doi.org/10.1093/infdis/165.6.1103. [ Links ]
17. Brink AATP, Meijer CJLM, Wiegerinck MAHM, Nieboer TE, Kruitwagen RFPM, van Kemenade F, et al. High concordance of results of testing for human papillomavirus in cervicovaginal samples collected by two methods, with comparison of a novel self-sampling device to a conventional endocervical brush. J Clin Microbiol. 2006;44:2518-23. https://doi.org/10.1128/JCM.02440-05. [ Links ]
18. Bais AG, van Kemenade FJ, Berkhof J, Verheijen RHM, Snijders PJF, Voorhorst F, et al. Human papillomavirus testing on self-sampled cervicovaginal brushes: An effective alternative to protect nonresponders in cervical screening programs. Int J Cancer. 2007;120:1505-10. https://doi.org/10.1002/ijc.22484. [ Links ]
19. Arbyn M, Verdoodt F, Snijders PJF, Verhoef VMJ, Suonio E, Dillner L, et al. Accuracy of human papillomavirus testing on self-collected versus clinician-collected samples: A meta-analysis. Lancet Oncol. 2014;15:172-83. https://doi.org/10.1016/S1470-2045(13)70570-9. [ Links ]
20. van Baars R, Bosgraaf RP, Harmsel BWA, Melchers WJG, Quint WGV, Bekkers RLM. Dry storage and transport of a cervicovaginal self-sample by use of the evalyn brush, providing reliable human papillomavirus detection combined with comfort for women. J Clin Microbiol. 2012;50:3937-43. https://doi.org/10.1128/JCM.01506-12. [ Links ]
21. Stewart DE, Gagliardi A, Johnston M, Howlett R, Barata P, Lewis N, et al. Self-collected samples for testing of oncogenic human papillomavirus: A systematic review. J Obstet Gynaecol Can. 2007;29:817-28. https://doi.org/10.1016/S1701-2163(16)32636-6. [ Links ]
22. Vassilakos P, Catarino R, Bougel S, Munoz M, Benski C, Meyer-Hamme U, et al. Use of swabs for dry collection of self-samples to detect human papillomavirus among Malagasy women. Infectious Agents and Cancer. 2016;11:13. https://doi.org/10.1186/s13027-016-0059-8. [ Links ]
23. Baay M, Verhoeven V, Lambrechts H, Pattyn G, Lardon F, Van Royen P, et al. Feasibility of collecting self-sampled vaginal swabs by mail: Quantity and quality of genomic DNA. Eur J Clin Microbiol Infect Dis. 2009;28:1285-9. https://doi.org/10.1007/s10096-009-0776-7. [ Links ]
Conflicto de intereses: los insumos para la recolección y el análisis de las muestras fueron donados por los fabricantes, quienes no participaron en el diseño del estudio, tampoco en la recolección de las muestras ni en el análisis o la interpretación de los resultados. Los autores han recibido apoyo para asistir a congresos por parte de Abbott, pero no recibieron honorarios para la realización del estudio.
Recibido: 22 de Febrero de 2018; Aprobado: 04 de Septiembre de 2018











 text in
text in