Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Colombiana de Psiquiatría
versão impressa ISSN 0034-7450
rev.colomb.psiquiatr. v.28 n.1 Bogotá jan./mar. 1999
SÍNDROME DE INTERRUPCIÓN DE LOS ISRS
(SSRI DISCONTINUATION SYNDROME)
1Jefe Departamento de Psiquiatría. Corporación Universitaria Ciencias de la Salud-Hospital San José Bogotá Director Científico Asociación Colombiana contra la Depresión y el Pánico.
Resumen
Los pacientes que suspenden la medicación (antidepresivos, estabilizadores del afecto o antipsicóticos) presentan con frecuencia síntomas somáticos y cognoscitivos que pueden, en algunos casos, como sucede con los IMAOS clásicos, requerir tratamiento intrahospitalario.
La sintomatología es inespecífica y difiere de los síntomas secundarios indeseables del fármaco o del síndrome de abstinencia que se presenta con hipnóticos, barbitúricos, benzodiacepinas, alcohol o sustancias adictivas.
En el presente trabajo se revisa la literatura sobre los aspectos clínicos, epidemiológicos y terapéuticos del Síndrome de interrupción del tratamiento con los inhibidores selectivos de la recaptación de serotonina (ISRS).
Palabras Clave: Síndrome de interrupción, ISRS, terapéutica, prevención.
Abstract
When patients stop long-term therapy with antidepressants, mood stabilizers or antipsychotics, discontinuation symptoms frequently occur. Their range in severity, from mild somatic distress and gastrointestinal symptoms to serious cognitive impairment, may lead to hospitalization, which can appear when monoamine oxidase inhibitors are discontinued.
Although severe, these non specific symptoms are distinctly different from the classic withdrawal syndrome associated with sedative hypnotics such as alcohol and barbiturates.
Existing hypotheses about mecanisms of Serotonin Reuptake Inhibitor Discontinuation Syndrome (SSRI) are here reviewed.
Key Words: Discontinuation syndrome, SSRI, Therapeutics, Prevention.
INTRODUCCIÓN
Los estudios epidemiológicos han mostrado que cerca del 70% de los pacientes con depresión suspenden el tratamiento antidepresivo entre el primero y el segundo trimestre después de iniciado porque creen que no es necesario continuar tomando la medicación, por temor a depender del medicamento o porque la terapia farmacológica ha resultado ineficaz.
Los nuevos antidepresivos, como los inhibidores selectivos de la recaptación de serotonina (ISRS) han mostrado ser tan eficaces como los antidepresivos tricíclicos y poseer menos efectos secundarios que dichos fármacos. Además, su esquema es más sencillo, ya que generalmente la dosis terapéutica es la misma dosis inicial y puede administrarse en una sola toma diaria,
La literatura médica ha registrado a partir de 1993 los efectos que origina la interrupción dei tratamiento con los ISRS, especialmente por parte de pacientes que olvidan tomar la dosis única diaria, cuando van de vacaciones, o durante el fin de semana.
Los pacientes que suspenden la medicación (antidepresivos, estabilizadores del afecto o antipsicóticos) presentan con frecuencia síntomas somáticos y cognoscitivos que, pueden en algunos casos, requerir tratamiento intrahospitalario, como sucede con los IMAOS clásicos. La sintomatología es inespecífica y difiere de los síntomas de abstinencia que se presentan con los hipnóticos, los barbitúricos, las benzodiacepinas y el alcohol.
El análisis de la sintomatología reportada por los médicos a las revistas especializadas ha puesto de presente la existencia de síntomas comunes que configuran un síndrome que en la Inglesa se ha denominado Discontinuation Syndrome para contraponerlo al Withdrawal Syndrome (síndrome de abstinencia), como se conoció en un principio. Los estudios clínicos han demostrado que la sintomatología no constituye un síndrome de abstinencia ni una recaída de la enfermedad depresiva.
La traducción al español del Discontinuation Syndrome presenta algunos inconvenientes. Se ha discutido si se debe llamar Síndrome de Descontinuación, Síndrome de Retiro o Síndrome de Interrupción.
He escogido el término Interrupción, porque creo que incluye los elementos etiológicos del síndrome. El Pequeño Larousse Ilustrado(1) define interrupción, del latín inferrumpere, como "la suspensión o ruptura del curso de sucesión de los acontecimientos o del nexo causal que los determina".
En el presente trabajo se ha hecho una revisión del Medline y una revisión manual cruzada de los artículos obtenidos del Medline para identificar los elementos clínicos, etiológicos, epidemiológicos y terapéuticos del Síndrome de Interrupción de los ISRS (SDI).
ASPECTOS HISTÓRICOS.
Malcolm Lader(2) describió el "Síndrome de Interrupción de las Benzodiacepinas", como "un síndrome de aparición, duración y terminación previsibles, que incluye síntomas somáticos y psicológicos que el paciente no había presentado anteriormente", definición que permitió diferenciar los síntomas de interrupción, de los síntomas de una recaída clínica.
El primer caso de síndrome de interrupción de antidepresivos fue descrito por Andersen y Kristiansen(3) con la imipramina, pero fueron Dilsalvery sus colaboradores(4) quienes propusieron las cinco categorías de síntomas del síndrome de interrupción de los antidepresivos tricíclicos:
-
Síntomas somáticos asociados a la ansiedad, tales como anorexia, náuseas, vómito, diarrea, sudoración, cefalea, astenia y escalofríos.
-
Alteraciones del sueño como insomnio, somnolencia diurna y pesadillas.
-
Trastornos del movimiento como acatisia y parkinsonismo.
-
Agitación psicomotriz: hipomanía, manía, delirium o ataques de pánico.
-
Arritmias cardíacas.
Seis años más tarde Halle y Dilsalver(5) describieron el síndrome de interrupción de los Inhibidores de la mono ammo-oxidasa (IMAOS) conformado por pensamiento desorganizado y delirante, depresión, déficit cognoscitivo, hipomanía o manía, agresividad, irritabilidad, agitación psicomotriz, mioclonías e insomnio.
Son escasos los reportes de síndrome de interrupción de los antidepresivos tricíclicos y los IMAOS a pesar de haber sido utilizados en las décadas de los setenta y los ochenta como principal alternativa psicofarmacológica. Al parecer, el esquema terapéutico de los antidepresivos tricíclicos, en donde la dosis inicial debe ser ajustada periódicamente hasta alcanzar la dosis terapéutica, así como la reducción paulatina de la dosis al terminar el tratamiento, impidió que los pacientes experimentaran los síntomas de interrupción. En cuanto a ios IMAOS su supuesta toxicidad hepática disminuyó su prescripción y la restringió para casos específicos.
Los ISRS hicieron su aparición hacia finales de la década de los ochenta pero es solamente en 1993, cuando D'Arcy(6) describe los primeros síntomas relacionados con la interrupción de la paroxetina.
El hecho de no haber sido publicados síntomas de interrupción durante los seis años que transcurrieron desde la aparición de la fluoxetina en 1987 y la primera comunicación sobre el síndrome de interrupción hecha por D'Arcy, parece deberse a que coincidencialmente los primeros antidepresivos inhibidores selectivos de la recaptación de serotonina que salieron al mercado (fluoxetina, fluvoxamma, sertralina) poseen un vida media más larga que la paroxetina.
ASPECTOS CLÍNICOS.
Los síntomas del "Síndrome de Interrupción de los ISRS (SID)" son similares a los descritos por Disalver(4) para los antidepresivos tricíclicos, excepto por la ausencia de los trastornos del movimiento y las arritmias cardíacas. Sin embargo, Stoukides(7) ha descrito un caso de distonía muscular con fluoxetina que mejoró con la administración de difenhidramina. Domínguez y Goodnick(8) consideran que los síntomas son parecidos a los descritos por Malcolm en la interrupción de las benzodiacepinas.
Lejoyeux(9) y Schatzberg(10) consideran que e! SID de los ISRS tienen las siguientes características:
-
Es un síndrome no atribuible a otras causas como una recaída clínica a un síndrome de abstinencia.
-
Aparición abrupta, durante la primera semana, cuando el tratamiento ha sido interrumpido por el paciente por dificultades en la aceptación del tratamiento (compliance) o porque ha olvidado tomar una dosis (vacaciones, fin de semana) y con menor frecuencia por disminuir las dosis al terminar el tratamiento antidepresivo.
-
Los síntomas aparecen hacia el quinto día de haberse interrumpido la medicación(11).
-
La sintomatología dura generalmente dos semanas, al cabo de las cuales desaparece en forma espontánea. En el meta-análisis realizado por Coupland(12) en 171 pacientes que fueron supervisados médicamente, los síntomas persistieron en promedio durante 11.8 días, con una duración máxima de 21 días.
-
Los síntomas desaparecen rápidamente en las primeras cuarenta y ocho horas, al reiniciar el fármaco antidepresivo o al utilizar otro similar. Keuthen(13) fue el primero en observar que los síntomas desaparecían rápidamente al utilizar otro fármaco, cuando administró a su paciente fluoxetina en lugar de paroxetina.
-
Su incidencia es mínima cuando se reduce lenta y gradualmente la dosis del ISRS o cuando se utilizan ISRS de vida media larga, como la fluoxetina.
Los síntomas del SID de los ISRS han sido descritos por diferentes autores (Tabla 1). La frecuencia con que los diferentes fármacos los originan, de acuerdo con el meta-análisis de Coupland(12) se incluyen entre paréntesis.

Síntomas orgánicos:
-
Alteraciones del equilibrio: mareo, vértigo y ataxia, (paroxetina 16%, fluvoxamina 9.3%, sertralina 2.2%)
-
Síntomas gastrointestinales: náuseas y vómitos, (clomipramina 15.4%, paroxetina 6%)
-
Síntomas que simulan resfriado o gripa: fatiga, letargía, mialgias y escalofríos, (paroxetina 12%)
-
Síntomas sensoriales: parestesias, tipo quemadura o sensación de corrientazos a nivel de la nuca o la cabeza; sensación de "estar embotado" o "estar borracho", sensación de zumbidos en la cabeza, (clomipramina 30.8%, paroxetina 12%)
-
Alteraciones del sueño: insomnio, sueños vividos o pesadillas, (clomipramina 15.4%)
B. Síntomas psicológicos:
Ansiedad, agitación psicomotriz, crisis de llanto, irritabilidad, hiperactividad, despersonalización, dificultad para la concentración, déficit en la memoria reciente, disminución del tono afectivo y confusión mental.
Price(16), en un análisis post-mercadeo en el Reino Unido, al revisar los reportes espontáneos de 271 pacientes que recibieron fluoxetina, fluvoxamina, paroxetina o sertralina, encontró que los cinco síntomas más frecuentes son: mareos, parestesias, temblores, náuseas y palpitaciones. Síntomas que fueron más frecuentes en pacientes que utilizaron la paroxetina y se presentaron con menor frecuencia en quienes utilizaron fluoxetina.
Sus hallazgos coinciden con los obtenidos por Coupland (12) en el metanálisis retrospectivo de 352 pacientes, quienes reportaron como síntomas más frecuentes mareos, parestesias, letargia y náuseas y en menor frecuencia sueños vividos, insomnio y cefalea.
Szabadi(17), Bloch y colab(18) y Haddad(19) han reportado casos de pacientes que han presentado conductas agresivas como pensamientos suicidas u homicidas. Además, uno de los pacientes realizó hurtos en supermercados, conducta cuya etiología no se ha dilucidado, pero que al parecer se trata de una simple coincidencia (Tabla 1).
ASPECTOS EPIDEMIOLÓGICOS
Existe subregistro y no se conoce la incidencia de los síntomas de interrupción de los ISRS porque los síntomas son generalmente leves y desaparecen espontáneamente o al reiniciar la medicación. Generalmente los pacientes no comunican a sus médicos la sintomatología y los médicos no están alertas sobre la aparición del síndrome, lo cual origina el subregistro estadístico.
El médico al desconocer la presentación del SID puede confundir sus síntomas con ia iniciación de una recaída clínica y reiniciar el tratamiento antidepresivo con el mismo fármaco o con otro, con lo cual la sintomatología desaparece. Tanto el médico como el paciente creerán que se trató de una recaída del cuadro depresivo cuando en realidad se trataba de un SID.
Por otro lado, los psiquiatras reconocen los síntomas del síndrome pero no los reportan a los entes adecuados o a las revistas médicas, como lo comprobaron Gillespie y su grupo de colaboradores(20) en una investigación que presentó en el X Congreso Mundial de Psiquiatría en Madrid.
Young y Currie(21) en una encuesta dirigida a psiquiatras y médicos generales del Reino Unido, encontraron que el 66% de los psiquiatras y el 42% de los médicos generales que diligenciaron la encuesta habían tratado pacientes con SID por ISRS, y consideraron que su incidencia era mayor que la presentada por la descontinuación de los tratamientos con antidepresivos tricíclicos o con IIMAOS.
Price y cols.(16) han tenido en cuenta los datos del Committee on Safety of Medications del Reino Unido y han calculado la incidencia de las reacciones de interrupción de tos ISRS por millón de prescripciones, para cada uno de los cuatro fármacos disponibles en esa época en el mercado del Reino Unido:
Paroxetina 300 por millón de prescripciones
SBTtralina 30 por millón de prescripciones
FiuVOXamina 30 por millón de prescripciones
FlUOXetina 2 por millón de prescripciones
Black y cols.(11) prescribieron fluvoxamina a 14 pacientes con pánico, sin que reportaran efectos secundarios indeseables, pero presentaron síntomas de interrupción al disminuir las dosis, al cabo de 8 meses de terapia (Con dosis de 300 mgrs diarios). Los síntomas fueron tan intensos que 5 de los 14 pacientes debieron faltar a su trabajo y en 12 de los 14 pacientes se presentó mareo, incoordinación, cefalea, nauseas e irritabilidad, en las primeras 24 horas.
Fava y cols.(22), Barr y cols.(23), Oehrberg y cols.(24), Pacheco y cols.(25) han reportado una frecuencia mayor del SID de ISRS cuando se interrumpe el tratamiento con paroxetina, observaciones concordantes con los resultados obtenidos por Haddad(19) quien al revisar los reportes que los médicos australianos hicieron al Australian Adverse Drug Reactions Advisory Committee en donde encontró 22 reportes asociados a paroxetina, 7 a sertralina y 3 a fluoxetina. En la revisión del Medline y el Psychlist hasta octubre de 1996 encontró 47 casos, 30 asociados a paroxetina, 10 a sertralina y 7 a fluoxetina.
La sintomatología que simula un resfriado se presenta con mayor frecuencia en pacientes que reciben paroxetina(26).
Se han informado síntomas de interrupción con sertralina(22,27,28), citalopram(29) y la venlafaxina(30,31). Zajecka y colb(14) sugieren que los médicos y psiquiatras debemos estar alerta con los nuevos antidepresivos como el nefazodone y la mirtazapina, de los cuales aún no hay reportes de producción de síntomas de interrupción.
Estudios multicéntricos.
Hasta el momento sólo existe un estudio multicéntrico que tenga en cuenta los diferentes fármacos ISRS y cumpla con el rigor investigativo. Se trata del trabajo desarrollado por Blogren y su grupo, presentado en el 150 Congreso de la Asociación Americana de Psiquiatría, en San Diego, en 1997.(32,33)
Es un estudio multicéntrico, controlado, paralelo, doble ciego, donde los autores compararon la incidencia de los síntomas de interrupción, al suspender durante una semana el fármaco y reemplazarlo por placebo, en 242 pacientes con tratamiento antidepresivo estables (promedio de 11 meses de estabilidad terapéutica). Los pacientes recibían fluoxetina (N=81, dosis 20-60 mgrs diarios), sertralina (N = 79, dosis 50-200 mgrs. efe) y paroxetina (N=82, dosis 20-60 mgrb diarios). Los pacientes reportaron espontáneamente los síntomas, y además debían responder al cuestionario Discontinuation Emergent Signs and Symptoms (DESS), una escala de 43 items que ha mostrado ser específica para medir los síntomas asociados al SID. Además se les aplicó las escalas de Montgomery-Asberg para la depresión (MADRS) y de Hamilton-D.
Los síntomas que con mayor frecuencia reportaron los pacientes en forma espontánea fueron nauseas, mareos, insomnio y nerviosismo. Su incidencia a nivel espontáneo y a nivel de la escala DESS fueron menores para la fluoxetina en relación con la sertralina (p<0.001) y con la paroxetina (p<0.001).
Antes de la sustitución por el placebo los puntajes de la escala de Hamilton-D fueron similares en cada grupo, pero después de la administración del placebo se incrementaron los puntajes en el grupo de la sertralina (p<0.001) y la paroxetina (p<0.001), indicando un deterioro en su estado afectivo, el cual no se encontró en los pacientes que recibían fluoxetina. Similares resultados se obtuvieron con la escala MADRS.
ASPECTOS ETIOLÓGICOS.
Los estudios de investigación sobre la etiología de los síntomas de interrupción se han concentrado en dos aspectos: el perfil farmacocinético del fármaco (vida media, metabolito activo y acción sobre los receptores) y en la acción a nivel de la neurona post-sináptica, donde se produciría el fenómeno de plasticidad neuronal.
Perfil farmacocinético del fármaco. Price y Waller (16) sugieren que los síntomas de interrupción están relacionados inversamente con la capacidad del fármaco para inhibir la recaptación de serotonina, razón por la cual la paroxetina es el que produce mayor sintomatología (tabla 2).
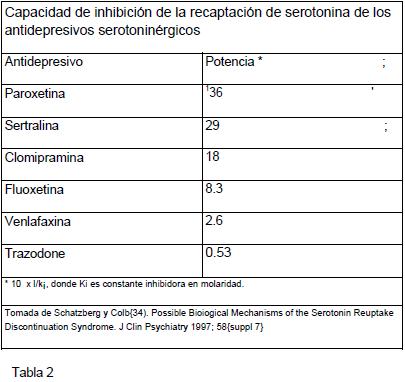
Los síntomas gastrointestinales, los trastornos del sueño, el parkinsonismo, la acatisia y la manía paradójica, ocurren también al interrumpir los antidepresivos tricíclicos. Dilsalver y cols.(4) sugieren que se presentan por un fenómeno de rebote, posterior al bloqueo colinérgico, en tanto que el parkinsonismo y la acatisia serían debidos al desequilibrio de la relación acetilcolina/dopamina. El incremento de la biodisponibilidad de acetilcolina puede activar el sistema límbico y originar el cuadro maníaco.
Los efectos colinérgicos son producidos exclusivamente por la clomipramina y la paroxetina porque los otros ISRS no poseen acción colinérgica.
Los síntomas restantes parecen ser debidos a la disminución de la biodisponibilidad de la serotonina a nivel de la sinapsis en la fase de down-regulation de los receptores post-sinápticos, originada por el ISRS. A este nivel resulta importante la vida media del fármaco, razón por la cual la fluoxetina al poseer una vida media larga y un metabolito activo, la norfluoxetina, que contribuye a prolongar la vida media, produce menos síntomas de interrupción, al no disminuir en forma brusca la disponibilidad de serotonina a nivel sináptico.
Los fármacos que poseen una vida media más corta (paroxetina, fluvoxamina y sertralina en su orden) tienden más a asociarse al SID. (Tabla 3)

Los mareos y las parestesias son debidos a la disminución de la concentración de serotonina, neurotrasmisor responsable de la coordinación de las funciones sensoriales y autonómicas con las funciones motrices gruesas y los músculos faciales. Las parestesias referidas por los pacientes con SID son más frecuentes en cara, nuca y tronco, y raramente se presentan en las extremidades. Además, se incrementan con el mínimo movimiento.
Coupland y su grupo(12) sugieren que el mareo, las nauseas, la letargia y los síntomas visuales simulan el cuadro clínico de cínetosis o "enfermedad del movimiento" (motion sickness), síndrome que puede ser suspendido en animales de experimentación con la administración de antagonistas de los receptores 5HT1 a.
El tratamiento con ISRS desensibiliza los receptores 5HT1 a de los núcleos del rafe, al aumentar la biodisponibilidad de serotonina. Al descontinuar el tratamiento, los receptores 5HT1 a son excitados nuevamente y originan los síntomas de nauseas, mareo y letargia.
La serotonina es considerada como un neuromodulador de otros neurotrasmisores. Zajecka y cols.(14) consideran que el estado hiposerotoninérgico que se produce al suspender la medicación actuaría directa o indirectamente sobre otros neurotrasmisores (noradrenalina, dopamina, acetilcolina y gaba) produciéndose los diferentes síntomas del SID.
Se ha invocado la acción de otros neurotrasmisores en la etiología de los síntomas de interrupción. Louie y cols.(27) consideran que los síntomas de interrupción que se presentan por el uso de sertralina pueden obedecer a la ligazón de la molécula a los receptores opioides sigma; en tanto que Lejoyeux y su grupo de investigadores(26) sugieren síntomas extrapiramidales que se presentan por fluoxetina pueden ser debidos a inhibición dopaminérgica.
Plasticidad Neuronal. La acción antidepresiva de los psicofármacos se debe a la inducción de plasticidad en la neurona, definida esta, como el proceso por el cual el funcionamiento neuronal es alterado por un estímulo previo.(36)
Los antidepresivos elevan en forma aguda los niveles de serotonina o noradrenalina a nivel de la sinapsis pero su efecto terapéutico aparece al cabo de varias semanas (período de latencia), cuando se han logrado cambios a nivel de la densidad y función de los receptores: down-regulation de los beta-receptores y receptores 5-HT2 post-sinápticos y aumento de la guanil -5- imidodifosfato (GPP-NH-P) de la membrana neuronal.
A nivel intraneuronal se produce un fenómeno de adaptación de las vías de transducción intracelular por acción de la adenilciclasa y las proteínas G y la traslocación de las protein kinasas dependientes del AMPc.(36,37) Es decir, los antidepresivos producen plasticidad neuronal a largo plazo.
La descontinuación abrupta del antidepresivo suspendería la estimulación (noradrenérgica o serotoninérgica) sobre los receptores post-sinápticos y dejaría de estimular los cambios adaptativos que ha logrado la neurona (plasticidad neuronal), originando los síntomas del síndrome de interrupción.
Al reiniciarse la administración del antidepresivo se estimularían de nuevo los receptores post-sinápticos y se reestablecerían en forma rápida, los mecanismos de transducción mira-celular.
Si no se restablece la terapia antidepresiva, los síntomas de interrupción continúan durante algunas semanas, al cabo de las cuales desaparecen, pero los cambios estructurales a nivel neuronal (plasticidad neuronal) pueden persistir indefinidamente.
El paciente dejará de experimentar el síndrome de interrupción y podrá continuar con la mejoría clínica obtenida por el antidepresivo.
Infortunadamente, aún no estamos en capacidad de medir la eficacia de los cambios de plasticidad neuronal para poderle afirmar que dichos cambios estructurales han sido suficientes para evitar la recaída o la aparición de una nueva crisis depresiva.
FACTORES DE RIESGO.
Los siguientes son factores de riesgo para la presentación del Síndrome de Interrupción:
-
Uso de un ISRS de vida media corta, o que no posea un metabolito activo o cuyo metabolismo no sea lineal.
-
Empleo de un antidepresivo que posea acción sobre los receptores muscarínicos (clomipramina, paroxetina).
-
Duración del tratamiento mayor a tres meses.(12,22)
-
Pacientes con dificultades para aceptar el tratamiento (compliance), especialmente cuando el tratamiento antidepresivo no ha sido efectivo.(34)
-
Pacientes que presentaron ansiedad, como efecto secundario al iniciar el tratamiento, La ansiedad puede disminuir la aceptación de la psicofarmacoterapia prolongada.(34)
-
Utilizar los ISRS en niños y adolescentes. (26,38)
DIAGNÓSTICO DIFERENCIAL
Las características clínicas del SID exigen un diagnóstico diferencial con los siguientes cuadros clínicos:
-
Efectos secundarios: Generalmente los efectos secundarios se presentan durante la primera semana de administración del fármaco y desaparecen o se hace tolerancia a los mismos en las semanas siguientes.
-
Síndrome de abstinencia: se presenta al suspender bruscamente la administración de fármacos como las benzodiacepinas o el consumo de sustancias como el alcohol o la cocaína. Está conformado por síntomas de origen simpático como sudoración, taquicardia, agitación psicomotriz, midriasis, dificultad respiratoria, en ocasiones se pueden producir convulsiones, colapso cardiovascular, coma o muerte.
-
Síndrome serotoninérgíco: caracterizado por confusión mental, hipomanía, inquietud, mioclonias, hiperreflexia, sudoración, temblor, diarrea e incoordinación psicomotriz, que puede progresar hasta el coma.(15)
-
Recaída del episodio depresivo: donde las alteraciones en el humor, el apetito, el sueño y la vivencia depresiva son más intensas y requieren el ajuste de las dosis antidepresivas o el adicionar un nuevo fármaco.
Los síntomas indeseables de los ISRS que se presentan con más frecuencia son náuseas, cefalea, ansiedad, trastornos del sueño, disfunción sexual y sudoración.
Algunos síntomas se presentan exclusivamente con un fármaco; por ejemplo la sertralina puede producir deposiciones blandas y la paroxetina crisis de hipomanía.
La aparición de los efectos secundarios puede hacer que el paciente suspenda el tratamiento durante el primer mes, período en el cual no se presentan los síntomas de interrupción.
Los efectos secundarios indeseables desaparecen al disminuir las dosis o al suspender la medicación.
La sintomatología del síndrome de abstinencia sugiere el compromiso del sistema gabaérgico sobre el cual los ISRS no tienen acción farmacológica.
Está comprobado que los ISRS no producen dependencia, tolerancia ni síndrome de abstinencia.
Sternbach(39) sugiere que el síndrome serotoninérgico se produce por compromiso de los auto-receptores 5HT1a del tallo cerebral que origina un aumento en la biodisponibilidad de la serotonina.
Los síntomas de la recaída no mejoran inmediatamente, como sí lo hacen los del SID al reiniciar la medicación.
ASPECTOS TERAPÉUTICOS
La presentación de los síntomas de interrupción aumenta en forma considerable los costos del tratamiento médico. El paciente es sometido a una serie de exámenes clínicos y paraclínicos para precisar la etiología de los síntomas, que como se ha descrito anteriormente, no representan peligro para su vida y desaparecen espontáneamente.
Los síntomas de descontinuación impiden que el paciente acepte en forma adecuada el tratamiento psicofarmacológico para sus crisis depresivas, con lo cual aumenta el riesgo que su cuadro clínico se cronifique.
La eficacia del fármaco es el factor más importante en la aceptación del tratamiento. El paciente suspende la medicación cuando cree que el tratamiento no es eficaz y, entonces al suspenderlo, experimenta los síntomas de interrupción.
Al mejorar del cuadro depresivo un buen porcentaje de pacientes suspende la medicación por el miedo a "ser dependientes" del fármaco antidepresivo.
Jean Fawcett(40) propone los siguientes items relacionados con la falta de aceptación del tratamiento por parte del paciente:
-
Resistencia a tomar la medicación por la aparición de sentimientos de culpa.
-
El médico no brinda seguridad y esperanza en el tratamiento.
-
Falta de continuidad en el tratamiento, que incluye controles médicos periódicos.
-
Complejidad del esquema terapéutico.
-
Alto costo de los psicofármacos.
-
Cronicidad de la sintomatología.
-
Comorbilidad: presencia de ataques de pánico, ansiedad severa, abuso de alcohol o sustancias adictivas.
-
Inconformidad con la respuesta terapéutica.
Para hacer frente a estos hechos se hace necesario que el médico diseñe una estrategia de psicoeducación para el paciente y la familia que ayude a impedir la suspensión de la medicación por parte del paciente y la aparición del síndrome de interrupción.
Desde el punto de vista del médico se hace necesario que el profesional tenga en cuenta la posibilidad de aparición de la sintomatología y ante la sospecha, pregunte a su paciente si interrumpió la medicación. Si la respuesta es positiva debe reiniciar la medicación.
Los médicos pediatras deberán, en su anamnesis, preguntar a la madre si ha recibido ISRS durante el embarazo y si han suspendido la medicación.
Si la aceptación del tratamiento por parte del paciente es deficiente y se sospecha que en un futuro no muy lejano, intentará suspender nuevamente la medicación, se debe tener como alternativa terapéutica la prescripción de ISRS de vida media larga, como la fluoxetina.
La fluoxetina y su metabolito la norfluoxetina pueden proteger al paciente por su vida media larga, por analogía como lo hace el clordiazepóxido que produce menos síntomas de abstinencia que las benzodiacepinas de vida media corta como el lorazepam y el alprazolam.(8)
Una estrategia eficiente para prevenir la aparición del SID debe incluir los siguientes aspectos:
-
Proporcionar elementos de educación al paciente sobre la enfermedad depresiva y su tratamiento.
-
Disminuir la dosis del antidepresivo en forma gradual, especialmente si se trata de un antidepresivo de vida media corta como paroxetina, fluvoxamina, venlafaxina o sertralina.
Rosembaum y Zajecka(41) recomiendan el esquema terapéutico descrito en la tabla 4.
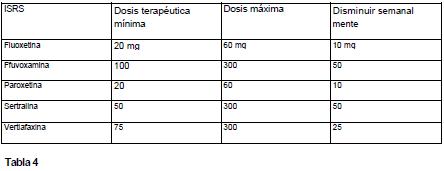
La aparición del síndrome de interrupción es un hecho clínico. Su presentación causa molestias al paciente y puede interferir en el tratamiento de su crisis depresiva o ansiosa y aumentar en forma importante los costos del tratamiento.
La etiología del síndrome no está dilucidada completamente. Es necesario realizar estudios controlados y comparativos que permitan evaluar variables como el diagnóstico clínico, la duración y eficacia del tratamiento, la forma de disminuir el fármaco y la utilización de medicaciones concomitantes.
REFERENCIAS
Pequeño Larousse Ilustrado. Ramón García - Pelayoy Gross. Editado por Printer Colombiana. Bogotá, 1991. [ Links ]
Lader M. Benzodiacepine with drawal states. ln: Trimble MR, ed. Benzodiacepines Divided. New York, NY. John Willey & sons. 1983:17-31. [ Links ]
Andersen H, Kristiansen ES. Tofranil treatment of endogenous depression. Acta Psychiatr Scand 1959; 34: 387-397. [ Links ]
Dilsalver SC, Greden JF, Snider RM. Anti depressant with drawal syndromes: phenomenology and physiopathology. Int Clin Psychopharmacol 1987; 2:1-19. [ Links ]
Halle MT, Dilsalver SC. Tranylcipromine with drawal phenomena. J Psychiatry Neurosci 1993; 18: 49-50. [ Links ]
D'arcy PF. Dystonia and with drawal symptoms with paroxetine (letter). Int Pharm J 1993; 7: 140. [ Links ]
Stoukides JA, Stoukides CA. Extrapyramidal symptoms upon discontinuation of fluoxetine (letter). Am J Psychiatry 1991; 148: 1263. [ Links ]
Domínguez RA, Goodnick PJ. Adverse events after the abrupt discontinuation of paroxetine. Pharmacotherapy 1995; 15: 778-780. [ Links ]
Lejoyeux M, Ades J, Mourad I, et al. Antidepressant withdrawal syndrome: recognition, prevention and management. CNS drugs 1996; 4: 278-292. [ Links ]
Schatzberg AF, Haddad P, Kaplan EM, Lejoyeux M, Rosenbaum JF, Young AH, Zajecka J. Serotonine up take inhibitor discontinuation syndrome: ahi pothetical definition. J Clin Psychiatry 1997;58(suppl7): 5-10. [ Links ]
Black DW, Wesner R, Gabel J. The abrupt discontinuation of fluvoxaminein patients with panic disorder. J Clin Psychiatry 1993; 54: 146-149. [ Links ]
Coupland NJ, Bel ICJ, Potokar JP. Serotoninre up take inhibitor with drawal. J Clin Psychopharmacol 1996; 16: 356-362. [ Links ]
Keuthen NJ, Cyr P, Riccliardi JA, et al. Medication with drawal symptoms in obssesive - compulsive disorder patients treated with paroxetine (letter). J Clin Psychopharmacol 1994; 14: 206-207. [ Links ]
Zajecka J, Tracy KA, Mitchell S. Discontinuation symptoms after treatment with serotonin reuptake inhibitors: A literature review. J Clin Psychiatry 1997; 58 (7): 291-297. [ Links ]
Tellez J. Inhibidores selectivos de la recaptación de serotonina. En: Antidepresivos en la práctica médica. Nuevo Milenio Editores. Bogotá, 1998. [ Links ]
Price JS, Waller PC, Wood SM, et al. A comparison of the post-marketing safety of four selective serotonin reuptake inhibitors including the investigation of symptoms ocurring in with drawal. Br J Pharmacol 1996; 42: 757-763. [ Links ]
Szabadi E. Fluvoxamine with drawal syndrome (letter). Br J Psychiatry 1992; 160: 283-284. [ Links ]
Bloch M, Stager SV, Braun AR, et al. Severe psychiatric symptoms associated with paroxetine with drawal (letter). Lancet 1995; 346:57. [ Links ]
Haddad P. Newer antidepressant and the discontinuation syndrome. J Clin Psychiatry 1997; 58 (suppl7): 17-22. [ Links ]
Gillespie C, Wildgust H, Haddad P, et al. SRSIS and with drawal syndrome. In: Proceedings of the 10th World Congress of Psychiatry 1996, august 23-28. Madrid, Spain. Abstract G2389. [ Links ]
Young AH, Currie A. Physicians' knowledge of antidepressant with drawal effects: a survey. J Clin Psychiatry 1997; 58(suppl 7): 28-30. [ Links ]
Fava AGA, Grand S. With drawal syndromes after paroxetina and sertraline discontinuation (letter). J Clin Psychopharmacol 1995; 15: 374-375. [ Links ]
Barr LC, Godman WK, Price LH. Physical symptoms associated with paroxetine discontinuation (letter). Am J Psychiatry 1994; 151: 289. [ Links ]
Oehrberg S, Christiansen PE, Behnke K, et al. Paroxetine in the treatment of panic disorder: a randomized, double-blind, placebo-controlled study. Br J Psychiatry 1995; 167: 374-379. [ Links ]
Pacholo L, Malo P, Aragues E, et al. More cases of paroxetine with drawal syndrome (letter) Br J Psychiatry 1996; 169: 384. [ Links ]
Lejoyeux M, Ades J. Antidepressant discontinuation: A review of the literature. J Clin Psychiatry 1997; 58 (suppl 7): 11-15. [ Links ]
Louie AK, Lannon RA, Aajari LJ. With drawal reactions after sertraline discontinuation (letter). Am J Psychiatry 1994; 151: 450-451. [ Links ]
Kent LSW, Laidlaw JDD. Suspected congenital sertraline dependence. Br J Psychiatry 1995; 167: 412-413. [ Links ]
Young AH, Currie A, Ashton CH. Antidepressant with drawal syndrome (letter). Br J Psychiatry 1997; 170: 288. [ Links ]
X. Rauch SL. O'sullivan RL, Jenicke MA. Open treatment of obssesive - compulsive is order with venlafaxine: a series of 10 cases (letter). J Clin Psychopharmacol 1996; 16:81-84. [ Links ]
Farah A, Laurt T. Possible venlafaxine with drawal syndrome (letter). Am J Psychiatry 1996; 153: 576. [ Links ]
Blomgren SL, Ascroft R, Krebs W, et al. Risk of adverse events and depressive symptoms break through following brief interruption od SSRS therapy. Presented at the 150th Annual Meeting of the American Psychiatric Association. 1997; San Diego, CA. May 20th. Abstract NR 188. [ Links ]
Stokes PE, Holdz A. Fluoxetine tenth anniversary update: the progress continues. Clin Therapeutics 1997; 19 (5); 1135-1250. [ Links ]
Schatzberg AF, Haddad P, Kaplan EM, Lejoyeux M, Rosenbaum JF, Young AH, Zajecka J. Possible biological mechanism of the serotonin reuptake inhibitor discontinuation syndrome. J Clin Psychiatry 1997; 58(suppl 7): 23-27. [ Links ]
Kaplan HI, Sadock BJ. Comprehensive Text book of Psychiatry- 6th edition. Williams & Wilkins (ed). Baltimore, 1995. [ Links ]
Nestler EJ, Dumand RS. Relevance on intra cellular signal trasduction pathways to Psychiatry En: American Psychiatric Press Annual Review Volume 15. American Psychiatric Press Inc. Washington, DC. 1996: 279-308. [ Links ]
Chen J, Rasenick NM. Chronic antidepressant treatment facilitates G protein activation of adenylyl cyclase without altering G protein content. J Pharmacol Exp Ther 1995; 275(1): 509-517. [ Links ]
Puerta G. Antidepresivos en niños y adolescentes. En: Tellez J, Antidepresivos en la práctica médica. Nuevo Milenio Editores, Bogotá, 1998. [ Links ]
Sternbach H. The Serotoninergic Syndrome. Am J Psychitry 1991; 148 (6): 705-713. [ Links ]
Fawcett J. Compliance: definitions and key issues. J Clin Psychiatry 1995; 56(suppl 1): 4-8. [ Links ]
Rosenbaum JF, Zajecka J. Clinical management of antidepressant discontinuation. J Clin Psychiatry 1997; 58 (suppl 7): 37-40. [ Links ]














