Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Colombiana de Psiquiatría
versão impressa ISSN 0034-7450
rev.colomb.psiquiatr. v.29 n.2 Bogotá abr./jun. 2000
EL SPECT EN LA EVALUACIÓN DE LAS DEMENCIAS
SPECT IN EVALUATION OF DEMENTIA
DIANA ISABEL PÁEZ G. Y LUZ MARITZA PABÓN C.*
*Unidad de Medicina Nuclear, Departamento de Medicina Interna, Fundación Clínica Valle Del Lili. Cali, Colombia.
RESUMEN
En los últimos años se ha logrado un gran progreso en el manejo de pacientes con demencia, debido a la implementación y desarrollo de las neuroimágenes, especialmente de los estudios funcionales que permiten obtener información acerca de las propiedades bioquímicas, fisiológicas o eléctricas cerebrales. Su principal aplicación es colaborar al diagnostico diferencial de los pacientes con alteraciones cognitivas.
Dentro del grupo de estudios funcionales se encuentra el SPECT cerebral de perfusión, que permite evaluar el flujo sanguíneo cerebral regional, mediante la utilización de trazadores radioactivos y mostrar de manera indirecta la actividad metabólica y sus alteraciones. Esta técnica evidencia los rasgos de los diferentes tipos de demencia: Alzheimer, alteraciones vasculares, frontotemporales, asociadas a SIDA y otras. Una ventaja adicional del SPECT es su amplia disponibilidad y su costo razonable.
Palabras Clave: Demencia; Imágenes Diagnósticas; Procesamiento de Imágenes Digitales.
ABSTRACT
Recent years have witnessed progress in management of patients with dementia, thanks to implementation and development of brain imaging, especially funcional srudies to elucídate biochemical physiological and electrical properties. Differential diagnosis of cognitive disturbances will have a broader basis.
Among functional studies, brain perfusión SPECT allows assessment of regional blood supply, through radiactive tracers which indirectly show metabolic activity and its alteration. This technique differentiates fearures of several types of dementia: Alzheimer, Vascular and fronto-temporal lesions, AIDS and Others. Additional ad vantages of SPECT are availability and reasonable cost.
Key Words: Dementia; Diagnostic Imagine; Computer Assisted Image Processing.
INTRODUCCIÓN
Cuando enfrentamos al diagnóstico de "demencia", imaginamos un panorama sombrío para quien la padece. Sin embargo, el desarrollo de técnicas que permiten un diagnóstico etiológico ha abierto una esperanza para los enfermos con patologías reversibles e incluso no reversibles, que se pueden beneficiar de un diagnóstico precoz y una terapia adecuada.
Para realizar un diagnóstico apropiado de demencia es necesario tener cuatro fuentes de datos, a saber: historia clínica completa, examen físico y neurológico detallado, evaluación neuropsicológica y técnicas de neuroimágen.
Las técnicas de neuroimágen que aportan información susbtancial son dos:
- Las que evalúan las alteraciones estructurales, como la Tomografía Axial Computarizada (TAC), o la Resonancia Nuclear Magnética (RMN).
- Las que evalúan posibles alteraciones funcionales, como la Tomografía por Emisión de Fotón Único (SPECT), la Tomografía por Emisión de Positrones (PET) y la Resonancia Magnética Nuclear Funcional y la Resonancia Magnética Nuclear con Espectroscopia.
LAS TÉCNICAS ESTRUCTURALES
Las técnicas estructurales pueden detectar anomalías como dilataciones ventriculares, atrofia cerebral o alteraciones vasculares. Su verdadera utilidad en la evaluación de pacientes con sospecha clínica de demencia radica en la evaluación de posibles diagnósticos diferenciales y la exclusión de otras patologías orgánicas.
LAS TÉCNICAS FUNCIONALES
Los estudios funcionales, de aplicación más reciente en neuropsiquia-tría, han significado un avance, ya que gracias a ellos se puede evaluar el flujo sanguíneo cerebral regional (FSCr), el metabolismo cerebral o los sistemas de neuroreceptores. Por sus características los estudios funcionales pueden detectar cambios antes que el déficit cognitivo sea evidente o se produzcan alteraciones visibles con las técnicas estructurales de imagen.
El SPECT y el PET, que pertenecen al área de Medicina Nuclear, permiten la evaluación tridimensional de la distribución y concentración de un trazador radioactivo (radio-trazador), cuya captación a nivel del tejido cerebral refleja la perfusión regional. Por utilizar moléculas biológicamente activas, se pueden lograr imágenes de la actividad cerebral (1-3).
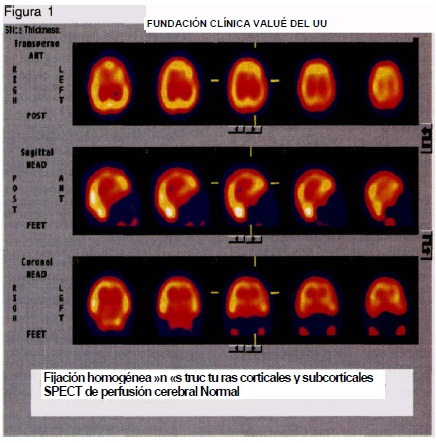
La diferencia entre el SPECT y el PET, es que este último utiliza trazadores como Oxígeno 15, Carbono 11 y Nitrógeno 13, elementos que marcan moléculas orgánicas como la glucosa o el agua y por tanto facilitan la evaluación del metabolismo in vivo, sin emplear marcadores que modifiquen su metabolismo. El C, O y 13N son producidos a partir de un ciclotrón y tienen una vida media corta (menor de 20 minutos)/ también se pueden usar isótopos como el Flúor 18, Galio 68 o Rubidio 82, con vida media un poco mayor (1 a 2 horas). Desafortunadamente los altos costos de estos trazadores y la instrumentación requerida, hacen al PET una técnica poco disponible a nivel mundial. Las principales diferencias entre estos dos examenes se presentan en la Tabla 1.
ASPECTOS TÉCNICOS DEL SPECT CEREBRAL
El SPECT es una técnica de imágenes tomográficas, que a diferencia del TAC no es el equipo el que emite la radiación (transmisión), sino el paciente (emisión) a quien se le ha administrado el material radioactivo (isótopo) por vía parenteral, oral o por inhalación.
El isótopo está ligado a un compuesto (trazador), formando el complejo conocido como radiotra-zador, que se incorpora en el metabolismo del órgano o sistema objeto de estudio. A partir de allí inicia la emisión de radiación en forma de rayos gamma, que son captadas por las gammacámaras y convertidas en una señal eléctrica cuyo registro queda almacenado en un computador provisto de un programa especial para su procesamiento, y su análisis cualitativo o cuantitativo.
Para la realización del SPECT cerebral se han utilizado diversos compuestos: Xenón 133, Xenón 127, Kriptón 85, Talio 201, Yodo 123 yodoisopropil anfetamina (IMP), Talio 201 dietilditocarbamato y más recientemente trazadores marcados con tecnecio 99 dímero de etil cisterna (ECD) descrito por Walo-vitch en 1988, hexametilpropilenaminooxima (HMPAO) descrito por Nowotnik en 1985(4), isonitrilos y tetrofosmin. Cada trazador tiene propiedades especiales y diferentes mecanismos de acción biológica que evalúan diversos aspectos funcionales: FSCr (flujo sanguíneo cerebral regional)(5-7) presencia y viabilidad de algunos tumores primarios o metastásicos (8), disponibilidad de neurorreceptores y utilización de neurotrasmisores(9-12).
Para el estudio de las demencias se utilizan fármacos capaces de atravesar la barrera hematoencefálica (BHE) intacta y que evalúan el FSCr como el 133Xe, el 123I-IMP, el 2Ü1T1 DDC, el HMPAO y el ECD, los dos últimos de uso mas generalizado por las ventajas que ofrece la marcación con tecnecio 99m: disponibilidad, bajo costo, vida media corta (6 horas), baja dosis de radiación, mejor calidad de imagen(1-7). Tabla 2.
En la actualidad se considera que el HMPAO es el fármaco de elección para la realización del SPECT de perfusión porque se puede marcar con Tecnecio, presenta una rápida y elevada eficiencia de extracción cerebral (70-80% en el primer paso), tiene una distribución cortical proporcional al FSCr, su aclara-miento cerebral es lento (menor a 1% en una hora) y no presenta redistribución intracelular temprana ni tardía; su desventaja es que puede infravalorar el FSCr en el rango de flujos altos.
Una vez atraviesa la barrera hematoencefálica, el radiofármaco se fija en forma directamente proporcional al FSCr, que a su vez depende de la actividad neuronal, mostrando de manera indirecta la actividad metabólica y sus alteraciones. Las imágenes definen patrones que están relacionados con las características neurofisiológicas y sus variaciones pueden evidenciar rasgos de algún tipo particular de demencia. Por ejemplo, en la Enfermedad de Alzheimer se presenta una hipo-perfusión generalmente bilateral de las regiones de asociación temporo-parietales con o sin compromiso frontal; en la demencia vascular tipo multiinfarto se aprecian defectos múltiples irregularmente distribuidos y en la fronto-temporal existe compromiso casi exclusivo de la corteza anterior. Se ha demostrado que los hallazgos del SPECT tienen una buena correlación con los estudios con PET en cuanto a las alteraciones de perfusión y metabolismo(7-13-15).
Para la interpretación de los estudios se requiere tener en cuenta múltiples aspectos: los diferentes patrones de captación considerados normales, la fijación homogénea o heterogénea del material radioactivo y la ausencia de movimiento. Todos los estudios se deben interpretar de acuerdo con el cuadro clínico/ los hallazgos del examen físico y neurológico y los estudios morfológicos (ver figura 1 al final del artículo).
Los pacientes con demencias generalmente presentan en el SPECT de perfusión áreas de disminución en la captación del radiofármaco, alteraciones que varían entre personas con el mismo diagnóstico, dependiendo del tiempo de evolución de la enfermedad o la presencia de patologías asociadas. En ellos la captación de los ganglios básales/ el tálamo/ la corteza sensitivo/motora/ el lóbulo occipital y el cerebelo es normal/ excepto en los pacientes con demencia relacionada con Enfermedad de Parkinson o asociada al Síndrome de Inmunodeficien-cia Adquirida.
La evidencia médica confirma que el SPECT cerebral es confiable en el diagnóstico diferencial de pacientes con demencias moderadas a severas y es capaz de reflejar el tipo y la severidad del deterioro cognitivo asociado con el proceso demencial. Su papel en la evaluación de los casos incipientes de demencia es incierto; para mejorar este aspecto se están desarrollando nuevos métodos como la evaluación de neuro-receptores, la activación cognitiva y la cuantificación(16).
DEMENCIA TIPO ALZHEIMER
En la demencia tipo Alzheimer existe disminución del metabolismo y la perfusión cerebral en los lóbulos parietal y temporal, regiones que muestran las mayores anormalidades neuroquímicas post mortem. Se ha sugerido que los pacientes con compromiso moderado pueden presentar cambios en los lóbulos temporo-parietales y frontal, mientras que los que presentan una mayor alteración pueden involucrar cambios en el lóbulo occipital(17). En los casos leves o atípicos, como se anotó, existen dificultades para establecer el diagnóstico diferencial con otros tipos de demencias, especialmente la vascular (18).
El Oxford Project To Investígate Memory (ÓPTIMA), recomienda el uso del SPECT en combinación con el TAC o la RMN para realizar el diagnóstico de Alzheimer y alcanzar una sensibilidad del 90%. La sensibilidad disminuye al utilizar una sola de las técnicas: para el SPECT es del 88% y una especificidad del 87% <19-20). El diagnóstico definitivo de Enfermedad de Alzheimer sólo se logra por la evidencia hispotatológica (biopsia o post mortem); es por esto que el diagnóstico basado en imágenes y clínica se presenta como probable y posible.
El hallazgo más característico en el SPECT de perfusión cerebral en pacientes con diagnóstico de Alzheimer es el patrón de hipoperfusión: disminución de captación de trazador radioactivo en la región tempero-parietal bilateral. Según Holman y Cois., este patrón predice la presencia de la enfermedad con una seguridad del 82 % (19). Sin embargo, se pueden presentar otros patrones gamagráficos (Tabla 3).
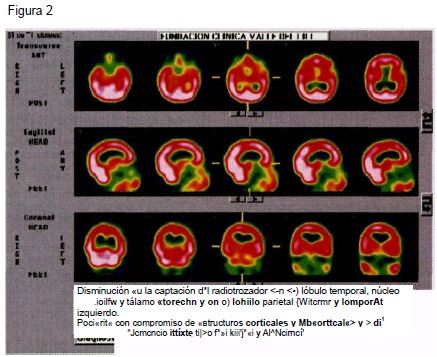
Las áreas con mayor déficit en la captación se relacionan con la disfunción cognitiva dominante. Por ejemplo: la hipoperfusión global del hemisferio izquierdo con alteraciones del lenguaje, la hipoperfusión temporal izquierda con trastornos de memoria, la temporal derecha con alteraciones en la percepción y la praxis. Por lo general, a mayor alteración en el SPECT mayor deterioro clínico (21). (Ver figura 2 al final del artículo).
Las demencias vasculares son la segunda causa del síndrome demencial. Sus principales factores de riesgo son hipertensión arterial no controlada y accidentes cerebro-vasculares. En las demencias vasculares el déficit cognitivo está en concordancia con la extensión y el número de fenómenos cerebrales isquémicos y los signos neurológicos que lo acompañan y con el área cerebral comprometida. Al igual que en otras patologías los estudios funcionales (SPECT) pueden mostrar cambios antes que los morfológicos (TAC, RMN) y la ventaja de la primera es que precisa la causa de la isquemia (embólica o hemodinámica).
La evaluación del riesgo embólico en más sencilla porque aumenta con el grado de estenosis arterial, en tanto que la evaluación del riesgo hemodinámico no esta en relación con el grado de estenosis ipsilateral, sino que depende de la capacidad funcional de la circulación colateral. Por esta razón la evaluación de la capacidad de reserva funcional cerebral, en pacientes con infarto cerebral, es mandatoria para el manejo clínico.
Exámenes como la TAC, la RMN y la angiografía miden el FSC en reposo, pero no evalúan la reserva por la circulación colateral, que puede ser estimada indirectamente, por medio del SPECT combinado con agentes vasodilatadores (dióxido de carbono inhalado, acetazolamida (22) y dipiridamol (23)); sustancias que producen alteración de la autoregulación cerebral por vasodilatación en los vasos de resistencia, generando un incremento en el flujo de las arterias intracraneales y en la captación cortical del trazador radioactivo. La vasodilatación que no se presenta en las arterias con estenosis crea, en las imágenes de perfusión, una diferencia entre la captación de la corteza irrigada por las arterias normales y la irrigada por las arterias comprometidas. Esto se observa en el estudio tomográfico como una variación interhemisférica en la fijación del trazador radioactivo y sugiere compromiso del flujo de reserva y pobre circulación colateral(22).
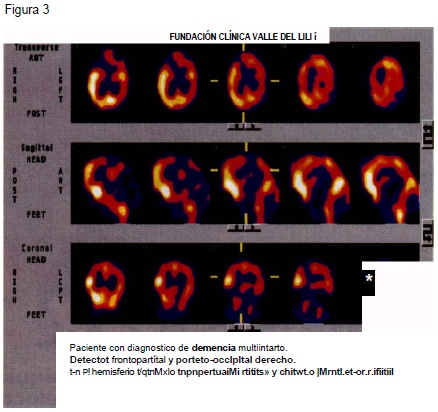
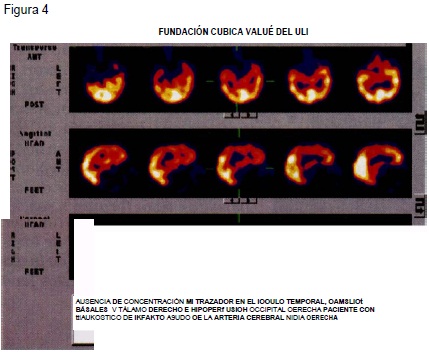
En las demencias de tipo vascular los cambios gamagráficos pueden ser muy variados y dependen del territorio comprometido y de la extensión de las lesiones. Al igual que en otras patologías, los defectos de perfusión están relacionados con el compromiso de las funciones cog-nitivas e intelectuales y se pueden presentar antes que se definan alteraciones morfológicas (Ver figuras 3 y 4 al final del artículo). Los patrones más característicos se describen en la tabla 4.
DEMENCIA RELACIONADA CON SÍNDROME DE INMUNODEFICIENCIA ADQUIRIDA (SIDA)
Los pacientes con síndrome de inmunodeficiencia adquirida pueden presentar diversos procesos que afectan el sistema nervioso central, entre ellas, la encefalopatía subcortical por HIV (complejo demencia-SIDA), cuyo diagnóstico se realiza en ausencia de otro proceso etiológico(17). En 25% de los pacientes con SIDA la demencia se presenta como la primera manifestación de la enfermedad (24).
Los síntomas son característicos del compromiso subcortical que puede involucrar estructuras como los ganglios básales, el tálamo y el tallo cerebral, como sucede en enfermedades como la corea de Huntington, la parálisis general progresiva o el Parkinson. Las características principales de estos pacientes son alteraciones en el humor, la motivación y la vigilia, acompañadas de trastornos de la memoria y del afecto.
Las neuroimágenes ayudan en el diagnóstico de la encefalopatía. Algunos de sus hallazgos son:
- TAC: puede ser normal o mostrar patologías asociadas como neoplá-sias o infecciones.
- RMN: puede evidenciar atrofia cortical, dilatación ventricular, anormalidades en la sustancia blanca, el tálamo y los ganglios básales.
- SPECT: presenta hipoperfusión cerebral focal o múltiple. Los pacientes seropositivos, con o sin síntomas, presentan asimetría meta-bólica en las regiones prefrontal, premotora y ganglios básales. Detecta alteraciones neuroanatómicas en forma temprana e incluso llega a diferenciar los cambios producidos por el virus HIV a nivel cerebral de los causados por el abuso de cocaína (hipoperfusión de las áreas frontales, temporales y parietales). Además, se utiliza para evaluar la respuesta a la terapia con antirretrovirales.
- PET: puede mostrar en forma precoz, hipermetabolismo en los ganglios básales y el tálamo. En los procesos más avanzados hay hipometabolismo de la sustancia gris cortical y subcortical.
Los hallazgos en SIDA se presentan en la tabla 5.
Las demencias frontotemporales son un desorden cortical con degeneración de las capas superficiales de la corteza frontal y temporal anterior, moderada gliosis y micro-vascularización; recientemente ha sido reconocida como una variedad de demencia progresiva de tipo no Alzheimer. Anteriormente se pensaba que correspondía al síndrome o a la demencia tipo Pick. Sin embargo/ hay datos de FSCr y fisiopa-tológicos que sugieren que las demencias frontotemporales forman parte de un síndrome clínico mayor y que, entre otros, incluye: la demencia de lóbulo frontal sin cuerpos de Pick, la atrofia fronte-temporal asociada a gliosis subcor-tical intensa y la atrofia frontal con evidente espongiosis(25). Aunque la etiología es desconocida, en un porcentaje elevado -60% para algunos estudios-se ha observado agregación familiar(26).
Los pacientes presentan alteraciones progresivas de la personalidad y la conducta social con funciones motoras preservadas. Los hallazgos en los estudios morfológicos de neuroimágenes (TAC, RMN) pueden ser normales o presentar atrofia cerebral frontal o generalizada. Los estudios funcionales (SPECT) muestran un patrón que corresponde a la disminución del FSCr, que se representa en disminución de la captación del trazador a nivel frontal o fronto-temporal bilateral. Como este patrón no es específico, ya que se observa en otras patologías como la enfermedad de Pick, la enfermedad de Creutzfeldt-Jacob, algunos casos de enfermedad de Alzheimer, esquizofrenia, encefalopatías tóxicas (alcohólica, solventes orgánicos) o depresión, es necesario evaluar los estudios funcionales con base en el cuadro clínico y los estudios morfológicos (ver Tabla 6).
PSEUDOMENCIA (DEPRESIÓN EN EL ANCIANO)
La depresión en el anciano puede ser la manifestación inicial de un cuadro demencial o estar acompañada por síntomas demenciales. Desafortunadamente, como las manifestaciones cognitivas en ambas patologías son similares y pueden atribuirse al proceso de envejecimiento, se dificulta el diagnóstico diferencial e impide un abordaje terapéutico adecuado. Debido a la dificultad en la diferenciación, se creó el término "pseudodemencia", dentro del cual se incluye este tipo de desordenes afectivos.
Los pacientes deprimidos presentan alteraciones en el SPECT que se caracterizan por hipometabolismo cerebral global e hipocaptación en el núcleo caudado o en la corteza frontal. El diagnóstico diferencial se establece por historia clínica/ examen neurológico negativo y estudios funcionales (SPECT o PET), porque las alteraciones mejoran con tratamiento antidepre^ivo (2).
Cuando a pesar de una terapéutica adecuada, persisten las alteraciones en el FSCr, se puede hablar de co-morbilidad depresión-demencia, lo cual ayuda como indicador pronóstico de ambos padecimientos.
Los hallazgos gamagráficos más frecuentes en el SPECT de perfusión cerebral son:
- Estudio normal o con cambios leves para la edad.
- Hipoperfusión frontal y temporal, en pacientes que no reciben tratamiento.
- Coexistencia de infartos cerebrales (depresión hasta en 30% después de un ACV).
DEMENCIA ASOCIADA CON PATOLOGÍAS QUE INVOLUCRAN LOS GANGLIOS BÁSALES
En general, las enfermedades que afectan los ganglios básales (Parkinson, Huntington y Wilson), se caracterizan por trastornos de movimiento y pueden estar asociadas a un síndrome demencial.
ENFERMEDAD DE HUNTINGTON
la enfermedad de Huntington es un trastorno neurodegenerativo poco frecuente, que se trasmite en forma autosómica dominante y se caracteriza por presentar: corea, síntomas psiquiátricos y demencia. Los pacientes presentan degeneración neuronal con muerte celular y gliosis reactiva, que afecta predominantemente de forma bilateral la cabeza del núcleo caudado y en menor grado el putamen. Sólo los estadios tardíos se acompañan de alteración de la corteza cerebral. Alteraciones que se observan como una disminución del volumen de la cabeza de ambos núcleos caudados en la TAC y la RMN.
En el SPECT cerebral existe hipo-captación en los núcleos caudados que se relacionan con los hallazgos de la RMN (atrofia); es posible que los cambios gamagráficos se presenten antes que existan alteraciones en la resonancia. La severidad de la demencia se correlaciona con el déficit metabólico observado en las regiones frontoparietal, tempo-ro-occipital y núcleo caudado. Estos hallazgos modifican el concepto que la demencia por corea de Huntington es una alteración puramente subcortical.
En la actualidad se han superado las limitaciones técnicas en la definición del núcleo caudado en el SPECT cerebral, mediante la cuan-tificación y cálculo de relación porcentual en áreas correspondientes a él y a la sustancia gris contralateral (27-29).
ENFERMEDAD DE WILSON
Es un trastorno autosómico recesivo que se caracteriza por una alteración en la excreción hepática de cobre, con acumulación de este metal en hígado, cerebro y otros órganos, debida a una deficiencia de ceruloplasmina. Su manifestación principal es el compromiso hepático, alteraciones neurológicas: movimientos extraños, espasticidad, temblor de intención, corea, rigidez y disartria, y trastornos psiquiátricos que pueden confundirse con síntomas esquizofrénicos y maniaco-depresivos.
La severidad de las alteraciones neurológicas está en relación a la concentración de cobre cerebral, que mejora con su disminución. Los estudios anatomo-patológicos evidencian el cúmulo de cobre en los ganglios básales, principalmente en el cuerpo estriado, en donde se encuentra la mayor cantidad de receptores dopaminérgicos D2. La pérdida de los receptores (D2) se puede evaluar a través del SPECT cerebral con iodobenzamida marcada con 123I (IBZM), observándose disminución de fijación del trazador y que es directamente proporcional con la severidad de los síntomas neurológicos y que mejora con el tratamiento. Aunque los estudios con HMPAO han sido poco utilizados en estos pacientes, se ha descrito disminución de concentración del trazador en los ganglios básales {29).
ENFERMEDAD DE PARKINSON
La enfermedad de Parkinson (EP) en una condición neurodegenerativa caracterizada por bradiquine-sia, temblor y rigidez. El defecto primario es una degeneración de las neuronas dopaminérgicas en la sustancia negra. Anatomopatológi-camente se observa degeneración de los núcleos pigmentados del tronco del encéfalo, particularmente la sustancia negra compacta, y el desarrollo de cuerpos eosinofílicos de inclusión (cuerpos de Lewy). Su diagnóstico diferencial con otras alteraciones degenerativas subcor-ticales corno la parálisis supranu-clear progresiva, la enfermedad de Huntington o la gliosis progresiva subcortical, es muy difícil y en ocasiones tan sólo se logra en el estudio post mortem.
La diferencia entre EP y otras patologías que involucran los ganglios básales es que en ella se presenta degeneración de las proyecciones dopaminérgicas nigroestriadas, pero las estructuras efectoras (estriado y globus pálidus) están intactas. Por lo tanto, se observa mejoría con la administración de levo-dopa.
Los estudios funcionales permiten evaluar:
- la función dopaminérgica presi-náptica, a través del PET con 18F-dopa o más recientemente con SPECT utilizando 123I-2-b-carbome-toxi-3-b-(4-iodofenil)-propano 123I-b-CIT) O "mTc-Trodat(30).
- la función adrenérgica post sináp-tica con SPECT -123IIBZM (29) o con PET-18F-fluoroetilespiperona, 76Br-broespiperona y "C-raclopride.
- demencia asociada, mediante SPECT de perfusión cerebral con "mTc HMPAO O9 y mTc-ECD.
La EP se asocia en 10 a 23% con demencia(28). En este caso hay compromiso de estructuras corticales a diferencia de los pacientes con EP sin demencia, en los cuales la captación cortical esta conservada. El diagnóstico diferencial en pacientes con EP y demencia se debe hacer principalmente con Enfermedad de Alzheimer. Desafortunadamente los hallazgos del SPECT de perfusión son similares para ambas patologías (hipoperfusión tempo-roparietal bilateral con o sin compromiso frontal). Entonces, se debe recurrir a los datos clínicos: aparición de los déficit cognitivo y motor, y presencia de signos específicos (rueda dentada, animia y temblor distal agitante). El diagnóstico diferencial es aún más difícil cuando se asocia a depresión.
REFERENCIAS
1. Rubens A, Branch Coslett H. Cerebral disease. En: Van Heertum R. and Tlkofsky R. Cerebral SPECT Imaglng Cerebral SPECT Imaging. Second edition. New York: Raven Press; 1995: 53-110. [ Links ]
2. Rubens A, Tikofsky R. Dementia. en: Van Heertum R. and Tikofsky R. Cerebral SPECT Imaging Cerebral SPECT Imaging. Second edition. New York, Raven Press; 1995: 111-150. [ Links ]
3. Talbot P, Lloyd J, Snowden J, Neary D, Testa H.Aclinical role of Tc99mHMPAO SPECT in the investigation of dementia. J Neurol Neurosurg Psychiatry 1998; 64: 306-313. [ Links ]
4. Lassen N. On The History Of Measurement Of Cerebral Flood In Man By Radioactivo Isotopes. en. Costa D.C. Morgan G.F. Lassen N.A. New Trends in Nuclear Neurology and Psychlatry. London: John Libbey; 1996:3-16. [ Links ]
5. Rattner Z, Smith E.O, Woods S, et al. Toward absoluta quantitation of cerebral blood flow using 99 m technetium HMPAO and single sean. J Nucí Med 1991; 32: 1506-1517. [ Links ]
6. Bonte F, Weiner M, Bigio E, White Ch. Brain Blood Flow in the Dementias: SPECT with Histopatologic correlation in 54 Patients. Radiology 1997; III: 793-797. [ Links ]
7. Devous MD. Sr. Imaging Brain Function by Single Photon Emission Computer Tomography, en: Brain Imaging: Applications in Psychiatry. American Psychiatric Press; 1988: 147-234. [ Links ]
8. Abdel - Dayem H, Scott A, Macapnüac H, et al. Role of Thallium 201 Chloride and Te 99m Sestamibi ¡n tumor imaging, en: Freeman L, Nuclear Medicine Annual 1 994. New York, Raven Press; 1994: 181 -234 [ Links ]
9. Abi - Dargham A, Laruelle M, Seibyl J, et al SPECT measurement of benzodiazepine receptors in human brain with iodine 123, lomazanil: Kinetic and equilibrium paradigms. J Nucí Med 1994; 35: 228-238. [ Links ]
10. Ichíse M.B, Allinger J. Editorial: SPECT imaging of Dopamine receptors. J Nucí Med 1996; 37: 1595-1599. [ Links ]
11. Leslie W D, Abraham's N.D. Greenberg C.R, Hobson D. Comparison of 1123 Epinephrine and 1'123 IBZM for Dopamine D2 Receptor imaging. J Nucí Med 1996; 37: 1589-1590. [ Links ]
12. Mozley PD, Zhu X, Kung HF, et al. The dosimetry of Iodine 123 - labeled TISCH: A SPECT imaging agent for the D1 dopamine receptor. J Nucí Med 1993; 34: 208-213. [ Links ]
13. Mielke R, Pietrzyk U, Jacobs A, Fink G, Ichimiya A, Kessler J. HMPAO - SPECT and FDG PET in Alzheimer's disease and vascular dementia: comparation of perfusión and metabolic pattern. Eur J Nucí Med 1994; 21: 1052-1060. [ Links ]
14. Devous Michael. Instrumentation, Radhíopharmaceuticals, and Technical Factors, en: Van Heertum R. and Tikofsky R. Cerebral SPECT Imaging. Second edition. New York: Raven Press; 1995: 3-19. [ Links ]
15. Van Heertum R. and Tikofsky R., Technique and Pittalls en: Van Heertum R. and Tikofsky R. Cerebral SPECT Imaging. Second edition. New York: Raven Press; 1995: 21-29. [ Links ]
16. Ring HA., George M., Costa DC., et al. The use of cerebral activation procedures with single photon emission computed tomography. Eur J Nucí Med 1991; 18: 131-139. [ Links ]
17. Domper M, Arbizu J, Martínez -lage JM. SPECT en demencias. Revista Española de Neurología 1994; 22, suplemento 1: S31-338. [ Links ]
18. Weinstein H.C, Haan J, Van Toyen E, et al. SPECT in the diagnosis of Alzheimer's disease and multi-infart dementia. Clin Neurol Neurosurg 1991; 93 (1): 39-43. [ Links ]
19. Holman BL, Johnson KA, Gerarda B. The scintigraphic appearance of Alzheímer's disease: A prospective study using Technetiun-99m HMPAO SPECT. J Nucí Med 1992; 33: 181-185. [ Links ]
20. Téllez Vargas J. Las Demencias, en: Neuropsiquiatría Imágenes del cerebro y la conducta Humana. Gaviria Vilches M, Téllez Vargas JE. Nuevo Milenio Editores; Santafé de Bogotá 1995: 221-252. [ Links ]
21. O' Brien JT, Eagger S, Syed GM, et al. A study of regional cerebral blood flow and cognitive performance in Alzheimer's disease. J. Neurol Neurosur Psychiatry 1992; 55: 1182-1187. [ Links ]
22. Knop J, Thie A. Fuchs C, Siepmann G, Zeumer H. 99mTc- HMPAO -SPECT with acetazolamide challenge to Detect Hemodynamic compromise in Occlusive Cerebrovascular Disease. Stroke 1992: 23: 1733-1742. [ Links ]
23. Hwang Te-Long, Saenz A, Farrell J, Brannon W. Brain SPECT with dipyndamole stress to Evalúate Cerebral Blood Flow Reserve ¡n Carotid Artery Disease. J Nucí Med 1996; 37: 95-114. [ Links ]
24. Téllez Vargas J. Aspectos neurobiológicos y cognoscitivos del SIDA, en: Neuropsiquiatría Imágenes del cerebro y la conducta Humana. Gaviria Vilches M, Téllez Vargas JE. Nuevo Milenio Editores; Santafé de Bogotá 1995: 359-387. [ Links ]
25. Pickut B, Saerens J, Marien P. Borggreve F, et al. Discriminative Use of SPECT in Frontal Lobe -Type Dementia versus (senile) Dementia of the Alzheimer's Type. J Nucí Med 1997; 38: 929-934. [ Links ]
26. Gustafson L. Clinical picture of frontal lobe degenerations of the nonAlzheimer type. Dementia 1993; 4:1431 -1448. [ Links ]
27. Nagel JS, Ichise M, Holman BL. The scintigraphic evaluation of Huntington's disease and other movements disorders using Single Photon Emission Computed Tomography perfusión brain sean. Sem Nucí Med 1991; 21: 11-23. [ Links ]
28. Butler RE, Costa DC, Katona CLE. PET and SPECT imaging in Dementias, en: Nuclear Medicine in Neurological and psychiatric diagnosis. Chapter 53: 613-627. [ Links ]
29. Luquin MR, García de Casasola MC, Domínguez J. SPECT cerebral y enfermedades de los ganglios básales. Revista Española de Neurología 1994; 22, suplemento 1: S57-S64. [ Links ]