Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Colombiana de Psiquiatría
versão impressa ISSN 0034-7450
rev.colomb.psiquiatr. v.36 n.3 Bogotá jul./set. 2007
Artículos de revisión/actualización
Manuel Martín Carrasco1 Antonio Bulbena Vilarrasa2
1 Médico psiquiatra. Director médico de la Clínica Psiquiátrica Padre Menni, Pamplona, España. mmartin@clinicapadremenni.org
2 Médico psiquiatra. Jefe del Servicio de Psiquiatría, Hospital del Mar, Barcelona, España.
Resumen
Introducción: Los avances en el estudio de las demencias han permitido establecer la presencia de fases preclínicas en las formas más frecuentes, como la enfermedad de Alzheimer (EA) o la demencia vascular. Asimismo, se ha avanzado en la caracterización de fases prodrómicas, pero no con la intensidad sufi ciente como para recibir un diagnóstico de demencia según los criterios empleados habitualmente. El término deterioro cognitivo ligero (DCL) es el más utilizado para defi nir una fase intermedia entre el envejecimiento normal y la demencia, aquella fase en la que el sujeto presenta un défi cit cognitivo apreciable, pero éste no interfi ere con su funcionalidad. Método: revisión de la literatura disponible. Resultados: dada la heterogeneidad de las enfermedades que pueden dar lugar a una demencia, necesariamente esto debe corresponder también a un concepto heterogéneo, tanto clínica como etiológicamente. En el momento actual, la utilidad del concepto de DCL deriva fundamentalmente de su capacidad de identifi car poblaciones de riesgo, sobre las que pueda efectuarse una prevención secundaria previa al diagnóstico de demencia. Conclusiones: Dado el carácter heterogéneo del DCL, las medidas empleadas pueden pecar también de ser poco específi - cas. Es de esperar que con el descubrimiento de un marcador biológico fi able de la EA en todas sus fases, la noción de DCL pase a tener un interés más relativo, abriendo paso a un verdadero tratamiento preventivo de la enfermedad.
Palabras clave: demencia, enfermedad de Alzheimer, envejecimiento, deterioro cognitivo.
Abstract
Introduction: Preclinical phases have been established in the more common forms of dementia such as Alzheimer’s disease and vascular dementia. Characterization of the prodromal phases has advanced as well, but not enough to allow for a diagnosis of dementia by current criteria. The term Mild Cognitive Disorder (MCD) is commonly used to defi ne an intermediate phase between normal aging and dementia, a phase in which the subject presents with cognitive impairment but remains functional. Method: Review of the available literature. Results:
Due to the heterogeneity of the illnesses that can give rise to a dementia, MCD also corresponds to a heterogeneous concept, both clinically and etiologically. At this time, the usefulness of the term MCD derives mainly from its capacity of identifying population at risk amenable to secondary prevention before the diagnosis of dementia is established. Conclusions: Due to the heterogeneity of MCD, measures taken may be unspecifi c. It is to be hoped that with the discovery of biological markers of AD in all its phases, the notion of MCD will come to be of minor interest, opening the way for a real preventive treatment of the disease.
Key words: Dementia, Alzheimer disease, aging. cognitive disorder.
Introducción
La zona limítrofe entre los cambios cognitivos que ocurren con el envejecimiento en sujetos sanos y la demencia incipiente ha sido objeto de interés clínico desde hace varias décadas, con el propósito de mejorar el diagnóstico precoz del síndrome demencial (1). En general, el debate se ha centrado en torno a dos puntos fundamentales: (a) qué cambios cognitivos pueden ser considerados parte del envejecimiento normal y (b) si el envejecimiento cerebral y las demencias degenerativas constituyen o no procesos diferentes. Ninguna de las dos cuestiones ha sido resuelta totalmente, pero en los últimos años el interés en ellas ha crecido enormemente, como resultado del descubrimiento de que la enfermedad de Alzheimer (EA), la forma más común de demencia, tiene un largo periodo preclínico, y, por lo tanto, existe la posibilidad de intervenir y detener o revertir el proceso antes de la aparición de los síntomas (2-3).
El inmenso interés despertado por la zona limítrofe entre el envejecimiento y la EA condujo a la defi nición de una serie de estados intermedios, caracterizados por la aparición de cambios cognitivos, pero sin llegar a constituir una demencia establecida con los criterios comúnmente utilizados (Tabla 1).
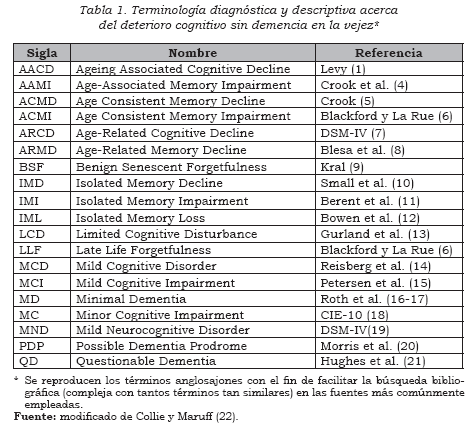
Cada uno de las expresiones anteriores implica la presencia de un défi cit cognitivo ligero apreciable, pero conceptualmente difi eren en cuanto a la intensidad y la extensión del défi cit, así como en cuanto al tipo de relación con el envejecimiento normal o con el síndrome demencial. En general, pueden agruparse en tres grandes grupos: (a) entidades que describen formas acusadas del deterioro cognitivo que normalmente se asocia con la edad; (b) entidades que se diferencian del declive cognitivo asociado con la edad, pero sin cumplir criterios de demencia, y (c) entidades que suponen una forma precoz de demencia.
Entre todos ellos, el concepto de deterioro cognitivo ligero3 (DCL) o mild cognitive impairment es el que ha terminado por imponerse, al menos por el momento, en gran parte gracias al trabajo realizado en el Mayo Clinic Alzheimer Disease Research Center, a la hora de caracterizar la entidad, tanto desde el punto de vista clínico como desde las técnicas de neuroimagen (15,23). Así mismo, organismos prestigiosos como la Academia Americana de Neurología4 han recomendado su uso para clasifi car a los sujetos en riesgo de desarrollar demencia (24); sin embargo, el debate está lejos de darse por zanjado, y como iremos viendo a lo largo de esta revisión, podemos considerar que el DCL es un concepto útil en el momento actual desde el punto de vista clínico, pero que plantea numerosas cuestiones acerca de los criterios de diagnóstico y de la conveniencia de ser tratado.
En el presente trabajo nos centramos en los correlatos cognitivos del envejecimiento normal, en los estados de transición (especialmente el DCL) y en las fases iniciales de demencia, especialmente de las asociadas con la EA, a fi n de destacar los estudios con carácter longitudinal, aquellos que en nuestra opinión más luz pueden arrojar sobre este fascinante problema clínico y conceptual.
Función cognitiva y envejecimiento
A pesar de constituir, durante décadas, un tema de atención constante para numerosos grupos de trabajo, todavía no existe una comprensión clara de la relación entre edad y funcionamiento cognitivo (Figura 1). En general, se admite que el envejecimiento se asocia con la presencia de un défi cit de algunas formas de memoria (p. ej., recuerdo reciente de listas de palabras o textos) y de otras capacidades cognitivas (25). Estos hallazgos se obtienen, principalmente, de estudios transversales que comparan muestras de sujetos ancianos con otras de personas más jóvenes.
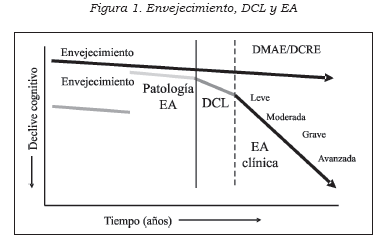
La edad supone una disminución de la memoria episódica (verbal y no verbal), la denominación, la capacidad visoespacial y, especialmente, la rapidez del rendimiento psicomotor. Sin embargo, los défi - cits son de pequeña magnitud y no dan lugar a una disminución de la capacidad funcional (26).
No obstante, hay que recordar que los estudios transversales pueden tener diferentes sesgos, que limitan el valor de estos hallazgos. Se destaca, sobre todo, el denominado efecto cohorte, que haría atribuir a la edad lo que en realidad son diferencias generacionales en experiencias educacionales, exposición ambiental o estilos de vida. Otra fuente potencial de error en los estudios transversales sobre envejecimiento es la inclusión de sujetos que se encuentran en un estado de demencia incipiente no diagnosticada.
Por el contrario, los estudios longitudinales o prospectivos, que siguen a la muestra de estudio a lo largo del paso de los años, no están sujetos a este tipo de sesgos, y refl ejan de manera consistente una menor repercusión de la edad en el funcionamiento cognitivo de los sujetos, aunque no existen diferencias cualitativas importantes en el perfi l de declive asociado con el envejecimiento.
Aun cuando este tipo de estudios también tiene sus fuentes posibles de error5, permiten excluir del análisis a los sujetos que en la evolución desarrollan demencia, lo cual aporta datos sobre población no aquejada de deterioro cognitivo para cada grupo de edad, lo que resulta imprescindible para establecer comparaciones y detectar las sutiles anomalías que indican el comienzo de una demencia (27).
De manera sorprendente, cuando se analizan muestras de sujetos ancianos de forma longitudinal empleando criterios estrictos para excluir a sujetos con deterioro, el rendimiento en las pruebas psicométricas se mantiene muy estable con el paso de los años. Un estudio reciente (28) sobre ancianos sin demencia incluía una muestra de 33 sujetos de edades entre los 65 y los 74 años y otra de 20 individuos con edades comprendidas entre los 84 y los 93 años.
Las dos muestras fueron valoradas anualmente con distintas pruebas neuropsicológicas a lo largo de cuatro años. En la valoración inicial existían diferencias signifi - cativas entre ambas muestras, en cuanto a la memoria inmediata y las pruebas de capacidad visomotora. Sin embargo, no se apreciaron diferencias a lo largo del período de cuatro años en la tasa de cambio de ninguna de las pruebas neuropsicológicas incluidas. Dentro de cada grupo de edad, los cambios fueron mínimos para la mayoría de las pruebas a lo largo de los cuatro años, aunque se pudo apreciar cierto efecto de aprendizaje, y, en algunas pruebas, una disminución mínima de rendimiento.
Otro estudio (29) examinaba los cambios más precoces asociados con el desarrollo de demencia, junto con los cambios cognitivos asociados con el envejecimiento normal. La muestra de estudio consistía en 82 sujetos (edad media al inicio=72 años) con una Clinical Dementia Rating Scale (CDR) (21) basal de 0, que fueron evaluados clínica y neuropsicológicamente a lo largo de 15 años. Al fi nalizar el estudio, el 40% de los participantes tenía una CDR>0 (deterioro cognitivo), de los cuales el 59% presentaba una demencia en fase inicial. De los 55 individuos sin demencia, 48 no presentaron declive en el funcionamiento cognitivo, medido por una puntuación factorial factorizada que representaba el rendimiento cognitivo global. Estos resultados, reproducidos en otros trabajos (30-31), sugieren que los individuos ancianos sanos mantienen un rendimiento cognitivo estable en la evaluación longitudinal, y que, por lo tanto, la aparición de un deterioro, aunque de carácter mínimo, representa habitualmente el comienzo de una demencia.
Por lo que respecta a los correlatos histopatológicos del envejecimiento normal, en la actualidad persiste la controversia acerca de si los hallazgos básicos de la EA —los ovillos neurofi brilares (ONF) y las placas seniles (PS)— son específi cos de la enfermedad o pueden aparecer también en el cerebro de ancianos sanos. El punto de vista más comúnmente aceptado es que las diferencias histopatológicas entre el envejecimiento normal y la EA son más cuantitativas que cualitativas, ya que existen diferentes estudios que muestran la presencia de ONF y PS en cerebros de ancianos sin demencia.
El origen de esta teoría se remonta al clásico trabajo de Tomlinson, Blessed y Roth (32)6, y ha sido consagrado posteriormente en los sucesivos criterios de diagnóstico anatomopatológico de la EA (33-34), aunque ya en el último de ellos (35) –el más empleado actualmente– se admite la posibilidad de que cualquier cambio puede ser considerado patológico, aun cuando no se encuentre una correlación clínica precisa.
De hecho, existe una creciente corriente de opinión que cuestiona la teoría ofi cial y argumenta que ésta se ha elaborado sobre trabajos en los cuales los sujetos supuestamente no dementes en realidad no estaban bien estudiados desde el punto de vista clínico, por lo que muchos de ellos podrían tratarse realmente de casos de demencia incipiente no diagnosticados.
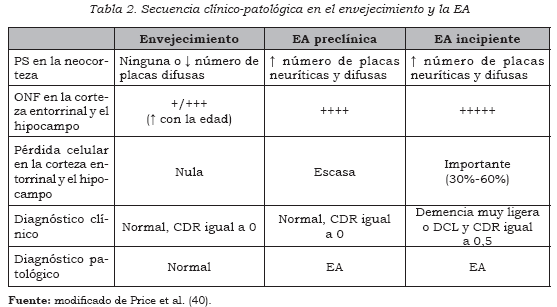
En consonancia con esta opinión, distintos trabajos han destacado que los cerebros de ancianos sin deterioro signifi cativo no cumplían criterios para ser diagnosticados de EA, desde el punto de vista anatomopatológico, y que es necesaria la presencia apreciable de ONF o PS (36-37), así como una pérdida neuronal signifi cativa para que aparezcan los síntomas de demencia (38-39). La Tabla 2 refl eja una hipotética secuencia clínicopatológica en el envejecimiento y la EA, de acuerdo con este último punto de vista (40).
Cuadros de deterioro cognitivo menor
Como ya se había comentado, el problema de la transición entre el síndrome demencial y el envejecimiento se ha planteado numerosas veces en las últimas décadas. Quizás la primera vez fue en 1962, cuando se presentaron las expresiones olvido benigno de la vejez y olvido maligno de la vejez (9), con las que se designaban sendos estados de disfunción de la memoria en ancianos.
La primera de ellas (olvido benigno de la vejez) ha tenido más fortuna, y se ha empleado intermitentemente desde entonces. Se refi ere a personas cuyo funcionamiento mnésico es menor en la edad avanzada, pero que no tienen otras dificultades. Se trataría de una disminución funcional benigna que no se agrava y no progresa hacia la demencia, aunque es diferente a la pérdida de memoria que ocurre con la edad. Sin embargo, la escasa defi nición operativa del concepto ha hecho inviable su aplicación práctica.
Posteriormente, en 1986, un grupo de trabajo del National Institute of Mental Health (NIMH) estadounidense introdujo la expresión deterioro de la memoria asociado con el envejecimiento (DMAE), para designar una alteración de la memoria que, medida por test psicométricos, se apartaría más de una desviación típica de lo esperable en adultos jóvenes sanos (4). Por lo tanto, se trata de medir deterioro de memoria, sin determinar a priori si ocurre en individuos sanos o no. El trastorno aparecería en personas de más de 50 años con alteraciones preferentemente de la memoria a corto plazo y ausencia de otro tipo de deterioro cognitivo y de enfermedades neurológicas, psiquiátricas o sistémicas que lo produzcan.
La introducción de este concepto generó una cantidad notable de estudios, y supuso un avance considerable en el área. La crítica principal a este concepto ha sido a su amplitud, ya que según las pruebas neuropsicológicas que se empleen para aplicarlo, podría llegar a comprender a la mayoría de la población de edad superior a 65 años sana. Por ejemplo, se ha demostrado que empleando una prueba de memoria exigente, como el Auditory Verbal Learning Test, más del 90% de los ancianos normales quedaría englobado dentro de esta categoría (41).
En un intento por superar este problema, años más tarde, en 1989, otros autores propusieron añadir al DMAE dos nuevas categorías (6). Una de ellas, el deterioro de la memoria consistente con la edad (DMCE), para los sujetos cuyo rendimiento se encuentra en el 75% o más de las pruebas de memoria administradas, dentro de una desviación típica con respecto al grupo de su misma edad, y el olvido de la edad avanzada (OV), aplicable a las personas con un rendimiento entre una y dos desviaciones típicas por debajo de su grupo etario, al menos en el 50% de las pruebas. Este sistema no ha sido estudiado con posterioridad, y no existen estudios epidemiológicos que confi rmen su valor predictivo (42).
Posteriormente se realizaron otros intentos de superar las limitaciones apreciadas en el DMAE. En 1994, la Asociación Internacional de Psicogeriatría (IPA, por su sigla en inglés) y la Organización Mundial de la Salud (OMS) apoyaron un grupo de trabajo que elaboró el concepto de declive cognitivo asociado con el envejecimiento (DCAE) (1). Este presenta varias diferencias con el DMAE: elimina el criterio de edad límite a partir de la cual puede realizarse el diagnóstico. El inicio del declinar cognitivo ha de ser gradual y estar presente durante al menos seis meses, criterio introducido con el fi n de eliminar las formas reversibles. Así mismo, se puede afectar cualquiera de las siguientes funciones: memoria y aprendizaje, atención y concentración, pensamiento, lenguaje y funciones visoespaciales, con un défi cit de rendimiento superior en una desviación típica al de los controles pareados en edad, sexo, raza y nivel educativo.
Estos défi cits no deben ser lo bastante intensos como para que se cumplan los criterios de demencia, ni deben ser la consecuencia de ninguna enfermedad médica o psiquiátrica presente o pasada, ni estar asociados con el consumo de sustancias (43). La prevalencia del DCAE ha sido estudiada en dos estudios epidemiológicos en población general, que arrojaron una tasa del 21% en sujetos de 60 o más años (44), y del 27% en población de edad igual o superior a 65 años (45). Así mismo, este último trabajo informó de una tasa de conversión en demencia del DCAE del 29% a los tres años.
También hay que mencionar las categorías introducidas en los sistemas de clasifi cación más empleados en psiquiatría: la Clasifi cación Internacional de Enfermedades (CIE-10) y el Manual diagnóstico y estadístico de los trastornos mentales (DSM-IV-TR). En la CIE-10 (18) se incluyó la categoría trastorno cognoscitivo leve (F06.70) con un carácter provisional, ya que se señala expresamente que “los límites de esta categoría están sin establecer defi nitivamente”.
La característica principal consiste en una disminución del rendimiento cognitivo, que puede incluir deterioro de la memoria y dificultades de aprendizaje o de concentración, detectables en las pruebas objetivas, en ausencia de diagnóstico de demencia u otros diagnósticos psiquiátricos. A diferencia de otras entidades descritas, se admite la presencia de trastornos somáticos, cerebrales o sistémicos como sus causas. Se ha informado de una prevalencia del 4% en sujetos de edad igual o superior a 70 años (46), aunque en el mismo estudio se mencionaba la escasa correlación interna entre los distintos descriptores de la entidad y la probable ausencia de un síndrome subyacente.
En la misma muestra de estudio, pasados 3,6 años, el 12% de los individuos clasificados como trastorno cognoscitivo leve había desarrollado una demencia, pero no se encontraban diferencias relevantes en la tasa de conversión en la población de referencia, por lo que los autores concluyen que esta categoría no puede considerarse un antecedente específi co de demencia, y la relacionan más en su defi nición actual con trastornos ansiosos, depresivos y neuroticismo (47).
En el DSM-IV-TR (19) se incluyó como un código Z —problemas adicionales que pueden ser objeto de atención clínica— la categoría deterioro cognoscitivo relacionado con la edad (R41.8/780.9). Se indica su empleo cuando se evidencia un deterioro de la actividad cognoscitiva, demostrado objetivamente, a consecuencia de la edad y que está dentro de los límites normales de esa edad. Los individuos con este défi cit pueden tener problemas para recordar nombres o citas y experimentar difi cultades para solucionar problemas complejos.
No debe emplearse sin haber descartado que el deterioro cognoscitivo sea atribuible a un trastorno mental específi co o a una enfermedad neurológica. No se explicitan los requerimientos psicométricos, lo que contribuye a la falta de operatividad de la categoría. Se ha descrito una prevalencia del 8% en población de edad igual o superior al 65 años (48), y una tasa de conversión de demencia del 28% a los dos años de seguimiento (49). El DSM-IV-TR (7) ha mantenido esta categoría y ha añadido la de trastorno neurocognoscitivo leve, con características similares al trastorno cognoscitivo leve de la CIE-10, dentro del Apéndice B (“Criterios y ejes propuestos para estudios posteriores”).
Finalmente, una categoría que aparece con frecuencia en los trabajos de investigación epidemiológica en este área es deterioro cognitivo, no demencia (DCND), que reúne todos los casos de deterioro cognitivo que no satisfacen la categoría de demencia, entre ellos casos producidos por enfermedades médicas o trastornos psiquiátricos (50-51). Generalmente se emplea como un concepto general, del que luego se extraen los casos de deterioro cognitivo ligero u otras categorías más específicas.
Fase preclínica de las escalas de estadificación del síndrome demencial
Existen varios instrumentos psicométricos desarrollados con la fi nalidad de establecer los diferentes estadios que suelen aparecer en la evolución de las demencias más comunes, desde la fase preclínica hasta las fases más avanzadas o terminales. La Tabla 3 recoge los instrumentos utilizados con mayor frecuencia, junto con la denominación de la fase preclínica en cada uno de ellos.
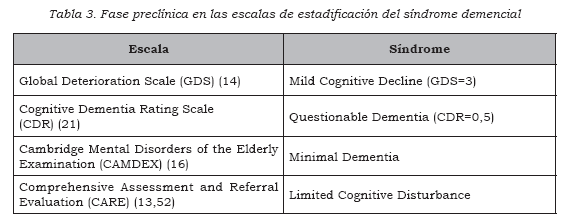
Todos estos instrumentos se emplean ampliamente en la literatura sobre la demencia, aunque con frecuencia los términos para referirse a la fase preclínica se utilizan indiscriminadamente, sin tener en cuenta el instrumento de referencia y el constructo teórico que existe tras ellos (42), lo que aumenta la confusión terminológica. Por ejemplo, el Consortium for the Establishment of Registries in Alzheimer’s Disease (CERAD) ha propuesto una nueva expresión posible demencia prodrómica, para referirse a la puntuación de 0,5 en la CDR (20).
Otra fuente de error en el empleo de estas categorías es causada por su poca defi nición operativa, en aspectos cruciales como la valoración cognitiva, por lo cual los resultados de estudios que emplean la misma escala pueden arrojar resultados muy diferentes según el tipo de muestra empleada. Lo mismo puede decirse de los criterios referentes al funcionamiento psicosocial, empleados, por ejemplo, en el Cambridge Mental Disorders of the Elderly Examination (CAMDEX). La variabilidad entre los resultados obtenidos con las diferentes escalas es también muy amplia, lo que refl eja los distintos puntos de partida y las concepciones teóricas en su desarrollo.
Por ejemplo, empleando la CDR, se ha estimado para la demencia cuestionable una prevalencia del 3% y una incidencia anual entre 12 y 15 por mil en la población general de edad igual o superior a 65 años, con una tasa de conversión a demencia que oscila entre el 6% y el 16% (53-54). Por el contrario, al utilizar el CAMDEX se obtiene una prevalencia de demencia mínima del 16% en población de edad igual o superior a 65 años (55) y una incidencia anual de 54 por mil a partir de los 75 años (56).
La tasa de conversión a demencia encontrada al cabo de un año es del 15% para sujetos de 65 o más años (55). Las cifras obtenidas con la Global Deterioration Scale (GDS) difi eren notablemente de las anteriores: una prevalencia del 22% en población de 65 o más años para la fase de GDS=3, con una tasa de conversión a demencia que oscila del 4% al 40% (57-58). Como puede apreciarse, la variabilidad es tan amplia que arroja sombras sobre la validez de constructo subyacente.
Deterioro cognitivo ligero (DCL)
Concepto
En los últimos años, la denominación DLC ha ido ganando adeptos, hasta convertirse en la más empleada en la actualidad. Sin embargo, como evidenció la Conferencia Current Concepts in Mild Cognitive Impairment, celebrada en Chicago, en 1999, los variados grupos de estudio implicados en diferentes países han empleado la expresión de manera distinta, lo que justifi ca los resultados dispares en cuanto a prevalencia, tasa de conversión a demencia y características clínicas refl ejadas en las publicaciones científi cas (59-60).
El concepto de DCL más en boga en el momento actual corresponde al empleado por el grupo de la Clínica Mayo (15), e incluye a pacientes con las siguientes características: (a) queja de pérdida de memoria, preferiblemente corroborada por un informador; (b) actividades de la vida diaria esencialmente preservadas; (c) función cognitiva general intacta; (d) trastorno de memoria objetivado superior al normal para su edad y educación (1-2 desviaciones típicas), y (e) no demencia.
Este grupo de sujetos puede diferenciarse tanto de la población normal como de la demencia incipiente, ya que, aun cuando su tasa de evolución hacia demencia es superior a la de la población normal (10%-15% anual frente a 1%-2% anual), se encuentran individuos que no desarrollan un síndrome demencial. Se trata de un concepto clínico, al que se adscriben los sujetos tras ser valorados por un equipo multidisciplinar —compuesto, entro otros, por psiquiatras, neuropsicólogos y neurólogos—, formulado desde una perspectiva preventiva, pues se trata sobre todo de identifi car sujetos con riesgo alto de desarrollar demencia.
Por ello, en la metodología de trabajo seguida por este grupo, la muestra de estudio se obtiene a través de una búsqueda activa, especialmente en los registros de médicos de familia. Una crítica a este concepto de DCL es que proviene de trabajos realizados sobre una muestra obtenida en un ambiente clínico altamente especializado, y que no ha podido demostrar su utilidad en estudios realizados en población general (45). Por otra parte, también se ha puesto en duda la validez misma del constructo por parte del grupo de la Universidad de Washington, el cual sigue la hipótesis de que la vejez saludable no se acompaña de un deterioro cognitivo ni funcional signifi cativo, por lo que cualquier deterioro constituiría un marcador de enfermedad (27).
La Conferencia de Chicago, antes mencionada, dada la heterogeneidad del concepto de DCL, recomendó su clasifi cación en tres subtipos (59): DCL amnésico, DCL con afectación múltiple y DCL con afectación única no de memoria. Por otra parte, la heterogeneidad también se manifi esta en que cada uno de los subtipos clínicos puede deberse a diferentes etiologías, que se manifi estan en la evolución a demencia (Tabla 4).
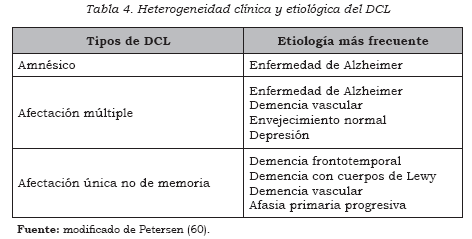
La forma amnésica del DCL es la más frecuente, y a ella se refi eren la mayor parte de los trabajos en el área, entre ellos los del grupo de la Clínica Mayo. Se caracteriza por la existencia de un défi cit aislado (en términos absolutos o relativos) de memoria. Cuando hay una enfermedad demenciante subyacente, la mayoría de las veces se trata de una EA.
El DCL con afectación múltiple se caracteriza por un deterioro en varias áreas de funcionamiento cognitivo, sin alcanzar la intensidad sufi ciente como para realizar un diagnóstico de demencia. Por ejemplo, una persona puede presentar una afectación ligera de la memoria, el lenguaje o las funciones ejecutivas. La diferencia con el DCL amnésico no sólo estriba en que está afectada únicamente la memoria, sino en que no existe una desproporción en la intensidad del défi cit en las distintas áreas afectadas.
El grado de deterioro se sitúa habitualmente entre 0,5-1 desviaciones típicas, aunque, como ya se ha comentado, se trata de un juicio clínico, no de uno psicométrico. Las personas incluidas en esta categoría pueden evolucionar a EA o demencia vascular. También es posible que algunos casos puedan englobarse dentro del envejecimiento normal, si no progresan a demencia, y se sitúan por lo tanto en una posición muy cercana al DCAE (1).
Una tercera variedad de DCL incluye los casos de deterioro ligero, que afectan un área cognitiva distinta a la memoria, por ejemplo, las funciones ejecutivas, las capacidades visoespaciales o el lenguaje. Cada uno de ellos podría corresponder a la fase prodrómica de un tipo de demencia, aunque esta hipótesis debe ser comprobada. Por ejemplo, en el caso de las alteraciones de las funciones ejecutivas, podría tratarse de demencia frontotemporal; en el caso de alteraciones visoperceptivas, de demencia con cuerpos de Lewy, y en el caso de alteraciones del lenguaje, de afasia progresiva primaria. O bien, podría tratarse de una lesión que afecte a la región correspondiente y que evolucione más tarde a una demencia vascular (61).
La Conferencia de Estocolmo, celebrada en 2003, ha confi rmado esta diferenciación, al apreciarse que no todos los sujetos con afectación de memoria progresan a EA; además, otros fenotipos clínicos pueden evolucionar hacia la enfermedad (62). Se establecieron dos subtipos de DCL: amnésico (con afectación de la memoria) y no amnésico (afectación de otras áreas cognitivas y no de la memoria) (63); mientras el concepto de DCL quedaba establecido como:
• La persona no está demente, pero no es normal.
• Hay evidencia de deterioro cog nitivo, apreciable bien por la puntuación de una medida objetiva a lo largo del tiempo, por el informe subjetivo del sujeto o por la apreciación de un informador confi able junto con la medición objetiva de défi cit.
• Las actividades de la vida diaria están preservadas y las funciones instrumentales complejas están preservadas o mínimamente afectadas.
Esta nomenclatura la está usando actualmente el Instituto Nacional de Envejecimiento estadounidense y la Alzheimer’s Disease Neuroimaging Initiative (64). En el lado europeo, el concepto de DCL ha tenido una evolución similar. El Grupo de Trabajo acerca del DCL del Consorcio Europeo sobre la Enfermedad de Alzheimer ha propuesto recientemente unos criterios, resumidos en la Tabla 5 (65).

Estos criterios hacen hincapié en la importancia de la evaluación clínica, que combine la exploración neuropsicológica y la entrevista a familiares para detectar la presencia de un deterioro en el estadio más temprano posible; pero se debe intentar, sobre todo, identifi car la presencia de un deterioro progresivo del funcionamiento cognitivo.
El diagnóstico se basa, por lo tanto, en la impresión clínica global, y no específi camente en la presencia de alteraciones de la memoria. Se concede mayor importancia a la queja cognitiva, tanto en términos cuantitativos como cualitativos, y se enfatiza su valor pronóstico. La alteración cognitiva puede tener una ligera repercusión en actividades complejas o instrumentales de la vida diaria. Los puntos débiles de esta aproximación son la falta de defi nición de qué instrumentos pueden ser útiles para valorar el funcionamiento y el declive cognitivo en los períodos propuestos, ya que se elimina la utilización de puntos de corte.
Una vez establecida la presencia de DCL puede valorarse el subtipo clínico –amnésico, no amnésico (DCL con afectación múltiple) y con afectación única no de memoria– para pasar luego a un aproximación etiopatogénica similar a la recogida en la Tabla 4. En el caso de un DCL de tipo amnésico, a la hora de considerarlo una situación prodrómica de la EA, es importante comprobar que la afectación de memoria sea de tipo hipocámpico; es decir, que se manifi este por un deterioro en el recuerdo libre (66).
Epidemiología
Dada la heterogeneidad y las imprecisiones que todavía rodean al concepto de DCL, no es de extrañar que las cifras sobre prevalencia, incidencia y tasa de conversión a demencia varíen ampliamente según los diferentes trabajos, dependiendo sobre todo del criterio de diagnóstico empleado, así como de la composición de la muestra de estudio, de los períodos de seguimiento o de las medidas neuropsicológicas empleados (67).
Los resultados del Canadian Study of Health and Aging, un estudio sobre población general con una muestra de 2.050 sujetos de edad igual o superior a 65 años, encontró una prevalencia de DCND del 16,8%, mientras que la tasa combinada de todos los tipos de demencia era del 8% (68). La prevalencia de pérdida de memoria circunscrita, la forma de DCND más frecuente en este estudio y que se corresponde aproximadamente con los criterios de DCL amnésico de la Clínica Mayo, fue del 5,3%.
En el Italian Longitudinal Study on Aging, la prevalencia de DCND fue del 10,7%, mientras que la de demencia era del 5,5%. Un estudio comunitario sobre 833 sujetos encontró una prevalencia de DCL amnésico y de DCAE del 3,2% y 19,3%, respectivamente (45). Otro estudio comunitario, realizado en Dinamarca sobre una muestra de 3.346 individuos de edad igual o superior a 65 años, encontró una prevalencia del 2,8%, sobre una tasa global de demencia del 7,1%, al emplear el criterio de demencia cuestionable (CDR=0,5) (69).
Actualmente no existe un criterio uniforme acerca de si la edad, la educación o el sexo afectan a la prevalencia de DCL. Por ejemplo, se ha informado de un aumento de la prevalencia tras los 65 años, aunque existen también datos sobre un estancamiento en el aumento de las cifras de prevalencia tras los 85 años (48,51). Por lo general, se ha encontrado una prevalencia mayor en individuos con nivel educativo bajo, aunque no existe unanimidad al respecto(42), y no suelen hallarse diferencias entre los sexos (51,70).
Los estudios de incidencia son muy escasos. Se ha informado una incidencia de 12-15 casos por mil en población de edad igual o superior a 65 años, utilizando la categoría de demencia cuestionable (69,71). En población de edad igual o superior a 75 años se ha informado una incidencia de 54 casos por mil (56). El número de trabajos es insufi ciente para extraer conclusiones acerca de la importancia del sexo, la edad o el nivel educativo en la incidencia del DCL.
Evaluación
A pesar del acuerdo entre clínicos e investigadores acerca de la necesidad de mejorar el reconocimiento precoz del deterioro cognitivo, no existe unanimidad a la hora de recomendar las pruebas neuropsicológicas que deberían emplearse para ello (24). No obstante, existe una actividad investigadora creciente en torno a este tema. En general, las pruebas de memoria episódica, lenguaje (capacidad nominativa y fl uencia verbal) y funciones ejecutivas son los mejores predictores de conversión entre DCL y EA, junto con el estudio longitudinal de cada caso, a fi n de comprobar la existencia de un défi cit progresivo (72-73); sin embargo, dado que no existe un patrón típico de défi cit cognitivo de la EA en la fase prodrómica del síndrome demencial, las probabilidades de confusión con otras causas de deterioro cognitivo son altas. En el momento actual, la mayoría de las pruebas diagnósticas muestran una buena sensibilidad y especifi - cidad en las fases moderadas de la enfermedad, pero no en las fases iniciales.
Snowdon et al. (74) han demostrado que la baja capacidad lingüística, medida incluso en épocas tempranas de la vida, puede ser un factor predictivo de deterioro cognitivo y EA en edades avanzadas. Estos autores evaluaron dos parámetros de capacidad lingüística (densidad ideatoria y complejidad gramatical) en los textos autobiográfi cos de religiosas escritos cuando contaban aproximadamente con 22 años de edad. Las mismas personas fueron valoradas cognitivamente 58 años más tarde, y a su muerte se procedió al estudio neuropatológico. Se encontró una asociación entre la presencia de baja capacidad ideatoria y complejidad gramatical en la juventud y una puntuación baja en las pruebas cognitivas en la vejez. Además, el estudio histopatológico realizado en las catorce religiosas fallecidas confi rmó la presencia de EA en todas las que presentaban baja densidad ideatoria en su juventud, así como la no presencia, en ningún caso, de las que tenían alta densidad ideatoria.
También existen numerosos datos sobre el deterioro selectivo de la memoria episódica, especialmente de tipo verbal, como factor predictivo del desarrollo de EA, basados en trabajos realizados sobre portadores asintomáticos de genes causantes de la EA, estudios epidemiológicos sobre casos incidentes y estudios longitudinales de pacientes con DCL.
Otros autores llegan a afi rmar que los problemas en el aprendizaje y la memoria episódica constituyen la mayoría de las veces la primera manifestación de la EA, mientras que la afectación de la memoria semántica sería generalmente un hallazgo más tardío. Por lo tanto, las pruebas neuropsicológicas más sensibles para la detección precoz de la EA son las que incluyen test que valoran la memoria episódica, como el Memory Impairment Screening (MIS) (75), el Cambridge Neuropsychological Test Automated Battery (CANTAB) (76) o el Free and Cued Selective Reminding Test (FCSRT) (77).
Entre tanto, otros instrumentos más amplios como el Cambridge Cognitive Examination (CamCog) (16), el SISCO —incluido en el Structured Interview for the Diagnosis of Dementia of the Alzheimer Type, Multi-Infarct Dementia and Dementias of Other Aetiology (SIDAM) (78)— o el Milan Overall Dementia Assessment (MODA) (79) son útiles sobre todo para el diagnóstico temprano de la demencia y para el seguimiento de su evolución.
Un estudio del 2001 (80) revisó 30 pruebas cognitivas destinadas al cribado de casos de DCL y las evaluó de acuerdo con el estándar metodológico propuesto por Gifford y Cummings (81), para valorar el rendimiento de este tipo de pruebas, de manera que sólo once pruebas lo cumplieron (Tabla 6). También en fechas recientes se ha desarrollado una versión modifi cada de la Escala de evaluación de la enfermedad de Alzheimer (ADAS-Cog), que incluye pruebas de recuerdo diferido y funciones ejecutivas, con la fi nalidad de mejorar su rendimiento en estudios clínicos en DCL (82).
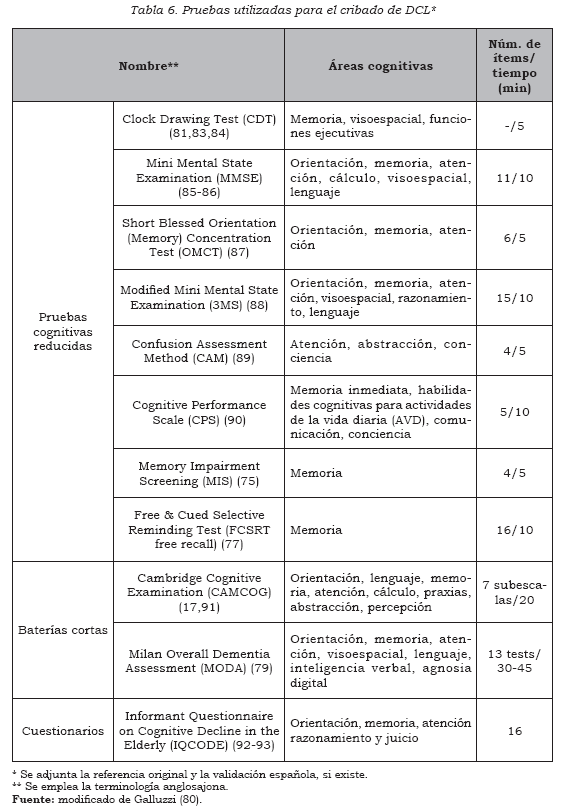
Una vez los síntomas están defi nidos desde el punto de vista clínico, el siguiente paso consiste en su determinación etiológica. En este punto tienen gran importancia la historia clínica obtenida del paciente y un informante cualifi cado, la realización de pruebas de laboratorio y las pruebas de neuroimagen. Al término de estos estudios, el clínico puede estar en condiciones de decidir si la causa probable del DCL es degenerativa (inicio gradual, progresión insidiosa), vascular (inicio brusco, factores de riesgo vascular, antecedentes de episodios vasculocerebrales), psiquiátrica (antecedentes de depresión, ansiedad, consumo de tóxicos) o secundaria a enfermedades médicas concomitantes (insufi ciencia cardiaca, diabetes, cáncer, etc.).
Patofisiología
Como ya se ha comentado, existen diversas patologías que pueden dar lugar a deterioro cognitivo sin demencia, que comienzan por el posible aporte del propio envejecimiento. Aunque se han propuesto diferentes mecanismos neurobiológicos para explicar el deterioro cognitivo asociado con la edad, lo que implica mecanismos noradrenérgicos y colinérgicos, este tema de enorme interés se encuentra a la espera de una respuesta más convincente. Para ello es necesario establecer defi nitivamente el patrón cognitivo del envejecimiento, mediante una batería estandarizada de pruebas que lo especifi que y el seguimiento longitudinal de una población representativa de individuos.
Además de la influencia del envejecimiento, la presencia de EA en fase prodrómica y de enfermedad cerebrovascular aparecen como las causas más importantes de DCL (94). En un individuo concreto, es probable que ambos o más factores actúen simultáneamente, pero vamos a prestarle atención por separado.
DCL y enfermedad de Alzheimer
Existen diversos estudios que demuestran la relación entre el DCL, especialmente de tipo amnésico, y la EA, desde el punto de vista anatomopatológico (38). Quizás el problema principal surja de las numerosas incógnitas que rodean todavía las alteraciones anatomopatológicas de la EA bien establecida, por lo que al intentar aplicar los conocimientos existentes a un área todavía poco defi nida, como la del DCL, los resultados son todavía más especulativos.
La evidencia más clara hasta ahora consiste en que los sujetos con DCL presentan, por lo general, en estudios post mórtem varios rasgos que los acercan más a los individuos con EA bien establecida, que a los controles sanos, aunque existen diferencias individuales importantes en cuanto a la capacidad de mantener un funcionamiento cognitivo normal con distinta intensidad de alzheimerización cerebral (95-96). Parece, así mismo, que la pérdida neuronal es la alteración que mejor se correlaciona con el deterioro cognitivo, tanto en la EA como en el DCL. Sin embargo, las diferentes opiniones que existen en torno a la importancia relativa de la degeneración neurofi brilar y las placas seniles neuríticas a la hora de defi nir anatomopatológicamente la EA se han trasladado al campo del DCL.
Los estudios sobre población normal revelan que con el paso del tiempo se produce un aumento de la densidad de ovillos neurofi brilares en la corteza entorrinal y en el hipocampo (27), aunque este fenómeno no se acompañaría de pérdida celular ni de deterioro cognitivo signifi cativos. Sin embargo, a partir de este hecho, algunos autores (2,38) sugieren que el paso a DCL se caracterizaría por un aumento anómalo de este fenómeno, acompañado de pérdida celular, especialmente en la capa II de la corteza entorrinal y otras poblaciones neuronales especialmente sensibles a la patología de tipo Alzheimer; mientras otros hacen hincapié en la presencia de placas seniles neuríticas y depósitos amiloides como el rasgo cualitativo más importante que diferencia tanto las fases preclínicas como la de DCL de la enfermedad de Alzheimer del envejecimiento normal (27).
Los resultados neuropatológicos del Nuns Study (97) también han evidenciado la relación existente entre la presencia de deterioro aislado de la memoria y la patología de tipo Alzheimer, especialmente la degeneración neurofi brilar, y han destacado también la importancia de las alteraciones cerebrovasculares, incluso en los sujetos con deterioro aislado de memoria, al excluir del análisis a los casos en los que existían indicios macroscópicos de infarto cerebral.
Los estudios de neuroimagen (tanto estructural como funcional) destacan, así mismo, la presencia de patrones alterados similares a la EA —por ejemplo, disminución en el volumen hipocámpico e hipometabolismo en la corteza temporoparietal—, aunque menos intensos, en una proporción signifi cativa de individuos con DCL de tipo amnésico, de manera que la presencia de dichas alteraciones predice la evolución hacia una demencia bien establecida (98-99).
En cuanto a los hallazgos de tipo genético, se ha informado que la frecuencia de alelo e4 de la ApoE es intermedia entre los controles y los pacientes con EA. Por ejemplo, Kurz (100) encontró que la frecuencia del alelo e4 era de 0,1 en sujetos sanos con quejas subjetivas de memoria, y de 0,24 en individuos con DCL. Por otra parte, los sujetos con DCL que tenían dicho alelo presentan un riesgo signifi cativamente mayor de evolucionar a EA que los que no lo tienen (101). Finalmente, los estudios de tipo bioquímico también han encontrado que los sujetos con DCL presentan unas concentraciones de proteínas tau en el líquido cefalorraquídeo y Aß en el plasma, intermedias entre el envejecimiento y la EA (102).
DCL y enfermedad cerebrovascular
La enfermedad cerebrovascular acompaña frecuentemente al envejecimiento (103), y diversos estudios (104) sugieren que puede desempeñar un papel muy importante en la aparición de demencia en el anciano y no sólo en la demencia vascular, sino también en la EA. Resulta, por lo tanto, bastante lógico pensar que la enfermedad cerebrovascular puede ejercer un papel importante en el DCL, lo que justifi ca los estudios realizados al respecto.
De Carli et al. (105) estudiaron sujetos sin demencia en una muestra comunitaria y compararon los individuos con deterioro en la memoria episódica mayor de 1,5 desvíos estándar con el resto de la muestra en una serie de aspectos, entre ellos neuroimagen y factores de riesgo vascular. Los individuos con DCL mostraron un aumento signifi cativo de factores de riesgo vascular y de lesiones vasculocerebrales. Sin embargo, no se ha podido establecer una relación clara entre la localización de las lesiones y la aparición del défi cit de memoria, aunque la hipótesis más actual apunta a la lesión de circuitos frontosubcorticales, que afectarían la memoria de trabajo (106).
Los datos de Riley et al., ya citados (97), proporcionan datos adicionales en este sentido: incluso en ausencia de infartos macroscópicos, los sujetos con presencia de cambios arterioescleróticos en el polígono de Willis presentaban un riesgo sustancialmente mayor de alteraciones de memoria.
Evolución a demencia
El aspecto crucial del concepto de DCL es su utilidad para predecir la evolución de la demencia. Dentro de los diversos subtipos, el más es tudiado desde este punto de vista es el amnésico, en el que se supone una posible evolución a enfermedad de Alzheimer. Ya se ha comentado que la tasa típica de progresión a EA es del 10% al 15% anual (107-108), aunque hay cierta variabilidad en los resultados debido generalmente a los distintos criterios empleados y a los distintos entornos de aplicación (45,109).
En cuanto a los factores que predicen si va a producirse una evolución, los estudios llevados a cabo van arrojando resultados interesantes. Ya hemos comentado que la presencia de ApoE4 es un factor de riesgo de una progresión más rápida a EA (110-111). También hay aspectos clínicos con poder predictivo. Por ejemplo, la incapacidad del paciente de benefi ciarse de claves semánticas indica una progresión más rápida (66).
Recientemente se ha prestado gran atención a los estudios de neuroimagen. En cuanto a la neuroimagen estructural, se ha encontrado que el grado de atrofi a del hipocampo predice la tasa de conversión (112), especialmente cuando se complementa con otras medidas, como el grado de dilatación ventricular o el grado de atrofi a cerebral global (112).
Por lo que respecta la neuroimagen funcional, algunos trabajos sugieren que la tomografía por emisión de positrones (PET, por su sigla en inglés) con fl uorodesoxiglucosa puede ser un buen marcador tanto de la presencia de DCL amnésico como de su evolución a EA (113). Más recientemente se han llevado a cabo estudios con PET empleando radioligandos, que se acoplan directamente a las placas de ß-amiloide, a la proteína tau o ambos y que permiten visualizar estas proteínas anómalas in vivo.
Una de estas sustancias, el denominado Pittsburg Compound-B (PIB), un derivado de la tiofl avina, parece ser altamente selectivo para las placas de ß-amiloide a las concentraciones empleadas en los estudios de neuroimagen, de manera que los sujetos con EA presentan una retención del PIB entre el 60% y el 90% superior a los controles. Por otra parte, el depósito de PIB se correlaciona bien con las cantidades totales de Aß, y presenta una buena fi abilidad test/retest (variabilidad menor del 10%) (114).
Los últimos resultados parecen situar esta técnica como un buen biomarcador de diagnóstico, pero su utilidad para refl ejar la progresión de la enfermedad y, por lo tanto, ser empleado como un CIVAC ha sido puesta en duda por el resultado de los estudios longitudinales, dado que la deposición de Aß podría alcanzar una fase de meseta años antes de la fase clínica fi nal de la enfermedad (115-116). Otro ligando prometedor es el llamado FDDNP7, con propiedades de unión tanto a placas como a ovillos neurofi brilares, por lo que podría tener un papel como biomarcador de diagnóstico tanto en la EA como en otras taupatías, así como a la hora de predecir la evolución de pacientes con DCL a EA (117-118).
Por ultimo, también merecen interés los estudios acerca de la utilidad de las determinaciones de proteína ß-amiloide y tau en el líquido cefalorraquídeo, que indican que empleando la combinación de cantidades bajas de la primera sustancia y elevadas de la segunda puede predecirse qué sujetos con DCL de tipo amnésico evolucionarán más rápidamente a EA (119). Quizás en un futuro próximo una combinación de varios de estos marcadores permita identifi car con una buena fi abilidad los sujetos que progresarán a demencia.
Terapéutica
Desde el punto de vista clínico, la importancia de defi nir correctamente el DCL proviene sobre todo de la posibilidad de establecer una prevención secundaria de la demencia, dado el gran impacto que puede tener sobre la calidad de vida del paciente y la salud pública la detención o el retraso en el inicio del cuadro demencial (120).
Dada la heterogeneidad del deterioro cognitivo en el anciano, a la hora de progresar en la terapéutica es necesario delimitar cuidadosamente las poblaciones diana. En el momento actual se está trabajando específicamente sobre muestras seleccionadas por su alto riesgo de desarrollar EA o enfermedad cerebrovascular, y ya se han obtenido los primeros resultados, pero todavía no ha podido establecerse la relevancia clínica de tratar el DCL (94).
Opciones terapéuticas vigentes para la EA
En general, se admite que las hipótesis en vigor acerca del tratamiento de la EA son también válidas para el DCL de tipo amnésico, por lo que se han realizado diversos estudios siguiendo las diferentes estrategias terapéuticas utilizadas (121). En lo que respecta al empleo de inhibidores de la colinesterasa (IChE), estas sustancias son, actualmente, el tratamiento más fi rmemente establecido en las fases iniciales de la EA, por lo que también constituyen el grupo idóneo para probar su efi cacia en el DCL de tipo amnésico.
El empleo de IChE se basa en la hipótesis colinérgica de la EA, establecida a partir del hallazgo de la desaferentización colinérgica de la corteza cerebral a consecuencia de la pérdida de neuronas colinérgicas en los núcleos colinérgicos basales, especialmente en el núcleo de Meynert (122). En este sentido, se ha encontrado en estudios post mórtem una disminución similar de marcadores colinérgicos en sujetos con DCL y EA en fase inicial, comparados con individuos sin deterioro cognitivo (123), lo que avalaría el empleo de sustancias colinérgicas en ambas entidades.
Sin embargo, existen otros estudios recientes que cuestionan el papel exacto de los IChE en el tratamiento del DCL. Davis et al. (124) han informado que el défi cit colinérgico aparece más tarde de lo que inicialmente se pensaba en la EA, y DeKosky et al. (125) han encontrado un aumento de la actividad de la colinoacetiltransferasa en zonas específi cas en sujetos con DCL, lo que sugiere que en esta fase inicial los sistemas de neurotransmisión son capaces todavía de una actividad compensatoria.
Los tres IChE actualmente empleados (donepezilo, rivastigmina y galantamina) son candidatos para el tratamiento del DCL, aunque presentan diferencias entre ellos tanto farmacocinéticas como farmacológicas, y carecemos de información sobre si estas tendrán relevancia en el tratamiento del DCL. En estos momentos contamos con resultados de diversos estudios multicéntricos a gran escala con galantamina (GALINT- 11 y 18) (126-127), donepezilo (Memory Impairment Study) (110) y rivastigmina (Investigation into Delay to Diagnosis of Alzheimer’s Disease with Exelon®, InDDEx) (128), para comprobar su efi cacia a la hora de disminuir la tasa de conversión de DCL en EA. A continuación resumiremos algunos de los resultados más interesantes.
La galantamina ha sido objeto de dos estudios multicéntricos internacionales aleatorizados, doble ciego y controlados con placebo para valorar la capacidad de esta sustancia de retrasar la conversión de DCL de tipo amnésico —medido por una CDR de 0,5— a EA (CDR de 1) a lo largo de dos años.
También se emplearon como variables secundarias mediciones de escalas cognitivas y de funcionamiento global. Participaron un total de 2.048 sujetos en ambos estudios, con una edad media de 70 años. La tasa de sujetos con ApoE4 fue del 43%. No se apreció una disminución de la tasa de conversión con galantamina en ninguno de los dos estudios, aunque sí se observó en ambos una tendencia no signifi cativa a reducir la tasa de progresión (13% galantamina contra 18% placebo y 17% galantamina contra 21% placebo).
En uno de los estudios se exploró con resonancia magnética, y sus resultados sugieren que la galantamina disminuyó la progresión de atrofi a cerebral a lo largo de los dos años. Por lo tanto, aunque no se apreciaron resultados signifi cativos, estos estudios sugieren que la galantamina puede resultar efi caz. Hay que señalar que se apreció un aumento de la mortalidad en el grupo tratado con la sustancia activa, que puede deberse a una inesperada baja mortalidad en el grupo control.
El estudio con donepezilo fue realizado por el Instituto Nacional de Envejecimiento de Estados Unidos estadounidense, en 69 centros de ese país y Canadá, a través de su consorcio de centros para el estudio de la EA, llamado Alzheimer’s Disease Cooperative Study (ADCS). Este estudio se realizó sobre 769 pacientes con DCL amnésico, asignados aleatoriamente a tres ramas tratadas con placebo, donepezilo y vitamina E. El objetivo primario fue el diagnóstico de EA, y los secundarios incluían una serie de medidas de funcionamiento cognitivo, índices de calidad de vida y evaluaciones farmacoeconómicas. Los participantes fueron evaluados a lo largo de tres años y se realizaron análisis de supervivencia para determinar los efectos del tratamiento. La tasa anual de conversión a EA fue del 16%. A lo largo del estudio, 214 casos progresaron a demencia, de los que 212 fueron diagnosticados de posible o probable EA.
Los análisis fi nales indicaron que no había diferencias signifi cativas entre los tres grupos al cabo de los tres años. Sin embargo, al efectuar análisis parciales de la evolución en períodos de seis meses se encontró que el grupo de donepezilo presentaba un menor riesgo de conversión a EA durante los primeros doce meses de estudio. Además, al estratifi car los efectos del tratamiento según el genotipo de la ApoE, pudo comprobarse que en los portadores de ApoE4 el efecto protector se prolongaba durante 24 meses. Este hallazgo es importante, dado que el 76% de todos los casos que evolucionaron hacia EA eran portadores de ApoE4.
Los análisis de las variables secundarias confi rmaron estos resultados: las medidas cognitivas y los índices funcionales evolucionaban mejor en el grupo de donepezilo durante los primeros 12 a 18 meses, y estos efectos eran más acentuados en los portadores de ApoE4. Los autores concluyeron que aunque no puede realizarse una indicación general de tratamiento con donepezilo para los sujetos con DCL de tipo amnésico, esta posibilidad debía discutirse individualmente con cada caso.
Otro estudio de grandes dimensiones evaluó en catorce países la efi cacia de la rivastigmina en 1.018 sujetos con DCL de tipo amnésico, para disminuir la tasa de progresión a EA a lo largo de dos años. Sin embargo, debido a una inesperada baja tasa de conversión, el estudio se prolongó hasta cuatro años. En este período, el 17,3% de los casos tratados con rivastigmina evolucionaron a EA, mientras que en el grupo placebo lo hizo el 21,4%, una diferencia no signifi cativa. Tampoco se apreciaron diferencias en las variables de tipo cognitivo. La tasa de portadores de ApoE4 fue del 41%. En este estudio se incluyó un número demasiado alto de casos con comorbilidad, entre ellos casos con depresión, lo que puede haber contribuido a la baja tasa de progresión a EA, de sólo un 9% anual. La gran mayoría de los casos que evolucionaron a demencia fueron diagnosticados de EA.
Por otra parte, ya se dispone de datos sobre el tratamiento del DCL amnésico per se, realizados con el objetivo de mejorar el deterioro cognitivo de los sujetos afectados, aunque proceden todavía de presentaciones en reuniones científi cas. Salloway et al. (129) llevaron a cabo un estudio doble ciego controlado con placebo de seis meses de duración sobre la efi cacia y tolerabilidad de donepezilo a dosis de 10 mg/día en pacientes con DCL de tipo amnésico (CDR: 0,5; MMSE=24), y obtuvieron diferencias signifi cativas en la puntuación total de la ADAS-Cog y otras escalas cognitivas empleadas a favor de donepezilo, sin que se apreciaran efectos adversos de importancia. En el estudio se utilizó una serie amplia de pruebas neuropsicológicas, y una de las conclusiones interesantes es que la ADASCog puede ser utilizada también en esta población para la valoración de la efi cacia terapéutica.
Por otra parte, las sustancias glutamatérgicas también se han revelado efectivas en el tratamiento de la EA, aunque sobre todo en las fases avanzadas. Una de las causas de neurotoxicidad implicadas en la EA es la actividad excesiva del neurotransmisor excitatorio glutamato. Teóricamente, el bloqueo o la modulación de los receptores glutamatérgicos N-metil-D-aspartato (NMDA) podría prevenir o aminorar el daño excitotóxico.
También, se ha establecido que la excitotoxicidad medida por el receptor NMDA aumenta la fosforilación de la protína tau, y por lo tanto, puede estar implicada en la degeneración neurofi brilar (130). La memantina, un antagonista del receptor de NMDA, ha estado disponible en Alemania durante más 20 años, y fue una de las primeras sustancias en ser estudiadas en la EA. Hasta ahora, está aprobado su uso en EA moderadamente avanzada (131), aunque también existen datos sobre su acción neuroprotectora, por lo que podría ser útil en el DCL (132-133). Otra vía para modular la neurotransmisión glutamatérgica consiste en actuar a través de los receptores AMPA; actualmente se está llevando a cabo un estudio con la ampakina CX516 en DCL, avalado por los resultados previos sobre el efecto positivo de dicha sustancia sobre la memoria y otros procesos cognitivos (134).
Otras estrategias
En cuanto a otras estrategias, la posibilidad de tratamiento del DCL con estrógenos ha recibido un serio revés, con la publicación de estudios con resultados negativos, tanto a la hora de prevenir la evolución a demencia como de mejorar el rendimiento cognitivo (135-136). La hipótesis del estrés oxidativo también ha merecido crédito sufi ciente como para realizar estudios en DCL, y existe un estudio importante con Ginkgo biloba (Ginkgo Evaluation of Memory Study: the GEM Study) 8, actualmente a la espera de publicar sus resultados defi nitivos (137-138).
Asimismo, se están haciendo trabajos con fármacos antiinfl amatorios no esteroideos (AINES) (139), basados en los hallazgos epidemiológicos acerca de una disminución de la incidencia de EA en sujetos que tomaban de forma mantenida estas sustancias por otra indicación (140). Por otra parte, existen datos de que este efecto benefi cioso aparecería únicamente en sujetos que no han desarrollado la enfermedad, ya que no se ha observado en pacientes con demencia bien establecida (141-142).
En concreto, el tratamiento con inhibidores de la ciclo-oxigenesa II (COX-2) podría ser interesante, dado que se ha sugerido que dicha enzima, que se expresa en tejido cerebral, puede estar implicada en procesos neurodegenerativos. Sin embargo, un estudio que evaluó la efi cacia del rofecoxib para prevenir la conversión a EA en sujetos con EA no ha dado resultados positivos (143). Finalmente, se ha sugerido la posibilidad de volver a emplear sustancias como el piracetam o la citicolina, descartadas en el tratamiento de la EA, pero que quizás puedan ser benefi ciosas en sujetos con DCL (144-145). No obstante, no se cuenta con datos sufi cientes, y serían necesarios nuevos estudios que empleen los criterios de diagnóstico de DCL actuales.
Tratamiento de factores de riesgo
Dado que la enfermedad cerebrovascular es un factor importante en el desarrollo de demencia, parece lógico pensar que el control de los factores de riesgo vasculares puede tener un efecto benefi cioso sobre el DCL, a la hora de mejorar sus síntomas o retrasar la aparición de demencia. En un estudio sobre población general se ha encontrado que el empleo de diuréticos como medicación antihipertensiva produce una disminución del 40% en el riesgo relativo de padecer demencia (146).
En el estudio Syst-Eur (147), realizado en varios países europeos, el tratamiento con nitrendipina, un antihipertensivo bloqueante de los canales del calcio, se asoció con una reducción del 50% en la frecuencia de demencia en una población de 200 ancianos con hipertensión sistólica aislada. Sin embargo, un estudio similar llevado a cabo en el Reino Unido no mostró benefi cio alguno en cuanto a mejora del funcionamiento cognitivo con el paso del tiempo (148).
En fechas recientes, tres estudios epidemiológicos retrospectivos han coincidido a la hora de señalar que las estatinas —sustancias que disminuyen el colesterol plasmático— podrían reducir el riesgo de desarrollar EA en un 70% (149-151). Además, existen otros trabajos que aportan datos complementarios en la misma dirección. Un estudio observacional sobre 1.037 mujeres postmenopáusicas con enfermedad coronaria encontró que las concentraciones altas de lipoproteína de baja densidad (LDL) y colesterol total se asociaban con deterioro cognitivo (153).
Otro estudio sobre una serie de autopsias en 218 hombres de etnia japonesa que formaban parte del Honolulu-Asia Aging Study encontró una fuerte asociación entre las concentraciones de colesterol de alta densidad (HDL) en las fases avanzadas de la vida y el número de placas neuríticas y ovillos neurofi brilares en el cerebro (153). El aumento del colesterol en el plasma puede estar asociado con un incremento en la tasa de producción de sustancia ß-amiloide (154), aunque se desconoce el mecanismo exacto por el que las estatinas podrían infl uir en la evolución de la EA.
Es probable que se relacione con actividad regulatoria microvascular, ya que sus efectos benefi ciosos aparecen con independencia de las cantidades de lípidos. Estos hallazgos han proporcionado la base para diversos estudios actualmente en curso sobre la capacidad de las estatinas de actuar tanto sobre la progresión de la EA9 (155) como en la prevención de la evolución del DCL hacia la EA.
Por lo que respecta a otros factores de riesgo, un estudio en una población comunitaria encontró una asociación signifi cativa entre la incidencia de EA y concentraciones bajas de vitamina B12 y folatos (156), lo que se relaciona con el papel de estas sustancias en la prevención del estrés oxidativo. Así mismo, se ha informado que las cantidades elevadas de homocisteína —un marcador de defi ciencia de vitamina B12 y ácido fólico— constituyen un predictor independiente de deterioro cognitivo en ancianos sanos (157). Estos hallazgos abren la puerta a estudios como el que se está realizando actualmente a cargo del grupo ADCS, con la fi nalidad de comprobar el efecto de la administración de folatos y vitaminas B6 y B12 sobre la progresión del défi cit cognitivo en la EA (158).
Conclusiones
La presencia de pacientes que pueden englobarse en la categoría de DCL es un hecho frecuente en la clínica, y a medida que la población envejece, va a constituir sin duda un motivo cada vez más habitual de consulta. El diagnóstico de DCL no presenta grandes difi cultades al aplicar los criterios actualmente en vigor, pero los problemas surgen a la hora de establecer un patrón adecuado para el manejo de estos casos.
Actualmente, el subtipo amnésico es el mejor estudiado, y se debate su inclusión en el DSM-V (159). La utilidad del diagnóstico de DCL amnésico deriva principalmente de su capacidad de seleccionar un grupo de pacientes con un riesgo más alto de presentar EA en fase demencial. Esta capacidad mejorará, sin duda, en el momento en que se disponga de un marcador o conjunto de marcadores fi able para la enfermedad.
Una vez que el paciente ha sido diagnosticado, surge el problema de comunicarle el diagnóstico y los riesgos asociados, así como de ofrecerle una pauta razonable de actuación. Es evidente que un elemento básico es la revisión periódica, con la fi nalidad de objetivar la evolución a demencia.
En este momento no existe un tratamiento farmacológico aprobado para el DCL, pero puede plantearse de forma individualizada en pacientes con características especiales. Por ejemplo, una prueba terapéutica con un IChE puede estar indicada en el caso de un sujeto relativamente joven y con responsabilidades laborales o familiares, o si existen antecedentes familiares sobresalientes. También puede realizarse un abordaje preventivo sobre los factores de riesgo (p. ej., dieta, ejercicio físico, etc.) o bien intentar optimizar el rendimiento cognitivo con estrategias no farmacológicas, fomentando la actividad intelectual.
En cualquier caso, el paciente debe conocer cuáles son las implicaciones del diagnóstico, sobre todo, en términos de la tasa esperable de conversión a demencia, y recibir consejo al respecto. Dada la expectativa razonable de que en un tiempo relativamente corto existan abordajes terapéuticos más efi caces para la EA, el diagnóstico de DCL también permitirá iniciar estos tratamientos de forma rápida, aprovechando una probable ventana terapéutica de estas nuevas intervenciones.
3 Hemos preferido el adjetivo ligero en lugar de leve, empleado a veces en este contexto, para evitar la implicaciones pronósticas del último en la terminología médica en castellano.
4 En concreto, el Quality Standards Subcommitte of the American Academy of Neurology.
5 Por ejemplo, puede existir un efecto de aprendizaje de las pruebas empleadas para medir el funcionamiento cognitivo y un efecto de selección positiva de los sujetos menos deteriorados conforme avanza el estudio.
6 Supuso el reconocimiento de la importancia de la EA como causa predominante de demencia en el anciano.
7 2-(1-{6-[(2-[F-18] fluoroetil)(metil)amino]-2-naftil}etllideno) malononitrilo.
8 Se trata de un estudio doble ciego, controlado con placebo, en ramas paralelas, sobre población sana o con DCL, prospectivo a cinco años de evolución. La fase de reclutamiento finalizó en mayo de 2002. Los seis centros participantes en Estados Unidos incluyeron un total de 3.074 sujetos.
9 Por ejemplo el estudio Cholesterol Lowering Agent to Slow Progression of Alzheimer’s Disease (CLASP), realizado en Estados Unidos con una metodología doble ciego controlado con placebo, y coordinado por Mary Sano, en el que se valora la eficacia de la simvastatina para retrasar la progresión de la EA en 400 sujetos tratados con el régimen de atención estándar.
Referencias
1. Levy R. Aging-associated cognitive decline. Working Party of the International Psychogeriatric Association in collaboration with the World Health Organization. Int Psychogeriatr. 1994;6(1):63-68. [ Links ]
2. Braak H, Braak E. Evolution of the neuropathology of Alzheimer’s disease. Acta Neurol Scand Suppl. 1996;165:3- 12. [ Links ]
3. Linn RT, Wolf PA, Bachman DL, Knoefel JE, Cobb JL, Belanger AJ, et al. The ‚preclinical phase‘ of probable Alzheimer‘s disease. A 13-year prospective study of the Framingham cohort. Arch Neurol. 1995;52(5):485-90. [ Links ]
4. Crook T, Bartus RT, Ferris SH, Whitehouse P, Cohen GD, Gershon S. Age-associated memory impairment: proposed diagnostic criteria and measures of clinical change. Report of a NIMH Work Group. Development Neuropsychology. 1986;2:261-76. [ Links ]
5. Crook T. Diagnosis and treatment of memory loss in older patients who are not demented. In: Levy R, Howard R, Burns A, editors. Treatment and care in old age psychiatry. Londres: Wrightson Biomedical; 2003. p. 95-111. [ Links ]
6. Blackford R, La Rue A. Criteria for diagnosing age-associated memory impairment: proposed improvements from the field. Development Neuropsychology. 1989;5:295-306. [ Links ]
7. American Psychiatric Association. Diagnostic and statistical manual of mental disorders. 4th ed. Text Revision (DSM-IV-TR). Washington: APA; 2000. [ Links ]
8. Blesa R, Adroer R, Santacruz P, Ascaso C, Tolosa E, Oliva R. High apolipoprotein E epsilon 4 allele frequency in age-related memory decline. Ann Neurol. 1996;39(4):548-51. [ Links ]
9. Kral VA. Senescent forgetfulness: benign and malignant. Can Med Assoc J 1962;86:257-60. [ Links ]
10. Small SA, Perera GM, DelaPaz R, Mayeux R, Stern Y. Differential regional dysfunction of the hippocampal formation among elderly with memory decline and Alzheimer‘s disease. Ann Neurol. 1999;45(4):466-72. [ Links ]
11. Berent S, Giordani B, Foster N, Minoshima S, Lajiness-O’Neill R, Koeppe R, et al. Neuropsychological function and cerebral glucose utilization in isolated memory impairment and Alzheimer’s disease. J Psychiatr Res. 1999;33(1):7- 16. [ Links ]
12. Bowen J, Teri L, Kukull W, McCormick W, McCurry SM, Larson EB. Progression to dementia in patients with isolated memory loss. Lancet. 1997;349(9054):763-65. [ Links ]
13. Gurland BJ, Copeland JR, Kuriansky J, Kelleher M, Sharpe L, Dean LL. The mind and mood of ageing: mental health problems of community elderly in New York and London. New York: Haworth Press; 1983. [ Links ]
14. Reisberg B, FerrisSH, de León MJ, Crook T. The Global Deterioration Scale for assessment of primary degenerative dementia. Am J Psychiatry. 1982;139(9):1136-9. [ Links ]
15. Petersen RC, Smith GE, Waring SC, Ivnik RJ, Tangalos EG. Mild cognitive impairment: clinical characterization and outcome. Arch Neurol. 1999;56(3):303-8. [ Links ]
16. Roth M, Tym E, Mountjoy CQ, Huppert FA, Hendrie H, Verma S, et al. CAMDEX: a standardised instrument for the diagnosis of mental disorder in the elderly with special reference to the early detection of dementia. Br J Psychiatry. 1986;149:698-709. [ Links ]
17. Roth M, Huppert FA, Tym E, Mountjoy CQ. (CAMDEX): The Cambridge Examination for Mental Disorders of the Elderly. Cambridge: Cambridge University Press; 1988. [ Links ]
18. Organización Mundial de la Salud. CIE-10: trastornos mentales y del comportamiento. Madrid: Meditor; 1992. [ Links ]
19. American Psychiatric Association (APA). DSM-IV: manual diagnóstico y estadístico de los trastornos mentales. Madrid: Masson; 1995. [ Links ]
20. Morris JC, Edland S, Clark C, Galasko D, Koss E, Mohs R, et al. The consortium to establish a registry for Alzheimer’s disease (CERAD). Part IV. Rates of cognitive change in the longitudinal assessment of probable Alzheimer’s disease. Neurology. 1993;43(12):2457-65. [ Links ]
21. Hughes CP, Berg L, Danziger WL, Coben LA, Martin RL. A new clinical scale for the staging of dementia. Br J Psychiatry. 1982;140:566-72. [ Links ]
22. Collie A, Maruff P. An analysis of systems of classifying mild cognitive impairment in older people. Aust N Z J Psychiatry. 2002;36(1):133-40. [ Links ]
23. Kantarci K, Reynolds G, Petersen RC, Boeve BF, Knopman DS, Edland SD, et al. Proton MR spectroscopy in mild cognitive impairment and Alzheimer disease: comparison of 1.5 and 3 T. AJNR Am J Neuroradiol. 2003;24(5):843-9. [ Links ]
24. Petersen RC, Stevens JC, Ganguli M, Tangalos EG, Cummings JL, DeKosky ST. Practice parameter: early detection of dementia: mild cognitive impairment (an evidence-based review). Report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology. 2001;56(9):1133-42. [ Links ]
25. Schaie KW. The hazards of cognitive aging. Gerontologist. 1989;29(4):484- 93. [ Links ]
26. Rubin EH, Storandt M, Miller JP, Grant EA, Kinscherf DA, Morris JC, et al. Influence of age on clinical and psychometric assessment of subjects with very mild or mild dementia of the Alzheimer type. Arch Neurol. 1993;50(4):380-3. [ Links ]
27. Morris JC, Price AL. Pathologic correlates of nondemented aging, mild cognitive impairment, and early-stage Alzheimer‘s disease. J Mol Neurosci. 2001;17(2):101-18. [ Links ]
28. Hickman SE, Howieson DB, Dame A, Sexton G, Kaye J. Longitudinal analysis of the effects of the aging process on neuropsychological test performance in the healthy young-old and oldest-old. Dev Neuropsychol. 2000;17(3):323-37. [ Links ]
29. Rubin EH, Storandt M, Miller JP, Kinscherf DA, Grant EA, Morris JC, et al. A prospective study of cognitive function and onset of dementia in cognitively healthy elders. Arch Neurol. 1998;55(3):395-401. [ Links ]
30. Collie A, Maruff P, Shafiq-Antonacci R, Smith M, Hallup M, Schofield PR, et al. Memory decline in healthy older people: implications for identifying mild cognitive impairment. Neurology. 2001;56(11):1533-8. [ Links ]
31. Howieson DB, Camicioli R, Quinn J, Silbert LC, Care B, Moore MM, et al. Natural history of cognitive decline in the old. Neurology. 2003;60(9):1489- 94. [ Links ]
32. Tomlinson BE, Blessed G, Roth M. Observations on the brains of nondemented old people. J Neurol Sci. 1968;7(2):331-56. [ Links ]
33. Khachaturian ZS. Diagnosis of Alzheimer‘s disease. Arch Neurol. 1985;42(11):1097-105. [ Links ]
34. Mirra SS, Heyman A, McKeel D, Sumi SM, Crain BJ, Brownlee LM et al. The Consortium to Establish a Registry for Alzheimer‘s Disease (CERAD). Part II. Standardization of the neuropathologic assessment of Alzheimer‘s disease. Neurology 1991; 41(4):479-486. [ Links ]
35. Newell KL, Hyman BT, Growdon JH, Hedley-Whyte ET. Application of the National Institute on Aging (NIA)-Reagan Institute criteria for the neuropathological diagnosis of Alzheimer disease. J Neuropathol Exp Neurol 1999; 58(11):1147-1155. [ Links ]
36. Morris JC, Storandt M, McKeel DW Jr., Rubin EH, Price JL, Grant EA, et al. Cerebral amyloid deposition and diffuse plaques in „normal“ aging: evidence for presymptomatic and very mild Alzheimer‘s disease. Neurology. 1996;46(3):707-19. [ Links ]
37. Haroutunian V, Perl DP, Purohit DP, Marin D, Khan K, Lantz M, et al. Regional distribution of neuritic plaques in the nondemented elderly and subjects with very mild Alzheimer disease. Arch Neurol. 1998;55(9):1185-91. [ Links ]
38. Gómez-Isla T, Hyman T. Neuropathological changes in normal aging, mild cognitive impairment and Alzheimer’s disease. In: Petersen RC, editor. Mild cognitive impairment. New York: Oxford University Press; 2003. p. 191- 204. [ Links ]
39. Kordower JH, Chu Y, Stebbins GT, De- Kosky ST, Cochran EJ, Bennett D, et al. Loss and atrophy of layer II entorhinal cortex neurons in elderly people with mild cognitive impairment. Ann Neurol. 2001;49(2):202-13. [ Links ]
40. Price JL, Ko AI, Wade MJ, Tsou SK, McKeel DW, Morris JC. Neuron number in the entorhinal cortex and CA1 in preclinical Alzheimer disease. Arch Neurol. 2001;58(9):1395-1402. [ Links ]
41. Smith G, Ivnik RJ, Petersen RC, Malec JF, Kokmen E, Tangalos E. Age-associated memory impairment diagnoses: problems of reliability and concerns for terminology. Psychol Aging. 1991;6(4):551-8. [ Links ]
42. Bischkopf J, Busse A, Angermeyer MC. Mild cognitive impairment: a review of prevalence, incidence and outcome according to current approaches. Acta Psychiatr Scand. 2002;106(6):403-14. [ Links ]
43. Caine ED. Should aging-associated cognitive decline be included in DSMIV? J Neuropsychiatry Clin Neurosci. 1993;5(1):1-5. [ Links ]
44. Hanninen T, Hallikainen M, Koivisto K, Helkala EL, Reinikainen KJ, Soininen H, et al. A follow-up study of age-associated memory impairment: neuropsychological predictors of dementia. J Am Geriatr Soc. 1995;43(9):1007-15. [ Links ]
45. Ritchie K, Artero S, Touchon J. Classification criteria for mild cognitive impairment: a population-based validation study. Neurology. 2001;56(1):37-42. [ Links ]
46. Christensen H, Henderson AS, Jorm AF, Mackinnon AJ, Scott R, Korten AE. ICD-10 mild cognitive disorder: epidemiological evidence on its validity. Psychol Med. 1995;25(1):105-20. [ Links ]
47. Christensen H, Henderson AS, Korten AE, Jorm AF, Jacomb PA, Mackinnon AJ. ICD-10 mild cognitive disorder: its outcome three years later. Int J Geriatr Psychiatry. 1997;12(5):581-6. [ Links ]
48. Di Carlo A, Baldereschi M, Amaducci L, Maggi S, Grigoletto F, Scarlato G, et al. Cognitive impairment without dementia in older people: prevalence, vascular risk factors, impact on disability. The Italian Longitudinal Study on Aging. J Am Geriatr Soc. 2000;48(7):775-82. [ Links ]
49. Celsis P, Agniel A, Cardebat D, Demonet JF, Ousset PJ, Puel M. Age related cognitive decline: a clinical entity?: a longitudinal study of cerebral blood flow and memory performance. J Neurol Neurosurg Psychiatry. 1997;62(6):601-8. [ Links ]
50. Ebly EM, Parhad IM, Hogan DB, Fung TS. Prevalence and types of dementia in the very old: results from the Canadian Study of Health and Aging. Neurology. 1994;44(9):1593-1600. [ Links ]
51. Ebly EM, Hogan DB, Parhad IM. Cognitive impairment in the nondemented elderly. Results from the Canadian Study of Health and Aging. Arch Neurol. 1995;52(6):612-9. [ Links ]
52. Gurland BJ, Dean LL, Copeland J, Gurland R, Golden R. Criteria for the diagnosis of dementia in the community elderly. Gerontologist. 1982;22(2):180- 6. [ Links ]
53. Devanand DP, Folz M, Gorlyn M, Moeller JR, Stern Y. Questionable dementia: clinical course and predictors of outcome. J Am Geriatr Soc. 1997;45(3):321-8. [ Links ]
54. Daly E, Zaitchik D, Copeland M, Schmahmann J, Gunther J, Albert M. Predicting conversion to Alzheimer disease using standardized clinical information. Arch Neurol. 2000;57(5):675- 80. [ Links ]
55. Cooper B, Bickel H, Schaufele M. Early development and progression of dementing illness in the elderly: a general-practice based study. Psychol Med. 1996;26(2):411-9. [ Links ]
56. Paykel ES, Brayne C, Huppert FA, Gill C, Barkley C, Gehlhaar E, et al. Incidence of dementia in a population older than 75 years in the United Kingdom. Arch Gen Psychiatry. 1994;51(4):325-32. [ Links ]
57. Reisberg B, Ferris SH, Shulman E, Steinberg G, Buttinger C, Sinaiko E, et al. Longitudinal course of normal aging and progressive dementia of the Alzheimer‘s type: a prospective study of 106 subjects over a 3.6 year mean interval. Prog Neuropsychopharmacol Biol Psychiatry. 1986;10(3-5):571-8. [ Links ]
58. Flicker C, Ferris SH, Reisberg B. Mild cognitive impairment in the elderly: predictors of dementia. Neurology. 1991;41(7):1006-9. [ Links ]
59. Petersen RC, Doody R, Kurz A, Mohs RC, Morris JC, Rabins PV, et al. Current concepts in mild cognitive impairment. Arch Neurol. 2001;58(12):1985-92. [ Links ]
60. Petersen RC. Conceptual overview. In: Petersen RC, editor. Mild cognitive impairment: aging to Alzheimer‘s disease. New York: Oxford University Press; 2003. p. 1-14. [ Links ]
61. Chui H. Vascular dementia, a new beginning: shifting focus from clinical phenotype to ischemic brain injury. Neurol Clin. 2000;18(4):951-78. [ Links ]
62. Winblad B, Palmer K, Kivipelto M, Jelic V, Fratiglioni L, Wahlund LO, et al. Mild cognitive impairment--beyond controversies, towards a consensus: report of the International Working Group on Mild Cognitive Impairment. J Intern Med. 2004;256(3):240-6. [ Links ]
63. Petersen RC. Mild cognitive impairment as a diagnostic entity. J Intern Med. 2004;256(3):183-94. [ Links ]
64. Petersen RC. Mild cognitive impairment: current research and clinical implications. Semin Neurol. 2007;27(1):22-31. [ Links ]
65. Portet F, Ousset PJ, Visser PJ, Frisoni GB, Nobili F, Scheltens P, et al. Mild cognitive impairment (MCI) in medical practice: a critical review of the concept and new diagnostic procedure. Report of the MCI Working Group of the European Consortium on Alzheimer‘s Disease. J Neurol Neurosurg Psychiatry. 2006;77(6):714-8. [ Links ]
66. Dubois B, Albert ML. Amnestic MCI or prodromal Alzheimer‘s disease? Lancet Neurol. 2004;3(4):246-8. [ Links ]
67. Schroder J, Kratz B, Pantel J, Minnemann E, Lehr U, Sauer H. Prevalence of mild cognitive impairment in an elderly community sample. J Neural Transm Suppl. 1998;54:51-9. [ Links ]
68. Graham JE, Rockwood K, Beattie BL, Eastwood R, Gauthier S, Tuokko H, et al. Prevalence and severity of cognitive impairment with and without dementia in an elderly population. Lancet. 1997;349(9068):1793-6. [ Links ]
69. Andersen K, Lolk A, Nielsen H, Andersen J, Olsen C, Kragh-Sorensen P. Prevalence of very mild to severe dementia in Denmark. Acta Neurol Scand. 1997;96(2):82-7. [ Links ]
70. Frisoni GB, Fratiglioni L, Fastbom J, Guo Z, Viitanen M, Winblad B. Mild cognitive impairment in the population and physical health: data on 1,435 individuals aged 75 to 95. J Gerontol A Biol Sci Med Sci. 2000;55(6):M322- M328. [ Links ]
71. Ganguli M, Dodge HH, Chen P, Belle S, DeKosky ST. Ten-year incidence of dementia in a rural elderly US community population: the MoVIES Project. Neurology. 2000;54(5):1109-16. [ Links ]
72. Albert MS, Moss MB, Tanzi R, Jones K. Preclinical prediction of AD using neuropsychological tests. J Int Neuropsychol Soc. 2001;7(5):631-9. [ Links ]
73. Smith GE, Petersen RC, Ivnik RJ, Malec JF, Tangalos EG. Subjective memory complaints, psychological distress, and longitudinal change in objective memory performance. Psychol Aging. 1996;11(2):272-9. [ Links ]
74. Snowdon DA, Kemper SJ, Mortimer JA, Greiner LH, Wekstein DR, Markesbery WR. Linguistic ability in early life and cognitive function and Alzheimer‘s disease in late life. Findings from the Nun Study. JAMA. 1996;275(7):528-32. [ Links ]
75. Buschke H, Kuslansky G, Katz M, Stewart WF, Sliwinski MJ, Eckholdt HM, et al. Screening for dementia with the memory impairment screen. Neurology. 1999;52(2):231-8. [ Links ]
76. Robbins TW, James M, Owen AM, Sahakian BJ, McInnes L, Rabbitt P. Cambridge Neuropsychological Test Automated Battery (CANTAB): a factor analytic study of a large sample of normal elderly volunteers. Dementia. 1994;5(5):266-81. [ Links ]
77. Grober E, Merling A, Heimlich T, Lipton RB. Free and cued selective reminding and selective reminding in the elderly. J Clin Exp Neuropsychol. 1997;19(5):643-54. [ Links ]
78. Zaudig M, Mittelhammer J, Hiller W, Pauls A, Thora C, Morinigo A, et al. SIDAM--A structured interview for the diagnosis of dementia of the Alzheimer type, multi-infarct dementia and dementias of other aetiology according to ICD-10 and DSM-III-R. Psychol Med. 1991;21(1):225-36. [ Links ]
79. Brazzelli M, Capitani E, Della SS, Spinnler H, Zuffi M. A neuropsychological instrument adding to the description of patients with suspected cortical dementia: the Milan overall dementia assessment. J Neurol Neurosurg Psychiatry. 1994;57(12):1510-17. [ Links ]
80. Galluzzi S, Cimaschi L, Ferrucci L, Frisoni GB. Mild cognitive impairment: clinical features and review of screening instruments. Aging (Milano). 2001;13(3):183-202. [ Links ]
81. Gifford DR, Cummings JL. Evaluating dementia screening tests: methodologic standards to rate their performance. Neurology. 1999;52(2):224-7. [ Links ]
82. Knopman DS, Kahn J, Miles S. Clinical research designs for emerging treatments for Alzheimer disease: moving beyond placebo-controlled trials. Arch Neurol. 1998;55(11):1425-9. [ Links ]
83. Crithley M. The parietal lobes. New York: Hafner; 2004. [ Links ]
84. Cacho J, García-García R, Arcaya J, Vicente JL, Lantada N. Una propuesta de aplicación y puntuación del test del reloj en la enfermedad de Alzheimer. Rev Neurol. 1999;28(7):648-55. [ Links ]
85. Folstein MF, Folstein SE, McHugh PR. “Mini-mental state”: a practical method for grading the cognitive state of patients for the clinician. J Psychiatr Res. 1975;12(3):189-98. [ Links ]
86. Lobo A, Saz P, Marcos G, Dia JL, de la Cámara C, Ventura T, et al. Revalidation and standardization of the cognition mini-exam (first Spanish version of the Mini-Mental Status Examination) in the general geriatric population]. Med Clin (Barc). 1999;112(20):767-74. [ Links ]
87. Katzman R, Brown T, Fuld P, Peck A, Schechter R, Schimmel H. Validation of a short Orientation-Memory-Concentration Test of cognitive impairment. Am J Psychiatry. 1983;140(6):734-9. [ Links ]
88. Teng EL, Chui HC. The Modified Mini- Mental State (3MS) examination. J Clin Psychiatry. 1987;48(8):314-8. [ Links ]
89. Inouye SK, van Dyck CH, Alessi CA, Balkin S, Siegal AP, Horwitz RI. Clarifying confusion: the confusion assessment method. A new method for detection of delirium. Ann Intern Med. 1990;113(12):941-8. [ Links ]
90. Morris JN, Fries BE, Mehr DR, Hawes C, Phillips C, Mor V, et al. MDS Cognitive Performance Scale. J Gerontol. 1994;49(4):M174-M182. [ Links ]
91. López PS, Llinás J, Amiel J, Vidal C, Vilalta J. [CAMDEX: a new psychogeriatric interview]. Actas Luso Esp Neurol Psiquiatr Cienc Afines. 1990;18(5):290-5. [ Links ]
92. Jorm AF. A short form of the Informant Questionnaire on Cognitive Decline in the Elderly (IQCODE): development and cross-validation. Psychol Med. 1994;24(1):145-53. [ Links ]
93. Morales JM, González-Montalvo JI, Bermejo F, Del Ser T. The screening of mild dementia with a shortened Spanish version of the “Informant Questionnaire on Cognitive Decline in the Elderly”. Alzheimer Dis Assoc Disord. 1995;9(2):105-11. [ Links ]
94. DeCarli C. Mild cognitive impairment: prevalence, prognosis, aetiology, and treatment. Lancet Neurol. 2003;2(1):15-21. [ Links ]
95. Petersen RC, Parisi JE, Dickson DW, Johnson KA, Knopman DS, Boeve BF, et al. Neuropathologic features of amnestic mild cognitive impairment. Arch Neurol. 2006;63(5):665-72. [ Links ]
96. Jicha GA, Parisi JE, Dickson DW, Johnson K, Cha R, Ivnik RJ, et al. Neuropathologic outcome of mild cognitive impairment following progression to clinical dementia. Arch Neurol. 2006;63(5):674-81. [ Links ]
97. Riley KP, Snowdon DA, Markesbery WR. Alzheimer’s neurofibrillary pathology and the spectrum of cognitive function: findings from the Nun Study. Ann Neurol. 2002;51(5):567-77. [ Links ]
98. Arnaiz E, Jelic V, Almkvist O, Wahlund LO, Winblad B, Valind S, et al. Impaired cerebral glucose metabolism and cognitive functioning predict deterioration in mild cognitive impairment. Neuroreport. 2001;12(4):851-5. [ Links ]
99. Jack CR Jr., Petersen RC, Xu Y, O’Brien PC, Smith GE, Ivnik RJ, et al. Rates of hippocampal atrophy correlate with change in clinical status in aging and AD. Neurology. 2000;55(4):484-9. [ Links ]
100. Kurz A, Riemenschneider M, Drzezga A, Lautenschlager N. The role of biological markers in the early and differential diagnosis of Alzheimer’s disease. J Neural Transm Suppl. 2002;62:127-33. [ Links ]
101. Petersen RC, Smith GE, Ivnik RJ, Tangalos EG, Schaid DJ, Thibodeau SN, et al. Apolipoprotein E status as a predictor of the development of Alzheimer’s disease in memory-impaired individuals. JAMA. 1995;273(16):1274-8. [ Links ]
102. Graff-Radford NR. Biological markers. In: Petersen RC, editor. Mild cognitive impairment. New York: Oxford University Press; 2003. p. 205-227. [ Links ]
103. Wolf PA, D’Agostino RB, Belanger AJ, Kannel WB. Probability of stroke: a risk profile from the Framingham Study. Stroke. 1991;22(3):312-8. [ Links ]
104. Kivipelto M, Helkala EL, Laakso MP, Hanninen T, Hallikainen M, Alhainen K, et al. Midlife vascular risk factors and Alzheimer’s disease in later life: longitudinal, population based study. BMJ. 2001;322(7300):1447-51. [ Links ]
105. DeCarli C, Miller BL, Swan GE, Reed T, Wolf PA, Carmelli D. Cerebrovascular and brain morphologic correlates of mild cognitive impairment in the National Heart, Lung, and Blood Institute Twin Study. Arch Neurol. 2001;58(4):643-7. [ Links ]
106. Reed BR, Eberling JL, Mungas D, Weiner MW, Jagust WJ. Memory failure has different mechanisms in subcortical stroke and Alzheimer’s disease. Ann Neurol. 2000;48(3):275-84. [ Links ]
107. Gauthier S, Reisberg B, Zaudig M, Petersen RC, Ritchie K, Broich K, et al. Mild cognitive impairment. Lancet. 2006;367(9518):1262-70. [ Links ]
108. Ganguli M, Dodge HH, Shen C, De- Kosky ST. Mild cognitive impairment, amnestic type: an epidemiologic study. Neurology. 2004;63(1):115-21. [ Links ]
109. Larrieu S, Letenneur L, Orgogozo JM, Fabrigoule C, Amieva H, Le Carret N, et al. Incidence and outcome of mild cognitive impairment in a populationbased prospective cohort. Neurology. 2002;59(10):1594-9. [ Links ]
110. Petersen RC, Thomas RG, Grundman M, Bennett D, Doody R, Ferris S, et al. Vitamin E and donepezil for the treatment of mild cognitive impairment. N Engl J Med. 2005;352(23):2379-88. [ Links ]
111. Aggarwal NT, Wilson RS, Beck TL, Bienias JL, Berry-Kravis E, Bennett DA. The apolipoprotein E epsilon4 allele and incident Alzheimer’s disease in persons with mild cognitive impairment. Neurocase. 2005;11(1):3-7. [ Links ]
112. Jack CR Jr., Shiung MM, Weigand SD, O’Brien PC, Gunter JL, Boeve BF, et al. Brain atrophy rates predict subsequent clinical conversion in normal elderly and amnestic MCI. Neurology. 2005;65(8):1227-31. [ Links ]
113. Drzezga A, Grimmer T, Riemenschneider M, Lautenschlager N, Siebner H, Alexopoulus P et al. Prediction of individual clinical outcome in MCI by means of genetic assessment and (18)F-FDG PET. J Nucl Med. 2005; 46(10):1625-32. [ Links ]
114. Klunk WE, Lopresti BJ, Ikonomovic MD, Lefterov IM, Koldamova RP, Abrahamson EE, et al. Binding of the positron emission tomography tracer Pittsburgh compound-B reflects the amount of amyloid-beta in Alzheimer‘s disease brain but not in transgenic mouse brain. J Neurosci. 2005;25(46):10598-606. [ Links ]
115. Klunk WE, Mathis CA, Price JC, Lopresti BJ, DeKosky ST. Two-year follow-up of amyloid deposition in patients with Alzheimer‘s disease. Brain. 2006;129(Pt 11):2805-7. [ Links ]
116. Engler H, Forsberg A, Almkvist O, Blomquist G, Larsson E, Savitcheva I, et al. Two-year follow-up of amyloid deposition in patients with Alzheimer‘s disease. Brain. 2006;129(Pt 11):2856- 66. [ Links ]
117. Small GW, Kepe V, Ercoli LM, Siddarth P, Bookheimer SY, Miller KJ, et al. PET of brain amyloid and tau in mild cognitive impairment. N Engl J Med. 2006;355(25):2652-63. [ Links ]
118. Shoghi-Jadid K, Small GW, Agdeppa ED, Kepe V, Ercoli LM, Siddarth P, et al. Localization of neurofibrillary tangles and beta-amyloid plaques in the brains of living patients with Alzheimer disease. Am J Geriatr Psychiatry. 2002;10(1):24-35. [ Links ]
119. Sunderland T, Hampel H, Takeda M, Putnam KT, Cohen RM. Biomarkers in the diagnosis of Alzheimer‘s disease: are we ready? J Geriatr Psychiatry Neurol. 2006;19(3):172-9. [ Links ]
120. Brookmeyer R, Gray S, Kawas C. Projections of Alzheimer‘s disease in the United States and the public health impact of delaying disease onset. Am J Public Health. 1998;88(9):1337-42. [ Links ]
121. Jelic V, Winblad B. Treatment of mild cognitive impairment: rationale, present and future strategies. Acta Neurol Scand Suppl. 2003;179:83-93. [ Links ]
122. Francis PT, Palmer AM, Snape M, Wilcock GK. The cholinergic hypothesis of Alzheimer‘s disease: a review of progress. J Neurol Neurosurg Psychiatry. 1999;66(2):137-147. [ Links ]
123. Mufson EJ, Ma SY, Dills J, Cochran EJ, Leurgans S, Wuu J, et al. Loss of basal forebrain P75(NTR) immunoreactivity in subjects with mild cognitive impairment and Alzheimer‘s disease. J Comp Neurol. 2002;443(2):136-53. [ Links ]
124. Davis KL, Mohs RC, Marin D, Purohit DP, Perl DP, Lantz M, et al. Cholinergic markers in elderly patients with early signs of Alzheimer disease. JAMA. 1999;281(15):1401-6. [ Links ]
125. DeKosky ST, Ikonomovic MD, Styren SD, Beckett L, Wisniewski S, Bennett DA et al. Upregulation of choline acetyltransferase activity in hippocampus and frontal cortex of elderly subjects with mild cognitive impairment. Ann Neurol. 2002;51(2):145-55. [ Links ]
126. Hawort J, Haworth J. GAL-INT-11: a randomised placebo-controlled trial to evaluate the efficacy and safety of galantamine in patients with minimal cognitive impairment (MCI) clinically at risk for development of probable Alzheimer‘s disease. National Research Register; 2003. [ Links ]
127. Gold M, Francke S, Nye JS. Impact of APOE genotype on the efficacy of galantamine for the treatment of mild cognitive impairment. Neurobiol Aging. 2004;25:S521. [ Links ]
128. Feldman H, Scheltens P, Scarpini E, Hermann N, Mesenbrink P, Mancione L, et al. Behavioral symptoms in mild cognitive impairment. Neurology. 2004;62(7):1199-1201. [ Links ]
129. Salloway SP, Goldman R, Kumar D, Ieni J, Griesing T, Richardson S. Donepezil treatment provides benefits in patients with Mild Cognitive Impairment. Proceedings of the11th IPA International Congress; 2003 August 17-22; Chicago, USA 2003. [ Links ]
130. Le DA, Lipton SA. Potential and current use of N-methyl-D-aspartate (NMDA) receptor antagonists in diseases of aging. Drugs Aging. 2001;18(10):717- 24. [ Links ]
131. Reisberg B, Doody R, Stoffler A, Schmitt F, Ferris S, Mobius HJ. Memantine in moderate-to-severe Alzheimer‘s disease. N Engl J Med. 2003;348(14):1333- 41. [ Links ]
132. Ambrozi L, Danielczyk W. Treatment of impaired cerebral function in psychogeriatric patients with memantine--results of a phase II double-blind study. Pharmacopsychiatry. 1988;21(3):144- 6. [ Links ]
133. Jain KK. Evaluation of memantine for neuroprotection in dementia. Expert Opin Investig Drugs. 2000;9(6):1397- 1406. [ Links ]
134. Johnson SA, Simmon VF. Randomized, double-blind, placebo-controlled international clinical trial of the Ampakine CX516 in elderly participants with mild cognitive impairment: a progress report. J Mol Neurosci. 2002;19(1- 2):197-200. [ Links ]
135. Rapp SR, Espeland MA, Shumaker SA, Henderson VW, Brunner RL, Manson JE, et al. Effect of estrogen plus progestin on global cognitive function in postmenopausal women: the Women‘s Health Initiative Memory Study: a randomized controlled trial. JAMA. 2003;289(20):2663-72. [ Links ]
136. Shumaker SA, Legault C, Rapp SR, Thal L, Wallace RB, Ockene JK, et al. Estrogen plus progestin and the incidence of dementia and mild cognitive impairment in postmenopausal women: the Women‘s Health Initiative Memory Study: a randomized controlled trial. JAMA. 2003;289(20):2651- 62. [ Links ]
137. DeKosky ST, Fitzpatrick A, Ives DG, Saxton J, Williamson J, López OL, et al. The Ginkgo Evaluation of Memory (GEM) study: design and baseline data of a randomized trial of Ginkgo biloba 138. Fitzpatrick AL, Fried LP, Williamson J, Crowley P, Posey D, Kwong L, et al. Recruitment of the elderly into a pharmacologic prevention trial: the Ginkgo Evaluation of Memory Study experience. Contemp Clin Trials. 2006;27(6):541-53. [ Links ]
139. Landi F, Cesari M, Onder G, Russo A, Torre S, Bernabei R. Non-steroidal anti-inflammatory drug (NSAID) use and Alzheimer disease in communitydwelling elderly patients. Am J Geriatr Psychiatry. 2003;11(2):179-85. [ Links ]
140. Pasinetti GM. From epidemiology to therapeutic trials with anti-inflammatory drugs in Alzheimer’s disease: the role of NSAIDs and cyclooxygenase in beta-amyloidosis and clinical dementia. J Alzheimers Dis. 2002;4(5):435- 45. [ Links ]
141. Knopman DS. Treatment of mild cognitive impairment and prospects for prevention of Alzheimer’s disease. In: Petersen RC, editor. Mild Cognitive Impairment. New York: Oxford University Press; 2003. p. 243-58. [ Links ]
142. Aisen PS, Schafer KA, Grundman M, Pfeiffer E, Sano M, Davis KL, et al. Effects of rofecoxib or naproxen vs placebo on Alzheimer disease progression: a randomized controlled trial. JAMA. 2003;289(21):2819-26. [ Links ]
143. Thal LJ, Ferris SH, Kirby L, Block GA, Lines CR, Yuen E, et al. A randomized, double-blind, study of rofecoxib in patients with mild cognitive impairment. Neuropsychopharmacology. 2005;30(6):1204-15. [ Links ]
144. Abad-Santos F, Novalbos-Reina J, Gallego- Sandin S, García AG. Treatment of mild cognitive impairment: value of citicoline. Rev Neurol. 2002;35(7):675- 82. [ Links ]
145. Waegemans T, Wilsher CR, Danniau A, Ferris SH, Kurz A, Winblad B. Clinical efficacy of piracetam in cognitive impairment: a meta-analysis. Dement Geriatr Cogn Disord. 2002;13(4):217- 24. [ Links ]
146. Guo Z, Fratiglioni L, Zhu L, Fastbom J, Winblad B, Viitanen M. Occurrence and progression of dementia in a community population aged 75 years and older: relationship of antihypertensive medication use. Arch Neurol. 1999;56(8):991-6. [ Links ]
147. Forette F, Seux ML, Staessen JA, Thijs L, Birkenhager WH, Babarskiene MR, et al. Prevention of dementia in randomised double-blind placebocontrolled Systolic Hypertension in Europe (Syst-Eur) trial. Lancet. 1998;352(9137):1347-51. [ Links ]
148. Prince MJ, Bird AS, Blizard RA, Mann AH. Is the cognitive function of older patients affected by antihypertensive treatment? Results from 54 months of the Medical Research Council‘s trial of hypertension in older adults. BMJ. 1996;312(7034):801-5. [ Links ]
149. Wolozin B, Kellman W, Ruosseau P, Celesia GG, Siegel G. Decreased prevalence of Alzheimer disease associated with 3-hydroxy-3-methyglutaryl coenzyme A reductase inhibitors. Arch Neurol. 2000;57(10):1439-43. [ Links ]
150. Jick H, Zornberg GL, Jick SS, Seshadri S, Drachman DA. Statins and the risk of dementia. Lancet. 2000;356(9242):1627-31. [ Links ]
151. Rockwood K, Kirkland S, Hogan DB, MacKnight C, Merry H, Verreault, R et al. Use of lipid-lowering agents, indication bias, and the risk of dementia in community-dwelling elderly people. Arch Neurol. 2002;59(2):223-7. [ Links ]
152. Yaffe K, Barrett-Connor E, Lin F, Grady D. Serum lipoprotein levels, statin use, and cognitive function in older women. Arch Neurol. 2002;59(3):378-84. [ Links ]
153. Launer LJ, White LR, Petrovitch H, Ross GW, Curb JD. Cholesterol and neuropathologic markers of AD: a population-based autopsy study. Neurology. 2001;57(8):1447-52. [ Links ]
154. Hartmann T. Cholesterol: a beta and Alzheimer‘s disease. Trends Neurosci. 2001;24(11 Suppl):S45-S48. [ Links ]
155. Sparks DL, López J, Connor D, Sabbagh M, Seward J, Browne P. A position paper: based on observational data indicating an increased rate of altered blood chemistry requiring withdrawal from the Alzheimer’s Disease Cholesterol-Lowering Treatment Trial (ADCLT). J Mol Neurosci. 2003;20(3):407-10. [ Links ]
156. Wang HX, Wahlin A, Basun H, Fastbom J, Winblad B, Fratiglioni L. Vitamin B(12) and folate in relation to the development of Alzheimer’s disease. Neurology. 2001;56(9):1188-1194. [ Links ]
157. McCaddon A, Hudson P, Davies G, Hughes A, Williams JH, Wilkinson C. Homocysteine and cognitive decline in healthy elderly. Dement Geriatr Cogn Disord. 2001;12(5):309-13. [ Links ]
158. Aisen PS, Egelko S, Andrews H, Díaz- Arrastia R, Weiner M, DeCarli C, et al. A pilot study of vitamins to lower plasma homocysteine levels in Alzheimer disease. Am J Geriatr Psychiatry. 2003;11(2):246-9. [ Links ]
159. Petersen RC, O’Brien J. Mild cognitive impairment should be considered for DSM-V. J Geriatr Psychiatry Neurol. 2006;19(3):147-54. [ Links ]
Recibido para evaluación: 10 de mayo de 2007 Aceptado para publicación: 16 de julio de 2007














