Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de la Facultad de Medicina
Print version ISSN 0120-0011
rev.fac.med. vol.56 no.1 Bogotá Jan./Mar. 2008
INVESTIGACIÓN ORIGINAL
DETERMINACIÓN DE LA SUSCEPTIBILIDAD A DROGAS DE PRIMERA LÍNEA EN AISLAMIENTOS DE MYCOBACTERIUM TUBERCULOSIS POR LA TÉCNICA DEL TUBO INDICADOR DE CRECIMIENTO MICOBACTERIANO
Determining the susceptibility to first-line drugs in M. tuberculosis isolates using the mycobacteria growth indicator tube method
Claudia Rocío Sierra Parada1, Edgar Alberto Sánchez Morales2, Sandra Consuelo Henao Riveros3, Alfredo Saavedra Rodríguez4
1. Profesora Cátedra, Bacterióloga, Universidad Colegio Mayor de Cundinamarca
2. Profesor Asistente, Especialista Medicina Interna -Neumología, Facultad de Medicina, Universidad Nacional de Colombia, Bogotá.
3. Profesora Asistente, Bacterióloga, Magíster en Microbiología, Facultad de Medicina, Universidad Nacional de Colombia, Bogotá.
4. Profesor Asociado, Especialista Medicina Interna -Neumología, Facultad de Medicina, Universidad Nacional de Colombia, Bogotá.
Correspondencia: easanchezm@unal.edu.co
Resumen
Antecedentes. La aparición de aislamientos de Mycobacterium tuberculosis resistentes a los medicamentos ha hecho que se busquen métodos más rápidos y confiables para la determinación de la susceptibilidad a las drogas antituberculosas.
Objetivo. Determinación de la susceptibilidad a drogas antituberculosas de primera línea en aislamientos de M. tuberculosis utilizando el método del tubo indicador de crecimiento micobacteriano (MGIT).
Material y métodos. Se estudiaron 49 aislamientos de M. tuberculosis procedentes del laboratorio de micobacteriología del departamento de Microbiología de la Universidad Nacional de Colombia. Se evaluó y comparó el método MGIT para la determinación de la resistencia o susceptibilidad a rifampicina, isoniacida, etambutol y estreptomicina con la prueba de oro, el método de las proporciones múltiples (PM).
Resultados. Por el método de las PM de los 49 aislamientos, 26 (53.0%) fueron sensibles a los cuatro antibióticos, 12 (24.5%) resistentes a un antibiótico y 11 (22.5%) a más de un antibiótico. Por el método MGIT de los 49 aislamientos, 31 (63.3%) fueron sensibles a los cuatro antibióticos, ocho (16.3%) resistentes a un antibiótico y 10 (20.6 %) resistentes a más de un antibiótico. Los porcentajes de concordancia observada oscilaron entre 83.7 y 97.9% y el índice kappa estuvo entre 0.61 y 0.83 para los diferentes antibióticos analizados. La sensibilidad del método MGIT a rifampicina, isoniacida, etambutol y estreptomicina fue de 88.9, 95.2, 62.5 y 58 por ciento respectivamente y la especificidad fue 97.7, 92.3, 98.8 y 98.4 por ciento respectivamente. Por el método MGIT se aislaron cepas resistentes de M. tuberculosis en un tiempo promedio de 7.85 días.
Conclusiones. El método MGIT permite la obtención de resultados confiables principalmente a isoniacida y rifampicina que son los antibióticos que determinan la multirresistencia del M. tuberculosis y en menor medida para estreptomicina y etambutol.
Palabras clave: tuberculosis, MGIT, resistencia bacteriana a drogas, susceptibilidad.
Summary
Background. The appearance of Mycobacterium tuberculosis isolates resistant to drugs has triggered the search for quicker and more reliable methods to determine the susceptibility to anti-tuberculosis drugs.
Objective. To evaluate the susceptibility of M. tuberculosis isolates to anti-tuberculosis first line drugs by Mycobacterium growth indicator tube method (MGIT).
Materials and methods. Forty-nine isolates of M. tuberculosis were tested, coming from the Mycobacteriology Laboratory of Microbiology Department of the Universidad Nacional de Colombia. The MGIT method was evaluated and compared in order to determine resistance or susceptibility to rifampicin, isoniazid, ethambutol and streptomycin with the gold standard method, the multiple proportion method (PM).
Results. With the PM method, of 49 isolates, 26 (53.0%) were sensitive to all four antibiotics, 12 (24.5%) were resistant to one antibiotic and 11 (22.5%) to more than one antibiotic. Using the MGIT method, of 49 isolates, 31 (63.3%) were sensitive to all four antibiotics, 8 (16.3%) were resistant to one antibiotic and 10 (20.6%) were resistant to more than one antibiotic. The concordance percentages observed oscillated between 83.7% and 97.9% and the kappa index was between 0.61 and 0.83 for the different antibiotics analyzed. The sensitivity of the MGIT method to the rifampicin, isoniazid, ethambutol and streptomycin was of 88.9, 95.2, 62.5 and 58% respectively and specifity was of 97.7, 92.3, 98.8 y 98.4% respectively. Using the MGIT method, isolates resistant to M. tuberculosis were determined in an average time of 7.85 days.
Conclusions. The MGIT method permits obtaining reliable results in less time than conventional methods with isoniazid and rifampicin which are the antibiotics that determine the multi-resistance of M tuberculosis and to a lesser degree to streptomycin and ethambutol.
Key words: tuberculosis, MGIT, drug resistance, susceptibility.
Introducción
La tuberculosis es en el mundo una enfermedad infecciosa, con alta tasa de incidencia y difícil control por parte de los organismos regionales de salud. Conocida desde la prehistoria, se considera que ha llevado a la muerte a más personas que cualquier otro patógeno microbiano (1). Las cepas de M. tuberculosis actuales parecen tener un ancestro común originado cerca de 20.000-15.000 años atrás y los análisis de mutación genética muestran que la actual diversidad genética se originó en cepas de entre 250 a 1000 años atrás (2). La información actual de la OMS, indica que para el año 2004 se presentaron 8.9 millones de casos nuevos (140/100.000), de los cuales 3.9 millones se diagnosticaron con baciloscopia positiva (62/100.000), se encontraron 741.000 adultos coinfectados con el virus de la inmunodeficiencia humana (VIH). Se tuvieron 14.6 millones de casos prevalentes (229/100.000) de los cuales 6.1 millones se diagnosticaron con baciloscopia. Más del 80 por ciento de los casos nuevos de 2004, provinieron de África, sur este de Asia y Pacífico Occidental. 1.7 millones de personas (27/100.000) murieron de tuberculosis en 2004 este dato incluye 248.000 personas coinfectadas con VIH (3). Hoy las recomendaciones de diagnóstico y manejo de la enfermedad, desde el punto de vista de programas de control han sido lideradas por la Organización Mundial de la Salud (OMS) con un programa lanzado en 1994, denominado estrategia DOTS (Estrategia de tratamiento directamente observado) que se mantiene como la intervención más costo-efectiva para detectar y curar casos, y prevenir diseminación de la tuberculosis multirresistente. La prevención es la mejor y más importante herramienta para el control de la tuberculosis multirresistente (TBC-MR) que se define como la resistencia a isoniacida y rifampicina (4). En la actualidad se conoce que la resistencia a las drogas antituberculosas no sólo es para los medicamentos de primera línea sino que se ha extendido a los de segunda línea. Así en marzo de 2006 el CDC reportó la aparición de Mycobacterium tuberculosis con resistencia extendida a drogas de segunda línea de tratamiento (XDR TB) (5). La Tuberculosis extremadamente resistente (XDR TB) se define como la presencia de tuberculosis en personas quienes tienen aislados de M. tuberculosis resistentes a isoniacida y rifampicina más resistencia a cualquier fluoroquinolona y por lo menos a una de las drogas inyectables de segunda línea (amikacina, kanamicina o capreomicina) (6).
La presencia o no de tuberculosis resistente a drogas se deriva de varios factores entre los que intervienen:
1. Inadecuados regímenes de tratamiento, sin orientación, guías, seguimiento inadecuado y pobre financiación.
2. Mala disponibilidad y calidad de los medicamentos antituberculosos, incluyendo problemas en almacenamiento y fallas en la dosificación y potencia de los medicamentos o sus combinaciones.
3. Inadecuada aceptación de los medicamentos, poca información al paciente, problemas socioeconómicos que inciden en la asistencia a los servicios de salud, efectos adversos, mala absorción y costos de los mismos (7).
Datos de la OMS estiman que para el año 2003 los casos nuevos y de retratamiento resistentes a drogas pudieron ser 458.000 con intervalo de confianza del 95 por ciento entre 321.000 -689.000. No se conocen con exactitud las cifras de resistencia a drogas en el mundo y se sabe que áreas como la China, la India, Nigeria y la antigua Unión Soviética presentan el mayor número de casos (3). La resistencia a drogas de primera línea en pacientes nunca tratados y especialmente para estreptomicina e isoniacida fue de 10.7 por ciento (0-57.1%). La prevalencia media de TBC-MR fue de 1,2 por ciento (0-14.2%). En los pacientes previamente tratados la prevalencia media de cualquier resistencia fue de 23,3 por ciento (0-82.1%) y de TBC-MR de 7.7 por ciento (0-58.3%).
Colombia reportó para el Proyecto Mundial de Vigilancia de la Resistencia a las Drogas Antituberculosas dirigido por la OMS y la UICTER una resistencia global del 15.6 por ciento y multirresistencia del 1.5 por ciento; cuando se tuvieron en cuenta todos los medicamentos evaluados fue del 28.2 por ciento; se encontró resistencia a pirazinamida en 9.3 por ciento, a isoniacida 9.5 por ciento y la más alta a estreptomicina en 11.5 por ciento, mientras las más bajas fueron etambutol 0.8 por ciento, rifampicina 1.7 por ciento, tioacetazona 2.6 por ciento y etionamida 6.2 por ciento. Al compararse con el estudio de 1992 respecto a la resistencia global no hubo diferencia significativa, (15.6% en el 2002 mientras 14.1% en 1992). Al compararse con otros países se encontró una resistencia global superior a la media encontrada en otros miembros de la UICTER, lo mismo que multirresistencia de 1.0 por ciento (8,9). La posibilidad de resistencia a un medicamento o la multirresistencia se incrementa si el paciente ha recibido tratamientos previos (10).
El diagnóstico de la resistencia o multirresistencia a nivel de laboratorio se puede obtener por diversas técnicas que implican métodos de genotipificación y fenotipificación. El método de las proporciones múltiples es la prueba de oro para la determinación de la susceptibilidad a los medicamentos antituberculosos. Técnica propuesta por Canetti y colaboradores y adoptada por la Organización Mundial de la Salud desde 1969 que sigue vigente para países en vía de desarrollo. Es la metodología más usada en el mundo para determinar la relación entre el número de bacilos que crecen en medio sólido con antibiótico y el número de bacilos que crecen en medio libre o sin antibiótico, indicando la proporción de bacilos de M. tuberculosis resistentes al fármaco en una población bacteriana, obteniéndose resultados entre cuatro y seis semanas (11). En la actualidad, para la obtención de resultados oportunos y que permitan intervenir en tiempo real en el tratamiento del paciente, se han encaminado esfuerzos para la implementación de nuevas metodologías que superen a ésta en tiempo y costo beneficio.
Este trabajo está dirigido fundamentalmente a la determinación de la susceptibilidad a drogas de primera línea en aislamientos de M. tuberculosis mediante la utilización de una de las técnicas de fenotipificación como es el tubo indicador de crecimiento micobacteriano (MGIT) el cual es útil en el diagnóstico rápido de la tuberculosis y detecta la resistencia a drogas antituberculosas de primera y segunda línea en presencia de concentraciones críticas de los antibióticos (12,13).
Material y métodos
Aislamientos bacterianos
Se evaluaron un total de 49 aislamientos de M. tuberculosis procedentes de diferentes hospitales y entidades de salud de Bogotá D.C. existentes en el Laboratorio de Micobacteriología del Departamento de Microbiología de la Universidad Nacional de Colombia. Estos aislamientos fueron recuperados para el estudio en medio de cultivo de Lowenstein Jensen. Los cultivos fueron incubados a 37°C por un tiempo de cuatro semanas con observación semanal. Al evidenciar crecimiento bacteriano se realizó coloración de Ziehl Neelsen para la confirmación de bacilos ácido alcohol resistentes. La identificación fenotípica consistió en la realización de una serie de pruebas bioquímicas que incluyeron: detección de niacina, detección de actividad de catalasa a temperatura ambiente y a 68°C y reducción de nitratos.
Método de las proporciones múltiples (PM)
Preparación del Inóculo
La masa bacilar del M. tuberculosis se tomó a partir del medio Lowenstein Jensen, mediante raspado con una espátula de madera por toda la superficie sembrada. Esta masa bacilar se colocó en frascos tapa rosca debidamente marcados con el número del aislamiento, que contenía 1ml de agua destilada estéril y perlas de vidrio. Inmediatamente se homogenizaron en agitador Vortex por 30 segundos, la suspensión fue calibrada nefelometricamente con el tubo número tres de la escala Mac Farland.
Preparación de los antibióticos
Para el método de las proporciones múltiples se utilizó el medio sólido de Lowenstein Jensen, al cual se le adicionaron los medicamentos a probar a una concentración crítica por mililitro antes de ser coagulados a 80°C. La proporción crítica ya establecida de cada medicamento, se obtuvo por dilución de soluciones madre preparadas el mismo día que fueron adicionadas al medio. A partir de las soluciones madre se prepararon las soluciones de trabajo, descritas por Canetti et al (11) para cada uno de los antibióticos. Las concentraciones críticas fueron: isoniacida (I): 0.2 ug/ml, estreptomicina (S): 4 ug/ml, etambutol (E): 2 ug/ml y rifampicina (R): 40 ug/ml.
Procedimiento
Se realizaron diluciones en base 10 de la suspensión bacteriana, se tomaron los tubos de las diluciones 10-3, 10-5 y 10-6 y se inocularon 0.2 ml en dos tubos sin antibiótico para cada dilución como control de viabilidad; con la dilución 10-3 y 10-5 se sembró un tubo para cada uno de los antibióticos antituberculosos de primera línea. Luego se incubaron a una temperatura de 37°C, en atmósfera aeróbica durante cuatro semanas, cuando se hizo la primera lectura; luego se incubaron por dos semanas más al cabo de las cuales se obtuvieron resultados definitivos de la prueba. Se utilizó la cepa de M. tuberculosis H37Rv como referencia.
Método del tubo indicador de crecimiento micobacteriano (MGIT)
Preparación del inóculo
Se obtuvo la masa bacilar de igual manera que para el método de las proporciones múltiples. La suspensión bacteriana se ajustó nefelométricamente al tubo número 0.5 de la escala de Mac Farland y a partir de allí se realizó una dilución 1:5 en solución salina.
Preparación de los antibióticos
La proporción crítica de cada medicamento se obtuvo por diluciones de soluciones madre preparadas el mismo día que fueron adicionadas al medio. A partir de las soluciones madre se prepararon las soluciones de trabajo cuyas concentraciones críticas fueron para isoniacida (I): 0.1 ug/ml, estreptomicina (S): 0.8 ug /ml, etambutol, (E): 3.5 ug /ml y rifampicina (R):1 ug/ml.
Procedimiento
Se utilizaron cinco tubos en total por aislamiento, un tubo para el control de viabilidad y uno por cada antibiótico a analizar. A los tubos MGIT que contenían medio Middlebrook modificado 7H9 se les adicionó suplemento antibiótico PANTA (polimixina B, anfotericina B, ácido nalidixico, trimetropin, y azlocilina) que a su vez se reconstituyó con OADC (ácido oleico, albúmina bovina, dextrosa y catalasa) y finalmente se adicionó el antimicobacteriano para dejar en cada tubo la concentración crítica respectiva de cada medicamento. Luego se agregó a cada tubo una concentración de la suspensión bacteriana y se llevó a incubar en el equipo automatizado BACTEC MGIT 960 (Becton Dickinson Microbiology Systems).
Las lecturas de los tubos del MGIT se realizaron diariamente a partir del segundo día de incubación (14). A los tubos con crecimiento bacteriano se les realizó coloración de Zielh Neelsen. Los tubos con posible contaminación bacteriana se sembraron en agar sangre. Como control del método se utilizó un control positivo preparado con sulfito de sodio al 0.4 por ciento y un control negativo para cada bloque de pruebas. Se utilizó la cepa de M. tuberculosis H37Rv como referencia.
Análisis estadístico
Se utilizaron pruebas de rendimiento operativo como la sensibilidad (la habilidad para detectar la verdadera resistencia a los antibióticos), especificidad (la habilidad para detectar la verdadera susceptibilidad a los antibióticos). Se obtuvo la concordancia observada y la concordancia por índice kappa. El valor del índice kappa fue interpretado así: menor de 0.2 malo; 0.21 a 0.4 bajo; 0.41-0.6 moderado; 0.61-0.8 bueno, 0.8 -1.0 muy bueno (15,16). Para corregir el tamaño de la muestra se utilizó un procedimiento similar a la corrección de Yates (17).
Resultados
Para evaluar la susceptibilidad de los aislamientos de Mycobacterium tuberculosis a cuatro antibióticos de primera línea (isoniacida, rifampicina, estreptomicina y etambutol) se utilizó el método del tubo indicador de crecimiento micobacteriano (MGIT) y la prueba de oro de las proporciones múltiples (PM). Por el método MGIT se obtuvieron diferentes patrones de resistencia y susceptibilidad; de los 49 aislamientos fueron sensibles a los cuatro antibióticos 31 (63.3%), resistentes a un antibiótico ocho (16.3%) y resistentes a más de un antibiótico 10 (20.6%). Por el patrón de oro de las proporciones múltiples, de los 49 aislamientos, 26 (53.0%) fueron sensibles a los cuatro antibióticos, 12 (24.5%) resistentes a un antibiótico y 11 (22.5%) a más de un antibiótico. Se encontró un mayor número de aislamientos de M. tuberculosis resistentes a estreptomicina (38.8%). En la tabla 1 se observa el número de aislamientos susceptibles a cada uno de los antibióticos, los susceptibles por PM y resistentes por el método MGIT, los resistentes por PM y susceptibles por MGIT, aislamientos que fueron resistentes por las dos metodologías y los porcentajes de concordancia observada y de concordancia aplicando el índice kappa para los dos métodos y para cada uno de los antibióticos analizados. En la tabla 2 se muestran los indicadores epidemiológicos de la prueba.
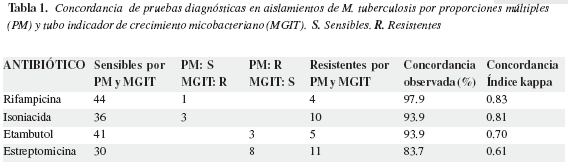
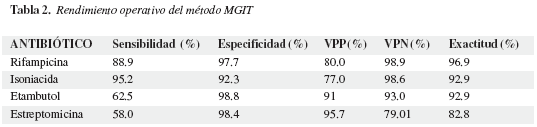
El tiempo establecido por la técnica de oro de las proporciones múltiples para el informe de los resultados fue entre 28 a 42 días y por el método MGIT el promedio en días para informar resistencia a cualquier antibiótico fue de 7.85 días, oscilando entre 4-17 días.
Discusión
La detección rápida y oportuna de la susceptibilidad del Mycobacterium tuberculosis a las drogas antituberculosas es de vital importancia en el tratamiento de enfermos, permitiendo que una terapia adecuada interrumpa la cadena de transmisión de la enfermedad y prevenga la posibilidad de tener cepas resistentes que lleven al fracaso de tratamientos y, peor aún, la aparición y transmisión de cepas multirresistentes en la comunidad. De esta manera, la vigilancia de la resistencia a los antibióticos permite evaluar los programas contra la TBC. Es claro que el diagnóstico eficiente de un enfermo de tuberculosis y la realización de pruebas de resistencia a los medicamentos son factores que mejoran los programas de control de la TBC.
Este estudio evaluó la susceptibilidad de aislamientos de M. tuberculosis a cuatro antibióticos de primera línea como son rifampicina, isoniacida, etambutol y estreptomicina por el método de el tubo indicador de crecimiento micobacteriano (MGIT) y se comparó con el patrón de oro de las proporciones múltiples (PM). Tradicionalmente se ha estudiado la susceptibilidad a las drogas antituberculosas con el método de las PM, que muestra ser una prueba confiable al detectar la proporción de bacilos resistentes en una población de bacilos tuberculosos (11). En el presente estudio se encontró que el tiempo promedio para la detección de la resistencia por el método MGIT fue de 7.85 días, mientras que con el método de las proporciones múltiples se detectó la resistencia entre los 28-42 días, tiempos muy similares a los encontrados por Walters y Hanna (18) y Rüsch-Gerdes y col (19) en una evaluación multicén¬trica del MGIT para examinar susceptibilidad a drogas antituberculosas. En la prueba de estudio los aislamientosson resistentes si el crecimiento es detectado en el tubo control y en el tubo que contiene la droga que se detecta por la emisión de fluorescencia.
La concordancia observada para los dos métodos, es decir la posibilidad de que ambos detecten aislamientos resistentes o susceptibles en la prueba fue para rifampicina de 97.9 por ciento, isoniacida 93.9 por ciento, etambutol 93.9 por ciento y estreptomicina de 83.7 por ciento mostrando que la técnica MGIT fue buena para detectar la resistencia y la susceptibilidad a las drogas en los aislamientos examinados. El nivel de concordancia estimado por el índice kappa fue muy bueno para isoniacida y rifampicina y bueno para etambutol y estreptomicina.
Para rifampicina la sensibilidad fue del 88.9 por ciento con una especificidad del 97,7 por ciento, como lo han mostrado los estudios de Rüsch-Gerdes y col (19), Bergmann y col (20), Goloubeva y col (21), y Bemer y col (22). Los datos obtenidos permiten establecer que el método de MGIT es una prueba confiable para la detección de la resistencia a rifampicina, como se encontró en aislamientos de muestras clínicas en el trabajo de Piffardi y col en Chile (23).
En cuanto a isoniacida la sensibilidad encontrada en el estudio fue del 95.2 por ciento con una especificidad de 92.3 por ciento, indicando que el método de MGIT es bueno para detectar los aislados verdaderamente resistentes a isoniacida cuando se compara con la prueba de oro de las proporciones múltiples, datos que fueron encontrados por otros autores confirmando así que el método MGIT es confiable para la detección de la multirresistencia en aislamientos clínicos y de labora¬to¬¬¬rio (19-25). Para¬ etam¬butol los resultados mostraron una variación importante con respecto a los anteriores, la sensibilidad de la prueba fue del 62.5 por ciento y la especificidad del 98.8 por ciento lo que indica que la detección de verdaderos resistentes por el método del MGIT no es suficiente y puede tener resultados falsos negativos. El etambutol es considerado un medicamento difícil de analizar; posiblemente por los mecanismos de acción al ser bacteriostático en lugar de bactericida, a la interferencia con algunos de los componentes del sistema MGIT (indicador fluorescente) o a los mecanismos de resistencia al medicamento; en varios estudios se encuentran valores de sensibilidad bajos que podrían llevar a un sub registro de la resistencia al medicamento (22,26). Sin embargo, la especificidad de la prueba fue alta a etambutol, indicando que estamos ante aislamientos susceptibles al medicamento. Existen trabajos que utilizan diferentes concentraciones de etambutol en las pruebas de resistencia y esto ha hecho que a concentraciones bajas, se detecte mayor cantidad de aislados resistentes. En este estudio se utilizó la concentración recomendada por la OMS de 3.5 ug/ml con lo cual los resultados son similares a otros estudios. Sin embargo, se requieren trabajos que comparen suficientes aislamientos de M. tuberculosis con resistencias conocidas y diferentes concentraciones del antibiótico y así poder tener una mejor seguridad en la detección de los verdaderos resistentes (24).
Por último, el etambutol ha sido considerado un medicamento de difícil evaluación, con resultados poco reproducibles, bajos valores de sensibilidad y altos de especificidad en los estudios de susceptibilidad de la OMS (22).
Con la estreptomicina, la primera droga antituberculosa descubierta y la cual presenta los más altos índices de resistencia, se encontró en el presente estudio una sensibilidad para el método MGIT de 58 por ciento con una especificidad de 98.4 por ciento, lo cual indica que el método MGIT no fue lo suficientemente bueno para detectar la resistencia de los aislamientos a estreptomicina. Sin embargo, se debe aclarar que es necesario realizar estudios con mayor cantidad de aislamientos y pruebas con diferentes concentraciones críticas del medicamento para obtener resultados más confiables (19,27).
Conclusiones
La búsqueda de la resistencia a las drogas antituberculosas de primera línea es una herramienta indispensable para el manejo de los enfermos tuberculosos y más aún, nos permite, a través de un tratamiento mejor planeado disminuir los casos de multirresistencia a nivel local y regional. Se concluye que el método de tubo indicador de crecimiento micobac¬teriano es una herramienta de laboratorio que detecta el crecimiento micobacteriano de forma rápida y permite el estudio de la resistencia a drogas antituber¬culosas de primera línea especialmente a isoniacida y rifampicina. Es importante recalcar que basados en la concordancia de las dos pruebas podría ser utilizada la técnica del MGIT en lugar de las proporciones múltiples cuando se requieran resultados con celeridad. Aunque es un método con mayor costo que el de las PM, tiene la ventaja de ser más sencillo en su implementación y bueno para la detección de la multirresistencia, que en la práctica clínica es de utilidad.
A pesar del bajo porcentaje de aislamientos resistentes a los medicamentos en la muestra examinada se presentó buena concordancia comparada con la prueba de las PM. Nuestros resultados sugieren que la prueba del tubo indicador de crecimiento micobacteriano (MGIT) para la determinación de la susceptibilidad a etambutol y estreptomicina por este método no es tan eficaz, como para isoniacida y rifampicina. Es necesario realizar estudios adicionales donde se analice una mayor proporción de aislamientos de M. tuberculosis tanto resistentes como susceptibles para la evaluación de las drogas de primera y segunda línea antituberculosa.
Financiación
División de Investigación Sede Bogotá. Universidad Nacional de Colombia.
Agradecimientos
División de Investigaciones de la sede Bogotá Universidad Nacional de Colombia. Dr. Manuel Alfonso Patarroyo Director Grupo Funcional Biología Molecular y TBC. Fundación Instituto de Inmunología de Colombia (FIDIC).
Referencias
1. Daniel TM. The history of tuberculosis. Respiratory Medicine (2006), doi:10.1016/j.rmed.2006.08.006. [ Links ]
2. Cave AJE. The evidence for the incidence of tuberculosis in ancient Egypt. Br. J Tubercl. 1939;33:142 -52. [ Links ]
3. Global Tuberculosis Control: Surveillance, Planning, Financing. WHO report 2006. Geneva, World Health Organization. (WHO/HTM/TB2006.362). [ Links ]
4. Espinal MA, The global situation of MDR-TB. Tuberculosis. 2003;83:44-51. [ Links ]
5. Centers for Disease Control and Prevention. Emergence of Mycobacterium tuberculosis with extensive resistance to second-line drugs – worldwide, MMWR Morb Mortal Wkly Rep. 2006;55:301-305. [ Links ]
6. Migliori GB, Loddenkemper R, Blasi F, Raviglione MC. 125 years after Robert Koch's discovery of the tubercle bacillus: the new XDR-TB threat. Is «science» enough to tackle the epidemic? Eur Respir. J. 2007;29:423-427.
7. Raviglione MC, Espinal MA. Towards optimization of surveillance resistence to antituberculosis drug resistance. Eurosurveilance Monthly 2000;10:103-104
8. Espinal MA, Laszlo A, Simonsen L, Boulahbal F, Kim SJ, Reiniero A. Global trends in resistance to antituberculosis drugs. N Engl J Med. 2001;344: 1294-1303.
9. León CI, Sierra CR, Naranjo ON, Garzón MC, Guerrero MI. Segundo estudio nacional de resistencia primaria del Mycobacterium tuberculosis a las drogas.INFECTIO.2002;6:83.
10. Guidelines for the programmatic management of drug-resistant tuberculosis. Geneva, World Health Organization (WHO/HTM/TB2006.361
11. Canetti G, Froman F, Grosset J, Hauduroy P, Langerova M, Meisser G, Mitchison DA, Sula L. Mycobacteria: Laboratory methods for testing drug sensitivity and resistance. Bull WHO. 1963;29;565-578.
12. Palomino JC. Newer diagnostics for tuberculosis and multi-drug resistant tuberculosis. Curr Opin Pulm Med 2006;12:172-178.
13. Robledo JR, Mejia GI. Actualidad en el diagnóstico de la tuberculosis por el laboratorio. INFECTIO. 2001;5:251-258.
14. Becton Dickinson Microbiology Systems. BACTEC MGIT 960 System product and procedure manual. USA, 2001.
15. Echeverry J, Ardila E. Pruebas diagnósticas y proceso diagnóstico. En: Estrategias de Investigación en medicina clínica. Bogotá: Editorial Manual Moderno. 2001.
16. Altman DG. Inter-rater agreement. In Practical Statistics for Medical Research, London, Chapman & Hall/CRC. 1999: 403-409.
17. Pagano M, Gauvreau K. Principles of Biostatistics. Contingency tables. Editorial Duxbury Press, California. 1993: 311-337.
18. Walters SB, Hanna B.A. Testing of Susceptibility of Mycobacterium tuberculosis to Isoniazid and Rifampicin by Mycobacterium Growth Indicator Tube Method. J Clin Microbiol. 1996;34:1565-1567.
19. Rusch-Gerdes S, Domehl C, Nardi G, Gismondo MR, Welscher HM, Pfyffer G. Multicenter Evaluation of the Mycobacteria Growth Indicador Tube for Testing Susceptibility of Mycobacterium tuberculosis to First. Line Drugs. J Clin Microbiol. 1999;37:45-48.
20. Bergmann J, Fish G, Woods G. Evaluation of the BBL MGIT (Mycobacterial Growth Indicador Tube) AST SIRE System for Antimycobacterial Susceptibility Testing of Mycobacterium tuberculosis to 4 Primary Antituberculous Drugs. Arch Pathol Lab Med. 2000;124:82-86.
21. Goloubeva V, Lecocq M, Lassowsky P, Matthys F, Portaels F, Bastian I. Evaluation of Mycobacteria Grow Indicator Tube for direct and indirect drug susceptibility testing of Mycobacterium tuberculosis from respiratory specimens in a Siberian prison hospital. J Clin Microbiol. 2001;39:1501-150
22. Bemer P, Palicova F, Rusch-Gerdes S, Drugeon HB, Pfyffer G. Multicenter Evaluation of Fully Automates BACTEC Mycobacteria Growth Indicador Tube 960 System for Susceptibility Testing of. Mycobacterium tuberculosis. J Clin Microbiol. 2002;40:150-154.
23. Piffardi S, Luna A, Sakurada A, Lepe R. Evaluación comparativa del método automatizado BACTER MGIT con el método de las proporciones para determinar susceptibilidad a drogas antituberculosas en Chile. Rev Chil Enf Respir. 2004;20:139-143.
24. Koskela KA, Katila ML. Susceptibility Testing with the Manual Mycobacteria Growth Indicator Tube (MGIT) and the MGIT 960 System Provides Rapid and Reliable Verification of Multidrug-Resistant Tuberculosis. J Clin Microbiol. 2003;41(3):1235-1239.
25. Mengatto L, Chiani Y,Imaz MS. Evaluation of rapid alternative method for drug susceptibility testing in clinical isolates of Mycobacterium Tuberculosis. Mem Inst Oswualdo Cruz, Rio de Janeiro. 2006; 10: 535-542.
26. Piersimoni C, Nista D, Bornigia S, De Sio G. Evaluation of a New Method for Rapid Drug Susceptibility Testing of Mycobacteruim avium Complex Isolates by Using the Mycobacteria Growth Indicator tube. J Clin Microbiol. 1998;3:64-67.
27. Bergmann J, Woods G. Reliability of Mycobacteria Growth Indicador Tube for Testing Susceptibility of Mycobacterium tuberculosis to Ethambutol y Streptomycin. J Clin Microbiol. 1997;35:3325-3327.













