Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de la Facultad de Medicina
Print version ISSN 0120-0011
rev.fac.med. vol.62 no.2 Bogotá Apr./June 2014
https://doi.org/10.15446/revfacmed.v62n2.45429
http://dx.doi.org/10.15446/revfacmed.v62n2.45429
Opiniones, debates y controversias
Avances genéticos y moleculares en el estudio de trastornos mentales
Genetic and molecular advances in the study of mental disorders
Daisy Natalia Salamanca-Ortíz1; Jorge Yamit Vergara-Vergara1; Franklin Escobar-Córdoba2; Álvaro Rodríguez-Gama2; Jorge Eduardo Caminos- Pinzón3
1 Facultad de Medicina. Universidad Nacional de Colombia. Bogotá, Colombia.
2 Departamento de Psiquiatría. Facultad de Medicina. Universidad Nacional de Colombia. Bogotá, Colombia.
3 Departamento de Ciencias Fisiológicas. Facultad de Medicina. Universidad Nacional de Colombia. Bogotá, Colombia.
Correspondencia: Franklin Escobar-Córdoba. Dirección: Departamento de Psiquiatría. Facultad de Medicina. Universidad Nacional de Colombia. Ciudad Universitaria. Bogotá, Colombia. Teléfono: +571 3165000 Extensión 15117.
Correo electrónico: feescobarc@unal.edu.co
Salamanca-Ortíz DN, Vergara-Vergara JY, Escobar-Córdoba F, Rodríguez-Gama Á, Caminos-Pinzón JE. Avances genéticos y moleculares en el estudio de trastornos mentales. rev.fac.med. 2014;62:319-324.
Recibido: 11/06/2014 / Aceptado: 29/06/2014
Resumen
Actualmente, con el aumento de la disponibilidad de técnicas para la realización de estudios genéticos, han aparecido nuevas áreas del conocimiento como la epigenética y la farmacogenética. Estas nuevas áreas han permitido esclarecer las bases genéticas implicadas en la aparición de las enfermedades que afectan al ser humano. Dada su aplicación global, la psiquiatría no ha sido ajena al alcance de estas nuevas disciplinas, lo cual se refleja en el gran número de estudios realizados a nivel mundial que han relacionado la presencia de variantes genéticas en los individuos con la aparición de trastornos mentales específicos. De la misma forma, otros estudios han evidenciado que la efectividad de los tratamientos farmacológicos empleados en psiquiatría se correlaciona con polimorfismos en las enzimas encargadas de metabolizar dichos medicamentos. Por lo tanto, es importante que los psiquiatras conozcan los aspectos básicos de estas relaciones para obtener mejores resultados en el diagnóstico y tratamiento de los principales trastornos mentales.
Palabras clave: Psiquiatría, Epigenómica, Farmacogenética, Trastornos Mentales (DeCS).
Summary
Nowadays, with the increased availability of techniques for genetic studies, there are new areas of knowledge, such as epigenetics and pharmacogenetics. These new areas clarify the genetic basis involved in the occurrence of diseases that affect humans. Given its global application, psychiatry has not been outside of the scope of these new disciplines. The large number of worldwide studies have linked the presence of genetic variants in individuals with signs of mental disorders. Furthermore, other studies show that the effectiveness of pharmacological treatments used in psychiatry are correlated with polymorphisms in the enzymes that metabolize these medicines. Therefore, it is important that psychiatrists know the basics of these relationships to get better outcomes in diagnosis and treatments of the major mental disorders.
Key words: Psychiatry, Epigenomics, Pharmacogenetics, Mental Disorders (MeSH).
Introducción
La aparición de los desórdenes mentales constituye un fenómeno de naturaleza compleja en el cual intervienen no solamente factores relacionados con el ambiente, sino que también se encuentran elementos asociados y componentes genéticos. En conjunto, estos dos elementos principales interactúan ocasionando alteraciones de la función celular a nivel del sistema nervioso central (SNC), manifestándose en un conjunto de signos y síntomas concernientes a las esferas mental, comportamental y conductual.
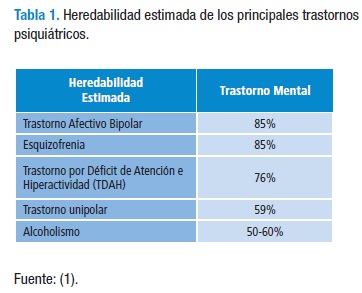
Teniendo en cuenta la heredabilidad estimada para los principales trastornos mentales (Tabla 1), se puede evidenciar que estas medidas son mayores que las calculadas para patologías con una clara asociación genética como el cáncer (1); por lo tanto, resulta importante establecer cuáles son los mecanismos moleculares responsables de esta asociación de carácter genético. Para tal propósito se han empleado varios métodos de estudio a nivel molecular y genético, que buscan variantes genéticas asociadas a trastornos psiquiátricos específicos.
Con el paso del tiempo se vienen empleando más marcadores, pasando desde cientos en los primeros años de estudio, hasta llegar a cientos de miles en los estudios de asociación de genoma completo. Además, se vienen empleando metodologías de secuencia masiva de transcriptomas, genomas y exomas con menores costos y mayor eficiencia en el diagnóstico, tratamiento y seguimiento de diferentes patologías (2). Estos estudios han permitido la identificación de variantes genéticas para enfermedades como esquizofrenia y trastorno afectivo bipolar, al igual que la caracterización del papel de la ApoE4 como factor de riesgo para el desarrollo de la enfermedad de Alzheimer (3). A pesar de esto, no se han identificado variantes genéticas de otras enfermedades, como el trastorno por déficit de atención e hiperactividad (TDAH) y el trastorno depresivo mayor (1), por lo cual se ha hecho evidente que estos métodos a nivel genómico deben ser complementados con análisis que abarquen los perfiles epigenéticos de estas patologías.
Epigenética y epigenómica
A mediados de la década de 1950, Waddington fusionó las teorías planteadas sobre la genética y el desarrollo, ya que estas se estudiaban por separado. Esto constituyó una revolución en el campo de la biología del desarrollo, pues se centró la atención en la interacción entre los factores genéticos y el crecimiento embrionario y la diferenciación. Este biólogo del desarrollo introdujo el término epigenética para describir esta novedosa área de investigación (4).
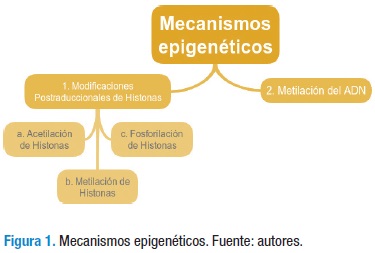
Debido a que esto ocurrió mucho antes de que se descubriera la estructura de los genes, el concepto de epigenética en la investigación biomédica hoy en día hace referencia al estudio de las modificaciones heredables y estables del ADN que alteran su capacidad de expresión pero sin afectar a las secuencias de los genes como tal (5). A su vez, la epigenómica hace referencia a la extensión de la genómica que se encarga de analizar y estudiar los cambios epigenéticos en un tipo de célula determinado. A nivel de las células que componen el SNC se han estudiado a la fecha 2 tipos principales de mecanismos epigenéticos como agentes reguladores de la expresión genética: las modificaciones postraduccionales de las histonas y la metilación del ADN (Figura 1).
Las modificaciones postraduccionales de las histonas se llevan a cabo en la región N-terminal e incluyen uniones covalentes como la acetilación, metilación, ubiquitinación y fosforilación, entre otras; mientras que las modificaciones epigenéticas que ocurren en el ADN (como la metilación) se basan en la transferencia de un grupo metilo desde la S-adenosil metionina (SAM), dando como resultado 5-metil citosina; este proceso es catalizado por un grupo de enzimas denominado ADN metiltransferasas.
Recientemente se ha descubierto una nueva forma de metilación del ADN, que ocurre en las denominadas islas CpG (regiones del ADN con elevada concentración de citosina y guanina entrelazadas por grupos fosfato, ubicadas en las regiones promotoras y el primer exón de los diferentes genes). Esta se produce en una alta proporción en las neuronas (4), sugiriendo que hacen parte del desarrollo y la capacidad de funcionalidad del SNC.
Los mecanismos epigenéticos nombrados previamente juegan un papel importante en el neurodesarrollo desde la etapa embrionaria y continúan su intervención durante el período posnatal, durante el cual el sistema nervioso alcanza su madurez funcional. Recientes estudios han demostrado que los cambios epigenéticos están involucrados en la formación, proliferación y diferenciación neuronal, así como en la formación de las dendritas (6). De esta manera, alteraciones en los procesos epigenéticos pueden contribuir a la producción de alteraciones en la esfera mental que se manifiesten de forma potencial en trastornos mentales.
Aunque anteriormente se pensaba que las modificaciones epigenéticas adquiridas a lo largo de la gestación serían estables en la vida adulta, hoy se sabe que estos cambios son dinámicos y pueden variar por efecto de factores ambientales durante el transcurso de la vida. Entre estos factores se incluyen el estilo de vida, los aspectos nutricionales, uso de medicamentos y condiciones psico-sociales (7). Esta naturaleza dinámica y cambiante de los elementos epigenéticos los hace blancos potenciales de intervenciones terapéuticas.
Farmacogenética y farmacogneómica
Como se mencionó previamente, durante la década de 1950 surgió un especial interés por la relación entre los elementos genéticos y el desarrollo embrionario durante el crecimiento. Observaciones clínicas como el reporte en 1956 de pacientes con deficiencia de la enzima butiril-colinesterasa (conocida como pseudocolinesterasa), quienes murieron luego de la administración de succinilcolina durante procedimientos de anestesia, y el hallazgo en 1957 de pacientes con deficiencia de la enzima N-acetiltransferasa, la cual participa en el metabolismo del fármaco isoniazida (empleado en el tratamiento de la tuberculosis), motivaron al Consejo de Medicamentos de la Asociación Médica Americana (Council on Drugs of the American Medical Association) a encargar a Motulsky el trabajo de resumir y publicar los datos disponibles al respecto en 1957. Utilizando estos datos, en 1959 Vogel propuso el término farmacogenética y en 1962 Kalow escribió la primera monografía sobre el tema (8).
En el contexto actual, la farmacogenética se constituye como la disciplina que estudia el papel de las variaciones genéticas en la respuesta de los individuos a fármacos y la aparición de reacciones adversas a los mismos (9). Su principal objetivo radica en optimizar el tratamiento de las enfermedades a nivel individual, llevando el manejo farmacológico hacía una terapia personalizada, segura y eficiente. Este enfoque produciría grandes cambios en la formulación de medicamentos en la práctica clínica, ya que se podría determinar de forma anticipada cuál sería el fármaco más apropiado para un paciente en particular, así como su dosis más efectiva. Todo esto produce una aparición menor de efectos adversos y en aumento de la efectividad del manejo farmacológico (10). Otro punto en el cual trabaja la farmacogenética consiste en obtener medicamentos nuevos y más efectivos ante enfermedades comunes que carecen de un tratamiento óptimo en la actualidad.
Con la implementación de pruebas moleculares in vitro e in vivo y con la aparición del proyecto genoma humano nace un nuevo campo de investigación: la farmacogenómica, la cual se ocupa del análisis y la comprensión de las bases genéticas de la enfermedad, con el propósito de puntualizar y definir nuevos blancos terapéuticos o marcadores moleculares que sean de utilidad para evaluar la eficacia de nuevos fármacos (4). Es necesario resaltar que, aunque para muchos autores los términos farmacogenética y farmacogenómica son intercambiables, son conceptos diferentes.
Teniendo en cuenta las posibles aplicaciones que se pueden generar en el área de la psiquiatría por medio de un abordaje farmacológico guiado tanto por la farmacogenética como por la farmacogenómica, se tendría un notable impacto en la reducción de la frecuencia de aparición de efectos adversos con el uso de los psicofármacos. De la misma forma, se incrementarían las ventajas en términos de costo-efectividad en dichos tratamientos.
Avances en psiquiatría
Desde la aparición del proyecto del genoma humano y el desarrollo de técnicas de estudio genético, se han llevado a cabo múltiples investigaciones encaminadas a develar el componente genético de las enfermedades. Inicialmente los estudios se centraban en enfermedades asociadas a un gen específico; sin embargo, muchas enfermedades son generadas por múltiples genes, por esto se buscaron técnicas que permitieran estudiar muchos genes al mismo tiempo, lo que a su vez disminuyó los costos de los estudios. De esta manera en 2005, se realizó con éxito el primer estudio de asociación del genoma completo (GWAS-Genome-wide association study). Este tipo de estudio permite identificar polimorfismos dentro del genoma que luego se correlacionan con la patología en estudio.
En psiquiatría se han llevado a cabo varios de estos estudios, los cuales han permitido encontrar varios genes involucrados en diferentes trastornos mentales. Actualmente hay disponibles cerca de 100 GWAS para TDAH, autismo, trastorno afectivo bipolar, esquizofrenia, trastorno depresivo mayor, trastornos ansiosos, trastornos de personalidad y neurocognición (11). En esquizofrenia, por medio de un estudio GWAS se han determinado varios polimorfismos de nucleótido simple (SNP) en las regiones de los cromosomas 9p21, 16p12 y 10q21 (11).
Diferentes SNPs de los genes que codifican receptores de opioides y aquellos que intervienen en los neurotransmisores y receptores del sistema GABA han sido implicados en la adicción a opioides y a estimulantes como la heroína y las metanfetaminas, entre otras. Estos SNPs también pueden modificar la respuesta a los tratamientos farmacológicos utilizados para el tratamiento de la drogadicción. Se ha identificado, por ejemplo, que individuos heterocigotos en el genotipo DRD2 -141C Del tienen mayores tasas de respuesta a los parches de nicotina para dejar de fumar, que con el bupropion. La naltrexona, agonista del receptor opioide usado para el tratamiento de la dependencia al alcohol, tiene mayor efectividad en pacientes con el alelo 118A del gen OPRM1 (12).
En el estudio del trastorno obsesivo compulsivo (TOC), se han encontrado diferentes regiones del genoma involucradas en el neurodesarrollo del cuerpo estriado, ubicadas en las regiones de los cromosomas 3q27-28, 7p, 1q, 15q15 y 6q27. Igualmente, se han identificado diferentes polimorfismos que pueden afectar la eficacia de los tratamientos farmacológicos, entre estos se encuentran los que involucran a los transportadores y receptores de serotonina y de dopamina y a las enzimas encargadas de la síntesis y degradación de catecol-O-metiltransferasa (13).
Estos son algunos de los estudios efectuados a nivel mundial, sin embargo, en Colombia no se han desarrollado estudios que permitan validar esta información en el contexto nacional o que sean útiles en la identificación de los polimorfismos propios de la población colombiana, teniendo en cuenta el origen multiétnico de la misma.
Panorama global de la investigación genética en psiquiatría
A nivel mundial se están llevando a cabo múltiples estudios y proyectos de investigación acerca de las implicaciones de los aspectos genéticos en el desarrollo de trastornos mentales, así como su relación con la eficacia de los tratamientos farmacológicos instaurados para dichos padecimientos. Estos estudios buscan la identificación de variantes genéticas implicadas en la aparición de los trastornos mentales y explicar las causas de por qué un mismo tratamiento farmacológico obtiene diferentes respuestas nivel farmacocinético y farmacodinámico.
Citando algunos ejemplos de las iniciativas que se vienen adelantando en esta área, se encuentran algunos grupos como el de evaluación de Aplicaciones en Práctica y Prevención (en inglés: EGAAP-Evaluation of Genomic Applications in Practice and Prevention). Es un grupo de trabajo multidisciplinario fundado en el 2005 que busca recopilar sistemáticamente la información validada en la práctica clínica sobre la utilización de pruebas genéticas, con el fin de desarrollar guías y recomendaciones de práctica clínica. Se han realizado diferentes publicaciones sobre temas como depresión, ideación suicida, enfermedad de Alzheimer, manejo del dolor, entre otros (14).
Otro grupo es el Instituto de Investigación Vall D'Hebron (Vall D'hebron Institut de Recerca-VHIR) que constituye una iniciativa gubernamental multidisciplinaria desde 2002, ubicada en Barcelona; cuenta con varios grupos de investigación, uno de ellos en neurociencias con énfasis psiquiatría, salud mental y adicciones. Allí tienen varios proyectos y publicaciones referentes al abordaje farmacogenético del tratamiento de TDAH, abuso y dependencia de sustancias (15). También se encuentra el grupo Centro Nacional de Análisis Genómico (CNAG): creado desde 2009 en Cataluña, se dedica a realizar proyectos de análisis y secuenciación de ADN a gran escala. Colaboran con grupos de investigación en diferentes áreas y realizan secuenciamiento masivo de genomas de pacientes con enfermedades poco conocidas. Han participado en múltiples estudios genéticos, algunos enfocados a la medicina personalizada (16).
Un cuarto grupo es el Instituto Nacional de Medicina Genómica (INMEGEN), fundado en 2004; tiene como objetivo ofrecer los fundamentos y parámetros para el ejercicio médico desde una perspectiva genética de la población mexicana, con el fin de atender con mayor precisión los problemas de salud con mayor prevalencia en su ubicación geográfica. Poseen una línea especializada en genómica de enfermedades psiquiátricas y neurodegenerativas, entre otras subespecialidades (17).
Como se puede evidenciar, a nivel mundial se están desarrollando múltiples iniciativas en el campo de la investigación genómica que generan, día a día, gran cantidad de información en el área, lo que demuestra la creciente importancia de incorporar en la práctica clínica todos estos conocimientos aportados desde la genética. Lo anterior, con el fin de mejorar y optimizar el ejercicio médico al disminuir los efectos adversos de los tratamientos farmacológicos y los costos de las fallas terapéuticas e incrementando de forma significativa la adherencia de los pacientes al tratamiento, así como su eficacia.
Medicamentos con enfoque farmacogenético
Cuando se prescribe un medicamento para el tratamiento de una patología determinada se pueden obtener diferentes resultados, debido a las variaciones genéticas de las enzimas encargadas de metabolizar los fármacos. En el caso de los medicamentos empleados para el manejo de la depresión y los episodios psicóticos, el metabolismo es efectuado por enzimas del citocromo P450 a nivel hepático, principalmente por CYP2D6, CYP1A2, CYP3A4 y CYP2C19. Dada la importancia de las principales enzimas del citocromo P450, las más importantes han sido secuenciadas y sometidas a procedimientos de clonación, identificando de esta manera las variantes genéticas más relevantes.
Gracias a esta información, ha sido posible establecer que algunas de estas variaciones genéticas ocasionan que determinados pacientes metabolicen con lentitud los medicamentos (por lo cual son llamados metabolizadores lentos) y que por este hecho requieran una formulación con dosis bajas para evitar la aparición de efectos secundarios. La contraparte de este fenómeno es producida por otras variaciones genéticas que originan una mayor tasa de metabolismo en pacientes denominados metabolizadores rápidos; estos requieren dosis anormalmente elevadas de los medicamentos para alcanzar un efecto terapéutico satisfactorio.
Con la información disponible sobre pacientes metabolizadores lentos o rápidos resulta factible llevar a cabo una formulación personalizada de medicamentos y así evitar la aparición de efectos secundarios potenciales (9). Al mismo tiempo, se obtendrían beneficios en términos de costo-efectividad, ya que se evitarían gastos de servicios médicos, utilizados para la atención de los efectos adversos de los medicamentos empleados y también se evitaría el uso fallido de múltiples fármacos ante la ausencia de resultados terapéuticos óptimos. En este contexto, la evaluación rutinaria del genotipo para el citocromo P450 que, como ya se mencionó, se realiza para sus principales enzimas, constituiría un procedimiento habitual previo a su formulación.
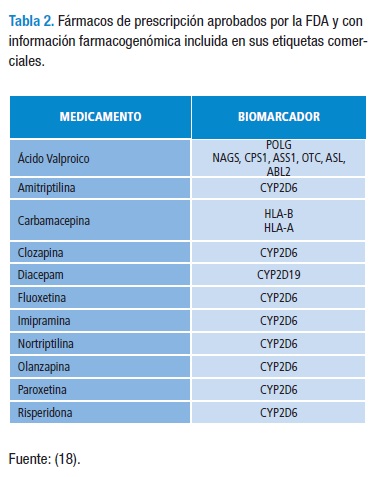
Atendiendo el creciente interés que estos aspectos farmacogenéticos han generado, la Agencia de Alimentos y Medicamentos (Food and Drug Administration-FDA) ha publicado unas recomendaciones para incluir aspectos farmacogenéticos en las etiquetas de algunos medicamentos (Tabla 2).
Con base en la información suministrada por la FDA, en México se han desarrollado algunas pruebas genéticas para emplearse en los pacientes antes de iniciar una medicación, lo cual evita los fenómenos descritos anteriormente. Aunque hay que resaltar que en este país no existen pruebas disponibles para medicamentos psiquiátricos, estos se han implementando para fármacos para el tratamiento de cáncer, hipercolesterolemia (estatinas) y anticoagulación (warfarina), entre otros (19).
Conflicto de interés: Ninguno declarado por los autores.
Financiación: Ninguna declarada por los autores.
Agradecimientos: Ninguno declarado por los autores.
Referencias
1. Lasky-Su J. A network medicine approach to psychiatric genetics. Am J Med Genet B Neuropsychiatr Genet. 2013;162B:579-86. [ Links ]
2. Avramopolus D. Genetics of psychiatric disorders methods: molecular approaches. Psychiatr Clin North Am. 2010;33:1-13. [ Links ]
3. Donix M, Small GW, Bookheimer SY. Family history and APOE-4 genetic risk in Alzheimer's disease. Neuropsychol Rev. 2012;22:298-309. [ Links ]
4. Boks MP, de Jong NM, Kas MJ, Vinkers CH, Fernandes C, Kahn RS , et al. Current status and future prospects for epigenetic psychopharmacology. Epigenetics. 2012;7:20-8. [ Links ]
5. Day JJ, Sweatt JD. Epigenetic Treatments for Cognitive Impairments. Neuropsychopharmacology. 2012;37:247-60. [ Links ]
6. Jakovcevski M, Akbarian S. Epigenetic mechanisms in neurodevelopmental and neurodegenerative disease. Nat Med. 2012;18:1194-204. [ Links ]
7. Lenroot RK, Giedd JN. Annual Research Review: Developmental considerations of gene by environment interactions. J Child Psychol Psychiatry. 2011;52:429-41. [ Links ]
8. Nebert DW, Zhang G, Vesell ES. From human genetics and genomics to pharmacogenetics and pharmacogenomics: past lessons, future directions. Drug Metab Rev. 2008;40:187-224. [ Links ]
9. Kalow W. Pharmacogenetics and pharmacogenomics: origin, status, and the hope for personalized medicine. Pharmacogenomics J. 2006;6:162-5. [ Links ]
10. Salari K, Watkins H, Ashley EA. Personalized medicine: hope or hype? Eur Heart J. 2012;33:1564-70. [ Links ]
11. Valiente A, Lafuente A, Bernardo M. Revisión sistemática de los Genowide Association Studies (GWAS) en esquizofrenia. Rev Psiquiatr Salud Ment. 2011;4:218-27. [ Links ]
12. Khokhar JY, Ferguson CS, Zhu AZ, Tyndale RF. Pharmacogenetics of Drug Dependence: Role of Gene Variations in Susceptibility and Treatment. Annu Rev Pharmacol Toxicol. 2010;50:39-61. [ Links ]
13. Sakolsky DJ, McCracken JT, Nurmi EL. Genetics of Pediatric Anxiety Disorders. Child Adolesc Psychiatr Clin N Am. 2012;21:470-500. [ Links ]
14. EGAPP Working Group. Evaluation of Genomic Applications in Practice and Prevention (EGAPP) [Internet]. Atlanta (US). 2009 [citado 2014 enero 7]. Disponible en: http://www.egappreviews.org/default.htm. [ Links ]
15. Vall D'hebron Institut de Recerca (VHIR). Fundación Instituto de Investigación Hospital Universitario Vall d'Hebron. [Internet] 2010 [citado 2013 enero 18]. Disponible en: http://www.vhir.org. [ Links ]
16. Centro Nacional de Análisis Genómico. Centre Nacional d'Analisi Genomica (CNAG) [Internet]. [citado 2013 diciembre 03]. Disponible en: http://www.pcb.ub.edu/homepcb/live/es/p3217.asp. [ Links ]
17. Instituto Nacional de Medicina Genómica (INMEGEN). Instituto Nacional de Medicina Genómica (INMEGEN). [Internet] 2013 [citado 2011 enero 13]. Disponible en: http://www.inmegen.gob.mx. [ Links ]
18. U.S. Department of Health and Human Services. U.S Food and Drug Administration. [Internet]. [citado 2014 enero 7]. Disponible en: http://www.fda.gov/drugs/scienceresearch/researchareas/pharmacogenetics/ucm083378.html. [ Links ]
19. GBC Group. Global Biotech Consulting Group. [Internet]. [citado 2011 julio 03]. Disponible en: http://www.gbcbiotech.com/farmacogenomica/index.html. [ Links ]