Introducción
La infección viral respiratoria superior (IVRS) es la enfermedad más prevalente de la primera infancia. Muchos niños que requieren ser sometidos a cirugía con anestesia general tienen historia de infección reciente o activa 1.
Las IVRS representan un factor de riesgo importante para el desarrollo de eventos adversos respiratorios perioperatorios (EARP), en su mayoría manejables y asociados a una morbilidad mínima 2,3. El espectro clínico de estas infecciones incluye resfriado común, faringoamigdalitis, sinusitis, laringotraqueitis, entre otras. Más de 200 tipos de virus se han asociado a este tipo de infección, siendo los rinovirus, los coronavirus, el virus sincitial respiratorio, la influenza y la parainfluenza los agentes etiológicos más comunes 4,5. Otros agentes etiológicos involucrados son adenovirus, enterovirus, sarampión, herpes tipo 3,6 y 7 y coxsackie 6.
La infección de la vía aérea determina una hiperreactividad que facilita la aparición de EARP que incluyen laringoespasmo, broncoespasmo, pausas apneicas, hipoxia, desaturación, tos, atelectasias, etc. En la mayoría de los casos estos eventos son de intensidad leve, de relativo fácil manejo y con consecuencias no demostradas a largo plazo; los casos severos son de difícil o inadecuado manejo y pueden conllevar a daño neurológico, discapacidad y muerte 7-11.
El laringoespasmo se constituye como la principal causa de paro cardiaco en población infantil, siendo los EARP la segunda causa 12,13. A pesar de que los niños con IVRS tienen tendencia a la desaturación, esta responde de forma adecuada a la administración de oxígeno 14,15.
Por 10 general, la infección respiratoria se autolimita entre 7-10 días después de iniciado el cuadro. En este período de tiempo la invasión viral del epitelio respiratorio conlleva a inflamación y edema, que sensibilizan la vía respiratoria a las secreciones y a la acción de los anestésicos volátiles, generando hiperreactividad bronquial y broncoconstricción persistentes 4. La infección interactua además con el sistema nervioso autónomo. Las neuraminidasas virales inhiben receptores M2 colinérgicos, con consecuente aumento en la liberación de acetilcolina y tendencia a la broncoconstricción 4,16). La hiperreactividad bronquial también puede resultar de la liberación de taquicininas y neuropeptidasas con constricción del músculo liso de las vías respiratorias hasta seis semanas más allá de la resolución de los síntomas 4.
La hiperreactividad bronquial es crítica en el primer mes, en especial en las primeras dos semanas tras el inicio de los síntomas. Estudios observacionales han mostrado un descenso importante del riesgo de EARP entre la segunda y la cuarta semana y un riesgo no significativo tras cuatro semanas de iniciado el proceso infeccioso 3,7,17,18. Otros factores que podrían contribuir a la aparición de dichos eventos adversos se describen en la Tabla 1 19-26.
Tabla 1 Factores de riesgo adicionales para infección viral respiratoria superior asociados a la aparición de eventos adversos respiratorios perioperatorios en niños.
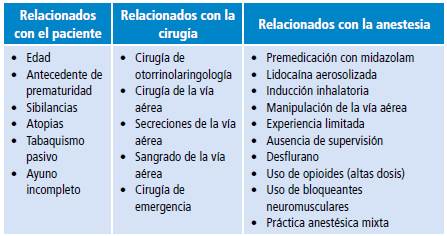
Fuente: Elabaración propia.
El objetivo del presente artículo es realizar una revisión narrativa para responder a la pregunta ¿cuál es el manejo perioperatorio actual de los niños con infección respiratoria superior que requieren ser llevados a un procedimiento quirúrgico bajo anestesia general? Esto en favor de determinar las pautas de manejo perioperatorio actual de dicha población.
Materiales y métodos
A enero de 2018, se realizó una búsqueda estructurada de la literatura en las bases de datos ProQuest, EBSCO, ScienceDirect, PubMed, LILACS, Embase, Trip Database, SciELO y Cochrane Library, sin límite de tiempo, con los términos: Anesthesia AND Respiratory Tract Infections AND Complications; Anesthesia AND Upper respiratory tract infection AND Complications; Anesthesia, General AND Respiratory Tract Infections AND Complications; Anesthesia, General AND Upper respiratory tract infection AND Complications; Anesthesia AND Laryngospasm OR Bronchospasm.
La búsqueda se realizó en inglés con sus equivalentes en español y estuvo limitada a revisiones sistemáticas con o sin metaanálisis y ensayos clínicos aleatorizados en favor de elaborar las recomendaciones de tratamiento. Se realizó una búsqueda secundaria con el fin de obtener información pertinente para los demás tópicos de la presente revisión. La calidad de la evidencia se evaluó mediante la aplicación de los instrumentos para lectura crítica del Critical Appraisal Skills Programme Español (CASPe).
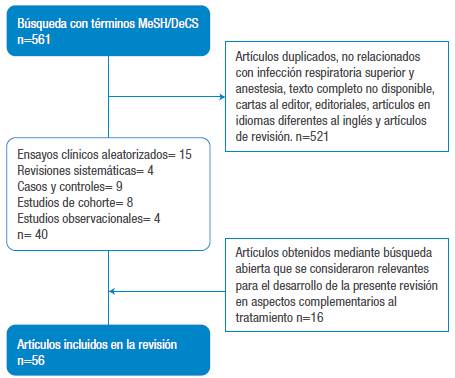
La inclusión de cada una de las referencias de la presente revisión se definió en consenso por dos coautores y fueron seleccionadas revisiones sistemáticas con o sin metaanálisis, ensayos clínicos, estudios de cohorte, casos y controles y estudios observacionales. Se desestimaron artículos que no tuvieran relación con la infección respiratoria superior y anestesia, manuscritos con texto completo no disponible, editoriales, cartas al editor y artículos de revisión narrativa. No obstante, hubo necesidad de incluir algunos manuscritos de este último tipo con el fin de complementar tópicos de la revisión diferentes al tratamiento (Figura 1 ).
Resultados
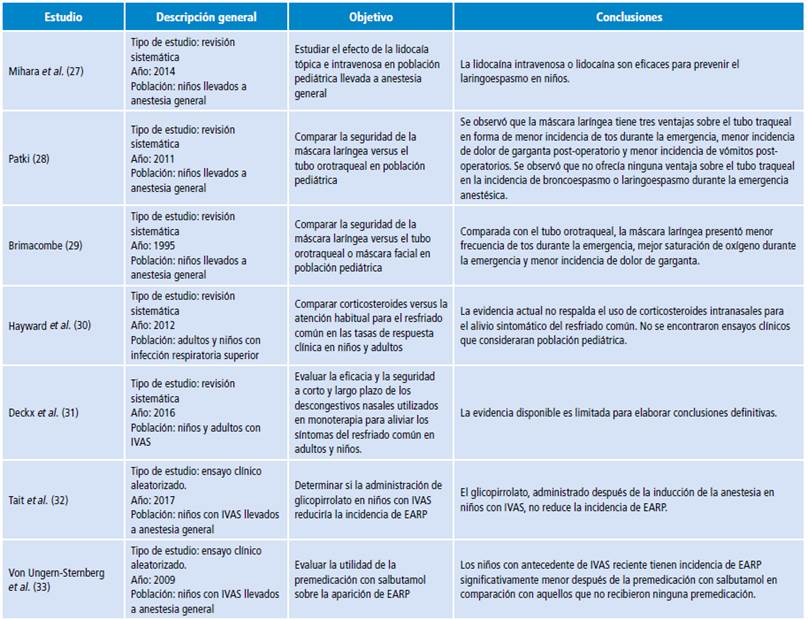
Mediante búsqueda estructurada, se encontraron 56 publicaciones con información relevante para el desarrollo de la presente revisión: 4 revisiones sistemáticas, i 5 ensayos clínicos, 8 estudios de cohorte, 9 estudios de casos y controles, 4 estudios observacionales y 16 artículos obtenido mediante búsqueda abierta (Tabla 2).
Discusión
El manejo perioperatorio de los niños con infección respiratoria superior reciente no está estandarizado y la evidencia al respecto continúa siendo deficiente, en especial en ensayos clínicos y revisiones sistemáticas que permitan realizar conclusiones definitivas al respecto. Existe consenso en que los niños con infección activa no deben ser llevados a procedimientos electivos; sin embargo, en niños con antecedente reciente (dos a cuatro semanas previas) no existe consenso de la optimización preoperatoria, siendo la mayoría de las recomendaciones una extrapolación derivada de estudios realizados en niños sin infección respiratoria o una patología similar como el asma. A continuación se describen más detalladamente los distintos enfoques de manejo.
Valoración preoperatoria
Historia clínica y examen físico
La valoración preanestésica está dirigida a determinar la presencia de infección reciente o activa de la vía aérea. El examen físico debe incluir el examen directo de la vía aérea superior y estructuras relacionadas y pretende buscar signos consistentes con la presencia o la severidad de la infección. Una auscultación sistemática puede informar hallazgos de infección respiratoria, incluyendo estridor, sibilancias, roncus y estertores gruesos, compatibles con infección no parenquimatosa de la vía aérea. El espectro de la enfermedad incluye apariencia enferma, irritabilidad, anorexia, astenia, adinamia, fiebre, rinorrea, congestión nasal, estornudos, dolor de garganta, tos, expectoración, eritema faríngeo, entre otros 34.
La percepción del padre acerca de la presencia de resfriado en el niño podría ser superior a los signos y síntomas clínicos clásicos. El estudio de casos y controles de Schreiner et al.26 realizado en 15 183 niños, 123 de los cuales sufrieron laringoespasmo, concluyó que el espasmo laríngeo fue dos veces más frecuente en los niños cuyos padres refirieron la presencia de síntomas respiratorios de la vía aérea superior (OR: 2.05, IC95%: 1.21-3.45).
Exámenes de laboratorio
Las ayudas de laboratorio deben solicitarse de forma individualizada con base en los datos de la historia clínica y los hallazgos del examen físico. Es usual que no sean de mayor utilidad en el contexto de la IVRS, que por lo general es de curso relativamente benigno 4.
Exámenes radiológicos
Al igual que ocurre con las demás ayudas del laboratorio, el apoyo imagenológico mediante la radiografía de tórax rara vez es necesario. Su solitud debe ser particularizada, en especial cuando existe sospecha de enfermedad parenquimatosa pulmonar concomitante 4.
Necesidad quirúrgica
No existe consenso en la literatura respecto al algoritmo de manejo de niños con infección de la vía aérea superior activa o reciente en el contexto de la cirugía electiva. Un abordaje lógico debería tomar en cuenta la cronología de la infección y la presencia de factores de riesgo para EARP concomitantes. A excepción del niño con rinorrea aislada, no debería programarse para cirugía electiva ningún paciente pediátrico con infección respiratoria de la vía aérea superior hasta cuatro semanas después del inicio de la enfermedad, aunque la reprogramación de la cirugía no garantiza la ausencia de IVRS, ya que los niños en edad preescolar y escolar pueden llegar a tener de seis a ocho episodios por año 25. En la Tabla 3 se describe un algoritmo de manejo en consideración a la disminución significativa del riesgo de EARP después de dos a cuatro semanas de instaurada la infección 35,36.
Tabla 3 Algoritmo de manejo de niños con infección viral respiratoria superior que van a ser sometidos a cirugía electiva.
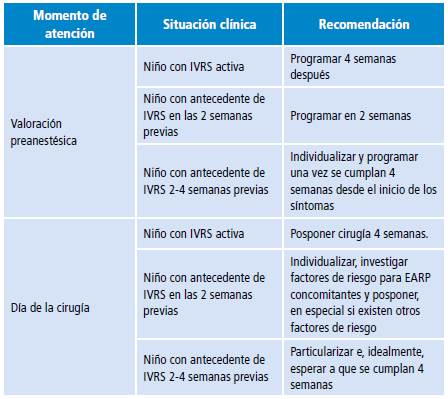
IVRS: infección viral respiratoria superior, EARP: eventos adversos respiratorios perioperatorios.
Fuente: Elaboración propia.
La mayoría de la evidencia sugiere que los procedimientos para niños que presentan rinitis purulenta, fiebre, tos productiva y alguna evidencia de infección respiratoria baja deben ser cancelados 35.
Cirugía de urgencia
Tampoco existe consenso en la literatura respecto al algoritmo de manejo del niño con infección de la vía aérea superior activa o reciente que requiere cirugía de urgencia. La literatura sugiere un análisis conjunto con el cirujano respecto a la necesidad quirúrgica. En aquellos menores que decidan llevarse a anestesia, aunque sin adecuado nivel de evidencia, podría recomendarse el uso de medidas medicamentosas de optimización prequirúrgica si la urgencia lo permite 35,36.
Medicación preoperatoria
La optimización preoperatoria consiste en la medicación del paciente en favor de mejorar la función respiratoria de base.
Agonistas inhalados de corta acción de receptores beta-2 agonistas
Son escasos los estudios que recomiendan el uso de broncodilatadores en pacientes con IVRS activa o reciente. Algunas referencias con nivel bajo de evidencia han sugerido que podrían ser útiles en esta población cuando se utilizan 20-30 minutos antes de la inducción anestésica, pero no existe claridad respecto a las dosis o la pauta de manejo. La evidencia que apoya el uso de beta-2 agonistas inhalados se basa en estudios que han mostrado su efectividad en pacientes asmáticos o con sibilancias recurrentes 37,38.
No existe consenso respecto a la utilización preoperatoria de estos fármacos para disminuir la incidencia de broncoespasmo y otros eventos adversos respiratorios 39,40; la evidencia es discrepante respecto a los resultados, en especial en pacientes con IVRS. Un ensayo clínico realizado con 109 pacientes de menos de 18 años con IVRS no encontró beneficio en la administración de broncodilatador (ipratropio o salbutamol) nebulizado en comparación con el placebo 41. En contraste, en el estudio de von Ungern-Sternberg et al.33 se comunicó una disminución en la tasa de broncoespasmo y tos en niños con IVRS en anestesia general y premedicados con salbutamol.
Antisialogogos
Un componente fundamental en la prevención de EARP, en especial del laringoespasmo, es la disminución del nivel basal de secreciones. A pesar de lo anterior, no existe evidencia fuerte para recomendar la administración rutinaria de atropina o glucopirrolato en pacientes con IVRS y por tanto su administración debería realizarse con base al criterio del anestesiólogo. El ensayo clínico de Tait et al.32, realizado con 130 niños con IVRS, no encontró ventaja en la administración de glucopirrolato para reducir la incidencia de EARP.
Oximetazolina
No existe evidencia que apoye el uso de oximetazolina (un agonista alfa-1 y agonista parcial alfa-2) como descongestionante nasal para la optimización preoperatoria de pacientes con IVRS que requieren anestesia general. Deckx et al.31, en su revisión sistemática, no determinan la eficacia y perfil de seguridad de los descongestionantes nasales, incluyendo la oximetazolina, en población pediátrica.
Corticosteroides
En su revisión, Hayward et al.30 no encontraron ensayos clínicos que apoyaran el uso de corticosteroides en pacientes con resfriado común. En general, no existe evidencia de primer nivel que sostenga el uso de corticoesteroides en el paciente con IVRS, por lo que su uso debería restringirse a los pacientes con asma no controlada.
Ansiolíticos
A pesar de que el efecto del midazolam sobre la capacidad residual funcional y la mecánica respiratoria es discreto a dosis usuales, este puede prolongar el plano excitatorio durante la emergencia de la anestesia, por lo que se ha sugerido que puede existir un incremento de EARP en pacientes premedicados con benzodiacepinas, sin que existan resultados concluyentes al respecto 42.
Aunque no ha sido demostrado y tiene escaso nivel de evidencia, la disminución de la ansiedad del menor fundamentada en la compañía de los padres o mediante técnicas de distracción (juegos) podría tener un papel fundamental dentro del manejo anestésico del paciente con IVRS. El llanto puede aumentar el nivel de secreciones, lo que a su vez produce un incremento de la reactividad de la vía aérea.
Tratamiento anestésico
Manejo de la vía aérea
La manipulación de la vía aérea, en especial en planos anestésicos superficiales, aumenta el riesgo de EARP. La frecuencia de estos es mayor con el tubo endotraqueal que con los dispositivos supraglóticos y mayor con estos que con la ventilación con máscara facial 43,44.
Un metaanálisis de ensayos clínicos realizados con 1 242 pacientes sin IVRS, menores de 12 años, con anestesia general y con máscara laríngea o tubo endotraqueal encontró aumento en la incidencia de la tos y el dolor de garganta post-operatorios con el uso de tubo endotraqueal, pero sin diferencias en la incidencia de laringoespasmo o broncoespasmo 28.
Por su parte, Gharaei et al.45, en un ensayo clínico aleatorizado, randomizado y con doble cegamiento que incluyó 145 niños con IVRS no complicada, no encontraron diferencia significativa entre el uso de máscara laríngea y máscara facial respecto a incidencia de laringoespasmo, broncoespasmo, apnea, desaturación y dolor de garganta.
Dada la evidencia, no es posible realizar conclusiones respecto al manejo de la vía aérea, por lo que cada caso debería particularizarse 29.
Inducción y mantenimiento de la anestesia
Las diversas pautas para la inducción y el mantenimiento de la anestesia general escapan a los objetivos de la presente revisión. Sin embargo, deberían evitarse medicamentos con capacidad de potenciar la hiperreactividad de la vía aérea.
La anestesia general produce alteración del aclaramiento ciliar más pronunciado con sevoflurano que con propofol. Aunque las implicaciones clínicas son desconocidas, debería considerarse evitar la inducción inhalatoria con sevoflurano. La disminución de la expulsión de las secreciones después de una IVRS, junto con el efecto estimulante de los gases inhalados, quizás tenga efectos acumulativos que contribuyan a los eventos adversos respiratorios 46.
Ventilación mecánica
La ventilación en el paciente con IVRS tiene como objetivo la prevención de complicaciones como las atelectasias y el barotrauma. Los parámetros de ventilación protectora, extrapolables al paciente con IVRS, incluyen un volumen corriente de 6-10 mL/kg de peso ideal, presión positiva al final de la espiración entre 5cm y 10cm de H2O y una relación inspiración:espiración (I:E) aumentada 47.
Laringoespasmo y broncoespasmo
El laringoespasmo causa cerca del 40% de las obstrucciones post-extubatorias de la vía aérea 48. La incidencia de laringoespasmo en la población pediátrica oscila entre 0.04% y 14% y se incrementa en pacientes con infección viral de la vía aérea superior, siendo aún más probable en cirugía de la vía aérea 49-51.
Extubación
Al menos dos estudios realizados con niños sin IVRS no han encontrado diferencias estadísticamente significativas entre la extubación en plano profundo o con el paciente despierto respecto a la incidencia de laringoespasmo y broncoespasmo 52,53, sin embargo ninguno de los dos incluyó pacientes con IVRS.
Una revisión sistemática de ensayos clínicos controlados encontró que la lidocaína, tanto tópica aplicada sobre el dispositivo supraglótico como por vía endovenosa a dosis de 1-2 mg/kg y en comparación con el placebo o con el no uso del medicamento, es útil para la prevención del laringoespasmo durante la inducción, el mantenimiento o la extubación 27. No existen estudios en niños con IVRS, por lo que estos resultados no pueden generalizarse. Además, el uso directo de lidocaína sobre las cuerdas podría desencadenar laringoespasmo 54,55.
Vigilancia post-operatoria
A pesar de que el laringoespasmo es una complicación usualmente intraoperatoria, el broncoespasmo, la tos y las desaturaciones pueden ocurrir en el ambiente post-operatorio, por lo que los niños deben tener al menos monitoría no invasiva básica durante su estancia en la unidad de recuperación post-anestésica. El antecedente de asma, sibilancias recurrentes, infección por virus sincitial respiratorio y las cardiopatías congénitas se consideran factores de riesgo para el desarrollo de EARP posoperatorios 56.
Conclusión
La IVRS condiciona un fenómeno hiperreactivo que induce mayor riesgo de complicaciones perioperatorias. Una adecuada valoración preanestésica, basada en la historia clínica, y un examen físico minucioso son necesarios para determinar el riesgo preoperatorio del paciente con este tipo de infección. No existe evidencia para recomendar las pautas de optimización preoperatoria de forma rutinaria; el uso de las mismas debe depender del criterio del anestesiólogo.
Es indispensable el manejo personalizado de los dispositivos de la vía aérea y una adecuada utilización de los medicamentos durante la inducción y el mantenimiento anestésicos. La lógica llama al retiro de los dispositivos de vía aérea, preferiblemente en plano profundo, a pesar de que no existe evidencia suficiente para recomendar tal práctica. La monitoria post-operatoria es una parte esencial del manejo post-operatorio del paciente con IVRS, activa o reciente.