Introducción
Al hablar de neuropatía periférica, por lo general se hace referencia al compromiso múltiple y simétrico de los nervios periféricos, el cual lleva a grados variables de debilidad muscular y cambios en la sensibilidad, lo que se conoce como polineuropatía 1; esta afección puede ser desencadenada por diversas afecciones como síndrome de Guillain-Barré (SGB), sida, intoxicación por talio, porfiria intermitente aguda (PIA), etc. 2-4.
La porfiria comprende un conjunto de enfermedades metabólicas y consiste en la deficiencia de enzimas encargadas de la biosíntesis del grupo hemo, lo que produce aumento y acumulación tóxica de los precursores, afectando diversos sistemas 5-8. Factores precipitantes pueden inducir dicha toxicidad, aumentando la demanda del grupo hemo e induciendo la actividad del ácido delta aminolevulínico (ALA) sintetasa; la síntesis de productos tóxicos también aumenta.
Por otro lado, el SGB es una enfermedad neurológica que incluye un grupo de neuropatías periféricas de origen autoinmune y con complicaciones graves que inician posterior a la presencia de factores desencadenantes; se manifiesta con parálisis motora, con o sin pérdida de sensibilidad y algunas veces con disautonomias 9-11.
La gran variedad de manifestaciones clínicas y agentes desencadenantes de la porfiria y el SGB pueden confundir el diagnóstico. Dentro de los factores desencadenantes de porfiria se encuentran fármacos (barbitúricos, rifampicina, diazepam, fenitoina, carbamezepina), sustancias psicoactivas, hormonas esteroideas, estrés, procedimientos quirúrgicos, alcohol, infecciones y factores endocrinos (ciclo menstrual y otros). Por su parte, en el SGB pueden influir vacunas (rabia, tétanos, virus del papiloma humano, influenza, sarampión), infecciones (Campylobacter jejuni, virus de Epstein-Barr, citomegalovirus, virus del Zika, virus del chikunguña, virus de la inmunodeficiencia humana), procedimientos quirúrgicos, neoplasias y enfermedades autoinmunes.
Gran parte de las patológicas quirúrgicas son orientadas por el dolor abdominal, síntoma poco específico que cursa con múltiples causas 12; aunado a lo anterior, las intervenciones quirúrgicas también se han reportado como un posible factor desencadenante del SGB 13. Pacientes en quienes se han excluido patologías típicas causantes de dolor abdominal sin mayores hallazgos que sostengan su diagnóstico deben generar sospecha de enfermedades poco frecuentes como las porfirias.
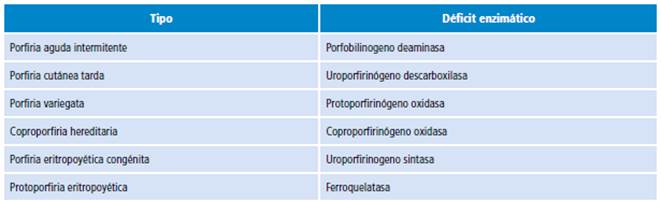
En la síntesis del grupo hemo (Figura 1) intervienen múltiples enzimas y la afección de cada una de ellas produce un subtipo diferente de porfiria (Tabla 1). La regulación descontrolada de ALA sintasa tipo 1 en el hígado es el problema principal en los ataques agudos de porfiria 14. La PIA se clasifica como porfiria hepática debido a que el principal sitio de expresión del defecto enzimático se encuentra en el hígado 15.
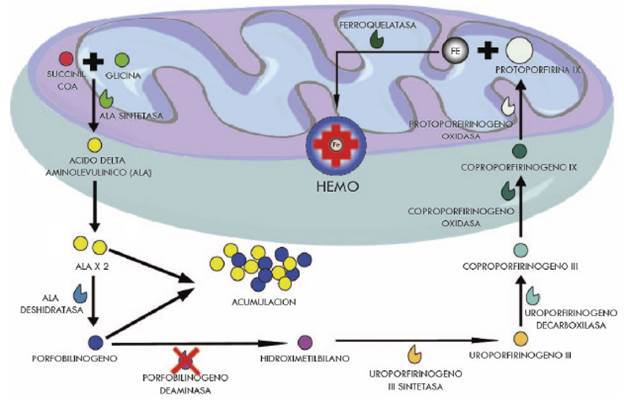
Fuente: Elaboración propia.
Figura 1 Síntesis del grupo hemo y afección enzimática en porfiria intermitente aguda. SUCCINIL COA: succinil coenzima A; ALA: acido delta aminolevulinico; Fe: Hierro.
En los ataques agudos, el déficit enzimático no es total y cerca de la mitad de las enzimas son activas, lo que permite mantener la homeostasis metabólica en ausencia de desencadenantes específicos 16,17.
En la PIA la deficiencia enzimática parcial de porfobilinogeno deaminasa (Figura 1) eleva la concentración de ALA y porfobilinogeno 6,14, relacionados con formación de complejos inmunes y actividad inflamatoria; a su vez, esto desencadena daño neurológico 18. Aunado a lo anterior, existen síntomas con la misma base fisiopatológica ubicados en otros sistemas orgánicos (Figura 2).
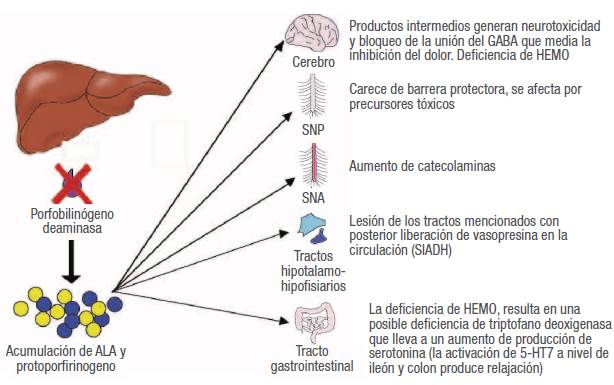
ALA: acido delta aminolevulinico; GABA: ácido gama aminobutírico; SNP: sistema nervioso periférico; SNA: sistema nervioso autónomo; SIADH: síndrome de secreción inadecuada de la hormona antidiurética; 5-HT7: receptor de serotonina (hidroxitriptamina). Fuente: Elaboración propia.
Figura 2 Fisiopatología de la porfiria.
Un ataque de polineuropatía porfírica se caracteriza por el desarrollo súbito de cólicos abdominales, vómito, estreñimiento, fiebre, taquicardia, hipertensión o hipotensión y leucocitosis 15,19. En el punto más alto de los síntomas se puede observar un hallazgo característico de cambio de color de la orina hacia un tono violáceo ante la exposición a la luz, lo cual se explica por la conversión mediante oxidación de porfobilinógeno en porfobilina 20,21.
No es infrecuente encontrar alteraciones psiquiátricas que conlleven a un diagnostico psiquiátrico errado 22,23. Las crisis de dolor abdominal pueden presentarse con alteraciones neurológicas como convulsiones o compromisos de pares craneanos bulbares 24,27. Posterior a las crisis recurrentes de dolor abdominal aparecen signos de polineuropatía con parálisis fláccida de rápido desarrollo en extremidades superiores e inferiores 24,28, extendiéndose hasta afectar los pares craneanos y aumentando el riesgo de paro respiratorio 5,27,29. Los dolores y parestesias en las extremidades son comunes y los trastornos objetivos de la sensibilidad suelen estar presentes 30. Debido a las diversas complicaciones ya descritas, la mortalidad en caso de polineuropatía en la porfiria es alta 23.
El objetivo del presente reporte de caso es dar a conocer el caso de una paciente quien presentó síntomas inespecíficos de porfiria y SGB, fue evaluada de manera integral y recibió tratamiento para ambas patologías, respondiendo de manera inusual a estos; además, se hace una breve revisión de la literatura.
Presentación del caso
Paciente femenino de 18 años quien consultó a un hospital de II nivel por dolor abdominal tipo cólico en fosa ilíaca derecha, fiebre, náuseas y vómito. La joven fue valorada por el servicio de cirugía general, el cual determinó realizar apendicectomía sin hallazgos quirúrgicos. Posterior a ello, persiste dolor abdominal en mesogastrio e hipogastrio, vómito y distensión abdominal. Sin mejoría, reconsulta y se remite a III nivel donde se realiza tomografía axial computarizada abdominal, que muestra un patrón de íleo adinámico que es confirmado en revisión quirúrgica.
Paralelo a la evolución, la paciente presenta ansiedad y angustia, síntomas vagos de tipo psiquiátrico, lo que lleva la impresión diagnóstica de neurosis histérica y por lo que se trata de afrontar a la paciente, sin mayores resultados. En búsqueda de nuevas posibilidades diagnósticas y durante evaluación por fisiatría, la joven hace signos de dificultad respiratoria y alteración motora en miembros inferiores, por lo que se solicita interconsulta con el servicio de neurología. El examen neurológico encuentra una paciente con notoria dificultad respiratoria, paraparesia flácida e hipotonía, pero sin compromiso de sensibilidad y reflejos de estiramiento muscular ausentes bilateralmente, planteándose el diagnóstico de SGB.
El trastorno motor ascendió a extremidades superiores en un lapso de 30 minutos, por lo que se ordenó traslado al servicio de emergencia donde se realizó intubación orotraqueal. El médico de la sala reinterrogó a los acompañantes, encontrando antecedentes familiares paternos de porfiria, por lo que se ordenó la exposición a la luz solar de orina, observando cambio en su color y considerando el diagnóstico de PIA. Debido a la sospecha inicial de SGB, se alcanzaron a administrar dos dosis de inmunoglobulina intravenosa, pero al conocer el resultado del cambio en el color de la orina, la presencia de insuficiencia respiratoria y la disponibilidad de cupo en unidad de cuidado intensivo, la paciente fue trasladada a este servicio y se suspendió tal medicamento.
Con el diagnóstico de porfiria se inició tratamiento con arginato de hematina, sin presencia de mejoría significativa durante las primeras 72 horas. En esta fase de la evolución se practicó electromiograma y velocidades de conducción nerviosa que determinaron una poliradiculoneuropatía aguda sensitiva motora y se aplicaron los criterios de Brighton, que la clasificaron en el nivel 2 de certeza diagnostica para SGB. Ante este resultado y después de interconsultar a hematología, los servicios de neurología y cuidado intensivo reiniciaron la inmunoglobulina.
La evolución después de la aplicación de inmunoglobulina mostró mejoría lenta desde el punto de vista motor, luego se tuvo acceso a los exámenes de laboratorio solicitados para el diagnóstico de porfiria: porfobilinogeno en orina en 24 horas elevado (146.5 mg/24 horas) y ácido delta aminolevulínico elevado (136 mg/24 horas), por 10 que se continuó con el tratamiento con arginato de hematina.
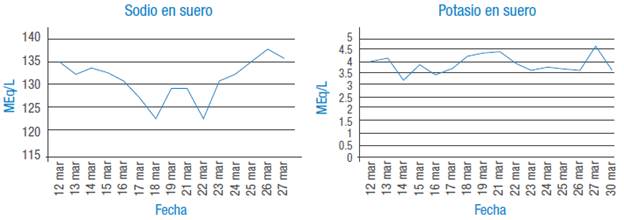
Aunado a la problemática planteada, la paciente cursó con taquicardia sinusal, alteraciones electrolíticas expresadas por constantes episodios de hiponatremia -sin alteraciones del potasio (Figura 3)-, neumonía e infección de vías urinarias, que fueron manejados a su tiempo.
Al momento de este estudio, y tras un enfoque multidisciplinario, la paciente ha evolucionado de manera satisfactoria en el aspecto motor, recuperando gran parte de su movilidad, aunque persiste marcha de Steppage. Asimismo se observa hiponatremia durante la evolución clínica sin alteraciones en los niveles de potasio.
Discusión
La presente investigación trata de un relato de caso clínico y una revisión de la literatura llevada a cabo mediante las bases de datos Medline y los buscadores específicos Imbiomed, PubMed, ScienceDirect y SciELO. Las palabras claves utilizadas fueron Hemina, porfirias, Polineuropatías, Síndrome de Guillain-Barré y dolor abdominal.
El caso tuvo una evolución clínica ensombrecida por la similitud semiológica de la porfiria con otro tipo de patologías de mayor frecuencia, razón por la cual esta patología es conocida como "la gran imitadora" 31,32, convirtiéndose en una enfermedad subdiagnosticada 33.
La incidencia en Colombia es de 1-2 por cada 100 000 personas, siendo más común en muj eres con una relación de 4-5:1 con respecto a los hombres 29,34.
La paciente presentó un cuadro clínico que inició con dolor abdominal acompañado de fiebre, náuseas, vómito y distención abdominal, síntomas que reporta la literatura con gran frecuencia 1,6,35; también se registró depresión y ansiedad, manifestaciones psiquiátricas que se presentan en la porfiria en cerca del 25% de los ataques agudos 36.
La evolución tórpida y las falsas sospechas diagnósticas permiten un progreso de síntomas hacia alteraciones motoras, paraparesia flácida hipotónica, manifestaciones neurológicas explicadas por la degeneración axonal difusa y signos de dificultad respiratoria debido a la afección de pares craneanos que podría progresar a parálisis respiratoria bulbar con una alta probabilidad de muerte. También se presentó hiponatremia, que en algunos pacientes se explica secundaria a la secreción inadecuada de hormona antidiurética la cual puede llevar a convulsión. Este tipo de alteraciones han tenido amplia investigación y son causantes del mimetismo casi exacto con el SGB (Tabla 2) 1,5,6,8,21,24,29,31,32,35,37-43.
Tabla 2 Manifestaciones clínicas de porfiria y síndrome de Guillain-Barre.
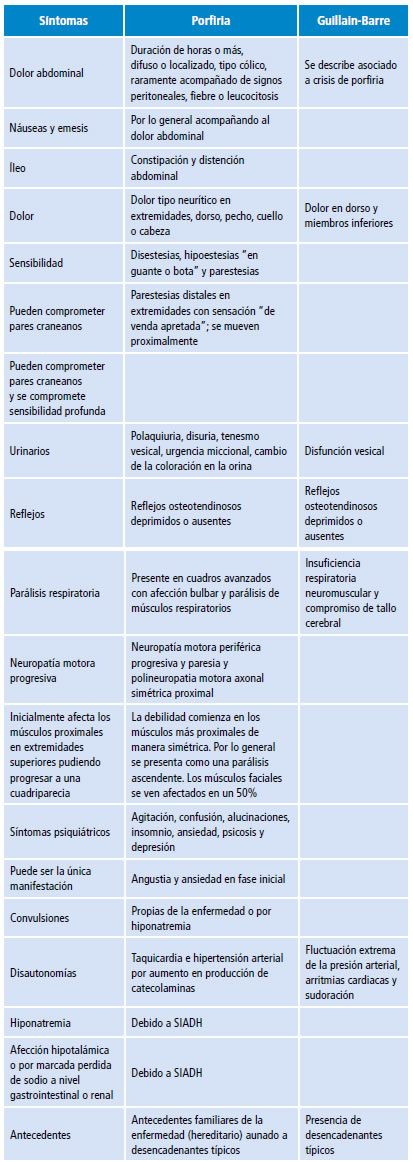
SIADH: síndrome de secreción inadecuada de la hormona antidiurética.
Fuente: Elaboración propia.
El caso clínico presentado se caracterizó por una marcada confusión en el diagnóstico debido a la gran similitud clínica y paraclínica entre ambas patologías (Tabla 3), aunque exámenes específicos como porfobirinogeno (PBG) urinario y medición de ALA para alteraciones porfíricas y medición de anticuerpos antigangliosidos para SGB son indicativos de las mismas 6,14,44-47. En el presente caso no se estudiaron agentes infecciosos que pudiesen haber desencadenado el SGB debido al limitado acceso a estas pruebas y la ausencia de síntomas infecciosos en la paciente.
Tabla 3 Paraclínicos en porfiria y síndrome Guillain-Barre.
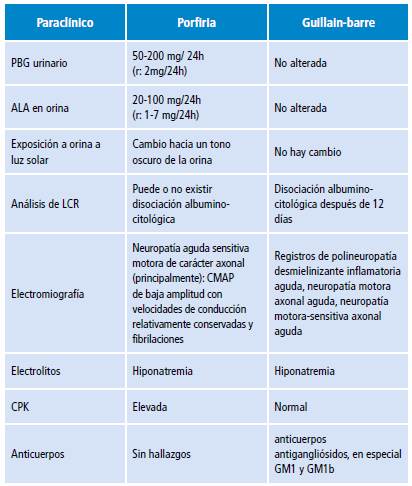
r: valor de referencia; ALA: acido delta aminolevulinico; LCR: líquido cefalorraquídeo; CMAP: potencial de acción motor compuesto; CPK: creatina-fosfocinasa.
Fuente: Elaboración propia.
El tratamiento se hizo en primera instancia con inmunoglobulina ante las sospechas de SGB; luego se inició tratamiento con hematina, base fundamental en el tratamiento de porfiria 6,14,15,29,43,48,49.
En medio de la confusión diagnostica y los múltiples tratamientos realizados, llamó la atención la recuperación significativa de las variables neurológicas al suministrar inmunoglobulina a dosis de tratamiento de SGB.
La acumulación de productos tóxicos en porfiria se ha relacionado con la formación de complejos inmunes y la reacción inflamatoria, que pueden explicar parte del daño neurológico presente 18 y da partir de lo cual puede plantearse la hipótesis de una relación causa-efecto entre ataque agudo de profiria y SGB, respectivamente 47,50, fundamentando la respuesta del cuadro porfirico al ciclo de inmunoglobulinas.
Conclusiones
La prevalencia de la PIA es baja, pero sus complicaciones pueden ser fatales y pueden presentarse debido a confusiones en la práctica clínica generadas por su similitud con patologías tales como el SGB. Si bien su diferenciación es importante para intervenir de manera adecuada, se debe tener presente un concepto importante y es el relacionado con dos hechos que se deben diferenciar: neuropatía de etiología en PIA y complicación de una crisis de PIA que produce SGB.
La respuesta generada por la paciente al tratamiento con inmunoglobulina y su posible explicación fisiopatológica debe dar inicio a estudios con mayor profundidad para el análisis de la misma y posteriores ensayos clínicos que permitan utilizar herramientas farmacológicas existentes, pero aún no relacionadas con la patología.