Introducción
En mujeres, el riesgo de desarrollar enfermedad tromboembólica venosa (ETV) es 5 a 6 veces mayor durante el embarazo.1 De igual forma, es importante anotar que con antecedentes familiares de estados protrombóticos este riesgo se incrementa de 3.7 a 8.5 veces2 y que cuando existe antecedente personal de trombofilia (especialmente mutación del factor V de Leiden y deficiencia de proteínas C y S y de antitrombina), se eleva hasta 34 veces.3
La ETV, que incluye el tromboembolismo pulmonar (TEP) y la trombosis venosa profunda (TVP), puede desarrollarse durante la totalidad de la gestación y hasta la sexta semana posparto; afecta entre 10 y 17 mujeres por cada 10 000 embarazos, y es una importante causa de morbimortalidad en esta población.4,6 Por lo anterior, es necesario realizar una adecuada clasificación de riesgo a todas las pacientes y controlar los factores de riesgo para desarrollar ETV.7
Dado el impacto de esta enfermedad, el objetivo del presente estudio fue describir el uso de pruebas de tamizaje de estados protrombóticos y de la tromboprofilaxis farmacológica y no farmacológica para prevenir la ETV durante la gestación, el parto y el puerperio. Con esta revisión se propuso responder a la siguiente pregunta de investigación ¿Qué se recomienda en cuanto al uso de pruebas de tamizaje de estados protrombóticos y la aplicación de tromboprofilaxis para prevenir la ETV en la gestación, el parto y el puerperio?
Materiales y métodos
Se realizó una revisión de la literatura en las bases de datos Embase, ClinicaIKey, ScienceDirect, Access Medicine, Scopus, ProQuest, PubMed y LILACS mediante la siguiente estrategia de búsqueda: periodo de publicación: enero de 2004 a marzo de 2018; idiomas: inglés y español; tipos de estudio: guías de práctica clínica, revisiones sistemáticas con o sin meta análisis, revisiones narrativas y de tema, capítulos de libro, boletines y consensos clínicos, reportes o series de caso y estudios transversales, de cohorte, experimentales o de casos y controles, cuya población de estudio fueran mujeres gestantes adultas; términos y ecuaciones de búsqueda: "Thromboprophylaxis AND pregnancy OR Thrombophilia AND pregnancy OR Inferior cava filter in pregnancy OR Anticoagulants in pregnancy" y sus equivalentes en español.
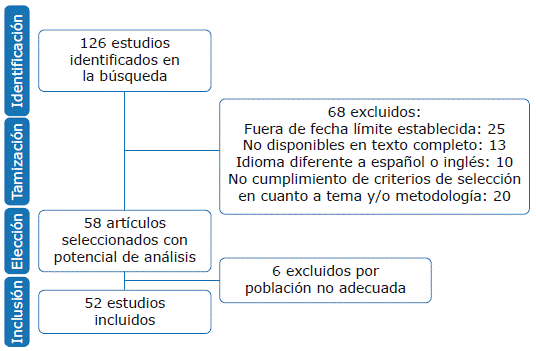
La búsqueda se realizó entre el 1 y el 30 de marzo de 2018 y se excluyeron aquellas referencias que no estuvieran disponibles en texto completo y que no tuvieran relevancia para los objetivos del estudio. Se recolectaron 126 publicaciones, de las cuales se excluyeron 74, por lo que finalmente se seleccionaron 52 para la investigación (Figura 1).
Resultados
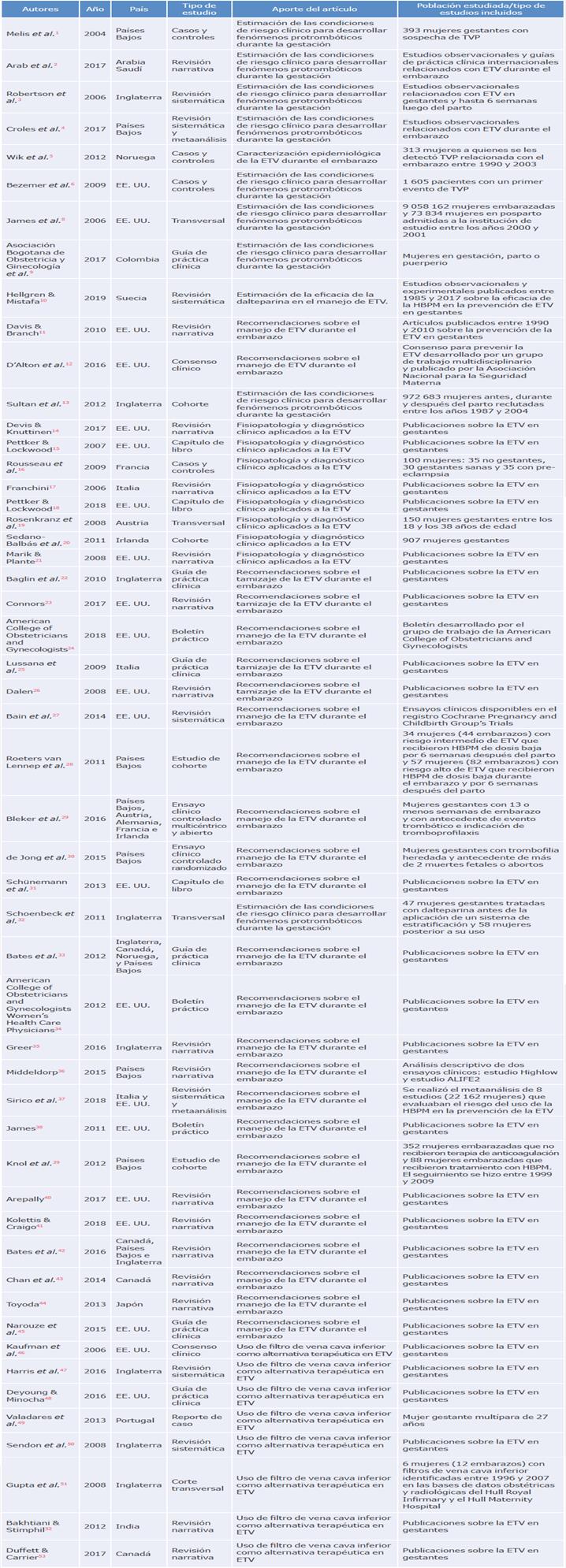
En total, se incluyeron 52 documentos que correspondieron a revisiones narrativas (n=15), revisiones sistemáticas (n=8), guías de práctica clínica (n=6) -de las cuales 1 es colombiana-, boletines y consensos clínicos (n=5), reportes de caso (n=1), capítulos de libro (n=3) y estudios transversales (n=4), de casos y controles (n=4), de cohorte (n=4) y experimentales (n=2). Solo 1 publicación fue de origen colombiano, las demás fueron inglesas, norteamericanasy asiáticas. Los documentos abarcaban desde recopilación teórica etiológica de la ETV, hasta recomendaciones de manejo terapéutico y profiláctico, aspectos que se exhiben en detalle en la Tabla 1.
Discusión
La gestación es un estado fisiológico protrombótico en el que la ETV tiene una prevalencia estimada de 0.61 a 1.72 casos por cada 1 000 nacimientos,8 lo que la convierte en una de las principales causas de mortalidad materna, tanto en países del primer mundo, como en vía de desarrollo.8,9 De acuerdo con la etapa del embarazo, la ETV presenta tasas de incidencia de 5.4, 7.2 y 4.3 casos por cada 10 000 embarazos en el anteparto, el periparto y el posparto, respectivamente. En cuanto a la TVP y TEP se ha reportado una incidencia en el primer y tercer trimestre de 12.1 y 5.4, respectivamente.10,11 Asimismo, D'Alton et al.12 evidencian mayor frecuencia diagnóstica de TVP en el miembro inferior izquierdo,12 debido, posiblemente, a la compresión que ejerce el útero grávido sobre la vena iliaca común izquierda.9 Si bien el desarrollo de TEP y TVP en cifras individuales no supera prevalencias del 20% para esta población, son condiciones que pueden impactar desfavorablemente al binomio madre-hijo.
Fisiopatología
Como lo indican la Asociación Bogotana de Obstetricia y Ginecología et al. ,9 en el desarrollo de un trombo pueden verse involucrados diferentes elementos, tales como los enumerados por la triada de Virchow: estasis venosa, trauma vascular e hipercoagulabilidad.
En ese sentido, la triada de Virchow puede evidenciarse en las mujeres embarazadas a través de la disminución gradual de la velocidad de flujo venoso (estasis venosa), la distensión venosa que lleva a daño endotelial (trauma vascular) y los cambios protrombóticos (hipercoagulabilidad).11 Estos factores están presentes durante toda la gestación y se extienden hasta aproximadamente el día 42 posparto, cuando la velocidad de flujo y el diámetro venoso retornan a las condiciones pregestacionales.13,14
De igual forma, es preciso indicar que factores característicos del embarazo como el incremento de los niveles de estrógeno plasmático, la producción local de prostaciclina y óxido nítrico,15 los estados patológicos como trastornos hipertensivos del embarazo, las complicaciones posparto como infección, los requerimientos transfusionales y las vías asistidas de nacimiento (cesárea) incrementan la capacitancia vascular durante este periodo y contribuyen al daño endotelial.16 Aunado a lo anterior, es prudente recordar que la gestación normal se acompaña de cambios en el sistema hemostático que resultan en estado protrombótico. De esta forma, cuando se tiene ETV, el nivel sérico de la mayoría de los factores de coagulación (V, VII, VIII, IX, XII y von Willebrand) aumenta, lo que se evidencia en la duplicación de los niveles de fibrinógeno.17,18 Asimismo, existe una disminución de los niveles normales de la proteína S (anticoagulante), lo cual sucede a medida que aumenta la edad gestacional y llega hasta alcanzar un nivel estable en el tercer trimestre; esta disminución puede acompañarse de resistencia relativa a la proteína C activada en 40-55% de los casos.19
De igual forma, se ha descrito una disminución de la fibrinólisis debido a la reducción de los niveles del activador tisular del plasminógeno y de posibles modificaciones genéticas, tales como la mutación del factor V de Leyden, el síndrome antifosfolípidos, el déficit de antitrombina, la mutación G20210A del gen de la protrombina, entre otros, que facilitan la formación y estabilización de la fibrina.20
De esta manera, es evidente que el antecedente genético de trombofilia juega un papel fundamental en el desarrollo de ETV durante el embarazo, en especial cuando se identifica mutación homocigota en algunos de los genes que codifican proteínas de interés (Tabla 3). Según Marik & Plane21, la presencia de este antecedente en la población gestante caucásica tiene una prevalencia del 10%.
Tabla 2 Condiciones clínicas de riesgo para enfermedad tromboembólica venosa durante el embarazo.
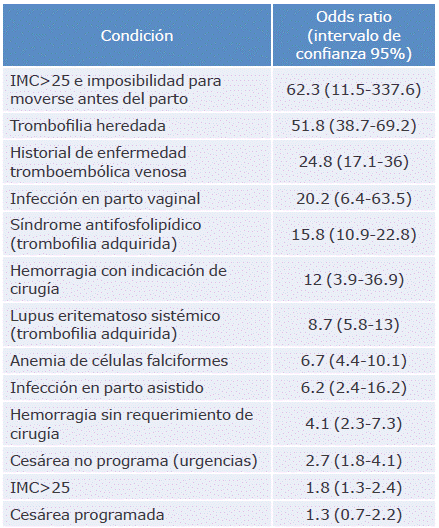
IMC: índice de masa corporal.
Fuente: Elaboración con base en Davis.11
Tabla 3 Estimado de riesgo de trombofilias en el desarrollo de enfermedad tromboembólica venosa durante el embarazo.
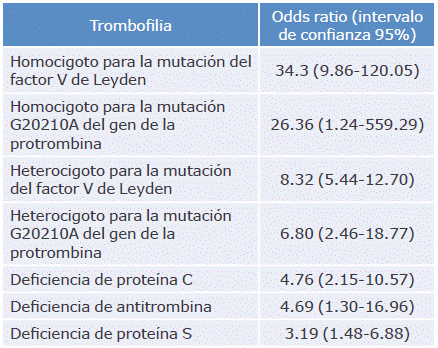
Fuente: Elaboración con base en Davis.11
Factores de riesgo clínicos
Existen algunas condiciones que contribuyen al desarrollo de estados protrombóticos (Tabla 2) y que, según Robertson et al.,3 pueden clasificarse de acuerdo a su odds ratio.
Tamizaje
La comunidad científica internacional se ha cuestionado sobre la pertinencia del tamizaje de la ETV durante el embarazo, encontrando que es necesario individualizar y racionalizar la solicitud de esta tamización,22,23 razón por la cual, la Sociedad Británica de Hematología señala varias recomendaciones con su respectivo nivel de evidencia según el sistema GRADE, donde las recomendaciones se dividen en grado 1 (fuertes) y grado 2 (débiles) de acuerdo con diferentes niveles de calidad de la evidencia, a saber, A (ensayos clínicos aleatorios de alta calidad), B (moderada) y C (baja);22 algunas recomendaciones incluyen:
a) No se recomienda tamizar pacientes no seleccionadas con trombosis venosa de miembros superiores (1B).
b) No se recomienda realizar tamizaje en pacientes con trombosis asociada a catéter venoso central (1C).
c) No se recomienda el tamizaje en pacientes con oclusión venosa retiniana (1B).
d) La mayoría de embarazadas con antecedentes de trombosis no provocada (1B) o de trombosis asociada al embarazo o al uso de anticonceptivos orales combinados (2C) califican para tromboprofilaxis tan solo por el riesgo clínico que tienen, por lo que no es necesario tamizarlas para trombofilia.
e) En embarazadas asintomáticas con antecedente familiar de trombosis venosa no se requiere tamizaje si el riesgo clínico por sí solo es suficiente para realizar la tromboprofilaxis (2C).
Al respecto, Connors23 sugiere, con el fin de optimizar el uso de recursos económicos del sistema de salud, practicar tamizaje para trombofilia solo en aquellas mujeres que hayan presentado fenómenos protrombóticos antes de los 50 años de edad, especialmente con desencadenantes como uso de anticonceptivos orales, incapacidad para moverse, cirugía menor y/o historia de familiar en primer grado de consanguinidad con fenómenos protrombóticos recurrentes y/o ETV en sitios poco frecuentes como la vena esplénica o las venas cerebrales.
Por su parte, el American College of Obstetricians and Gynecologists24 indica la pertinencia de realizar tamizaje en gestantes que tengan ETV aguda, antecedente de ETV recurrente y que presenten historia familiar de ETV sin antecedente personal conocido. La indicación de otros estudios25,26 para el tamizaje en esta misma población es realizar las siguientes pruebas:
Anticuerpos anticardiolipina y anti-beta 2 glicoproteína, y anticoagulante lúpico (en caso de que haya historia personal de ETV).
Niveles de actividad de las proteínas C y S.
Niveles de actividad de antitrombina.
Mutación G20210A del gen de la protrombina.
Mutación del factor V Leiden.
Recomendaciones de manejo profiláctico
En la actualidad no hay evidencia suficiente para dar indicaciones sobre la tromboprofilaxis en mujeres gestantes en cuanto al tipo de fármacos, la dosis a utilizar ni la duración del tratamiento,27 y, por lo tanto, no se cuenta con evidencia de calidad para realizar recomendaciones sobre el uso de los diferentes tipos de heparinas disponibles, así como las dosis a administrar,28-30 lo que sin duda tendría un impacto favorable en la morbimortalidad de la ETV en esta población. Motivado por esto, el Ministerio de Salud y Protección Social de Colombia9 clasificó las condiciones predisponentes para desarrollar un evento tromboembólico de la siguiente manera: de riesgo bajo cuando el riesgo relativo (RR) es <2, de riesgo moderado cuando el RR está entre 2 y 4, de riesgo alto cuando el RR está entre 5 y 9 y de riesgo muy alto cuando el RR es >10,; a partir de esta clasificación puede definirse un posible tratamiento31,32 (Tabla 4).
Tabla 4 Indicaciones de tromboprofilaxis durante la gestación y el puerperio.
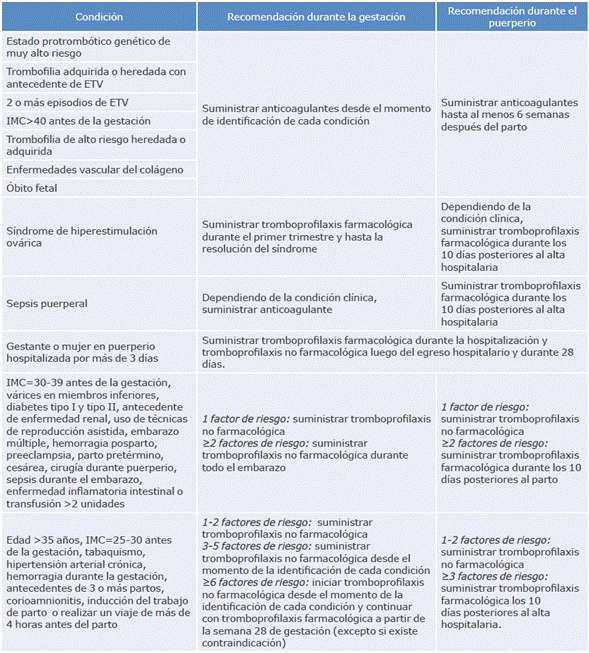
ETV: enfermedad tromboembólica venosa; IMC: Índice de masa corporal.
Fuente: Elaboración con base en datos de la Asociación Bogotana de Obstetricia y Ginecología.9
El American College of Chest Physicians33 y el American College of Obstetricians and Gynecologists Women's Health Care Physicians34 también se han interesado en la prevención de la ETV; ambas instituciones afirman que la evidencia que soporta el uso de tromboprofilaxis farmacológica en las poblaciones indicadas previamente se encuentra extrapolada de estudios epidemiológicos retrospectivos de tromboprofilaxis en poblaciones de alto riesgo mundial y del criterio médico de cada profesional,35 por lo cual se observa una falta de homogeneidad en las recomendaciones, siendo este un posible tema de investigación futura.
Elección de anticoagulante
Una vez se dé la indicación de iniciar tromboprofilaxis, es pertinente elegir la opción farmacológica más adecuada. Las heparinas, al no atravesar la barrera hematoplacentaria y no representar riesgos fetales, son los agentes de primera línea de manejo profiláctico; dentros de estas se recomiendan las de bajo peso molecular (HBPM) sobre las no fraccionadas (HNF), dado que las primeras son de fácil administración, tienen una eficacia anticoagulante más predecible y no requieren seguimiento o control por parte del laboratorio.36,37 La indicación de las HBPM se debe hacer de acuerdo al peso y función renal de cada paciente (Tabla 5).
Tabla 5 Dosis de heparinas de bajo peso molecular durante la gestación.
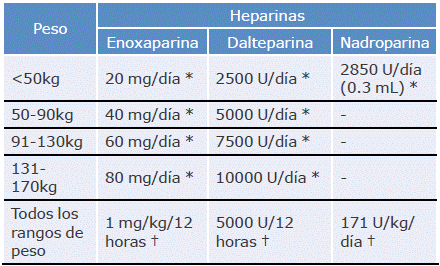
* Dosis para tromboprofilaxis farmacológica.
† Dosis para anticoagulación plena.
Fuente: Elaboración con base en datos de la Asociación Bogotana de Obstetricia y Ginecología.9
De otra parte, las HNF son una alternativa aceptable, segura para el binomio y apropiada en situaciones de la gestación donde es necesaria una mayor administración de anticoagulantes, como por ejemplo el estado perioperatorio, y en aquellas gestantes con contraindicación para el uso de HBPM, por ejemplo las que padecen enfermedad renal o tienen una tasa de filtración glomerular <30 mL/min.38 La posología recomendada para las HNF es de 5 000 UI subcutáneas cada 12 horas. Es importante mencionar que dentro de las posibles reacciones adversas a este tipo de medicamentos se encuentran la trombocitopenia inducida por heparina (TIH) y la osteoporosis.39-41
Así, para la elección del tratamiento de la ETV durante el periparto, se deben seguir las siguientes indicaciones:38,42-45
Las mujeres gestantes con dosis terapéuticas de HBPM deben recibir la última dosis de este medicamento 24 horas antes de la aplicación de analgesia epidural y/o de la hora estimada de parto.38,43
Las mujeres gestantes con manejo tromboprofiláctico deben recibir la última dosis de HBPM 10-12 horas antes de la analgesia epidural.44,45
Las mujeres con partos programados deben recibir su última dosis de HNF 4-6 horas antes de recibir analgesia epidural o del parto, lo cual debe estar acompañado de una evaluación estricta del nivel de tiempo de tromboplastina parcial activado (TTP).42
Las mujeres gestantes con dosis terapéuticas de HNF administradas de manera subcutánea deben recibir la última dosis preferiblemente 24 horas antes de la analgesia epidural o del parto, lo cual debe estar acompañado de una evaluación estricta del nivel de TTP.42
En caso de requerimiento de intervención quirúrgica, las gestantes con HNF en dosis profiláctica deben suspender la medicación 8-10 horas antes del procedimiento.42
Las HBPM y las HNF profilácticas se pueden reiniciar 6-12 horas luego del parto, pero las primeras se deben retomar después de 4 horas de la remoción de catéter epidural45 y las segundas, después de 8 horas de este procedimiento.
Las HBPM y las HNF en dosis terapéutica se pueden reiniciar 24 horas luego del parto, pero no antes de 24 horas del retiro del catéter epidural.42
Filtro de vena cava inferior como alternativa terapéutica
El filtro de vena cava inferior es un dispositivo diseñado para evitar la presentación de ETV durante el embarazo46,47 que se indica cuando la terapia médica anticoagulante falla48,49 y cuando se presentan complicaciones de anticoagulación (incluyendo TIH),50 alergia a las heparinas,51 sangrado significativo durante la administración de anticoagulante52 y alto riesgo de TEP durante el parto, especialmente cuando se ha identificado un trombo en la región ileofemoral y el parto se estima en las siguientes 2 a 3 semanas.
Esta alternativa terapéutica también es recomendable si se identifica contraindicación del uso de la anticoagulación farmacológica,53 tal como ocurre cuando hay antecedentes de neurocirugía, evento cerebrovascular agudo reciente o riesgo alto de sangrado.
Por otro lado, es importante mencionar que el presente estudio tuvo limitaciones derivadas de su diseño, pues este se basa en la descripción del estado del arte de la ETV y es evidente la escasez de referencias bibliográficas colombianas que permitan ajustar las recomendaciones en la población local.
Conclusiones
La gestación constituye un estado fisiológico procoagulante que se prolonga hasta aproximadamente seis semanas luego del parto, siendo aún mayor la tendencia trombótica en aquellas mujeres con antecedente personal o familiar de estos eventos. Por lo tanto, la ETV durante el embarazo constituye un problema de salud pública con alto riesgo de compromiso del bienestar materno-fetal.
La identificación oportuna de condiciones de riesgo trombótico permite estratificar la población gestante para facilitar la atención oportuna y el manejo anticoagulante profiláctico o terapéutico, lo cual permite impactar de manera positiva la morbimortalidad de la ETV durante la gestación y el puerperio.
Se recomienda realizar pruebas de tamizaje de estados protrombóticos durante la gestación, el parto y el puerperio, ya que la identificación oportuna de la ETV permitirá disminuir las tasas de morbimortalidad en esta población mediante la implementación de medidas tromboprofilácticas tanto farmacológicas como no farmacológicas. En relación a la tromboprofilaxis, se recomienda su uso en condiciones clínicas tales como estado protrombóticos heredado, ETV recurrentes, obesidad mórbida y enfermedad vascular del colágeno.
Finalmente, a partir de los hallazgos se puede concluir que es necesario que en Colombia se realicen nuevos estudios que aborden la prevención, el diagnóstico y el manejo de los fenómenos protrombóticos durante la gestación y a partir de los cuales sea posible generar recomendaciones específicas para la población local.