Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Entomología
Print version ISSN 0120-0488On-line version ISSN 2665-4385
Rev. Colomb. Entomol. vol.36 no.2 Bogotá July/Dec. 2010
Culícidofauna (Diptera: Culicidae) presente en los distintos enclaves hídricos de la ciudad de Valencia (España)
Mosquito fauna (Diptera: Culicidae) present in the distinct hydric enclaves of the city of Valencia (Spain)
RUBÉN BUENO-MARÍ1,2, ENRIQUE CORELLA-LÓPEZ1 y RICARDO JIMÉNEZ-PEYDRÓ1
1 Laboratorio de Entomología y Control de Plagas Instituto Cavanilles de Biodiversidad y Biología Evolutiva Universitat de València (Estudi General). Apartado oficial 22085.46071 Valencia (España).
2 ruben.bueno@uv.es autor para correspondencia.
Recibido: 30-dic-2009 • Aceptado: 24-sep-2010
Resumen: Durante 20 años (1987-2007) se hizo un exhaustivo seguimiento de las poblaciones larvarias de culícidos (Diptera: Culicidae) en el Término Municipal Valencia (España) que propició la prospección de 667 focos de cría y la colecta de 47.131 ejemplares. Se aporta información acerca de las ocho especies capturadas, pertenecientes a los géneros Culex, Culiseta y Ochlerotatus, y se discute la ausencia de hallazgos de ejemplares del género Anopheles que tanto abundaron en el área de estudio durante el pasado. Por último, también se calcularon los índices de biodiversidad de Ribeiro (δ = 3,28) y Shannon (H´ = 1,46) para la familia Culicidae en el área de estudio y se señala a la antropización como uno de los elementos explicativos más importantes de la pérdida de la biodiversidad de estos dípteros nematóceros.
Palabras clave: Vectores de enfermedades. Antropización. Biodiversidad. Anopheles.
Abstract: Over 20 years (1987-2007) a comprehensive monitoring of the larval populations of mosquitoes (Diptera: Culicidae) was conducted in the Municipality of Valencia (Spain) which amounted to the inspection of 667 breeding sites and the collection of 47,131 specimens. Information is provided on the eight species captured, belonging to the genera Culex, Culiseta and Ochlerotatus, and we discuss the lack of findings of Anopheles specimens which were so abundant in the study area during the past. Finally, we also calculated the biodiversity indices of Ribeiro (δ = 3.28) and Shannon (H´ = 1.46) for the family Culicidae in the study area and we postulate anthropization as one of the most important explanatory elements for the loss of biodiversity in these nematoceran diptera.
Key words: Pests. Disease vectors. Anthropization. Biodiversity. Anopheles.
Introducción
El Término Municipal de Valencia presenta una importante heterogeneidad de ambientes propios del desarrollo de la cultura agrícola, pesquera e industrial de la ciudad en los últimos siglos. Esta diversidad de ambientes propicia la proliferación de diferentes especies de mosquitos (Diptera: Culicidae) en función de, entre otros aspectos, las características físicas y químicas de los biotopos larvarios concretos, así como de la presencia de hospedadores adecuados en las inmediaciones y de la climatología local (Service 1993). Al respecto, diversos autores han propuesto la utilidad de los culícidos como bioindicadores de la degradación forestal (Dorvillé 1996) y, en general, de la presión antrópica sobre diversos ambientes naturales (Montes 2005). No obstante, son escasos los estudios acerca de la utilización de los mosquitos como organismos sensibles a las variaciones de la calidad ambiental.
Por otra parte, resulta evidente que el conocimiento minucioso de la biodiversidad, distribución, bioecología y dinámica poblacional de las distintas especies de culícidos, contribuye de manera decisiva al éxito de los programas de control (Simsek 2004; Bueno Marí et al. 2008). El presente trabajo se desprende de un proyecto técnico de colaboración con la Delegación de Sanidad del Ayuntamiento de Valencia (España) en el que se contemplaba la consecución de dos objetivos principales: por un lado el conocimiento exhaustivo de los culícidos existentes en el área considerada y, paralelamente, el estudio y mejora de las técnicas de control de las poblaciones de mosquitos con la aplicación de los métodos científicamente más aconsejables y priorizando, a su vez, la minimización de los efectos dañinos sobre las personas y el ambiente. En este contexto, el presente manuscrito aporta información relativa a las diferentes especies de culícidos no limnodendrófilas capturadas en el Término Municipal de Valencia. Teniendo en cuenta la influencia en el estudio de las continuas acciones de control poblacional a las que han sido sometidos estos dípteros, también se ofrecen aspectos de su distribución y bioecología, y se discuten cuestiones referentes a la ausencia de especies del género Anopheles Meigen, 1818, cuya presencia en el área de estudio fue frecuente en el pasado, manteniendo elevados niveles de endemia palúdica (Bueno Marí y Jiménez Peydró 2008).
Materiales y Métodos
Descripción del área de estudio. El área de estudio presenta un clima típicamente Mediterráneo, por tanto se caracteriza por presentar una baja oscilación térmica intranual, alrededor de los 13ºC, acaeciendo en consecuencia inviernos suaves y veranos muy calurosos. Además, la máxima pluviosidad tiene lugar en la época otoñal, con un segundo periodo de lluvias de menor cuantía en primavera. En términos medios anuales, la temperatura y la precipitación se sitúan en los 17,8°C y 454 mm respectivamente (Aemet 2010).
El Término Municipal tiene una superficie de 13.465 hectáreas de las que aproximadamente 4.000 se destinan a fines hortícolas, fundamentalmente cultivos de regadío. Ello es posible merced a una vasta red de acequias de gran caudal, que permiten a través de canales de menor caudal llevar el agua hacia sus fértiles tierras, pudiendo por tanto señalar que la práctica totalidad del Término Municipal se halla recorrido por una intrincada red de acequias de evidente influencia en la proliferación de las poblaciones de mosquitos.
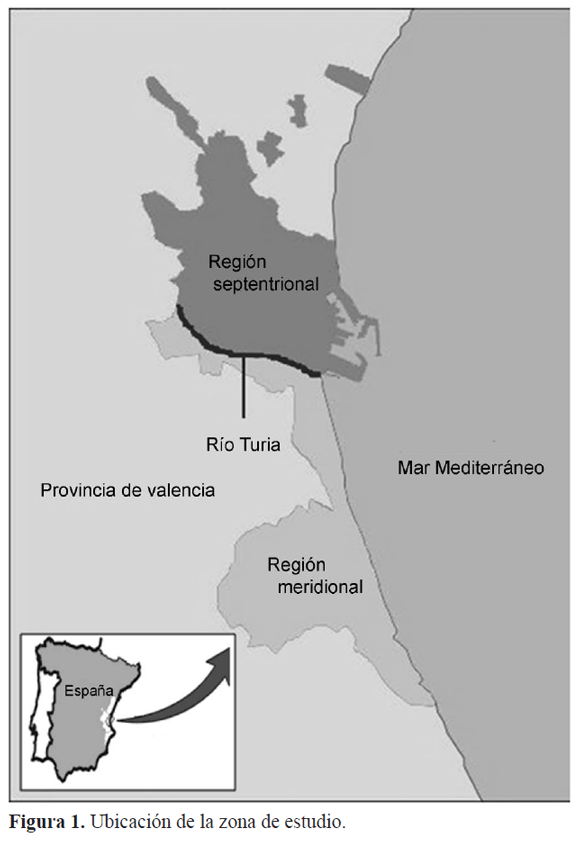
Para una mejor comprensión de los datos, se ha dividido el Término Municipal en dos regiones claramente diferenciadas a nivel geográfico, hidrográfico y de influencia antrópica (Fig. 1):
Región meridional o de antropización baja: comprende toda el área que limita al norte de la misma con el nuevo cauce del río Túria. Destaca por albergar la mayoría de la extensión ocupada por el Parque Natural de L´Albufera. Los criaderos larvarios más frecuentes son los numerosos canales de irrigación, así como las áreas deprimidas de habitual inundación debido a su elevado nivel freático, comúnmente denominadas “malladas”, situadas tras la primera línea del cordón dunar que discurre paralelo a la costa. También cabe mencionar a los arrozales adyacentes al lago como ocasionales focos de anidamiento, sin obviar la omnipresencia de pequeños recipientes de origen antrópico, tales como bidones, cubos, abrevaderos, etc. Por otra parte, el lago de L´Albufera no se posiciona como un biotopo adecuado, ya que se trata de un cuerpo hídrico de gran magnitud, donde, además de albergarse abundante fauna piscícola larvívora, también se manifiestan intensos oleajes que imposibilitan la proliferación larvaria.
Región septentrional o de antropización alta: abarca la parte del Término que linda al sur con el nuevo cauce del río Túria. El propio río ha sido incluido en esta subdivisión debido a la evidente presión ejercida por el hombre sobre el mismo, en forma de vertidos y modificaciones de cauce y caudal. Además, esta región engloba al denso núcleo urbano de la ciudad, con centenares de imbornales sifónicos y decenas de fuentes ornamentales como principales focos de cría. Asimismo, el tradicional cultivo de irrigación de diversas pedanías, hoy en día transformadas en barrios anexos de la ciudad por el exacerbado crecimiento urbanístico de ésta, lo que posibilita la presencia de abundantes acequias de riego, tanto de uso vigente como obsoleto.
Muestreo. La técnica empleada para la recolección de estados inmaduros fue la conocida como “dipping”, consistente en la introducción de un recipiente de 350 ml de capacidad en el medio hídrico del cual se desee obtener una alícuota y cuya utilización para dicho fin está ampliamente contrastada (Service 1993). En el caso de microambientes hídricos que no permitieron la utilización de la técnica “dipping” (pequeños recipientes, imbornales sifónicos, encharcamientos reducidos de escasa profundidad, etc.) se procedió a la captura de ejemplares larvarios mediante el pipeteado directo con pipetas tipo Pasteur de 150 mm de longitud sobre el biotopo. Para sistematizar los datos, el esfuerzo muestral se fijó en diez minutos que incluían la búsqueda y captura de larvas en cada punto de muestreo con independencia del método de muestreo llevado a cabo. Para enriquecer la información obtenida, de forma puntual también se recolectaron individuos adultos mediante el empleo de una manga o red entomológica, la cual se batía sobre la vegetación, recogiendo los ejemplares con la ayuda de un aspirador entomológico. Asimismo, en ciertas ocasiones la captura de imagos se realizó directamente sobre cebo humano mediante el uso de dicho aspirador.
Los muestreos larvarios intensivos se efectuaron entre los meses de marzo y octubre, ambos inclusive, por ser este el periodo más adecuado para la proliferación de culícidos en nuestra latitud. La frecuencia de muestreo fue de dos veces por semana, aunque de manera abierta a posibles modificaciones reguladas por las condiciones pluviométricas. Fuera del periodo de muestreo intensivo, también se llevaron a cabo capturas puntuales con el objetivo de estudiar la extensión temporal de la actividad larvaria y posibles modificaciones en los patrones de hibernación tradicionalmente descritos.
La determinación taxonómica de los ejemplares se realizó con base en los criterios de Encinas Grandes (1982), Darsie y Saminadou Voyadjoglou (1997) y Schaffner et al. (2001). Para el análisis de la biodiversidad se seleccionó el Índice de Ribeiro (δ) (Ribeiro 1983) debido a la posibilidad de establecer comparaciones por su constatada utilización para la estimación de la diversidad de culícidos en otras áreas de la Península Ibérica:
δ = E-1 / Loge (A+1)
E = número de especies o subespecies capturadas en el área de estudio.
A = extensión del área de estudio, expresada en Km2.
Asimismo, se utilizó el Índice de Shannon (H´) (Shannon y Weaver 1949) por, entre otros motivos, ser uno de los más empleados para dicho fin en multitud de grupos zoológicos. Este índice mide el grado promedio de incertidumbre en predecir a qué especie pertenecerá un individuo escogido al azar de una colección. Asume que los individuos son muestreados al azar y que todas las especies están representadas en la muestra (Magurran 1988).
H´ = Σpi In pi
pi = proporción de individuos de la especie i respecto al total de individuos (abundancia relativa de la especie i).
El valor de H´ oscila entre 0, cuando hay una sola especie, y el logaritmo neperiano del número total de especies (Hmax), cuando todas las especies están representadas por el mismo número de individuos. Con el fin de mejorar las propiedades comparativas del índice se calculó además el valor de Equidad o Uniformidad (J) (Pielou 1975). Este índice de Equidad mide la proporción de la diversidad observada con relación a la máxima diversidad esperada. Su valor oscila entre 0 y 1, donde 1 corresponde a situaciones en las que todas las especies son igualmente abundantes (Magurran 1988).
J = H´ / Hmax = H´ / lnS
Resultados y Discusión
Análisis faunístico y bioecológico. Se capturaron e identificaron 47.131 ejemplares larvarios pertenecientes a las siguientes especies: Culex modestus Ficalbi, 1890, Culex pipiens Linnaeus, 1758, Culex theileri Theobald, 1903, Culiseta annulata (Schrank, 1776), Culiseta longiareolata (Macquart, 1838), Culiseta subochrea (Edwards, 1921), Ochlerotatus caspius (Pallas, 1771) y Ochlerotatus detritus Haliday, 1833.
El estudio pormenorizado de las capturas corrobora la ubicuidad y la plasticidad bioecológica descrita para Cx. pipiens y Cs. longiareolata (López Sánchez 1989; Schaffner et al. 2001), hallándose ambas en todos los criaderos larvarios (Tabla 1). Comparativamente Cx. pipiens muestra una adaptabilidad similar a todos los biotopos, si bien sus colectas han sido más frecuentes en acequias y canales, fruto de la destacada abundancia de éstas en el área de estudio (más de 400 catalogadas). En el caso de Cs. longiareolata, las preferencias de oviposición están claramente dirigidas hacia pequeñas colecciones de agua, tales como recipientes domésticos y peridomésticos, imbornales sifónicos o fuentes ornamentales, que pueden llegar a presentar importantes niveles de eutrofización. Precisamente en estos microambientes hídricos es donde se han observado elevados porcentajes de cohabitación larvaria con Cx. pipiens, hecho también constatado por otros autores (Encinas Grandes 1982). El río Túria tan sólo se presenta en condiciones óptimas para albergar larvas de culícidos en épocas concretas. Esto sucede cuando las modificaciones bruscas de su caudal posibilitan la aparición de charcos o reductos de agua, ya sea en los terrenos colindantes al cauce por agua extravasada en épocas de caudal creciente o en el propio cauce cuando el paupérrimo caudal dibuja un perfil discontinuo del río. Sea como fuere, estos focos son colonizados, en exclusividad, de nuevo por Cx. pipiens y Cs. longiareolata, y se encuentran siempre varios kilómetros antes de la desembocadura debido a la fuerte intrusión marina que tiene lugar. En consecuencia, puede afirmarse que ambas especies son el máximo exponente del oportunismo, entendido éste como la capacidad de explotar ambientes que aparecen y desaparecen de forma intermitente (Begon et al. 1996), que suele caracterizar a la familia Culicidae.
Las malladas suponen un lugar ideal para la proliferación de Oc. caspius y Oc. detritus. La periodicidad de sus inundaciones se correlaciona con el multivoltinismo de estos aedinos, ya que ambos basan su estrategia vital en la deposición de huevos quiescentes a la espera de ser hidratados para su rápida eclosión. Estos huevos pueden resistir la desecación y las temperaturas extremas incluso durante años (Schaffner et al. 2001). Además, cabe señalar que estos dos aedinos presentan una elevada antropofilia que justifica, en gran medida, el hecho de que sean unos de los principales protagonistas de las campañas de control poblacional llevadas a cabo en la totalidad de los países mediterráneos.
El elevado porcentaje de capturas de Cx. theileri en las malladas, obedece más a la escasez de sus capturas en el área de estudio que a su ubicuidad en las propias malladas. Pese a que es una especie frecuentemente asociada con los arrozales, especialmente con aquellos situados en el sur de la Península Ibérica (Ruiz y Cáceres 2004; Almeida et al. 2008), nuestros datos indican un desplazamiento de la misma en beneficio de Cx. modestus en los campos de cultivo de arroz, situación también observada en el sur de Francia (Pongon et al. 2007). Cabe señalar que las capturas de adultos de Cx. modestus, gran parte de ellas sobre cebo humano, tuvieron lugar a menos de 800 metros de distancia de constatados biotopos larvarios de la especie. Esta situación se relaciona a la perfección con la elevada antropofilia y bajo rango de vuelo descrito para los imagos (Schaffner et al. 2001).
Respecto a Cs. annulata y Cs. subochrea, son dos especies próximas taxonómica, morfológica y etológicamente, que han sido recolectadas mayoritariamente en receptáculos hídricos como bidones, neumáticos y fosas de riego, y en menor medida en amplias colecciones de agua como canales y malladas con abundante vegetación herbácea.
En general, a nivel fenológico puede indicarse que los meses de mayo y junio (Figs. 2 A-H) coinciden con las épocas de mayores capturas para la mayoría de especies. Sin embargo, existen ciertas excepciones en función de la ocurrencia o no de bruscas oscilaciones de los niveles hídricos de los biotopos larvarios. Así por ejemplo, puede observarse que los picos de captura de Oc. caspius y Oc. detritus coinciden con las épocas equinocciales en las que se concentran las precipitaciones en el área de estudio. En el caso de Oc. detritus la diferencia entre los picos de captura primaveral y otoñal es más acusada. Esta situación ya ha sido advertida por otros autores para el sur de Europa, apuntándose hacia un posible univoltinismo de la especie (Schaffner et al. 2001). No obstante, a nuestro juicio no puede descartarse ni un univoltinismo asincrónico, caracterizado por un mayor porcentaje de eclosión en la época primaveral, ni tampoco la coincidencia de poblaciones univoltinas y bivoltinas, aunque con mayor abundancia de las primeras. Respecto a Cs. annulata y Cs. subochrea, éstas también presentan un descenso de actividad en los meses veraniegos fruto del acusado estiaje que caracteriza a la totalidad de los humedales mediterráneos. La especie Cx. modestus se adapta mejor a estas condiciones adversas al aprovechar la disponibilidad hídrica propiciada por acciones antrópicas, fundamentalmente la inundación de los arrozales, mientras que la elevada plasticidad ecológica descrita previamente para Cx. pipiens y Cs. longiareolata permite que ambas especies colonicen asiduamente multitud de microambientes hídricos también asociados a la explotación humana.
Por otra parte, las capturas invernales, desde noviembre a febrero, también nos aportan información interesante. Las especies más frecuentes en este periodo de nuevo fueron Cs. longiareolata y Cx. pipiens. En cuanto a la primera, debemos señalar que sus colectas invernales destacan por una homogeneidad en el desarrollo de sus estados larvarios, fundamentalmente en los meses más fríos, apareciendo habitualmente en forma de L3-L4. Este hecho secundaría la hibernación larvaria descrita para regiones de clima templado como la nuestra (Schaffner et al. 2001). Respecto a Cx. pipiens, sus hallazgos invernales fueron más frecuentes y heterogéneos en el grado de desarrollo larvario que los de Cs. longiareolata. En concreto, en el caso de Cx. pipiens la cohabitación de una elevada multiplicidad de formas preimaginales en distinto grado de desarrollo fue comúnmente detectada. En consecuencia, achacamos estas observaciones a un posible homodinamismo de Cx. pipiens, aspecto ya reseñado para la especie por otros autores en situaciones similares (Merdić y Vujičić-Karlo 2005). Por tanto, podemos indicar que Cs. longiareolata hiberna en estado larvario y que Cx. pipiens presenta un desarrollo reproductivo continuo a lo largo de todo el año en el área de estudio.
Tales circunstancias no deben excluir la posibilidad de que también existan poblaciones de estas especies que modifiquen los patrones de desarrollo previamente descritos, pudiéndose detectar consecuentemente hembras quiescentes de ambas especies. Por lo que respecta a Oc. caspius y Oc. detritus, también se hallaron larvas de manera puntual en los meses invernales, fundamentalmente a finales de enero y principios de febrero. Esto puede ser debido a que los pequeños incrementos termofotoperiódicos, que suelen acontecer durante esta época en la zona estudiada, hayan provocado la ruptura de la quiescencia de los huevos en presencia de agua procedente, en su mayoría, de las copiosas precipitaciones otoñales (Roubaud 1944). En el caso de estos dos aedinos, la asincronía que suele regir su eclosión larvaria (López Sánchez 1989), explicaría la abundancia de muestras obtenidas con gran variabilidad en cuanto al desarrollo de los estados larvarios.
Desde un punto de vista antrópico, el balance alimenticio zoo-antropofílico de los culícidos es sesgado hacia el ser humano fundamentalmente por Cx. pipiens, Cx. modestus, Oc. caspius y Oc. detritus, mientras que Cx. theileri, por su exigüidad, Cs. annulata, Cs. longiareolata y Cs. subochrea únicamente incluyen al hombre entre sus hospedadores de forma ocasional. Estas cuestiones implican un grado más de preocupación que las simples molestias que su acción hematofágica pueda ocasionar, ya que algunas de estas especies son importantes vectores de enfermedades humanas y animales. Así por ejemplo Cx. modestus, Cx. pipiens, Cx. theileri y Oc. caspius son destacados agentes diseminadores de arbovirosis como el Virus West Nile, Sindbis o Tahyna (Hannoun et al. 1964; Danielova y Holubova 1977; Danielova 1984; Harbach 1988; Schaffner et al. 2001; Bueno Marí y Jiménez Peydró 2010a), mientras que otras zoonosis como la dirofilariasis o el paludismo aviar tienen en Cx. pipiens, Cx. theileri, Cs. annulata, Oc. caspius y Oc. detritus a excelentes vectores (Gutsevich et al. 1974; Ribeiro et al. 1983; Moussiegt 1987; Aranda et al. 1998).
Análisis de la Biodiversidad. La aplicación de los Índices de Biodiversidad de Ribeiro (δ) y Shannon (H´) para toda el área de estudio originó los siguientes resultados: δ = 3,28, H´ = 1,46 y J = 0.702. El valor de δ es similar, aunque ligeramente más elevado, en comparación con otros datos disponibles para la Península Ibérica. Así pues destacamos δ = 1,90 para la Comunidad de Madrid en España (Melero Alcíbar 2004), δ = 1,59, δ = 1,64, δ = 2,49 y δ = 2,13, para Alentejo, Algarbe, Beiras y el Parque Natural de la Arrábida respectivamente en Portugal (Ribeiro et al. 1996).
Respecto a J, si contrastamos nuestro valor con los escasos datos de Equidad existentes para la familia Culicidae en diferentes ambientes presentes en España, observamos un valor intermedio entre regiones interiores semiáridas (J = 0,638) y litorales húmedas (J = 0,713), del noreste (Demba et al. 2005) y del suroeste del país (López Sánchez 1989) respectivamente. No obstante, la Equidad calculada en nuestro estudio se sitúa más próxima a la estimada en zonas litorales quizás dada la evidente mayor similitud fisiográfica entre ambas regiones.
Debido a la heterogeneidad de nuestra área de estudio, aplicamos los índices de biodiversidad de forma separada alas regiones de antropización baja y alta (Tabla 2). Los resultados indican claramente que existe una influencia negativa de la explotación ambiental humana sobre la biodiversidad de los culícidos. Así pues, en la región septentrional o de antropización alta los valores de δ y H´ han disminuido considerablemente, menguando también la Equidad hasta 0,609. En contraposición, en la región meridional o de antropización baja, los valores de δ y H´ son sensiblemente más altos que incluso para la totalidad del área estudiada, situándose la Equidad en 0,808; lo que se traduce en una aproximación al 80,8 % de la diversidad máxima de una comunidad de ocho especies que tuviesen la máxima abundancia.
Consideraciones finales
El trabajo pone de manifiesto la contribución negativa de las acciones ligadas a los asentamientos humanos en la biodiversidad de esta familia de dípteros nematóceros. Como también ha sido expuesto, esta cuestión no implica, ni mucho menos, una reducción poblacional de mosquitos en ambientes urbanos, sino más bien un filtro de selección que únicamente es superado por unas pocas especies. Entre los elementos asociados a la antropización y que conforman este filtro específico, se encuentran un evidente empeoramiento en la calidad de las aguas, una reducción en la tipología de los criaderoslarvarios disponibles, una disminución en la biodiversidad de posibles hospedadores y una baja humedad ambiental relativa que mengua sensiblemente el tiempo de supervivencia de los imagos (López Sánchez 1989). En este sentido, la llegada del “mosquito tigre”, Aedes albopictus (Skuse, 1894), culícido de excepcional adaptación a las condiciones urbanas (Aranda et al. 2006), transmisor de arbovirosis como el dengue o la fiebre amarilla y una preocupación creciente para la salud pública española (Eritja et al. 2005; Bueno Marí et al. 2009a), no ha sido evidenciada hasta el momento en el Término Municipal de Valencia. No obstante, desde su primigenia detección en España en el año 2004 (Aranda et al. 2006), su expansión por nuestro país no ha cesado, encontrándose ya en regiones situadas tanto al norte como al sur del área investigada en el presente trabajo (Roiz et al. 2007; Bueno Marí et al. 2009b).
Aunque las especies más antropofílicas han sido capturadas en ambientes alejados de los grandes núcleos de ocupación humana, su control poblacional es igualmente prioritario; ya que las hembras de Oc. detritus y Oc. caspius pueden desplazarse a distancias de entre 10 y 40 kilómetros desde sus biotopos larvarios en busca de hospedadores adecuados (Clavero 1946; Senevet y Andarelli 1964). Por el contrario, Cx. modestus también exhibe una marcada preferencia frente al hombre pero, debido a su baja capacidad de vuelo, únicamente causa molestias en las inmediaciones de sus criaderos larvarios, siendo infrecuente la colecta de imagos más allá del kilómetro de distancia con respecto a sus focos de anidamiento (Schaffner et al. 2001).
A pesar de que durante la primera mitad del siglo XX en los arrozales adyacentes a L´ Albufera fueron comunes las citas de Anopheles hyrcanus (Pallas, 1771), Anopheles maculipennis s. l. Meigen, 1818 y Anopheles melanoon Hackett, 1934 (Romeo Viamonte 1950), desde entonces no hay hallazgos de anofelinos en el área de estudio. El efecto letal de la gran cantidad de insecticidas empleados, en su origen, para la lucha contra diversas plagas del arroz (Tarazona et al. 2003), puede ser una de las causas que explique esta ausencia. Sin embargo, la presencia relativamente frecuente de Cx. pipiens y Cx. modestus, siempre en los márgenes más estáticos y aislados de los arrozales, puede relacionarse con un menor grado de contacto con los insecticidas y una mayor tolerancia, en comparación con los anofelinos, frente a los altos niveles de eutrofia (López Sánchez 1989) que exhiben los campos de arroz, fruto de un masivo abonado con compuestos nitrogenados. Situaciones similares están observándose en los arrozales del sur de Francia, donde las especies tradicionalmente mayoritarias, An. hyrcanus y Cx. modestus, están incrementando su abundancia en los últimos años debido a un resurgimiento del cultivo y a modificaciones de las políticas que regulan las estrategias de control de plagas, redireccionadas hacia una mayor especificidad en los tratamientos contra las plagas del arroz (Pongon et al. 2007). Otros factores que dificultan la proliferación de anofelinos en esta área son la drástica disminución de apropiados biotopos larvarios circundantes a los campos de arroz, fundamentalmente debido al exacerbado desarrollo urbano, así como también la masiva presencia de Gambusia holbrooki (Girard, 1859) (Poecilidae) en los escasos canales de riego que permanecen activos (Bueno Marí y Jiménez Peydró 2010b).
Agradecimientos
Se desea agradecer todo el apoyo recibido por parte del Excelentísimo Ayuntamiento de Valencia y la colaboración de las diferentes empresas encargadas del control poblacional de culícidos que se han ido sucediendo a lo largo de los veinte años de estudio. Asimismo, se manifiesta nuestra gratitud hacia el Ministerio de Ciencia e Innovación de España, por la financiación de una parte del estudio a través del proyecto CGL 2009-11364 (BOS).
Literatura citada
AGENCIA ESTATAL DE METEOROLOGIA (Aemet). MINISTERIO DE MEDIO AMBIENTE Y MEDIO RURAL Y MARINO DE ESPAÑA. Disponible en: http://www.aemet.es/es/elclima/datosclimatologicos/valoresclimatologicos?l=8416&k=val Fecha revisión: 9 septiembre 2010. [ Links ]
ALMEIDA, A. P.; GALAO, R. P.; SOUSA, C. A.; NOVO, M. T.; PARREIRA, R.; PINTO, J.; PIEDADE, J.; ESTEVES, A. 2008. Potential mosquito vectors of arboviruses in Portugal: species, distribution, abundance and West Nile infection. Transactions of the Royal Society of Tropical Medicine and Hygiene 102 (8): 823-832. [ Links ]
ARANDA, C.; PANYELLA, O.; ERITJA, R.; CASTELLA, J. 1998. Canine filariasis Importance and transmission in the Baix Llobregat area, Barcelona (Spain). Veterinary Parasitology 77 (4): 267-275. [ Links ]
ARANDA, C.; ERITJA, R.; ROIZ, D. 2006. First record and establishment of the mosquito Aedes albopictus in Spain. Medical and Veterinary Entomology 20 (1): 150-152. [ Links ]
BEGON, M.; HARPER, J. L.; TOWNSEND, C. R. 1996. Ecology. Individuals, Populations and Communities. 3ª Ed. Blackwell, USA. 1068 p. [ Links ]
BUENO MARÍ, R.; JIMÉNEZ PEYDRÓ, R. 2008. Malaria en España: aspectos entomológicos y perspectivas de futuro. Revista Española de Salud Pública 82 (5): 467-489. [ Links ]
BUENO MARÍ, R.; RUEDA SEVILLA, J.; BERNUÉS BAÑERES, A.; LACOMBA ANDUEZA, I.; JIMÉNEZ PEYDRÓ, R. 2008. Contribución al conocimiento de las poblaciones larvarias de culícidos (Diptera, Culicidae) presentes en el Marjal dels Moros (Valencia). Boletín de la Asociación Española de Entomología 32 (3-4): 351-365. [ Links ]
BUENO MARÍ, R.; MORENO MARÍ, J.; OLTRA MOSCARDÓ, M. T.; JIMÉNEZ PEYDRÓ, R. 2009a. Artrópodos de interés vectorial en la Salud Pública española. Revista Española de Salud Pública 83 (2): 199-212. [ Links ]
BUENO MARÍ, R., CHORDÁ OLMOS, F. A.; BERNUÉS BAÑERES, A.; JIMÉNEZ PEYDRÓ, R. 2009b. Detección de Aedes albopictus (Skuse, 1894) en Torrevieja. Boletín de la Asociación Española de Entomología 33 (3-4): 529-532. [ Links ]
BUENO MARÍ, R.; JIMÉNEZ PEYDRÓ, R. 2010a. Situación actual en España y eco-epidemiología de las arbovirosis transmitidas por mosquitos culícidos (Diptera: Culicidae). Revista Española de Salud Pública 84 (3): 255-269. [ Links ]
BUENO MARÍ, R.; JIMÉNEZ PEYDRÓ, R. 2010b. New anopheline records from the Valencian Autonomous Region of Eastern Spain (Diptera: Culicidae: Anophelinae). European Mosquito Bulletin 28: 148-156. [ Links ]
CLAVERO, G. 1946. Aedinos de España. Revista de Sanidad e Higiene Pública 20: 1205-1232. [ Links ]
DANIELOVA, V. 1984. To the problem of the vector of Lednice virus. Folia Parasitologica 31 (4): 379-382. [ Links ]
DANIELOVA, A.; HOLUBOVA, J. 1977. Two more mosquito species proved as vectors of Tahyna virus in Czechoslovakia. Folia Parasitologica 24 (2): 187-189. [ Links ]
DARSIE, R. F.; SAMINADOU VOYADJOGLOU, A. 1997. Keys for the identification of the mosquitoes of Greece. Journal of the American Mosquito Control Association 13 (3): 247-254. [ Links ]
DEMBA, M.; REMUS ZAMFIRESCU, S.; THIAM, N.; PALANCA SOLER, A. 2005. Diversity of mosquitoes in a semiarid environment from San Juan del Flumen (Los Monegros, Huesca, Spain) (Diptera, Culicidae). Boletín de la Asociación Española de Entomología 29 (3-4): 23-33. [ Links ]
DORVILLÉ, L. F. M. 1996. Mosquitoes as bioindicators of forest degradation in southeastern Brazil, a statistical evaluation of published data in the literature. Studies on Neotropical Fauna and Environment 31: 68-78. [ Links ]
ENCINAS GRANDES, A. 1982. Taxonomía y biología de los mosquitos del área salmantina (Diptera, Culicidae) [tesis doctoral]. CSIC, Centro de edafología y Biología aplicada. Ed. Universidad de Salamanca. Salamanca (España). 437 pp. [ Links ]
ERITJA, R.; ESCOSA, R.; LUCIENTES, J.; MARQUÈS, E.; MOLINA, R.; ROIZ, D.; RUIZ, S. 2005. Worldwide invasion of vector mosquitoes: present European distribution and challenges for Spain. Biological Invasions 7: 87-97. [ Links ]
GUTSEVICH, A. V.; MONCHADSKII, A. S.; SHTAKELBERG, A. A. 1974. Fauna of the USSR, Diptera, mosquitoes family Culicidae. Academy of Sciences of the USSR. 408 p. [ Links ]
HANNOUN, C.; PANTHIER, R.; MOUCHET, J.; EOUZAN, J. P. 1964. Isolement en France du virus West Nile à partir de malades et du vecteur Culex modestus Ficalbi. Comptes Rendus de l´Académie des sciences 259: 4170-4172. [ Links ]
HARBACH, R. E. 1988. The mosquitoes of the subgenus Culex in southwestern Asia and Egypt (Diptera: Culicidae). Contributions of the American Entomological Institute 24 (1): 1-240. [ Links ]
LÓPEZ SÁNCHEZ, S. 1989. Control integral de mosquitos en Huelva. Junta de Andalucía, Consejería de Salud y Servicios Sociales. Sevilla (España). 340 pp. [ Links ]
MAGURRAN, A. E. 1988. Ecological diversity and its measurement. Princeton University Press. New Jersey (EEUU). 179 pp. [ Links ]
MELERO ALCÍBAR, R. 2004. Biología y fenología de los Culicinae (Diptera: Culicidae) de la Comunidad de Madrid [tesis doctoral]. Ed. Universidad Complutense de Madrid. Madrid (España). 219 pp. [ Links ]
MERDIC, E.; VUJICIC-KARLO , S. 2005. Two types of hibernation of Culex pipiens complex (Diptera: Culicidae) in Croatia. Entomologia Croatica 9 (1-2); 71-76. [ Links ]
MONTES, J. 2005. Culicidae fauna of Serra da Cantareira, Sao Paulo, Brazil. Revista de Saúde Pública 39 (4): 578-584. [ Links ]
MOUSSIEGT, O. 1987. Aedes (Ochlerotatus) detritus (Haliday, 1833) Bibliographie. Document Entente Interdépartementale pour la Démoustication du Littoral Méditerranéen (France) 54: 1-43. [ Links ]
PIELOU, E. C. 1975. Ecological diversity. John Wiley, New York (EEUU). 165 pp. [ Links ]
PONGON, N.; BALENGHIEN, T.; TOTY, C.; FERRE, J. B.; THOMAS, C.; DERVIEUX, A.; L´AMBERT, G.; SCHAFFNER, F.; BARDIN, O.; FONTENILLE, D. 2007. Effects of local anthropogenic changes on potential malaria vector Anopheles hyrcanus and West Nile virus vector Culex modestus, Camargue, France. Emerging Infectious Diseases 13 (12): 1810-1815. [ Links ]
RIBEIRO, H. 1983. Sobre un novo índice de diversidade faunística. Boletim da Sociedade Portuguesa de Entomologia 42 (2): 129- 135. [ Links ]
RIBEIRO, H.; RAMOS, H. C.; ALVES PIRES, C. 1983. Contribução para o Estudo dos Vectores das Filaríases Animais em Portugal. Jornal da Sociedade das Ciências Médicas de Lisboa 97 (2): 143-146. [ Links ]
RIBEIRO, H.; ALVES PIRES, C.; RAMOS, H. C., 1996. Os mosquitos do Parque Natural da Arrábida (Insecta, Diptera, Culicidae). Garcia de Orta, Série de Zoologia (Portugal) 21 (1): 81- 110. [ Links ]
ROIZ, D.; ERITJA, R.; MELERO ALCIBAR, R.; MOLINA, R.; MARQUÈS, E.; RUIZ, S.; ESCOSA, R.; ARANDA, C.; LUCIENTES, J. 2007. Distribución de Aedes (Stegomyia) albopictus (Skuse, 1894) (Diptera, Culicidae) en España. Boletín de la Sociedad Entomológica Aragonesa 40: 523-526. [ Links ]
ROMEO VIAMONTE, J.M. 1950. Los anofelinos de España y de la zona española del Protectorado de Marruecos. Su relación con la difusión del paludismo. Revista de Sanidad e Higiene Pública 24: 213-295. [ Links ]
ROUBAUD, E. 1944. Etude sur les moustiques de la Crau. IV. Facteurs. de l´oeuf chez l´Aedes caspius Pallas. Bulletin de la Societe de Pathologie Exotique 37: 153-158. [ Links ]
RUIZ, S.; CÁCERES, F. 2004. Bases técnicas para el control de mosquitos culícidos en los arrozales de la Comarca de La Janda, Cádiz (SW España). Boletín de Sanidad Vegetal. Plagas 30: 753-762. [ Links ]
SCHAFFNER, F.; ANGEL, G.; GEOFFROY, B.; HERVY, J. O.; RHAEIM, A. 2001. The mosquitoes of Europe / Les moustiques d´ Europe [programa de ordenador]. Montpellier, France: IRD Éditions and EID Méditerranée. [ Links ]
SENEVET, G.; ANDARELLI, L. 1964. Les moustiques de l´Afrique du Nord et du Bassin Méditeterranéen. III.- Les Aedes. Deuxieme partie: Description des especes. Sous-genre Ochlerotatus group H. Archives de l´Institut Pasteur d´Algérie 44: 51-74. [ Links ]
SERVICE, M.W. 1993. Mosquito Ecology. Field Sampling Methods. 2nd edition. Elsevier Science Publishers. United Kingdom. 988 pp. [ Links ]
SHANNON, C. E.; WEAVER, W. 1949. The mathematical theory of communication. University of Illinois Press. Illinois, EEUU. 144 pp. [ Links ]
SIMSEK, F. M. 2004. Seasonal Larval and Adult Population Dynamics and Breeding Habitat Diversity of Culex theileri Theobald, 1903 (Diptera: Culicidae) in the Gölbaci District, Ankara, Turkey. Turkish Journal of Zoology. 28: 337-344. [ Links ]
TARAZONA, C.; CARRASCO, J. M.; SABATER, C. 2003. Monitoring of the rice pesticides thiobencarb, bensulfuron-methyl, molinate, pyridaphenthion and tebufenozide in an aquatic system of Natural Park of Albufera, Valencia, Spain. Hazard evaluation of these pesticides. En: Del Re, A. A. M.; Capri, E.; Padovani, L.; Trevisan, M. Pesticide in air, plant, soil & water system. Proceedings of the XII Symposium Pesticide Chemistry. Piacenza (Italia). 995 pp. [ Links ]