Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Entomología
Print version ISSN 0120-0488
Rev. Colomb. Entomol. vol.41 no.1 Bogotá Jan./June 2015
Hormigas y carábidos en cuatro ambientes del piedemonte del Parque Nacional Natural Farallones de Cali, Colombia
Soil ants and carabids in four environments of the piedmont from National Natural Park Farallones de Cali, Colombia
ANDERSON ARENAS1,2, GERMÁN CORREDOR1,3 e INGE ARMBRECHT1,4
1 Departamento de Biología. Universidad del Valle. A.A 25360 Cali, Colombia.
2 Biólogo. anderson.arenas@correounivalle.edu.co. Autor para correspondencia.
3 Biólogo. M. Sc. german.corredor@gmail.com.
4 Bióloga. Ph. D. inge.armbrecht@correounivalle.edu.co.
Resumen:
Con el objetivo de examinar la fauna de hormigas y escarabajos Carabidae asociada al suelo de pastizales, matorrales, cañadas y bosque primario en el piedemonte del Parque Nacional Natural Farallones de Cali, Colombia se hicieron muestreos utilizando el método de cernido de hojarasca y saco Winkler. Se evaluaron la abundancia, riqueza y se realizó un análisis de especies indicadoras para el grupo de las hormigas. Se encontró un total de 4524 hormigas (Hymenoptera: Formicidae) pertenecientes a 89 morfoespecies y 30 carábidos (Coleoptera: Carabidae) de cuatro especies. El bosque fue el ambiente más rico y diverso para hormigas (55 especies) seguido por la cañada (44 spp.), matorral (43 spp.) y pastizal (19 spp.) con una tendencia similar para Carabidae (2, 3, 2 y 0 especies, respectivamente). La especie de hormiga más abundante fue Wasmannia auropunctata, mientras que en Carabidae fue Notiobia sp. Se hallaron 11 especies de hormigas que podrían funcionar como indicadoras ambientales. Poco se puede decir de la fauna de carábidos, puesto que el número de individuos fue relativamente bajo, sin embargo, las especies encontradas ofrecen una primera aproximación al inventario de este grupo, para esta localidad en particular. Nuestros hallazgos apoyan la hipótesis que actividad antropogénica manifestada en la potrerización de la zona, es degenerativa para la diversidad de la mirmecofauna silvestre en esta vital zona de amortiguación del Parque Nacional Natural Farallones de Cali.Palabras clave: Especies indicadoras. Coleoptera. Formicidae. Perturbación antropogénica. Valle del Cauca.
Abstract: With the aim of examining the ants and carabid beetles fauna associated to the soil of grasslands, scrublands, glens and primary forest at the National Natural Park Farallones de Cali piedmont, Colombia leaf litter sifting samplings using the Winkler sac extraction method were carried out. Both, richness and abundance were evaluated and an analysis of indicator species for the ants group was done. A total of 4524 ants (Hymenoptera: Formicidae) belonging to 89 species and 30 carabids (Coleoptera: Carabidae) from four species were found. Forest was the most diverse and richest habitat (55 species) followed by glen (44 spp.), scrubland (43 spp.) and pasture (19 spp.) with a similar trend for Carabidae (2, 3, 2 and 0 species, respectively). The most abundant ant species was Wasmannia auropunctata, while for carabidae it was Notiobia sp. Eleven ant species could function as habitat indicators. Little can be said about the carabid fauna, due to a relatively low number of individuáis, nevertheless, the species found do offer a first approach to the species inventory of this group for this particular locality. Our findings support the hypothesis that anthropogenic activity associated to the increase of pastures is deletereous for the diversity of the myrmecofauna from the Natural National Park Farallones of Cali's buffer zone.
Key words: Indicator species. Coleoptera. Formicidae. Anthropogenic disturbance. Valle del Cauca.
Introducción
La transformación de los paisajes para urbanización, ganadería, minería y agricultura se generaliza cada vez más en los Andes colombianos y todo indica que no se detendrá (Etter 2006). Lo anterior, sumado a un pensamiento extractivista, va en detrimento de la diversidad natural y exacerba algunos problemas relacionados con la prestación de servicios ecológicos, como la polinización, el reciclaje de nutrientes y el control de plagas de cultivos (Matson et al.1997; Altieri 1999).
La instalación de asentamientos humanos y la deforestación llevan generalmente a la fragmentación de los bosques y a una consecuente disminución de la diversidad (Fahrig 2003), esto ha ocurrido cerca de Cali, en el corregimiento de Pance, de forma sistemática y creciente sin la generación de alerta alguna por parte de las autoridades ambientales y de la sociedad en general. Dado que es difícil y costoso estudiar cómo se pierde la biodiversidad a medida que se va destruyendo un ambiente, teniendo en cuenta todas las especies que lo habitan, se han escogido grupos representativos y sensibles como las hormigas (Hymenoptera: Formicidae) y los escarabajos carábidos (Coleoptera: Carabidae) del suelo, que son importantes en las redes alimenticias de los ecosistemas y han servido como indicadores ecológicos de la calidad de ambientes (Peck et al.1998; Sanabria et al. 2014).
El grado de especialización que tienen las hormigas es útil para conocer el estado ecológico de muchas zonas de vida en el planeta (Andersen 1997). Lo anterior implica que si se conoce la respuesta de las hormigas como grupo ecológico (comunidades o ensambles), se puede conocer si un ecosistema se está recuperando o al contrario, si se está degradando. Por ejemplo, si una especie de hormiga prefiere exclusivamente un ambiente que ha sido intervenido por humanos y se le encuentra ingresando o rodeando un área que ha sido catalogada como bosque, se podría discutir que algún proceso ecológico degradativo puede estar ocurriendo, aunque no sea evidente para los humanos. En Colombia se encuentran comunidades de hormigas que reflejan estados de degradación asociados a las transformaciones humanas e intensificación de la agricultura andina y a los pastizales abiertos (Armbrecht et al.2005; Rivera et al.2013). Por otra parte, las experiencias de restauración en Colombia han demostrado que el proceso de degradación se puede revertir o recuperar, pues la riqueza biológica de las hormigas aumenta a medida que se regenera la cobertura vegetal (Domínguez et al.2011; Calle et al.2013).
Los carábidos por su parte, son agentes bien conocidos de control natural de plagas de cultivos (Lundgren 2009), su diversidad es alta y son especializados en la ocupación de microambientes (Antvogel y Bonn 2001). Dado lo anterior, el análisis de su diversidad puede ofrecer información sobre estado de fragmentación de un área y los usos del suelo. Más importante aún, la composición de los carábidos en los ecosistemas puede proveer información sobre procesos ecológicos, ya sean degradativos o regenerativos (Davies y Margules 1998; Rainio y Niemela 2003).
Dado que el riesgo de perder fauna nativa aumenta con el paso del tiempo, el presente estudio se constituye en la primera aproximación al inventario de hormigas y carábidos del suelo del piedemonte de los Farallones de Cali, al mismo tiempo que busca evaluar el recambio de especies de hormigas, teniendo en cuenta cuatro ambientes en diferentes estados de sucesión ecológica. Se plantea la hipótesis que los ambientes más perturbados poseen menor riqueza de hormigas y carábidos que los menos perturbados. Se predijo además que la riqueza de especies de ambos grupos sería mayor en el bosque, seguida por la cañada, el matorral y el pastizal.
Materiales y métodos
Área de estudio. El área de estudio está localizada en el corregimiento de Pance, vereda el Peón, al sur del municipio de Cali y norte del municipio de Jamundí, corresponde a una transición entre el bosque seco tropical (bs-T) y el bosque húmedo premontano (bh-pm). Su elevación varía entre 1.100 y 1.600 m, con temperatura media de 23,8 °C, con máximas y mínimas de 36,4 °C y 17,5 °C, respectivamente. En el área se encuentran varios asentamientos como Chontaduro y El Peón (municipios de Jamundí y Cali) y Loma Larga (municipio de Cali), el paisaje es un mosaico que presenta algunospastizales para ganadería, matorrales y bosques ribereños intervenidos que acompañan las quebradas que corren por la localidad (cañadas) y bosques relictuales. En ese orden de ideas, los ambientes estudiados, de mayor a menor estado de degradación fueron pastizal, matorral, cañada y bosque. Los muestreos en los tres primeros se llevaron a cabo en Loma Larga, mientras que el muestreo en bosque se realizó en la parte de la vereda El Peón, jurisdicción del municipio de Jamundí (Fig. 1). En este último, los habitantes del sector extraen madera para diferentes usos, explotan minas de oro y realizan talas para la introducción de cultivos y ganado de forma periódica.
Muestreo e identificación de hormigas. En este estudio no se usaron réplicas a nivel espacial, (diferentes lotes aislados de pastizales o matorrales, cañadas o bosques), porque el paisaje todavía se encuentra interconectado y no existen áreas completamente aisladas unas de otras. Por lo que se realizaron cuatro sesiones de muestreo en cada ambiente -dos para cada período estacional seco y húmedo- en febrero, abril, agosto y noviembre de 2013.
En cada sesión de muestreo, la colecta de insectos se hizo dejando un margen de 10 m desde el borde de cada ambiente para minimizar el posible efecto de borde. En cada ambiente se hizo un transecto de 90 m, en el que se tomaron 10 muestras de hojarasca en intervalos de 10 m cada uno, usando el método de cernido de hojarasca según el protocolo de Agosti et al.(2000). Los transectos de muestreo dentro de cada ambiente fueron trazados en diferentes lugares para cada sesión, de modo que se disminuyera cualquier riesgo de seudorre-plicación. Para ello, cada unidad muestral consistió de un metro cuadrado marcado sobre el suelo, de cuyo interior se tomó toda la hojarasca y el mantillo. La hojarasca se depuró con un cernidor estándar, la fracción mayor de hojarasca se devolvió al bosque y el cernido se transportó al laboratorio, donde se dejó en sacos mini-winkler durante 48 horas para la obtención de los artrópodos. Los individuos colectados fueron puestos en alcohol etílico al 96% y posteriormente identificados con claves taxonómicas (Fernández 2003; Martínez 2005), finalmente se depositaron en la colección del Museo de Entomología de la Universidad del Valle (MUSENUV).
Análisis de diversidad de hormigas. Las abundancias de hormigas por unidad de muestreo fueron convertidas a datos de presencia/ausencia, de modo que el análisis de datos fuera el apropiado para los insectos sociales (Agosti et al.2000). La diversidad alfa de hormigas se calculó en cada uno de los ambientes, usando los estimadores basados en la incidencia de especies (ICE, Jackknife 1 y Jackknife 2) y se establecieron comparaciones entre ambientes usando el estimador Jac-kknife 2, también se incluyeron análisis con el índice inverso de Simpson (1-D) -que mide la probabilidad de encontrar dos individuos de diferente especie en dos muestras seguidas- y de Shannon -un valor numérico que permite determinar qué ambientes son más diversos- para describir la diversidad alfa. Para conocer si las diferencias entre las diversidades fueron significativas se hizo un análisis de varianza (ANOVA). Dado que el presente estudio no pretende obtener conclusiones universales sobre la diversidad, sino sobre un paisaje dado, se consideró que cada unidad muestral fue independiente, tomando como referencia los comentarios de Oksanen (2001), quien argumenta que la seudorreplicación es un seudo-problema, puesto que la estadística inferencial se puede usar en la mayoría de los casos, generando así una discusión sobre los patrones aparentes de las variables respuesta en las muestras, y si éstos son reales o no. Se sugiere por lo tanto, que la aplicación de estadística inferencial es válida para el análisis de los datos obtenidos. Por otro lado, se hizo un análisis de diversidad beta para las especies de hormigas, usando el índice de similitud de Jaccard, con los programas EstimateS 8.2 (Colwell 2009) y PAST (Hammer et al.2001), de libre distribución. Finalmente, se realizó un análisis de especies indicadoras (IndVal), para conocer qué especies se encuentran asociadas a determinados ambientes, usando el programa Pc Ord (McCune y Mefford 2011).
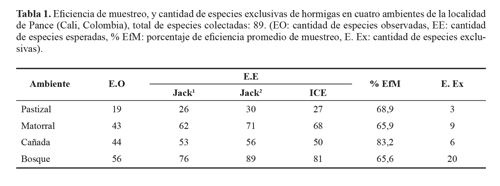
ResultadosDiversidad de hormigas. Se encontraron 4524 individuos de 89 morfoespecies diferentes (Anexo 1). La especie más abundante fue Wasmannia auropunctata (Roger, 1863), con 1096 individuos, es decir un 25,26% de la abundancia total, de esta especie se colectaron solo dos individuos en bosque. Los estimadores de la diversidad mostraron que la eficiencia de muestreo promedio fue superior al 65% en todos los ambientes. El ambiente que presentó mayor cantidad de especies fue el bosque (Tabla 1).
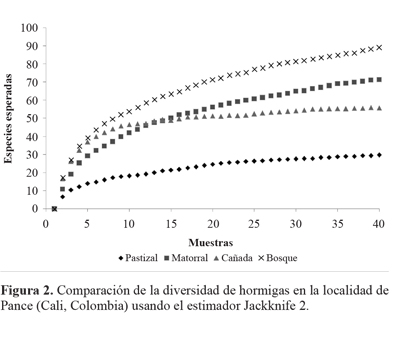
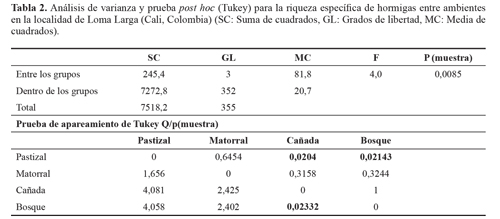
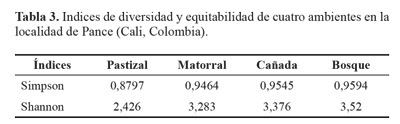
La comparación gráfica del estimador Jackknife 2 evidenció que a baja intensidad de muestreo, la diversidad de hormigas en la cañada parece ser mayor. Sin embargo, al intensificar el esfuerzo de muestreo, el bosque fue el ambiente más diverso (Fig. 2), por otra parte, el ANOVA mostró diferencias significativas entre los grupos (Tabla 2). Los índices de diversidad mostraron que el ambiente más diverso fue el bosque, mientras que el menos diverso fue el pastizal (Tabla 3).
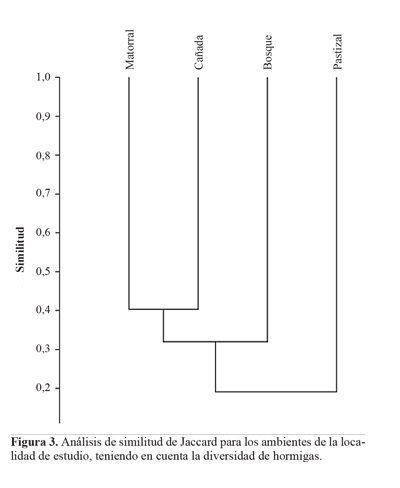
El análisis de diversidad beta mostró que los ambientes más parecidos entre sí fueron el matorral y la cañada, más cercanos al bosque que al pastizal (Fig. 3).
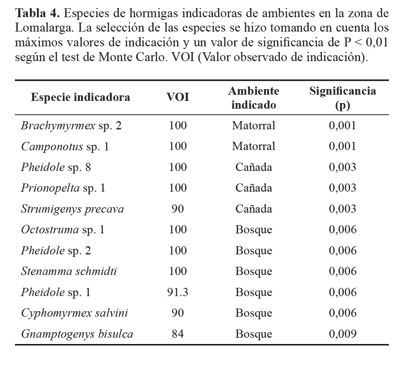
Hormigas indicadoras. Se encontró que once especies de hormigas podrían funcionar como indicadoras de ambiente, siendo el bosque, la cañada y el matorral los ambientes que presentaron especies indicadoras (Tabla 4).
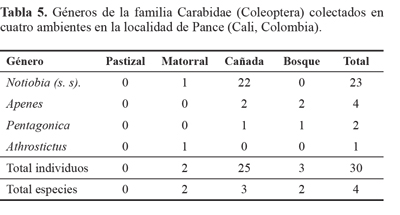
Carábidos de hojarasca. En Loma Larga se encontraron cuatro géneros, siendo NotiobiaPerty, 1830 (s. s.), el más abundante con 23 inividuos, seguido de ApenesLeConte, 1851 (4), PentagonicaSchmidt-Gobel, 1846 (2) y Athrostic-tusBates, 1878 (1). La mayoría de los especímenes se colectó en cañada (Tabla 5).
DiscusiónLos estimadores e índices de diversidad, así como sus respectivas comparaciones demuestran que la diversidad disminuye a medida que se cambia de un ambiente menos perturbado a uno más perturbado. La anterior evidencia apoya la hipótesis de la pérdida biológica, que está ocurriendo en el piedemonte del Parque Nacional Natural Farallones de Cali debido a la creciente intervención humana, a los asentamientos, a la tala de los bosques y la conversión del paisaje en potreros. Sin embargo, el mosaico de ambientes presente en la zona de Loma Larga y la vereda El Peón puede ser recuperado, porque la interconectividad del paisaje todavía permite que los propá-gulos colonicen de nuevo las zonas degradadas cuando éstas se avanzan en matorrales a través de la sucesión ecológica.
Diversidad de hormigas. Las hormigas demostraron una alta sensibilidad a la transformación de los ambientes en la zona de estudio, esto se manifestó en un descenso de su diversidad cuando el bosque fue comparado con el pastizal. La riqueza de hormigas se perdió al menos en un 12% del bosque a las cañadas y más del 40% en los pastizales. Sin embargo, al observar un ambiente sucesional, como el matorral, se evidenció que la riqueza de hormigas fue el doble, esto significa que la interconectividad puede proveer propágulos para la recuperación ecológica. El mismo fenómeno se observó para los índices de diversidad, que fue mayor en el bosque y menor en los pastizales. La composición, como se demuestra en el análisis de aglomeración, fue muy diferente en el pastizal comparado con los bosques y matorrales. El presente trabajo es consistente con lo hallado por Bustos y Chacón de Ulloa (1996-1997), en un gradiente sucesional cercano al mismo Parque Natural, quienes demostraron que el bosque primario fue el más rico en hormigas (15,7 especies en promedio), seguido por el bosque secundario (13,3 especies) y la zona en regeneración (6 especies). Las curvas de saturación de especies en el presente estudio, con más del 65% de la fauna muestreada, permiten confiar que los muestreos reflejan la realidad ecológica de los ambientes que ofrece este paisaje para las hormigas. Las hormigas responden fielmente a la perturbación y a la recuperación ecológica (Lach et al.2010) y los diferentes ambientes en la zona de estudio son comparables por encontrarse aproximadamente a la misma altura, región, y compartir la misma historia reciente de intervención antrópica. El análisis de IndVal reveló que el recambio ambiental que está ocurriendo puede tener impacto a mediano y largo plazo en la composición de especies de hormigas. Es notorio que en un tiempo relativamente corto de la escala en décadas (con mayor intensidad en los últimos años) la actividad humana degradativa puede generar cambios detec-tables en la composición de la comunidad de hormigas. Las hormigas cazadoras GnamptogenysRoger, 1863 y Octostru-maForel, 1912 (Bolton 1995), así como otras especialistas crípticas de hojarasca como StenammaWestwood, 1839 fueron indicadoras de bosque, demostrando que este ecosistema natural es refugio de delicada biodiversidad. A su vez, también las cañadas son ambientes irremplazables que albergan hormigas indicadoras muy sensibles, que anidan en madera en descomposición como Strumigenys precava Brown, 1954 y Tatuidris tatusiaBrown & Kempf, 1968, esta última presentó individuos (35) únicamente en este ambiente, principalmente en temporada de lluvias. Este hallazgo es consistente con los ambientes en los que se ha registrado previamente, poco se conoce sobre esta especie y sus hábitos alimenticios siguen siendo un misterio, aunque se cree que estas hormigas pueden operar como depredadores máximos de las redes tróficas en hojarasca (Jacquelim et al.2014). En pastizales no se presentaron hormigas indicadoras mientras que en matorrales sí pero menos especializadas que las del bosque, como CamponotusMayr, 1861 y Brachymyrmex Mayr , 1868, lo que significa que las hormigas responden a la recuperación ecológica. Este estudio es consistente con otro que muestran la rápida y consistente respuesta de las hormigas de suelo a los cambios ambientales (Armbrecht et al.2005; Sanabria et al. 2014).
Las evidencias encontradas en este estudio a partir de las comunidades de hormigas apoyan la idea que el descenso de diversidad, riqueza y cambios en la composición de hormigas están relacionados con los cambios de ambientes originados por la perturbación humana.
Carábidos de la hojarasca. La abundancia de carábidos fue relativamente baja, sin embargo esta es la primera aproximación a su diversidad para esta zona del país, más allá de la presentada por Martínez (2005). El ambiente que presentó mayor cantidad de carábidos de hojarasca fue la cañada, con casi todos los individuos. Esta tendencia se puede explicar si se tiene en cuenta que el factor que más favorece la presencia de carábidos es la alta humedad (Rainio y Niemela 2003), condición más común en las quebradas que en los demás ambientes.
En el pastizal no se encontraron individuos de Carabidae, lo más probable es que la tendencia de este ambiente a ser seco, no presente abundante hojarasca ni recursos de refugio para ellos. La poda de la vegetación arbustiva y arbórea parece afectar negativamente la posibilidad de presencia de carábidos en pastizales. El género que presentó mayor cantidad de individuos fue Notiobia,un habitante común de los sitios con gran disponibilidad de semillas, ya sea de plantas arvenses de cultivos o de ambientes boscosos (Paarman et al.2002; Arenas et al.2013). Es importante resaltar que el género Apenes es considerado depredador de otros artrópodos y algunas de sus especies pertenecen al gremio de los habitantes de frutos de higo caídos (Moraceae) en el interior de bosques (Erwin et al.2012). Pese al bajo número de carábidos encontrados en hojarasca (influenciado también por el método de mues-treo, que está más orientado hacia las hormigas), se pueden tomar en cuenta las características naturales de las especies halladas para desarrollar estrategias de manejo de cultivos que favorezcan la conservación de ambientes con gran cantidad de hojarasca, limitando la presencia de algunas especies de pastos invasores, como lo podría hacer Notiobiasp. Mientras que algunas plagas de insectos comunes, como las moscas de la familia Tephritidae y Lonchaeidae podrían sufrir algún tipo de ataque en sus estados larvarios por individuos de Apenes sp. Dado lo anterior, sería ideal poder realizar estudios cuantitativos en la zona de estudio -con los métodos de colecta apropiados- sobre la capacidad de remover presas por parte de los carábidos y no refugiarse solamente en las observaciones cualitativas de campo sobre su comportamiento.
En síntesis, este estudio se constituye en la primera aproximación a la evaluación de carábidos en diferentes ambientes de la zona de amortiguación del Parque Nacional Natural Farallones de Cali, en el que nuestros hallazgos apoyan la hipótesis que actividad antropogénica, manifestada en la potrerización de la zona, disminuye la diversidad de fauna silvestre.
AgradecimientosAgradecemos la ayuda en los muestreos a Pedro José Cardona, Diego Guillén, Paola Olaya, Stephanie Valderrama, y Florentino Martínez. En la primera fase de revisión de muestras agradecemos a Humberto Calero y Stephanie Valdés. Elizabeth Jiménez colaboró con algunos análisis de datos. A Colciencias a través del programa de Jóvenes Investigadores e Innovadores "Virginia Gutiérrez de Pineda" otorgado a Anderson Arenas. Este trabajo fue financiado por la Universidad del Valle, Vicerrectoría de Investigaciones, en el marco del Proyecto de convocatoria interna "Uso delhábitat por aves caminadoras de sotobosque en el piedemonte del Parque Nacional Natural Farallones de Cali", código CI 7897.
Literatura citadaAGOSTI, D.; MAJER, J.; ALONSO, L.; SCHULTZ, T. (Eds.). 2000. Ants, Standard methods for measuring and monitoring biodiversity. Smithsonian Institution Press. Washington. 280 p. [ Links ]
ALTIERI, M. 1999. The ecological role of biodiversity in agro-ecosystems. Agriculture, Ecosystems and Environment 74: 1931. [ Links ]
ANDERSEN, A. N. 1997. Using Ants as bioindicators: Multiscale Issues in Ant Community Ecology. Conservation Ecology 1 (1): 8. [ Links ]
ANTVOGEL, H; BONN, A. 2001. Environmental parameters and microspatial distribution of insects: a case study of carabids in an alluvial forest. Ecography 24 (4): 470-482. [ Links ]
ARENAS, A.; ARMBRECHT I.; CHACÓN, P. 2013. Carábidos y hormigas del suelo en dos áreas cultivadas con maracuyá amarillo (Passiflora edulis) en el Valle del cauca, Colombia. Acta Biológica Colombiana 18 (3): 439-447. [ Links ]
ARMBRECHT, I.; RIVERA L.; PERFECTO, I. 2005. Reduced diversity and complexity in the leaf litter ant assemblage of Colombian coffee plantations. Conservation Biology 19 (3): 897-907. [ Links ]
BOLTON, B. 1995. A new general catalogue of the ants of the world. Harvard University Press. Cambridge- Massachussets. 504 p. [ Links ]
BUSTOS, J; ULLOA-CHACÓN, P. 1996-1997. Mirmecofauna y perturbación en un bosque de niebla neotropical (Reserva Natural Hato Viejo, Valle del Cauca, Colombia). Revista de Biología Tropical 44/45: 259-266. [ Links ]
CALLE, Z.; HENAO-GALLEGO, N.; GIRALDO, C.; ARMBRECHT, I. 2013. A Comparison of vegetation and ground-dwelling ants in abandoned and restored gullies and landslide surfaces in the western Colombian Andes. Restoration Ecology 21:729-735. [ Links ]
COLWELL, R. K. 2009. Estimates: Statistical estimation of species richness and shared species from samples. Version 8.2. User's Guide and application. Disponible en: URL: http://viceroy.eeb.uconn.edu/estimates/ [ Links ]
DAVIES, K.; MARGULES, C. 1998. Effects of habitat fragmentation on carabid beetles, experimental evidence. Journal of Animal Ecology 67: 460-471. [ Links ]
DOMÍNGUEZ-HAYDAR, Y.; ARMBRECHT, I. 2011. Response of ants and their seed removal in rehabilitation areas and forests at El Cerrejón coal mine in Colombia. Restoration Ecology 19 (201): 178-184. [ Links ]
ERWIN, T.; MICHELI, C.; HEVEL, G. 2012. The beetle family Carabidae of Guyane (French Guyana): the tribes, genera, and number of species known, with notes on their ways of life. (Insecta: Coleoptera: Adephaga). ACOREP, Paris, 92 p. [ Links ]
ETTER, A.; MCALPINE, C.; WILSON, K.; PHINN, S.; POS-SINGHAM, H. 2006. Regional patterns of agricultural land use and deforestation in Colombia. Agriculture, Ecosystems and Environment 114: 369-386. [ Links ]
FAHRIG, L. 2003. Effects of habitat fragmentation on biodiversity. Annual Review of Ecology, Evolution and Systematics 34: 487-515. [ Links ]
FERNÁNDEZ, F. (Ed). 2003. Introducción a las hormigas de la región neotropical, Instituto de Investigaciones y Recursos Biológicos Alexander Von Humboldt. Bogotá. 398 p. [ Links ]
HAMMER, O.; HARPER, D. A. T.; RYAN, P. D. 2001. PAST: Paleontological statistics software package for education and data analysis. Palaeontologia Electronica 4 (1): 1-9. [ Links ]
JAQUELIM, J.; DELSINNE, T.; MARAUN, M.; LEPONCE, M. 2014. Trophic ecology of the armadillo ant, Tatuidris tatusia , assessed by stable isotopes and behavioral observations. Journal of Insect Science 14 (108): 1-12. [ Links ]
LACH, L.; PARR, C.; ABBOTT, K. (Eds.). 2010. Ant Ecology. Oxford University Press. Oxford Reino Unido. 432 p. [ Links ]
LUNDGREN, J. 2009. Relationships of natural enemies and non-prey foods. Springer. Brookings SD. 453 p. [ Links ]
MARTÍNEZ, C. 2005. Introducción a los escarabajos Carabidae (Coleoptera) de Colombia. Instituto de Investigaciones y Recursos Biológicos Alexander Von Humboldt. Bogotá. 546 p. [ Links ]
MATSON, P. A.; PARTON, W. J.; POWER, A. G., SWIFT, M. J. 1997. Agricultural intensification and ecosystem properties. Science 277: 504-509. [ Links ]
MCCUNE, B.; MEFFORD, M. J. 2011. PC-ORD. Multivariate Analysis of Ecological Data. Version 6. MjM Software, Gleneden Beach, Oregon, EEUU. [ Links ]
OKSANEN, L. 2001. Logic of experiments in ecology: is pseudore-plication a pseudoissue?. Oikos 94 (1): 27-38. [ Links ]
PAARMANN, W.; GUTZMANN, B.; STUMPE, P; BOLTE, H.; KÜPPERS, S.; HOLZKAMP, K.; NIERS, C.; ADIS, J.; STORK, N.; DA FONSECA, C. 2002. The structure of ground beetle assemblages (Coleoptera: Carabidae) at fruit falls of Melastomataceae trees in a Brazilian Terra Firme rain forest. Biotropica 34 (3): 368-375. [ Links ]
PECK, S., MCQUAID, B.; CAMPBELL, L. 1998. Using ant species (Hymenoptera: Formicidae) as biological indicator of agroecosystem condition. Community and Ecosystem Ecology 27 (5): 1102-1110. [ Links ]
RAINIO, J.; NIEMELÁ, J. 2003. Ground beetles (Coleoptera: Carabidae) as bioindicators. Biodiversity and Conservation 12: 487-506. [ Links ]
RIVERA, L. F.; ARMBRECHT, I.; CALLE, Z. 2013. Silvopastoral systems and ant diversity conservation in a cattledominated landscape of the Colombian Andes. Agriculture, Ecosystems and Environment 181: 188-194. [ Links ]
SANABRIA, C.; LAVELLE, P.; FONTE, S. J. 2014. Ants as indicators of soilbased ecosystem services in agroecosystem of the Colombian Llanos. Applied Soil Ecology 84: 24-30. [ Links ]
Recibido: 3-sep-2014
Aceptado: 24-mar-2015
ARENAS, A.; CORREDOR, G.; ARMBRECHT, I. 2015. Hormigas y carábidos en cuatro ambientes del piedemonte del Parque Nacional Natural Farallones de Cali, Colombia. Revista Colombiana de Entomología 41 (1): 120-125. Enero-Junio 2015. ISSN 0120-0488.