Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista ION
Print version ISSN 0120-100X
Rev. ion vol.25 no.spe Bucaramanga Oct. 2012
oxidación electrolítica por plasma
Oscar Galvis1,2*; David Quintero1,2; Juan José Pavón3; Juan G. Castaño1,2; Félix Echeverría1,2
1 Grupo de Corrosión y Protección, Universidad de Antioquia,
Calle 62 # 52-59, Medellín, Colombia.
*oscargalvis@udea.edu.co
2 Centro de Investigación, Innovación y Desarrollo de Materiales(CIDEMAT), Universidad de Antioquia,
Calle 62 # 52-59, Medellín, Colombia.
3 Grupo de Investigación en Biomateriales. Universidad de Antioquia,
Calle 62 # 52-59 - Edificio SIU, Medellín, Colombia.
Fecha Recepción: 2 de septiembre de 2011
Fecha Aceptación: 24 de enero de 2012
Se obtuvieron recubrimientos anódicos sobre Ti mediante oxidación electrolítica por plasma en soluciones de ácido sulfúrico (H2SO4) con diferentes concentraciones de ácido fosfórico (H3PO4) como aditivo. Se evaluó el comportamiento frente a la corrosión de los recubrimientos mediante Espectroscopía de Impedancia Electroquímica (EIE) en soluciones simuladas de fluidos corporales (SBF). La caracterización mediante SEM/EDS y espectroscopía Raman permitió observar una alta influencia del contenido de H3PO4 en la morfología y composición de los recubrimientos.
Palabras clave: óxidos de titanio, oxidación electrolítica por plasma, recubrimientos anódicos, SBF, biomateriales.
electrolytic oxidation
Anodic coatings were obtained on Ti through plasma electrolytic oxidation in sulfuric acid (H2SO4) solutions containing phosphoric acid (H3PO4) as an additive. The coatings corrosion behavior was evaluated by means of Electrochemical Impedance Spectroscopy (EIS) in Simulated Body Fluid solution (SBF). Characterization of the coatings was made using SEM/EDS and Raman spectroscopy, It allowed to observe great influence in its morphology and composition due to phosphoric acid content into the coatings.
Keywords: titanium oxides, plasma electrolytic oxidation, anodic coatings, SBF, biomaterials.
En el sector de los biomateriales, el titanio y sus aleaciones son materiales ampliamente empleados debido a las buenas propiedades mecánicas y anticorrosivas que presentan. Sin embargo, a pesar de sus notables ventajas y de su buen comportamiento, estos biomateriales pueden presentar fallas ó aflojamientos en procedimientos médicos. Estas fallas según estudios previos, están asociadas a una pobre formación de tejido óseo alrededor del implante. Las propiedades superficiales de estos materiales como porosidad, rugosidad, morfología y composición juegan un papel muy importante en el fenómeno de formación de dicho tejido y por ende en la funcionalidad de estos materiales [1-4].
En la actualidad, los estudios en este campo están dirigidos a modificar la superficie de estos biomateriales y así tratar de solventar este problema. Las estrategias están dirigidas a recubrir titanio con materiales bioactivos base Ca-P con el objetivo de combinar las buenas propiedades mecánicas del titanio y sus aleaciones y las ya conocidas propiedades biológicas de los materiales cerámicos base [5, 6, 7]. Otra estrategia es la de realizar un pretratamiento al titanio en una solución de hidróxido de sodio bajo condiciones hidrotermales con la subsiguiente exposición a soluciones corporales simuladas para permitir la formación de una capa de apatita sobre la superficie [7,8]. Entre las técnicas de modificación superficial usadas, la oxidación anódica permite la formación de un recubrimiento anódico sobre la superficie del titanio con morfología, composición y estructura dependiente de las características de la solución electrolítica y de las condiciones eléctricas del proceso.
Las capas anódicas de óxidos de titanio nanoporosas exhiben propiedades interesantes para ser empleadas en biomateriales, debido a su alta área superficial y a su alta compatibilidad como material de implante, además de mejorar considerablemente sus propiedades anticorrosivas [9, 10].
La bioactividad del titanio es afectada por las propiedades físicas y químicas del recubrimiento anódico; sin embargo, los efectos de las características superficiales del titanio y sus aleaciones sobre sus propiedades como biomaterial aún no están completamente entendidas [11, 12]. Las aleaciones de titanio, debido a su alta biocompatibilidad, a las buenas propiedades mecánicas y al buen comportamiento ante la corrosión, son los materiales más empleados en la actualidad para reemplazar y mejorar la funcionalidad del tejido óseo del cuerpo humano.
Sin embargo, a pesar de sus notables ventajas, estos materiales pueden presentar problemas asociados a una pobre formación de tejido óseo alrededor del implante. En estudios previos, se halló que las propiedades superficiales de estos materiales tales como porosidad, rugosidad, morfología y composición, son fundamentales en la formación de tejido óseo alrededor del implante; por tanto, el propósito de la modificación superficial mediante el anodizado es el de mejorar la compatibilidad del material con el tejido.
Las muestras empleadas en esta investigación fueron monedas de Titanio comercialmente puro grado 2 (ASTM F-67) [13], con las siguientes dimensiones: 1,3mm de espesor y 22 mm de diámetro. Su superficie fue pulida con papel abrasivo de SiC hasta grado 600, luego fueron desengrasadas mediante ultrasonido con acetona. Para el proceso de anodizado se emplearon dos soluciones de anodizado compuestas por H2SO4/ H3PO4 en relaciones 5/1 y 2,5/1 respectivamente.
Para la fabricación de los recubrimientos anódicos, se empleó una fuente de potencia marca Kepko Inc. El proceso tuvo una duración total de 40 minutos, empleando una malla cilíndrica de platino como cátodo. Se aplicó a las muestras una densidad de corriente constante de 35mA/cm2 y se dejó evolucionar el potencial del sistema hasta que alcanzara un valor de 180V, momento en el cual el proceso fue transferido a modo potenciostático, manteniendo el potencial en este valor durante el tiempo restante.
Para observar las microestructuras y obtener la composición elemental de los recubrimientos anódicos se utilizó un microscopio electrónico de barrido JEOL JSM 6940 LV, equipado con una microsonda de energía dispersiva de Raxos X (EDS). La identificación de las fases presentes en los recubrimientos fue realizada mediante espectroscopía Raman (Micro-Raman, Horiba Jovin Yvon).
La resistencia a la corrosión de los recubrimientos anódicos se determinó mediante medidas de impedancia electroquímica, realizadas en un Potenciostato Autolab PGSTAT 302 controlado por un software NOVA 1,6 a potencial de circuito abierto (PCA), en modo potenciostático, con un barrido de frecuencias entre 0,1MHz y 1mHz usando una perturbación de 10mV de amplitud. Los potenciales fueron medidos con respecto a un electrodo saturado de Calomel (ESC). La solución SBF reportada por Kokubo T et al. [14] fue empleada como electrolito para los ensayos de resistencia a la corrosión.
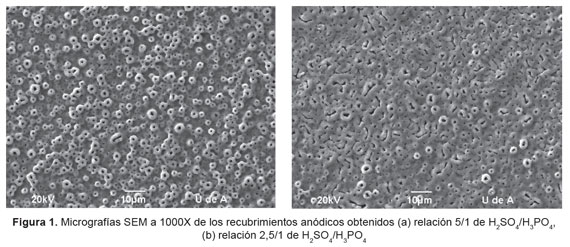
En la Figura 1 se muestran las micrografías SEM de los recubrimientos anódicos obtenidos en las dos soluciones de anodizado. En estas se observa que los recubrimientos anódicos son porosos, que presentan diferencias en su morfología y una distribución de poros uniforme en toda el área analizada.
También se evidencia una diferencia notoria en el tamaño y forma de los poros en los dos recubrimientos obtenidos, y se observa en el recubrimiento obtenido en el electrolito con mayor contenido de H3PO4 que algunos de estos poros presentan coalescencia. Adicionalmente, la variación en la composición de la solución de anodizado genera cambios tanto en el espesor de pared de los poros como en la rugosidad de las capas anódicas.
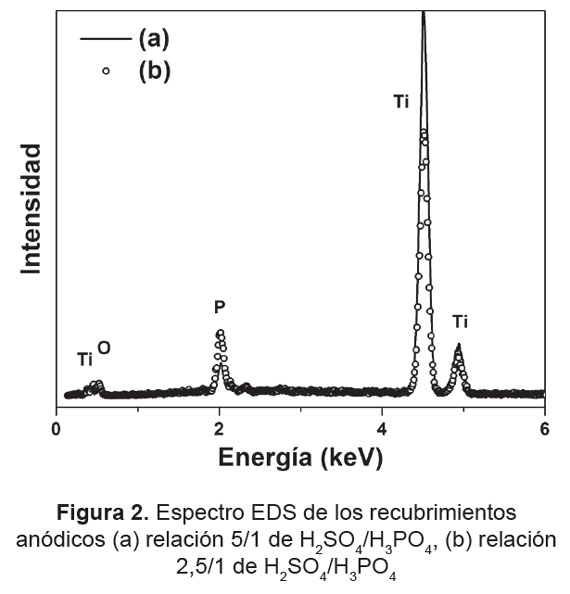
El análisis de los espectros EDS de los recubrimientos obtenidos en ambos electrolitos se muestra en la Figura 2, donde se evidencia la presencia de fósforo en el interior del recubrimiento. Este proviene de especies iónicas contenidas en la solución de anodizado que se incorporan en el recubrimiento durante el proceso de anodizado. La mayor concentración de este elemento se encuentra en el recubrimiento (b) [15,16].
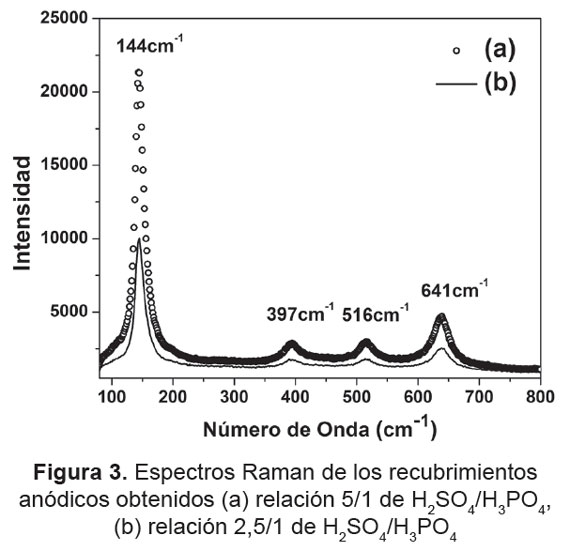
En la Figura 3, se muestran los espectros Raman de los recubrimientos anódicos obtenidos en las dos soluciones de anodizado. En ambos se observan las cuatro bandas características de la fase anatasa a 144, 397, 516 y 641cm-1 [17]. Al igual que en los difractogramas, en estos espectros no se evidencia la presencia de bandas pertenecientes a otras fases y se confirma la disminución en la intensidad de las bandas a medida que el contenido de H3PO4 se incrementa en la solución de anodizado empleada para su obtención.
Los espesores de los recubrimientos anódicos obtenidos fueron determinados mediante Microscopía Electrónica de Barrido. Sus valores se encuentran entre 3 y 4μm para ambos recubrimientos. Esto indica que los cambios observados en las intensidades de los espectros EDS y Raman no son debidos a diferencias entre los espesores de los recubrimientos y sí a cambios estructurales y/o composicionales debidos a la incorporación de especies que contienen fósforo y que provienen de la solución de anodizado empleada en su obtención.
Marino et al. [18], reportaron la incorporación de fosfatos y fosfuros al interior del recubrimiento durante el proceso de anodizado de Ti en soluciones buffers de fosfatos a pH 1 y 5; además, encontraron que la cantidad de especies compuestas por fósforo incorporadas en el recubrimiento anódico variaba con el espesor, encontrándose mayor incorporación en la zona más externa; este fenómeno podría explicar el efecto en la propiedades anticorrosivas de los recubrimientos; sin embargo, aún no está completamente estudiado el efecto de la incorporación de estas especies [18].
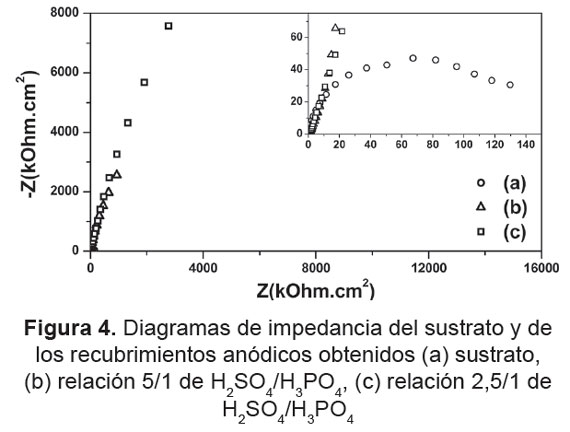
Las curvas de impedancia de los recubrimientos obtenidos y del sustrato son mostrados en la Figura 4. Se puede observar que los recubrimientos presentan valores de impedancia considerablemente mayores a los del sustrato desnudo. Además, al realizar la lectura en el eje real de la impedancia a bajas frecuencias, se encuentra que el valor más alto de ésta lo presenta el recubrimiento (b), obtenido en la solución de anodizado con mayor concentración de H3PO4, lo que indica que su comportamiento anticorrosivo en SBF es mejor que el del recubrimiento (a). Es claro, además, que ambos recubrimientos tienen un comportamiento mucho mejor que el del sustrato. Estos resultados están acorde con el trabajo realizado por Fadl-allah et al. [10], donde reportaron que la resistencia a la corrosión de recubrimientos anódicos obtenidos sobre Ti c.p en soluciones de anodizado compuestas por 1,4M H3PO4 fue considerablemente superior al que presentó el titanio sin recubrimiento; además, concluyeron que los recubrimientos anódicos obtenidos en H3PO4 presentan un importante aumento de la resistencia a la corrosión del Ti c.p en medios biológicos. Jakubowicz J [19], también concluyó en su trabajo de investigación que los recubrimientos anódicos obtenidos sobre Ti en soluciones H3PO4, presentan una resistencia a la corrosión considerablemente superior a la del titanio puro lo cual es extremadamente importante para aplicaciones en biomateriales.
Se obtuvieron recubrimientos anódicos porosos sobre titanio empleando la técnica de anodizado en dos diferentes soluciones de anodizado. Las características morfológicas y estructurales del los recubrimientos anódicos fueron dependientes de la composición y concentración de H3PO4 en la solución de anodizado empleada en el proceso. En el recubrimiento obtenido en la solución de anodizado con mayor contenido de H3PO4 se halló un mayor contenido de fósforo incorporado dentro de la película anódica, lo cual ha sido confirmado con los análisis de espectroscopía Raman. Finalmente, la presencia de fósforo en el recubrimiento mejora su comportamiento anticorrosivo en soluciones SBF, según los diagramas de impedancia.
Los autores quieren expresar agradecimientos al Departamento Administrativo de Ciencia, Tecnología e Innovación âColcienciasâ por el apoyo financiero brindado por medio del proyecto de investigación 111545221209.
[1] Cui X, Kim H, Kawashita M, Wang L, Xiong T, Kokubo T, Nakamura T. Preparation of bioactive titania films on titanium metal via anodic oxidation. Dent. Mater. 2009;25(1):80-6. [ Links ]
[2] Kizuki T, Takadama H, Matsushita T, Nakamura T, Kokubo T. Preparation of bioactive Ti metal surface enriched with calcium ions by chemical treatment. Acta Biomat. 2010;6(7):2836-42. [ Links ]
[3] Fujibayashi S, Neo M, Kim HM, Kokubo T, Nakamura T. Osteoinduction of porous bioactive titanium metal. Biomaterials. 2004;25(3):443-50. [ Links ]
[4] Kokubo T, Matsushita T, Takadama H, Kizuki T. Development of bioactive materials based on surface chemistry. J. Eur. Ceram. Soc. 2009;29(7):1267-74. [ Links ]
[5] Liu X, Chu P, Ding C. Surface modification of titanium, titanium alloys, and related materials for biomedical applications. Mater. Sci. Eng. R-Rep. 2004;47(3):49-121. [ Links ]
[6] Becker I, Hofmann I, Müller FA. Preparation of bioactive sodium titanate ceramics. J. Eur. Ceram. Soc.. 2007;27(16):4547-53. [ Links ]
[7] Frauchiger VM, Schlottig F, Gasser B, Textor M. Anodic plasma-chemical treatment of CP titanium surfaces for biomedical applications. Biomaterials. 2004;25(4):593-606. [ Links ]
[8] Oh S, Jin S. Titanium oxide nanotubes with controlled morphology for enhanced bone growth. Mater. Sci. Eng. C. 2006;26(8):1301-6. [ Links ]
[9] Fadl-Allah S, El-Sherief R, Badawy W. Electrochemical formation and characterization of porous titania (Tio2) films on Ti. J. Appl. Electrochem. 2008;38(10):1459-66. [ Links ]
[10] Fadl-Allah S, Mohsen Q. Characterization of native and anodic oxide films formed on commercial pure titanium using electrochemical properties and morphology techniques. Appl. Surf. Sci. 2010;256(20):5849-55. [ Links ]
[11] Yang B, Uchida M, Kim H, Zhang X, Kokubo T. Preparation of bioactive titanium metal via anodic oxidation treatment. Biomaterials. 2004;25(6):1003-10. [ Links ]
[12] Song HJ, Kim MK, Jung GC, Vang MS, Park YJ. The effects of spark anodizing treatment of pure titanium metals and titanium alloys on corrosion characteristics. Surf. Coat. Technol.. 2007;201(21):8738-45. [ Links ]
[13] ASTM. Standard Specification for Unalloyed Titanium, for Surgical Implant Applications. ASTM, Pennsylvania. Estados Unidos; 2006. [ Links ]
[14] Kokubo T, Kushitani H, Sakka S, Kitsugi T, Yamamuro T. Solutions able to reproduce in vivo surface-structure changes in bioactive glass-ceramic A-W3. J. Biomed. Mater. Res. Part A.. 1990;24(6):721-34. [ Links ]
[15] Oh HJ, Lee JH, Jeong Y, Kim YJ, Chi CS. Microstructural characterization of biomedical titanium oxide film fabricated by electrochemical method. Surf. Coat. Technol.. 2005;198(1-3):247-52. [ Links ]
[16] Lee JH, Kim SE, Kim YJ, Chi CS, Oh HJ. Effects of microstructure of anodic titania on the formation of bioactive compounds. Mater. Chem. Phys. 2006;98(1):39-43. [ Links ]
[17] Arsov L, Kormann C, Plieth W. In Situ Raman Spectra of Anodically Formed Titanium Dioxide Layers in Solutions of H2SO4, KOH, and HNO3. J. Electrochem. Soc. 1991;138(10):2964-70. [ Links ]
[18] Marino CEB, Nascente P, Biaggio S, Rocha-Filho R, Bocchi N. XPS characterization of anodic titanium oxide films grown in phosphate buffer solutions. Thin Solid Films. 2004;468(12):109-12. [ Links ]
[19] Jakubowicz J. Formation of porous TiOx biomaterials in H3PO4 electrolytes. Electrochem. Commun. 2008;10(5):735-9. [ Links ]