Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista ION
versão impressa ISSN 0120-100X
Rev. ion vol.28 no.1 Bucaramanga jan./jun. 2015
de aceros inoxidables austeníticos: influencia de la
adición de manganeso en solución sólida
José Wilmar Calderón-Hernández*; Iara Beatriz Braga Luz; Duberney Hincapie-Ladino;
Neusa Alonso-Falleiros
Departamento de Engenharia Metalúrgica e de Materiais, Escola Politécnica, Universidade de São Paulo (USP).
Av. Prof. Mello Moraes n. 2463, cidade universitária, São Paulo, Brasil.
* wilmarcalderon100@gmail.com
Fecha Recepción: 2 de julio de 2014
Fecha Aceptación: 15 de enero de 2015
Este documento presenta los resultados de una investigación sobre la influencia del Mn en solución sólida sobre la resistencia a la corrosión por picadura de dos aceros inoxidables austeníticos, uno denominado 17Cr6Mn5Ni y un acero comercial UNS S304L utilizado como material de referencia. Fueron usadas soluciones electrolíticas de 0,6M NaCl en tres diferentes condiciones de concentración de oxígeno (solución desaireada, naturalmente aireada y aireada artificialmente). El desempeño de cada condición fue medido a través de ensayos de polarización potenciodinámica y mediante exámenes metalográficos. Se determinaron los potenciales de corrosión (Ecorr) y de picadura (Ep). La concentración de oxígeno en la solución electrolítica influenció el parámetro Ecorr, pero no el Ep.
El manganeso en solución sólida beneficia la absorción de iones Cl- en aceros inoxidables austeníticos, ejerciendo por tanto un efecto negativo en cuanto a resistencia a corrosión por picadura. A través de datos experimentales de energía libre de Gibbs de formación de compuestos (ΔG°) y de la teoría de absorción competitiva, fue propuesto un mecanismo para explicar este fenómeno.
Palabras clave: corrosión por picadura, manganeso, oxígeno, aceros inoxidables austeníticos.
steels: influence of the manganese addition in solid solution
In this research are shown the results about the study of the influence of manganese in solid solution on the pitting corrosión resistance of austenitic stainless steels, a steel is referred to as 17Cr6Mn5Ni and the UNS S304L steel as benchmarking material. Electrolytic solution containing 0.6M NaCl in three different oxygen concentration were used (aerated, non aerated and naturally aerated). The behavior of each condition was measured through potentiodynamic polarization tests and metallographic examinations. The values of corrosion potential (Ecorr) and pitting potential (Ep) were determined. The oxygen concentration of the electrolytic solution influenced the Ecorr but not the Ep parameter.
Manganese in solid solution benefits the Cl- ions absorption in austenitic stainless steels. Therefore, causes negative effect on pitting corrosion resistance. A mechanism was proposed through the standard Gibbs free energy of formation of compounds (ΔG°) data, and through the competitive absorption theory.
Keywords: pitting corrosion, manganese, oxygen, austenitic stainless steels.
austeníticos: influência da adição de manganês em solução solida
Este documento apresenta os resultados de uma pesquisa sobre a influencia do Mn em solução sólida sobre a resistência à corrosão por pite de aços inoxidáveis austeníticos, um denominado 17Cr6Mn5Ni e um aço comercial UNS S304L utilizado como material de referencia. Foram usadas soluções electrolíticas de 0,6M NaCl em três diferentes condições de concentração de oxigênio (solução desaerada, naturalmente aerada e aerada artificialmente). O desempenho de cada condição foi medido a través de testes de polarização potenciodinâmica e mediante exames metalográficos. Determinaram-se os potencias de corrosão (Ecorr) e de pite (Ep). A concentração de oxigênio na solução eletrolítica influenciou o parâmetro Ecorr, mas não o Ep.
O manganês em solução sólida beneficia a absorção de íons Cl- em aços inoxidáveis austeníticos, exercendo, portanto um efeito negativo quanto à resistência à corrosão por pite. Através de dados experimentais de energia livre de Gibbs de formação de compostos (ΔG°) e da teoria de absorção competitiva, foi proposto um mecanismo para explicar este fenômeno.
Palabras-chave: corrosão por pite, manganês, oxigênio, aços inoxidáveis austeníticos.
Cita: Calderón-Hernández JW, Braga Luz IB, Hincapie-Landino D, Alfonso-Falleiros N. Estudio de la resistencia a la corrosión por picadura de aceros inoxidables austeníticos: influencia de la adición de manganeso en solución sólida. rev.ion. 2015;28(1):63-72.
En los últimos 60 años se realizaron numerosas investigaciones con el objetivo de alcanzar mejores propiedades mecánicas combinadas con buena resistencia a corrosión. Esto llevó al diseño de materiales que en la actualidad son altamente comercializados, tales como los aceros inoxidables austeníticos (AIA) de la Serie 300 [1]. A pesar de que los AIA cumplen con las exigencias actuales del mercado, se sabe también que su microestructura austenítica depende del contenido de níquel, cuyo precio es altamente oscilante, desestabilizando en varias épocas el mercado mundial de los aceros inoxidables [2].
La escasez de níquel ocurrida durante la segunda guerra mundial (1939-1945), y de nuevo durante el conflicto en Corea (1950-1953), impulsó una considerable cantidad de investigaciones en Alemania y los Estados Unidos sobre sustitutos para el níquel en aceros inoxidables austeníticos. Desafortunadamente son pocos los elementos que sustituyen el níquel ampliando la zona austenítica en el diagrama del sistema hierro-cromo. Estos elementos son: carbono, nitrógeno, manganeso, cobre y cobalto. Ninguno de estos elementos en adición única es completamente satisfactorio. Por ejemplo, el carbono en cantidades necesarias para formar una estructura completamente austenítica tiene un efecto negativo sobre la ductilidad, además de afectar la resistencia contra corrosión intergranular, puesto que promueve la formación de carburos de tipo M23C6 (principalmente Cr23C6), estos carburos precipitan en los contornos de grano empobreciendo la matriz en Cr que es el elemento básico para la formación de la película protectora [3,4]; el nitrógeno no puede ser adicionado en cantidades suficientes para obtener la estructura deseada; el manganeso en cantidades por encima de 25%p en masa no forma una estructura completamente austenítica en aleaciones conteniendo cromo por encima de 15%p en masa; el cobre tiene un efecto negativo sobre la ductilidad en caliente y el cobalto sólo tiene un leve efecto y es bastante costoso [5].
Aceros inoxidables austeníticos donde parte del níquel es sustituido por manganeso y nitrógeno son conocidos como aceros de la Serie 200, la composición química del acero 17Cr6Mn5Ni encaja dentro de esta familia de aceros [1]. Los estudios realizados sobre resistencia contra corrosión de AIA de tipo 17Cr6Mn5Ni son pocos, la mayoría de la década del 70 o anteriores, además son estudios realizados con electrólitos ácidos (H2SO4). Estas soluciones no son adecuadas para estudiar corrosión por picadura sobre AIA; las soluciones ácidas son comúnmente utilizadas para estudiar corrosión generalizada y evaluar el desempeño de películas pasivas [6-10].
El efecto de la concentración de oxígeno sobre la resistencia a corrosión de AIA Cr-Ni conteniendo Mn también ha sido poco explorada. Por tanto, lo que se propone en este trabajo es medir el desempeño de dos aceros inoxidables austeníticos, uno denominado 17Cr6Mn5Ni y otro estandarizado UNS S304L (utilizado como referente), en soluciones 0,6M de NaCl y diferentes condiciones de aireación (solución desaireada, aireada naturalmente y aireada artificialmente).
Materiales
Para el desarrollo experimental fueron utilizadas placas laminadas en caliente, de acero inoxidable austenítico 17Cr6Mn5Ni y UNS S304L de 2,8 y 4mm de espesor respectivamente, la composición química se presenta en la Tabla 1.
Nótese en la Tabla 1, que ambos aceros poseen contenido similar de cromo, bajo contenido carbono, que evita corrosión intergranular y bajo contenido de azufre, para evitar la precipitación de sulfuros de manganeso (MnS) manteniendo el manganeso en solución sólida. La diferencia más importante entre los aceros estudiados está en el contenido de Ni y Mn.
Las muestras se prepararon cortando pequeños pedazos cuadrados de 10mm de lado, estos se pulieron gradualmente con papel abrasivo de SiC hasta llegar a una granulometría #600, seguidamente se embutieron en baquelita, teniendo en cuenta que el área expuesta fuera perpendicular al sentido de laminación (área expuesta: ~ 0,35cm2). En cada muestra se hizo un agujero roscado en la baquelita para acoplar una varilla metálica la cual permite el contacto eléctrico con el circuito del potenciostato. La Figura 1 muestra la configuración de la muestras y su acople con la celda electroquímica.
La caracterización microestructural se realizó con exámenes por medio de microscopia óptica (MO) y electrónica de barrido (MEB). Para revelar la microestructura del material, las muestras se prepararon metagráficamente utilizando 3 paños metalográficos con sus respectivas suspensiones de diamante (6μm, 3μm y 1μm), el material fue atacado electrolíticamente en solución de 10%p de ácido oxálico, aplicando un voltaje de 4V durante 60s.
Ensayos electroquímicos
Para los ensayos electroquímicos se utilizó una celda electroquímica tipo balón, con electrodo de referencia de Calomel Saturado (ECS) y como contra-electrodo un alambre de platino en forma de espiral, para mayor área de contacto con la solución electrolítica (Figura 1). La adquisición de datos se realizó a través de Potenciostato/ Galvanostato Princeton Applied Research (PAR) modelo 273A y software 352 SoftCorr III.
Como medio electrolítico se utilizaron soluciones con concentración 0,6M de NaCl en tres diferentes condiciones de aireación: solución desaireada inyectando nitrógeno gaseoso durante 1h para garantizar la estraccion de oxígeno, solución aireada naturalmente agitando mecanicamente durante 0,5h (usando un agitador magnético) y solución aireada inyectando oxígeno gaseoso a la solución durante una hora. En los procesos de inyección de nitrógeno y de oxígeno, el montaje era debidamente sellado para evitar el ingreso de oxígeno desde el ambiente (en el caso de las soluciones desaireadas), o garantizar la saturación (en el caso de las soluciones aireadas), en ambos casos se dejaba un orificio de salida de gas para evitar el exceso de presión al interior de la celda. Cuando el proceso de agitación mecánica o de inyección de gas (nitrógeno u oxígeno) terminaba, la muestra se dejaba durante 5 minutos inmersa sin registrar datos (con el objetivo de estabilizar el potencial de corrosión), a partir de ese momento se iniciaba la polarización desde una sobretensión catódica de 250mV con velocidad de barrido de 1mV/s; la polarización se interrumpía después de alcanzar el potencial de picadura (Ep) y densidad de corriente de 1E-3 A.cm-2. Para garantizar la reproducibilidad de los datos fueron realizados como mínimo 8 ensayos por cada condición.
La caracterización microestructural se realizó con ayuda de microscopio óptico OLYMPUS BX60M, microscopio electrónico de barrido PHILIPS XL30, difractómetro Multi-propósito PANalytical modelo X'Pert equipado con tubo de Rayos-X de Cu (condiciones de trabajo Kv=40, mA=40) y un ferritoscópio FISHER modelo MP3.
Caracterización microestructural
Las Figuras 2 y 3 muestras imágenes de microscopía electrónica de barrido (MEB) de los aceros 17Cr6Mn5Ni y UNS S304L, respectivamente.
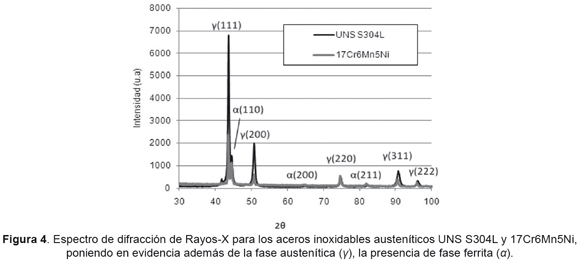
En ambos aceros se hace evidente la presencia de una segunda fase dispersa por la matriz. A través de difracción de Rayos-X fue constatada la presencia de una fase ferrítica (picos 110, 220, 211). La Figura 4 presenta los difractogramas realizados obtenidos de ambos aceros.
Análisis químicos realizados a través de espectroscopia de energía dispersiva (EDS), determinaron que se trataba de ferrita rica en cromo (24% Cr). Por medio de mediciones a través de ferritoscopio, se determinó el volumen de esta fase ferrítica, para ambos aceros fue similar, aproximadamente 3,5%v. Por tanto, los dos aceros tienen la misma cantidad de ferrita, lo que garantiza que ambos aceros sean similares en cuanto a su microestructura.
Ensayos de polarización
Las Figuras 5 y 6 muestran curvas de polarización potenciodinámicas representativas. Las curvas presentaron rangos de pasividad y potenciales de picadura bien definidos. Se observan en el rango de pasividad (poco antes de Ep) algunas oscilaciones de corriente, estas oscilaciones pueden ser atribuidas a la formación de picaduras inestables (picaduras que intentan iniciar pero no crecen debido a una rápida repasivación).
La Figura 7 presenta los resultados de potencial de picadura (Ep) obtenidos a partir de las curvas de polarización potenciodinámica en función de la concentración de oxígeno en la solución electrolítica.
Nótese en la Figura 7, que el acero UNS S304L presentó siempre mayor potencial de picadura que el acero 17Cr6Mn5Ni. Las bandas de error colocan el Ep del acero UNS S304L básicamente en la misma condición de resistencia a corrosión para las tres condiciones de aireación, se aprecia un leve aumento de Ep en el sentido creciente de la oxigenación más puede ser considerado despreciable. Por su lado, el acero 17Cr6Mn5Ni mostró un leve aumento en la condición aireada.
La Figura 8 presenta los valores promedio y desviación estándar obtenidos para el potencial de corrosión (Ecorr), la cual, teóricamente corresponde a la intersección de la curva catódica del oxígeno con la curva anódica del metal.
El parámetro Ecorr es más susceptible a las condiciones de aireación que el Ep; en el caso del acero 17Cr6Mn5Ni en las dos soluciones de mayor concentración de oxígeno los valores de Ecorr están muy cerca entre ellos, pero el valor promedio de Ecorr en la condición desaireada es considerablemente menor. Por su lado, el acero UNS S304L mostró aumento progresivo en el valor de Ecorr en la medida que el contenido de oxígeno aumentó.
Morfología de las picaduras. Después del levantamiento de las curvas de polarización, las muestras se examinaron en microscopio óptico, imágenes de la morfología de las picaduras son mostradas en la Figura 9.
Discusión de resultados
Comparando las imágenes de microscopía electrónica de barrido (Figuras 2 y 3), se puede apreciar la estructura mayoritariamente austenítica, con tamaño de grano similar para ambos aceros. También se observó la presencia de una segunda fase. Análisis de difracción de Rayos-X (XRD) (Figura 4) y de composición química utilizando la técnica de energía dispersiva de Rayos-X (EDS), determinaron que se trataba de un residual de ferrita-α rica en cromo (24% Cr), la cual, posiblemente precipitó durante el proceso termo-mecánico de laminación.
Teniendo en cuenta que existe precipitación de una segunda fase rica en cromo (ferrita), es lógico inferir que la matriz del acero en contacto con esos precipitados fue empobrecida en cromo; medidas a través de ferritoscopio determinaron contenidos similares para los dos materiales (alrededor de 3,5%v en volumen de ferrita).
Fueron estudiados dos aceros en tres ambientes electrolíticos (un total de 6 condiciones), para cada condición fueron realizados mínimo 8 ensayos de polarización potenciodinámica. Las Figuras 5 y 6 muestran ejemplos de curvas obtenidas durante la investigación; todas las curvas analizadas presentaron potencial de corrosión y de picadura bien definido, en general las corrientes de pasivación no mostraron alguna tendencia particular, en todos los casos, se presentaron corrientes bajas, correspondientes a estados de pasivación (en su mayoría densidades de corriente menores a 1E-5 A/cm2).
Los resultados son discutidos y apoyados en la literatura especializada. El PRE (Pitting Resistance Equivalent) es un número que se utiliza para estimar la tendencia a corrosión por picadura de aceros inoxidables austeníticos en medios salinos; han sido desarrolladas varias ecuaciones para determinar el PRE, en general involucrando tres de los principales elementos para resistencia a la corrosión por picadura: cromo, molibdeno y nitrógeno. La Tabla 2 presenta una recopilación de ecuaciones PRE encontradas en la literatura.
Las ecuaciones anteriores (Tabla 2) no consideran otros elementos presentes en los aceros inoxidables estudiados, tales como níquel y/o manganeso, los cuales existen en cantidades considerables. Por otro lado, Speidel [13] presenta una ecuación denominada MARC (Measure of Alloying for Resistance to Corrosion) para estimar la tendencia a corrosión por picadura de aceros inoxidables austeníticos en soluciones electrolíticas con iones de Cl-; esta ecuación, además de involucrar cromo, molibdeno y nitrógeno, también tiene en cuenta carbono, manganeso y níquel, siendo esta ecuación más conveniente en la presente investigación.
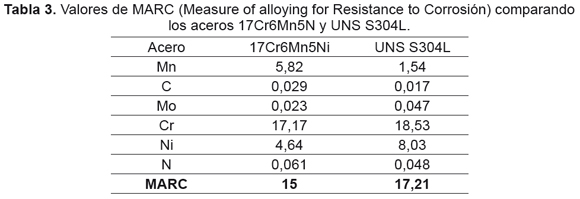
Obsérvese en la ecuación MARC, que el manganeso tiene coeficiente negativo, lo que permite inferir inicialmente que ejerce un efecto negativo sobre la resistencia a la corrosión por picadura; las investigaciones hasta la década de los 70's fueron realizadas principalmente en medios ácidos, mostrando en general que la capacidad de pasivación disminuía con el aumento de Mn [6-10]. La Tabla 3 muestra los resultados aplicando la Ecuación MARC para los aceros estudiados.
Según la ecuación MARC, la resistencia a la corrosión por picadura del acero UNS S304L es superior a la del acero 17Cr6Mn5Ni (17,21 y 15, respectivamente). De acuerdo con esta expresión, eso se debe al efecto negativo del manganeso, el cual se encuentra en mayor cantidad en el acero 17Cr6Mn5Ni (5,8% Mn), el níquel también tienen coeficiente negativo, encontrándose en mayor cantidad en el acero UNS S304L (4,6% Ni), pero analizando los coeficientes en la ecuación MARC, el coeficiente de daño generado por este elemento es menor (0,5% Mn contra 0,25% Ni). Es bien conocido que el manganeso ejerce un efecto negativo sobre la resistencia a corrosión localizada debido a la formación de sulfuros de manganeso (MnS), los cuales actúan como sitios altamente preferenciales para la nucleación de picaduras [14-18]. Se reitera que en este trabajo se investigó el efecto del manganeso en solución sólida, no en la forma de precipitado, pues estos aceros fueron producidos mediante procesos altamente tecnológicos, que disminuyen el contenido de azufre al mínimo (10 y 20ppm, Tabla 1), evitando con esto, la precipitación de MnS.
De acuerdo con las primeras investigaciones [6- 10], el aumento de manganeso en solución sólida en aceros inoxidables austeníticos ejerce un efecto negativo sobre la capacidad de pasivación, lo anterior es otra evidencia, de que el aumento de manganeso puede afectar la resistencia a la corrosión por picadura. Estos autores [6-10] trabajaron con soluciones ácidas (ácidos en altas concentración son adecuados para estudiar corrosión generalizada, no para corrosión por picadura). Kyung y Kyuk [19] investigaron el efecto del manganeso sobre la corrosión localizada de tres aleaciones Fe-18Cr-xMn (x: 0, 6, 12) en soluciones salinas (0,1M NaCl), a través de ensayos de polarización potenciodinámica y espectroscopia de impedancia electroquímica, encontrando que las propiedades de la película pasiva eran debilitadas con las adiciones de manganeso. En ninguno de los trabajos anteriormente citados fueron propuestos mecanismos explicando estos fenómenos.
El mecanismo propuesto en esta investigación para explicar el efecto negativo producido por el manganeso, está basado en la teoría de la absorción competitiva entre iones de Cl- y los átomos de oxígeno adyacentes a la superficie de la película pasiva [20]. Los iones Cl- son perjudiciales debido a que ingresan en la película pasiva e incentivan el desprendimiento de cationes metálicos degradando el material de manera localizada [21], por tanto, se propone que para el acero 17Cr6Mn5Ni, los iones Cl- son absorbidos preferencialmente para ocupar sitios activos de la película pasiva.
Este comportamiento puede ser sustentado termodinámicamente mediante la variación de la energía libre de Gibbs estándar para la formación de compuestos (ΔG°). No se sabe con exactitud cuáles son los compuestos formados en una película pasiva, ya que ésta es del orden de unas cuantas capas atómicas, pero utilizando valores de ΔG° de compuestos conocidos [22], se puede estimar (cualitativamente) la afinidad entre Cl y algunos de los elementos que componen los aceros estudiados (Mn, Ni e Cu), la Tabla 4 muestra el valor de ΔG° para tres compuestos.
Los datos de la Tabla 4 exponen que existe mayor potencial termodinámico para la formación de cloruro de manganeso (MnCl2), que para la formación de cloruro de níquel (NiCl2) o cloruro de cobre (CuCl2). Lo anterior puede explicar por qué a pesar de que ambos aceros son básicamente iguales en cuanto a microestructura y al contenido de cromo, el acero 17Cr6Mn5Ni presenta menos resistencia a la corrosión por picadura.
El aumento en el contenido de manganeso en solución sólida produce dos efectos negativos para la resistencia a la corrosión por picadura, los cuales pueden ser explicados a través de la teoría de la absorción competitiva. El primer efecto negativo es que gracias a su afinidad con el cloro, el manganeso aumenta la probabilidad de que los iones de Cl- (contenidos en la solución electrolítica y cercano a la superficie del acero) sean absorbidos por la película pasiva, pasando a formar parte de su estructura de capas atómicas, y posteriormente penetrando hasta alcanzar la interface metal/película; el segundo efecto negativo es una consecuencia del primero, más sitios activos siendo ocupados por Cl- generan como efecto secundario menos sitios para la absorción de oxígeno en la película pasiva.
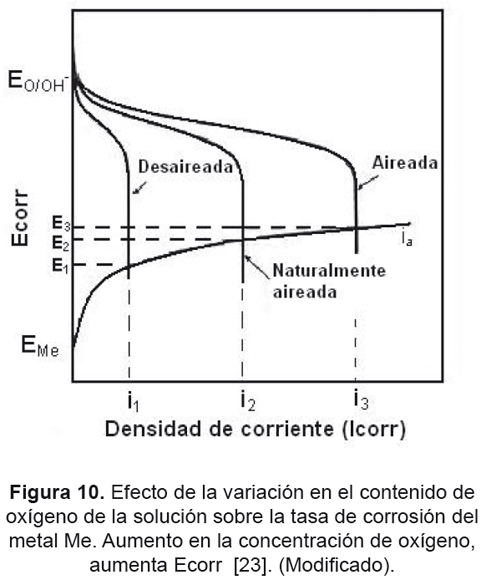
El potencial de corrosión (Ecorr) (Figura 8), resultó ser más susceptible a las diferentes condiciones de aireación que el Ep (Figura 7). En el caso del acero 17Cr6Mn5Ni el valor promedio de Ecorr en la condición desaireada es considerablemente menor que las otras dos soluciones. Por su lado, el acero UNS S304L mostró aumento progresivo en el valor de Ecorr con el aumento en la concentración de oxígeno; esto se debe a que Ecorr es un parámetro que representa le intersección de la curva catódica del oxígeno (regida por la reacción O2+2H2O+4e→4OH-) con la curva anódica del metal (regida por la reacción Me→ Mez++ze), por tal motivo, una modificación en el contenido de oxígeno en la solución electrolítica se verá reflejada también en el Ecorr, la Figura 10 representa este fenómeno.
Esta dependencia se debe probablemente a dos situaciones, por un lado, el aumento de oxígeno mejora la calidad de la película pasiva, pues su materia prima es cromo y oxígeno, por otro lado, la velocidad de la reacción O2+2H2O+4e→4OHposiblemente se altera con los cambios en la concentración de oxígeno.
A pesar de que el aumento en la concentración de oxígeno mejora la calidad de la película pasiva, este hecho no se vio reflejado en el potencial de picadura, debido posiblemente a que la solución 0,6M de NaCl es un electrolito bastante agresivo y no permitió diferenciar el desempeño de la película pasiva formada para cada condición de aireación.
El acero UNS S304L posee mayor resistencia a la corrosión por picadura que el acero 17Cr6Mn5Ni en solución conteniendo 0,6M de NaCl inclusive para diferentes condiciones de aireación.
El manganeso en solución sólida ejerce un efecto negativo en la resistencia a corrosión por picadura de aceros inoxidables austeníticos.
La concentración de oxígeno en la solución electrolítica influencia el potencial de corrosión (Ecorr), puesto que Ecorr representa la intersección entre la reacción catódica del oxígeno (O2+2H2O+4e→4OH-) y la reacción anódica del metal (Me → Mez++ze). Para el caso del potencial de picadura (Ep) no necesariamente pues a pesar de que el aumento en la concentración de oxígeno mejora la calidad de la película pasiva, existen otros factores que también intervienen y pueden ser dominantes.
[1] Sedriks AJ. Corrosion of Stainless Steel. New York: John Wiley & Sons Inc; 1996. [ Links ]
[2] London metal Exchange, LME Steel Billet price graph. Disponible en: http://www.lme.com/steel/steel_price_graphs.asp. Acceso el 15 de Agosto de 2012. [ Links ]
[3] Pecker D, Bernstein IM. Structure and Constitution of Wrought Austenitic Stainless Steels. En: Handbook of stainless steels. USA: McGraw-Hill; 1977. p. 35 [ Links ]
[4] Jian Xu, Xinqiang Wu, En-Hou Han. Acoustic emission response of sensitized 304 stainless steel during intergranular corrosion and stress corrosion cracking. Corrosion Science. 73;2013:262-73. [ Links ]
[5] Mc Gannon HE. The making, shaping and treating of steel. Pittsburg: United States Steel Corporation; 1964. [ Links ]
[6] Murgulescu JG, Radovici ZO. Uber die anodishe Passiviering einiger Chom-Nickel- Mangan-Stähle bei konstantem strom. Phys. Chem. 1960:214-88. [ Links ]
[7] Condylis A, Bayon F, Desestret A. Aciers inoxydables austénitiques au chrome-manganèse-azote. Revue de Metallurgie.1967:67. [ Links ]
[8] Shams AM, Madran MM, Khalil SE. Corrosion behavior of Manganese-Containig stainless steel. I. Galvanostatic Measurement in H2SO4 Soplution. Werks.u.korros. 1973;24:576. [ Links ]
[9] Lunarska EZ, Szklarska-Smialowska, Janik- Czachor M. Susceptibility of Cr-Ni-Mn Stainless steel to Pitting In Choride Solution. Corrosion. 1975;31(7):231. [ Links ]
[10] Knyazheva VM, Vedeneesa MA, Esseldin- Halil S, Kolotyrkin YA. Zashchita Metallov. Vol. 1. 1965: 465. [ Links ]
[11] Wenming Tian, Nan Du, Songmei Li, Sibing Chen, Qunying Wu. Metastable pitting corrosion of 304 stainless steel in 3.5% NaCl solution. Corrosion Science. 2014;85:372-9. [ Links ]
[12] Alfonsson E, Qvafort R. Investigation of the applicability of some PRE expressions for austenitic stainless steels. Avesta Corrosion Management. 1992;1:1-6. [ Links ]
[13] Speidel MO. Nitrogen Containig Austenitic Stainless steel.Mat-wiss. U. Werkstoiftech. 2006;37(10):877. [ Links ]
[14] Mitrovic-Scepanovic V, Brigman RJ. Effect of manganese on pitting properties of type 301 stainless steel. Corrosion. 1996;52(1):23-7. [ Links ]
[15] Park JO, Suter T, Bohni H. Role of manganese sulfide inclusions on pit initiation of super austenitic stainless steels. Corrosion. 2003;59(1):59-67. [ Links ]
[16] Eklund GS. Initiation of pitting at sulfide inclusions in stainless steel. Corrosion.1974;121(4):467-73. [ Links ]
[17] Szklarska-Smialowska Z. Influence of sulfide inclusions of the pitting corrosion of steels. Corrosion. 1972;28(10):388-96. [ Links ]
[18] Dowling NJE, Duret-Thual C, Auclair G, Audouard JP, Combrade P. Effect of complex inclusions on pit initiation in 18% chromium-8% nickel stainless steel types 303, 304, and 321. Corrosion. 1995;51(5):343-55. [ Links ]
[19] Kyung Jin Park, Hyuk Sang Kwon. Effects of Mn on the localized corrosion behavior of Fe-18Cr alloys. Electrochimica Acta. 2010;55:3421-7. [ Links ]
[20] Szklarska-Smialowska. Pitting and crevice corrosion. NACE International. HOUSTON, TEXAS. 2005: 559. [ Links ]
[21] Fontana MG. Corrosion Engineering. 3. Ed. New York, McGraw-Hill; 1987. [ Links ]
[22] Weast R. Handbook of chemistry and physics 1st student edition. Florida. 1988. [ Links ]
[23] Wolynec S. Técnicas eletroquímicas em Corrosão. Escola Politécnica da Universidade de São Paulo. São Paulo. 2003. [ Links ]