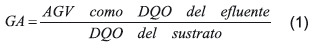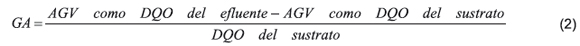Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista ION
Print version ISSN 0120-100X
Rev. ion vol.29 no.1 Bucaramanga Jan./June 2016
https://doi.org/10.18273/revion.v29n1-2016006
DOI: http://dx.doi.org/10.18273/revion.v29n1-2016006
de AGV de melaza de la industria azucarera
como valorización de este subproducto
María Angélica Palomino2; María Fernanda Ortegón2; Tatiana Rojas Betancourt1; Julián Martínez1; Juan
Valderrama1; Rafael Barragán2; Aníbal Pérez1; Héctor Luna Wandurraga1*
1 Facultad de Ingeniería Ambiental. Universidad Antonio Nariño. Carrera 3 Este No 47 A- 15, Bogotá, Colombia.
*hectorlunaw@hotmail.com
2 Facultad de Ingeniería Ambiental. Universidad Santo Tomás. Carrera 9 No 72 - 90, Bogotá, Colombia.
Fecha Recepción: 22 de noviembre de 2015
Fecha Aceptación: 5 de enero de 2016
Se evaluó el potencial acidogénico de la melaza de la industria azucarera en 4 diferentes OLR (6,02±4,33; 13,96±7,11; 15,81±4,83; 26,94±13,27kgDQO/m3.d) en un reactor de flujo ascendente, con lodo granular. El sistema no contó con control de pH e inhibición de la fase metanogénica. El reactor operó en continuo durante 148 días. Para evaluar el potencial acidogénico se utilizó el grado de acidificación neto (GAn). Los resultados mostraron que durante las tres primeras OLR el %GAn (29,46 ± 13,01; 20,23 ± 13,67; 24,63 ± 19,49) se mantuvo sin diferencias significativas, pero para la mayor OLR el %GAn disminuyó a la tercera parte (10,21 ± 7,14), mientras la concentración de AGV fue la mayor para esta fase (2644,89mgDQO/L), además se avaluó el balance de DQO para cada una de las fases, donde el % de AGV en el efluente representó el porcentaje orgánico fermentable rápidamente en el efluente, estos valores indican que con una recirculación interna se podría mejorar el %GAn u obtener otra serie de productos de base biológica para el aprovechamiento de este residuo. En este artículo se utilizó un reactor de flujo ascendente como alternativa a los estudiados (CSRT y batch) presentando diferentes resultados.
Palabras clave: digestión anaerobia, grado de acidificación neto, ácidos grasos volátiles, biorefinerias, melaza de caña de azúcar.
sugar cane molasses as valorization of this by-product
The acidogenic potential of molasses from the sugar industry was evaluated using 4 different Organic Loading Rates (OLR) (6.02±4.33; 13.96±7.11; 15.81±4.83; 26.94±13.27kgCOD/m3.d) in an upflow reactor with granular sludge. No pH control or methanogenesis inhibitors were used. The reactor was continuously operated during 148 days. The acidogenic potential was evaluated based on the net degree of acidification (DAn). For the first 3 OLR, %DAn did not show any significant variability (29.46 ± 13.01; 20.23 ± 13.67; 24.63 ± 19.49), but for the highest OLR, %DAn dropped to a third of its initial value (10.21 ± 7.14), although the volatile fatty acid (VFA) concentration was the highest (2644.89mgCOD/L). Also, a COD balance was done for each of the 4 OLR. The VFA percentage in the effluent was assumed to be the most easily fermentable organic fraction in the effluent. The obtained results suggest that an internal recirculation of the effluent could help to increase the %DAn so the produced VFA can be used as substrate for the obtention of other valuable bioproducts. This article describes an upflow reactor is used as an alternative to those studied (CSRT and batch) presenting different results.
Keywords: anaerobic digestion, net degree of acidification, volatile fatty acids, biorefineries, sugarcane molasses.
de VFA de melaço da industria de cana de açúcar
como valorização deste subproduto
O potencial acidogênica de melaço da indústria de cana de açucar foi avaliado em 4 diferentes OLR (13,96 ± 7,11; 15,81 ± 4,83; 6,02 ± 4,33; 26,94 ± 13,27kg DQO/m3.d) num reator de fluxo ascendente com lodo granular. O sistema não tinha controle de pH e também nao inibição da fase metanogênica. O reactor foi operado continuamente durante 148 dias. O grau de acidificação (GaN) foi usado para avaliar o potencial acidogênica. Os resultados mostraram que durante os três primeiros OLR o %GAn (29,46 ± 13,01, 20,23 ± 13,67, 24,63 ± 19,49) permaneceu sem diferenças significativas, mas para a maior OLR o %GAn caiu para terceira parte (10,21 ± 7,14), mas a concentração de AGV foi maior para esta fase (2644,89mgDQO/L), alem disso o balance para a DQO foi avaliado para cada uma das fases, onde o % AGV no efluente foi o percentagem orgânico rapidamente fermentável no efluente, istos valores indicam que a recirculação interna poderia melhorar melhorar o %GAn ou obter outro conjunto de produtos de base biológica para a utilização destes resíduos. Este artigo descreve um reactor de fluxo ascendente é utilizado como uma alternativa aos estudados (CSRT e batch) apresentando diferentes resultados.
Palabras-chave: digestão anaeróbia, grau de acidificação, ácidos graxos voláteis, biorrefinarias, melaço de cana.
Cita: Palomino MA, Ortegón MF, Rojas Betancourt T, Martínez J, Valderrama J, Barragán R, Pérez A, Luna Wandurraga H. Evaluación del potencial acidogénico para producción de AGV de melaza de la industria azucarera como valorización de este subproducto. rev.ion. 2016;29(1):71-80.
La digestión anaerobia se ha aplicado a través de los años para el tratamiento de una variedad de sustratos orgánicos. Este proceso ha mostrado proveer muchas ventajas sobre otros sistemas de tratamiento como los aerobios, dado que permiten disminuir los costos operacionales en los reactores, disminuyen la producción de lodos, necesitan de bajos requerimientos energéticos y soportan altas cargas orgánicas de diseño. Este tipo de sistema ha ofrecido igualmente soluciones costo-efectivas para la transformación de sustratos complejos en productos estables que pueden tener un valor a nivel industrial (biogás) [1].
Una de las etapas de la digestión anaerobia poco explorada es la acidogénesis, la cual consiste en la conversión de compuestos complejos, como los aminoácidos, glucosa y ácidos grasos de cadena larga, por medio de la fermentación, en ácidos grasos volátiles (C2-C5) [2]. Los sistemas de fermentación de sustratos complejos que existen actualmente para la producción de ácidos grasos volátiles (AGV) involucran diferentes tipos de microorganismos y rutas bioquímicas [3]. En años recientes, la producción de los diferentes AGV (acético, butírico, propíonico, valérico) se ha venido estudiando por sus aplicaciones innovadoras, ya que ha sido considerada como la principal plataforma para el desarrollo de las biorefinerías debido a que son la materia prima para la obtención de biocombustibles, biomateriales y bioquímicos [1]. Las biorefinerías combinan la tecnología necesaria para convertir materias primas renovables en productos intermediarios y finales (biomateriales, biocombustibles y bioquímicos) [4]. A escala industrial, el ácido acético es ampliamente utilizado en la síntesis de una variedad de productos, como el acetato de vinilo, el cual hace parte de la producción de textiles, PVC, aditivos de cemento, pegamento blanco, bolsas de papel, entre otros [3]. Las principales aplicaciones industriales del ácido butírico son la manufactura del plástico acetato-butirato y la producción de un tipo de polímero biodegradable, que recientemente ha venido siendo explotado y es conocido como polihidroxibutirato (PHB) [4]. Actualmente, la atención del ácido butírico se ha enfocado en la síntesis de biocombustibles debido a que se puede convertir en butanol a través de transformaciones químicas y biológicas [1], además su densidad energética corresponde a 29,2MJ/L, valor similar al que registra la gasolina de 32MJ/L [6]. Otras aplicaciones de los AGV incluyen su conversión térmica a cetonas y su subsecuente hidrogenación a alcohol que puede ser utilizado como combustible [3], o su uso como donador de electrones en celdas de combustible microbianas [4]. Las diferentes aplicaciones de los AGV hacen que el proceso de fermentación acidogénica tome importancia y sea campo de estudio. Este proceso ha permitido generar un valor agregado a una variedad de residuos (industriales y agrícolas) al generar productos de alto valor e incursionar en el mercado.
Varios estudios han determinado que es posible producir AGV a partir de una variedad de residuos agro-industriales [4], residuos de comida [5-7], aguas residuales de aceite de oliva [8,9], vinazas de la industria tequilera [10] y aguas residuales de gaseosas [11]. Para un país como Colombia, donde la actividad agrícola es uno de los principales motores en la economía y al mismo tiempo genera diferentes tipos de residuos sólidos y líquidos, la búsqueda de alternativas que permitan tratar esos residuos para producir materiales o productos de alto valor es una prioridad [12].
La producción de caña de azúcar es una de las actividades agroindustriales más tradicionales de Colombia. En el departamento del Cauca, los cultivos superan las 225.560 hectáreas y se producen más de 14 toneladas de azúcar por hectárea al año [13]. En el año 2014 el consumo nacional aparente de azúcar (ventas de los ingenios nacionales más las importaciones de azúcar) en Colombia fue de 1,73 millones de toneladas [16]. Adicionalmente se exportaron 796 mil toneladas de azúcar especialmente a Chile, Perú, Estados Unidos, Haití, Trinidad y Tobago, Ecuador y Jamaica [16]. La industria azucarera en la producción de azúcar y alcohol se caracteriza por generar grandes cantidades de residuos y subproductos en su transformación, se estima que por cada tonelada cosechada se producen 800 litros de vinaza, 330kg de bagazo y de 30-50kg de cachaza [12]. La melaza es un subproducto (alto contenido de azúcares: 62% de sacarosa y 38% de fructosa) [14] que actualmente se aprovecha en la producción de alcohol y como alimento para animales. La producción constante de la industria azucarera requiere de otros procesos que aprovechen sus subproductos y residuos como la melaza con el objetivo de valorizarlos. Una alternativa puede ser la fermentación acidogénica, la cual permite producir AGV como materia prima para la obtención de diferentes productos de biorefinería como los polihidroxialcanoatos (PHA), biocombustible, acetato de vinilo, entre otros; aumentando el beneficio económico adicional al actual en la industria y contribuyendo a la disminución de los impactos ambientales.
Lo anterior muestra que la digestión anaerobia puede ser una buena alternativa para el aprovechamiento de la melaza como subproducto de la industria azucarera. Por lo tanto el objetivo principal de este artículo fue, evaluar el potencial de acidificación para la producción de AGV de la melaza residual de la industria azucarera, como principal plataforma de las biorefinerías ya que a partir de estos ácidos se pueden sintetizar una variedad de bioquímicos y biomateriales para la industria. Esto se realizó en un reactor de flujo ascendente operado bajo condiciones anaerobias.
Reactor anaerobio de flujo ascendente
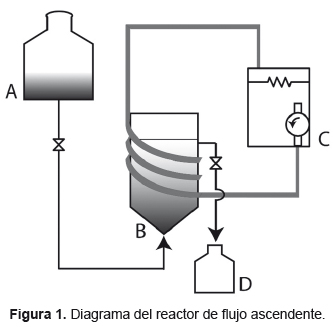
Para la operación de este trabajo, se realizó el montaje de un reactor anaerobio de configuración de flujo ascendente de lecho fijo con cultivo microbiano mixto como se muestra en la Figura 1B, operado en continuo, con un volumen efectivo de 2L y de 2,5L nominal, de material de polietileno. El reactor contó con una chaqueta de calentamiento de recirculación de agua. El sistema de calentamiento (Figura 1C) consistió en un tanque con agua, una resistencia y una bomba sumergible para la recirculación del agua. El sistema de alimentación (Figura 1A) del reactor fue por gravedad con un sistema de goteo. El efluente fue almacenado en un tanque (Figura 1D) donde se realizó la medición del caudal. La operación se realizó sin ninguna fuente externa de inhibición de la metanogénesis y sin control de pH.
El inóculo utilizado consistió de lodo granular anaerobio proveniente de una planta de tratamiento de aguas residuales de la industria láctea de un reactor UASB. La biomasa fue almacenada bajo condiciones anaerobias a 4°C hasta el inicio de los experimentos. El lodo inoculado inicialmente en el reactor fue de 300mL/L de sólidos sedimentables, equivalente al 30% del volumen efectivo.
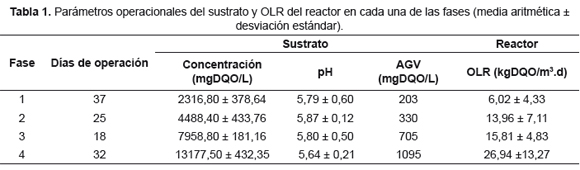
El agua sintética utilizada en esta evaluación, fue preparada por dilución de melaza comercial con agua potable para simular la melaza de la industria azucarera. La operación de los reactores se realizó en cuatro fases continuas correspondientes a cada una de las concentraciones de DQO del sustrato preparado, con el objetivo de aumentar la carga orgánica aplicada (OLR) hasta alcanzar una concentración de 13000mgDQO/L. En la Tabla 1 se muestra la OLR del reactor y los parámetros operacionales del sustrato, la concentración de DQO, pH y AGV correspondientes a cada una de las fases en los días de operación medidos inmediatamente después de realizar cada una de las diluciones. Las fases 1, 2, 3 y 4 corresponden a concentraciones en el sustrato alrededor de los 2000, 4000, 8000 y 13000mgDQO/L respectivamente, las cuales presentaron una OLR promedio de 6,02kgDQO/m3.d en la fase 1, 13,96kgDQO/m3.d en la fase 2, 15,81kgDQO/m3.d en la fase 3 y 26,94kgDQO/m3.d en la fase 4. Las concentraciones de los nutrientes fueron adicionadas al agua sintética de acuerdo con acuerdo con Zehnder et al. [15].
Métodos analíticos
Se realizaron dos tipos de muestreo en el reactor acidogénico: frecuente y regular. Los muestreos frecuentes se realizaron diariamente y correspondieron a la medición de los parámetros de pH, temperatura y caudal. Los muestreos regulares se realizaron cada 3 o 2 días y se midió la concentración de los AGV por medio de la técnica de titulación y la demanda química de oxígeno (DQO) por reflujo cerrado. En la Tabla 2 se muestran los parámetros medidos en el reactor dependiendo del tipo de muestreo y los métodos empleados.
Cálculos
El grado de acidificación (GA) fue el principal parámetro usado para la evaluación del potencial de acidificación [1], está definido por la Ecuación 1:
Debido a la naturaleza ácida del sustrato fue necesario corregir este parámetro por el grado de acidificación neto (GAn), el cual tiene en cuenta la concentración de AGV del sustrato, este parámetro se calculó por medio de la Ecuación 2:
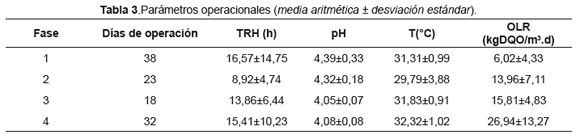
La Tabla 3 muestra los principales parámetros de operación del reactor anaerobio de flujo ascendente para cada fase. La variación del tiempo de retención hidráulico (TRH) entre cada una de las fases fue debido al difícil control del caudal, debido a que se usó un sistema de alimentación por goteo. Por lo tanto esta variación también fue reflejada en la variación de la OLR. El pH se mantuvo sin diferencias significativas entre las fases 1 y 2 y las fases 2 y 3, pero presentó una disminución significativa en las fases 3 y 4 comparados con las fases 1 y 2, lo cual se debe al aumento significativo de la OLR. La temperatura no presentó diferencias significativas entre las fases de la operación del reactor anaerobio de flujo ascendente.
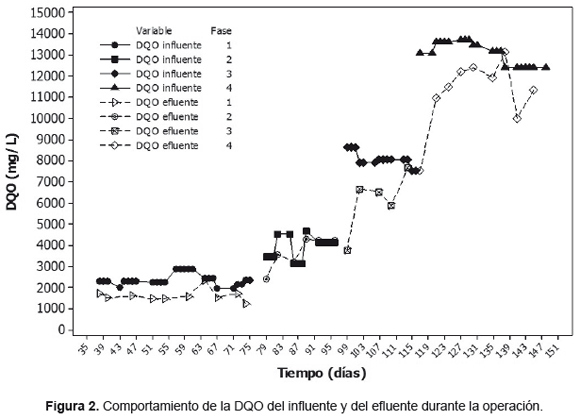
La Figura 2, muestra el comportamiento de la DQO del influente y del efluente durante la operación del reactor anaerobio de flujo ascendente. La Figura 2 comienza desde el día 38, porque durante los 37 días iniciales, el reactor se aclimató con el mismo sustrato pero con una concentración de DQO de 1000mg/L, con el objetivo que los microorganismos se adaptaran al sustrato. En esta figura también se muestra el comportamiento de la operación de cada fase al aumentar la concentración inicial de DQO de la melaza, la cual fue usada para aumentar la OLR, llevando a una disminución significativa del pH en las fases 3 y 4. La diferencia entre la DQO del sustrato y la DQO del efluente permitió evaluar la DQO que fue removida, como más adelante se muestra en el balance de DQO para cada fase.
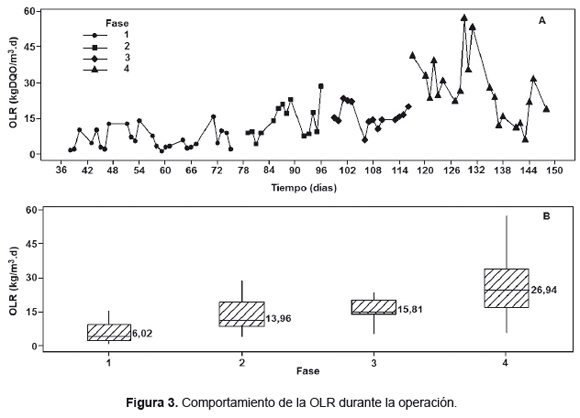
El aumento de la OLR durante la operación se muestra en la Figura 3A, y los valores de la media aritmética se muestran en la Figura 3B, lo cual permite establecer que entre las fases 2 y 3 no existieron diferencias significativas. Por lo tanto para el análisis de los datos se consideró que se obtuvieron 3 cambios de OLR significativos, siendo la menor OLR de operación la fase 1, OLR intermedia fase 2 y 3 y OLR mayor la fase 4.
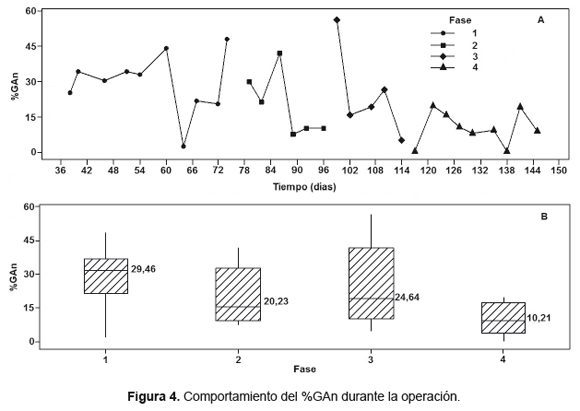
El porcentaje del grado de acidificación neto para cada una de las fases de operación se muestra en la Figura 4, el mayor porcentaje de acidificación se obtuvo en la fase 1 con una media aritmética de 29,46% y el menor en la fase 4 con una media aritmética de 10,21%. Al comparar las Figuras 3 y 4 es posible establecer que el grado de acidificación se logra mantener sin diferencias significativas entre las fases 1, 2 y 3 ante el aumento de la OLR, pero en la fase 4 cae a un valor de 10,21%, casi la tercera parte que la fase 1. Esto puede ser debido a la alta concentración de DQO (13000mg/L) y al alto contenido de AGV en el influente (1497mgDQO/L) que pueden inhibir los microorganismos. En este artículo se deseaba conocer los rangos máximos de OLR de trabajo utilizando la melaza producida en la industria azucarera como sustrato y bajo las condiciones de operación mencionadas anteriormente. Los valores del grado de acidificación obtenidos en las tres primeras fases (29,46%, 20,23% y 24,64), son valores que se pueden considerar de un buen rendimiento acidogénico para este sustrato, teniendo en cuenta que en este estudio no se tuvo control de pH e inhibición de la metanogénesis. Algunos autores como Silva et al. [1] también han estudiado la melaza como sustrato de acidificación, obteniendo un grado de acidificación neto de 37,3±1,2 con una DQO inicial de 8101±60mg/L en reactores batch a 37°C con control de pH e inhibiendo la metanogénesis y una producción de AGV neto en el efluente de 3110±124mgAGV(DQO)/L. Igualmente en el estudio de Albuquerque et al. [14] donde trabajaron con reactores CSTR con control de pH (5, 6, 7), produciendo 8329mgAGV(DQO)/L en el efluente con una OLR de 26,9 y un grado de acidificación del 77% (este valor no tiene en cuenta los AGV del influente).
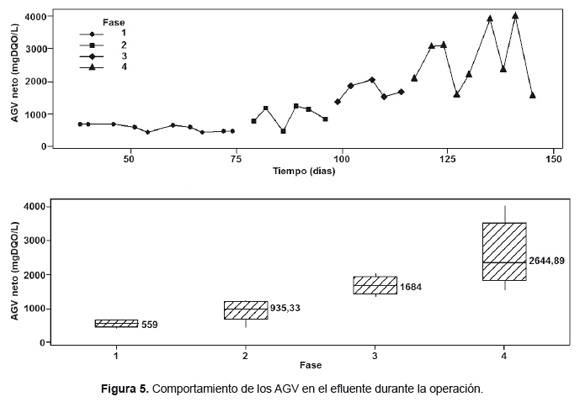
La producción de AGV netos en el efluente para este estudio se presenta en la Figura 5, lo cual muestra el incremento en la producción de AGV para cada una de las fases de operación y aumentan con el aumento de la OLR. Estos resultados también pueden ser comparados por los obtenidos por Silva et al. [1] en un reactor Batch con una DQO inicial de 8101±60mg/L y llegaron a una producción de AGV netos de 3110±124mgDQO/L, en condiciones similares en este estudio corresponde a la fase 3 la cual produjo 1684mgAGV(DQO)/L netos. Condiciones similares a la fase 4 fueron encontradas por Albuquerque et al. [14] en reactores CSTR donde produjeron 83110±124mgAGV(DQO)/L, con una OLR de 26,9kg/m3.d, teniendo en cuenta que el valor de AGV no es neto, en este estudio la fase 4 produjo 2644,89mgAGV(DQO)/L neto.
Al comparar los estudios mencionados con dilución de melaza como sustrato, se observó que se obtuvieron diferentes resultados con condiciones de operación similares pero usando diferentes configuraciones de reactor. En el estudio realizado por Silva et al. [1] se trabajó con un reactor Batch, en el estudio realizado por Albuquerque et al. [14] se emplearon reactores CSTR y en este estudio con un reactor de flujo ascendente, por lo tanto esta puede ser una variable de interés para próximos estudios. Además en los otros trabajos se realizó control de pH e inhibición de la metanogénesis mientras que en este estudio el objetivo de la producción de AGV era sin control de pH y sin inhibición de la metanogénesis.
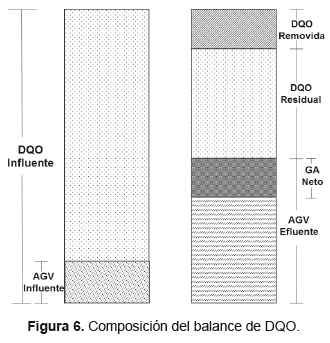
La Figura 6, muestra la composición de la DQO bajo la cual se realizó el balance de materia para cada una de las fases. La DQO influente contiene los AGV expresados en términos de DQO y para el efluente se determinó la DQO (en el efluente) y los AGV (en el efluente), con estos valores se determinó la DQO removida como la diferencia entre la DQO del efluente con la del influente, el grado de acidificación neto por la Ecuación 2 y por diferencia se obtuvo la DQO residual.
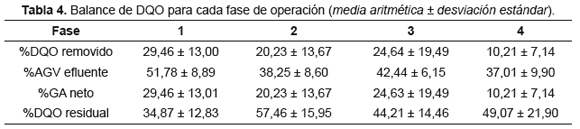
La Tabla 4 muestra los resultados del balance de materia de la DQO para cada una de las fases de operación. El % de AGV efluente representa el porcentaje orgánico fermentable rápidamente en el efluente. Estos valores muestran que una posible opción para mejorar el porcentaje del grado acidificación puede ser la recirculación interna del efluente. También que si se pudiera acoplar a una segunda fase de metanogénesis un alto porcentaje de la DQO (%AGV efluente), podría ser convertido fácilmente a metano. Una de las ventajas de tratar la melaza para la producción de AGV a altas OLR, sin control de pH e inhibición de la fase de metanogénesis, es el ahorro de agua para dilución de la melaza a tratar. Por lo tanto esta puede ser una alternativa para el aprovechamiento de este residuo en la industria azucarera.
El mayor porcentaje de GAn (29,46 ± 13,01%) se presentó en la fase 1 correspondiente a 651,62±110,58mgAGV(DQO)/L con una OLR de 6,02 ± 4,33kgDQO/m3.d. Al relacionar la Tabla 4 con la OLR que se presenta en cada una de las fases se puede observar que el aumento de la OLR es inversamente proporcional a la producción de AGV.
Este artículo muestra a la fermentación acidogénica como una alternativa para el aprovechamiento de la melaza proveniente de los residuos de la industria azucarera, para convertirla en AGV como producto de base biológica. Usando el caldo mixto de AGV producido, para la síntesis de bioproductos (biomateriales, biocombustibles y bioquímicos) como los PHA o PHB. Los resultados del porcentaje del grado de acidificación neto para cada una de las fases (29,46 ± 13,01; 20,23 ± 13,67; 24,63 ± 19,49; 10,21 ± 7,14) muestran que es posible trabajar hasta una OLR de 15,81±4,83 (fase 3) sin necesidad de controlar el pH y de inhibir la metanogénesis, con una OLR superior a 26,94±13,27 (fase 4), el grado de acidificación neto disminuye de forma significativa, pero igualmente la producción de AGV en esta fase fue la máxima (2644,89mgDQO/L). En este artículo se utilizó un reactor de flujo ascendente como alternativa a los estudiados (CSRT y batch) presentando diferentes resultados.
[1] Silva FC, Serafim LS, Nadáis H, Arroja L, Cápela I. Acidogenic fermentation towards valorisation of organic waste streams into volatile fatty acids. Chem Biochem Eng Q. 2013;11(4):467-76. [ Links ]
[2] Pavlostathis SG, Giraldo-Gomez E. Kinetics of anaerobic treatment. Water Sci Technol. 1991;24:35-59. [ Links ]
[3] Bastidas-Oyanedel J-R, Bonk F, Thomsen MH, Schmidt JE. Dark fermentation biorefinery in the present and future (bio)chemical industry. Rev Environ Sci Bio/Technology. 2015;14(3):473-98. [ Links ]
[4] Demirbas A. Biorefineries: Current activities and future developments. Energy Convers Manag. 2009;50(11):2782-801. [ Links ]
[5] Reddy CSK, Ghai R, Rashmi, Kalia VC. Polyhydroxyalkanoates: an overview. Bioresour. Technol. 2003;87(2):137-46. [ Links ]
[6] Lee SY, Park JH, Jang SH, Nielsen LK, Kim J, Jung KS. Fermentative butanol production by clostridia. Biotechnol Bioeng. 2008;101(2):209-28. [ Links ]
[7] Hong C, Haiyun W. Optimization of volatile fatty acid production with co-substrate of food wastes and dewatered excess sludge using response surface methodology. Bioresour. Technol. 2010;101(14):5487-93. [ Links ]
[8] Dahiya S, Sarkar O, Swamy YV, Venkata Mohan S. Acidogenic fermentation of food waste for volatile fatty acid production with co-generation of biohydrogen. Bioresour. Technol. 2015;182:103-13. [ Links ]
[9] Lim S-J, Kim BJ, Jeong C-M, Choi J, Ahn YH, Chang HN. Anaerobic organic acid production of food waste in once-a-day feeding and drawing-off bioreactor. Bioresour. Technol. 2008;99(16):7866-74. [ Links ]
[10] Gameiro T, Sousa F, Silva FC, Couras C, Lopes M, Louros V, et al. Olive oil mill wastewater to volatile fatty acids: statistical study of the acidogenic process. Water, Air, Soil Pollut. 2015;226(4):115-28. [ Links ]
[11] Bertin L, Lampis S, Todaro D, Scoma A, Vallini G, Marchetti L, et al. Anaerobic acidogenic digestion of olive mill wastewaters in biofilm reactors packed with ceramic filters or granular activated carbon. Water Res. 2010;44(15):4537-49. [ Links ]
[12] Marino-Marmolejo EN, Corbalá-Robles L, Cortez-Aguilar RC, Contreras-Ramos SM, Bolaños-Rosales RE, Davila-Vazquez G. Tequila vinasses acidogenesis in a UASB reactor with Clostridium predominance. Springerplus. 2015;4(1):419. [ Links ]
[13] Vergine P, Sousa F, Lopes M, Silva F, Gameiro T, Nadais H, et al. Synthetic soft drink wastewater suitability for the production of volatile fatty acids. Process Biochem. 2015;50(8):1308-12. [ Links ]
[14] Cardona Echavarría AC, Mora Martínez AL, Marín Montoya M. Identificación molecular de bacterias productoras de polihidroxialcanoatos en subproductos de lácteos y caña de azúcar. Rev Fac Nac Agron. 2013;66(2):7129-40. [ Links ]
[15] Asocaña. Informe anual de Asocaña 2011- 2012. Asocaña. Colombia; 2012;1-104. [ Links ]
[16] Asocaña. Aspectos Generales del Sector Azucarero El dulce sabor del 2013-2014. Colombia; 2014;116. [ Links ]
[17] Albuquerque MGE, Eiroa M, Torres C, Nunes BR, Reis MAM. Strategies for the development of a side stream process for polyhydroxyalkanoate (PHA) production from sugar cane molasses. J. Biotechnol. 2007;130(4) 411-21. [ Links ]
[18] Zehnder AJB, Huser BA, Brock TD, Wuhrmann K. Characterization of an acetate-decarboxylating, non-hydrogen-oxidizing methane bacterium. Arch Microbiol. 1980;124:1-11. [ Links ]
[19] Field J. Medición de parámetros en reactores del manto de lodos anaeróbicos de flujo ascendente, Universidad Agrícola de Wageningen Holanda En: Universidad del Valle, Corporación Autónoma Regional del Cauca, Universidad Agrícola de W ageningen. Arranque y operación de sistema de flujo ascendente con manto de lodos UASB. Santiago de Cali: Universidad del Valle; 1987. [ Links ]
[20] APHA, AWWA, and WEF. Standard Methods for the Examination of Water and Wastewater 21st ed. Washington D.C.: American Public Health Association; 2005. [ Links ]