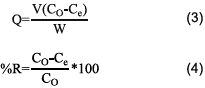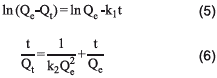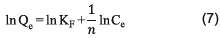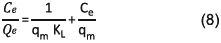Introducción
Entre los contaminantes de aguas de mayor impacto en el medio ambiente, se encuentran los colorantes utilizados en distintas actividades industriales, principalmente la textil. Se estima que entre el 10-15% de estos colorantes son arrojados directamente a las aguas residuales por lo que en la actualidad existe una preocupación creciente con respecto a los potenciales efectos adversos de estos contaminantes y lo convierte en una problemática de interés para investigadores y entes ambientales [1]. El azul de metileno es uno de los contaminantes más comunes que son descargados en los cuerpos de agua, un adsorbente catiónico que reduce la penetración de la luz en el agua por su alta demanda química de oxígeno, y es causante de aumento de la frecuencia cardíaca, vómitos, cianosis, ictericia y tetraplejía en seres humanos [2]. Por lo tanto, es extremadamente importante encontrar alternativas de bajo costo para la remoción de este contaminante de los efluentes industriales antes de descargarlo al medio ambiente. Muchos tratamientos, incluyendo la degradación fotocatalítica [3], coagulación y floculación [4], separación con membranas [5] y degradación electroquímica [6] han sido aplicados para la remoción de tales colorantes de las aguas residuales, no obstante, estos métodos no son usados a gran escala debido a su alto costo. En adición, la técnica de adsorción es considerada la más usada y versátil [7]. Sin embargo, los adsorbentes convencionales, como el carbón activado, todavía presentan algunas desventajas: a pesar de su eficacia, muchos de ellos son bastante costosos [8].
Recientemente, se ha reportado la adsorción de azul de metileno utilizando adsorbentes de bajo costo como residuos de agricultura, desechos sólidos industriales y biomasa [9,10], jojoba [11], cascarillas de arroz [12], conchas de mango [13], conchas de trigo [14], hierbas de césped [15], los cuales han resultado económicamente factibles y constituyen un método simple en la remoción de azul de metileno de soluciones acuosas. En esta investigación se utilizó uno de los residuos sólidos de las industrias de alimentos tradicionales más abundantes en la costa norte colombiana, la cáscara de yuca (Manihot esculenta), derivado de un proceso fotosintético y una combinación de lignina, celulosa y hemicelulosa [16]. Estos compuestos orgánicos son útiles para la remoción de colorantes orgánicos sintéticos mediante la donación de un par de electrones y formando complejos en soluciones acuosas [17]. En particular la cáscara de yuca a mostrado ser un adsorbente rápido, pero de baja capacidad para algunos metales [18-20]. Este efecto, que retiene las partículas del colorante en los grupos funcionales de la biomasa, puede ser mejorado con la esterificación térmica de la biomasa con un ácido carboxílico, los cuales tienen una fuerte tendencia hacia los colorantes catiónicos [8,12,21]. En el presente trabajo, la modificación se realizó con ácido oxálico, el cual ha demostrado que aumenta la capacidad de adsorción de la biomasa [22].
La identificación de los diferentes mecanismos de adsorción que se presentan durante la remoción de sustancias contaminantes en soluciones acuosas, son fundamentales para el diseño de equipos depuradores de agua a gran escala, ya sean para vertimientos industriales o para consumo humano, por lo cual, en esta investigación, se realizó el estudio termodinámico y cinético de la adsorción del azul de metileno de soluciones acuosas usando cáscara de yuca modificada con ácido oxálico.
Metodología
Preparación del adsorbato
Una solución patrón de azul de metileno de 500 mg/L fue preparada a partir de 0,5 g de azul de metileno sólido en un litro de agua desionizada, la cual fue posteriormente diluida volumétricamente según los requerimientos.
Preparación de la biomasa
La cáscara de yuca se obtuvo de los cultivos del municipio de Baranoa en el departamento del Atlántico. La biomasa se lavó con agua desionizada para eliminar el exceso de tierra e impurezas. Se sometió a exposición solar durante dos días (48 horas) y luego a un horno de convección Esco Isotherm a 90 °C por 12 horas. La cáscara de yuca fue molida en un triturador de alimentos y tamizada hasta tamaños de partículas entre 250 y 400 um. A continuación, la cáscara de yuca fue sometida a un segundo lavado con hidróxido de sodio 0,1 M y abundante agua desionizada para eliminar la pigmentación natural de la cáscara de yuca; por último, la biomasa fue secada en un horno de convección durante 24 horas a 90°C.
Modificación de la biomasa
La cáscara de yuca lavada se mezcló con soluciones de ácido oxálico (0,51-0,68 M) a distintas relaciones másicas en un termorregulador VELP Scientifica bajo agitación constante de 400 rpm a diferentes temperaturas y tiempos de contacto. El pH de los experimentos se mantuvo neutro usando una solución de NaOH 0,1 M. Luego, para eliminar el exceso de ácido, las muestras modificadas fueron filtradas y secadas en un horno de convección a una temperatura de 90 °C durante 12 horas. Finalmente, las muestras fueron lavada con agua desionizada hasta conseguir un pH neutro, nuevamente filtradas y secadas en el horno de convección a 90°C por 12 horas. Para estudiar la modificación química de la cáscara de yuca se tuvieron en cuenta tres factores: la relación másica ácido oxálico/biomasa (AO/CY), la temperatura (°C) y el tiempo de contacto (h). El diseño experimental se obtuvo mediante la herramienta Statgraphics Centurión®, con la capacidad de adsorción y el porcentaje de remoción como variables de respuestas. Se utilizó un diseño factorial con punto central para un total de 18 experimentos cuyos niveles se muestran en la Tabla 1.
Caracterización del adsorbente
Tanto a la cáscara de yuca modificada como sin-modificar se le realizaron análisis próximo, último y cálculos del contenido de lignina y densidad aparente.
Contenido de Lignina: El contenido de lignina se determinó según la norma TAPPI 222 os-74 (Technical Association for the Pulp and Paper Industries). Cinco gramos de la biomasa se sometieron a un pre-tratamiento con acetona como agente lixiviante por 16 horas en un "Soxhlet", y a un secado durante 24 horas a 105°C. Luego, a un gramo de esta biomasa se le adicionó una solución de 15 mL de ácido sulfúrico al 72% para ser mezclado por dos horas con agitación constante. Posteriormente, se adicionó agua desionizada hasta reducir la concentración del ácido hasta un 3% en peso y se llevó a ebullición por 4 horas. Por último, se filtró la solución y se llevó a pH neutro con agua caliente. El producto Anal correspondió a la lignina que no hidroliza con el ácido sulfúrico. El porcentaje de lignina se calculó con la Ecuación 1.
Densidad Aparente: La densidad aparente correspondiente a la relación de masa por unidad de volumen, incluyendo el espacio entre partículas y los poros [17], se determinó pesando 5 g de la biomasa y midiendo su volumen en una probeta. La ecuación 2 expresa la fórmula para el cálculo de la densidad aparente.
Donde p es la densidad aparente expresada en g/ cm3, w es el peso de la biomasa en g, v el volumen ocupado por la biomasa en cm3 y H es el porcentaje de humedad.
Análisis de espectroscopia de infrarrojo con transformada de Fourier (FT-IR). Con el fin de determinar los principales grupos funcionales que se encuentran en la biomasa se tomaron los espectros de IR con transformada de Fourier de la cáscara de yuca y de la cáscara de yuca modificada utilizando un espectrofotómetro de luz infrarroja de transformada de Fourier (FTIR) marca Shimadzu IR Affinity. 1,0 mg de la biomasa pulverizada se mezcló con 50 mg de Bromuro de potasio (KBr) (previamente secado durante tres horas a 110 °C), para introducir una pequeña muestra en forma de una película delgada en el equipo. El rango de medición fue de 400 cm-1 a 4000 cm-1.
Determinación sitios ácidos y básicos. La acidez y la basicidad total de la cáscara de yuca modificada se determinaron por el método de Boehm [23]. Se pesó 1,00 g de la biomasa y se mezclaron con 50 mL de hidróxido de sodio (NaOH) 0,1 N. Otro 1,00 g de la muestra se mezclaron con 50 mL de ácido clorhídrico (HCl) 0,1 N. Las soluciones se dejaron reposar durante cinco días, a temperatura de 30 °C y se agitaron al menos dos veces por día. Finalmente, se tomaron muestras de 10 mL de cada una de las soluciones para titular con soluciones estándar de hidróxido de sodio y ácido clorhídrico.
Determinación de pH en el punto de carga cero (PCC). El pH en el punto de carga cero (pHPCC) de un adsorbente es una característica importantísima que determina el pH al cual la superficie adsorbente tiene neutralidad eléctrica neta. A este valor, los grupos funcionales ácidos o básicos ya no contribuyen al pH de la solución [24]. Esto es, se establece la carga promedio superficial del sólido dependiendo de las condiciones de pH, así para la cáscara de yuca la carga superficial será positiva para valores de pH menores al pHPCC que se obtenga, neutra cuando el pH sea igual al pHPCC y negativa para valores mayores al pHPCC. Si la cáscara de yuca presenta una carga neta negativa se favorecerá la adsorción de los cationes, por el contrario, si es negativa, se favorece la adsorción de aniones. Para la determinación del pH en el punto de carga cero se llevó a cabo el procedimiento presentado por Leyva-Ramos [25]. Se calentó 100 mL de agua hasta ebullición por 20 minutos para eliminar el CO2 disuelto en el agua y luego se dejó enfriar a temperatura ambiente. Se añadieron 0,5 g de la biomasa a 10 mL del agua libre de CO2 bajo agitación y temperatura constante de 30 °C durante 48 horas, para que las cargas del bioadsorbente se equilibren. Finalmente, se midió el pH de la solución.
Ensayos de adsorción
Cada una de las muestras obtenidas por el diseño experimental fue puesta a prueba con una solución de azul de metileno para el estudio de remoción en batch. Estos ensayos se realizaron añadiendo 0,25 g de la biomasa en 50 mL de una solución de 125 mg/L de azul de metileno, bajo agitación constante de 300 rpm durante dos horas. Alícuotas de 1 mL se tomaron cada 0,5 horas para filtrar. Las concentraciones finales de las soluciones de azul de metileno fueron calculadas en un espectrofotómetro UV-Visible Evolution 60S. Las variables de respuesta, capacidad de adsorción (Q en mg/g) y porcentaje de remoción (%R), fueron calculados con las ecuaciones 3 y 4, respectivamente.
Donde Co y Ce corresponden a las concentraciones iniciales y finales de azul de metileno en mg/L, Q es la capacidad de adsorción en mg/g, W es la masa del adsorbente en g y V es el volumen de la fase acuosa en L.
Cinética de adsorción
Para el estudio cinético del proceso de adsorción de azul de metileno con cáscara de yuca modificada se realizaron ensayos de remoción utilizando dos soluciones de azul de metileno concentradas a 18 y 113 mg/L. En cada ensayo, fueron agregadas 1,00 g de biomasa en 100 mL de las soluciones de azul de metileno. El pH fue ajustado a 6 en todos los casos con una solución buffer. Alícuotas de 1 mL fueron recolectadas a 2, 5, 15, 40, 60, 100, 140 y 180 minutos, y las concentraciones de las soluciones de azul de metileno fueron medidas en el espectrofotómetro UV- Visible. Los valores del estudio de adsorción fueron ajustados a las formas lineales de los modelos de pseudo primer orden y pseudo segundo orden regidos por las ecuaciones 5 y 6, respectivamente.
Donde Qe y Qt son la capacidad de adsorción del adsorbente en el equilibrio y en el tiempo en mg/g, respectivamente, t es tiempo (min), k y k2 son las constantes de los modelos cinéticos pseudo primer y segundo orden, respectivamente.
Equilibrio de adsorción
Para el análisis del equilibrio de adsorción se construyeron isotermas a tres temperaturas diferentes (25 °C, 35 °C y 45 °C). Para su construcción se agregaron 0,25 g de biomasa en 25 mL de diferentes soluciones de azul de metileno (50, 80, 100, 120, 140, 160, 180, 200 mg/L) por 50 minutos a las diferentes temperaturas. El pH de la solución se ajustó a 6 utilizando una solución buffer. La temperatura de las muestras se mantuvo constante utilizando balanzas termorreguladoras y agitación.
Los datos del equilibrio se probaron en los modelos de adsorción de Freundlich y Langmuir. La isoterma de Freundlich [26] es una ecuación empírica empleada para describir sistemas no ideales de superficie heterogénea el cual sugiere que la energía de la biosorción decrece exponencialmente cuando la cantidad de sitios activos del biosorbente disminuye. Esta isoterma se expresa en su forma lineal como se muestra en la ecuación 7.
Donde Qe es la capacidad de adsorción en el equilibrio por unidad de adsorbente (mg/g), KF y 1/n son constantes de Freundlich asociadas a la intensidad y capacidad de adsorción, respectivamente y Ce es la concentración en el equilibrio en mg/L.
Por su parte, el modelo de Langmuir [27], asociado a procesos de adsorción que toman lugar en sitios homogéneamente específicos en el biosorbente y sugiere que la superficie del adsorbente está constituida por "parches" de adsorción pequeños que son energéticamente equivalentes entre sí con respecto al fenómeno de adsorción, en su forma lineal, se expresa en la ecuación 8.
Donde qm es la capacidad máxima de biosorción (mg/g) y KL (L/mg) es la constante de Langmuir asociada a la energía de adsorción.
Efecto de la temperatura sobre el proceso de adsorción
La energía de activación del proceso de adsorción ayuda a determinar la cantidad mínima de energía que las moléculas del adsorbato necesitan para atravesar la diminuta interfase sólido líquido y reaccionar con los sitios activos del adsorbente [28]. La energía de activación del proceso de adsorción de azul de metileno utilizando cáscara de yuca modificada con ácido oxálico fue determinada usando la Ecuación de Arrhenius en su forma linealizada como se muestra en la ecuación 9.
Donde K es la constante que rige el proceso de adsorción, A es el factor de frecuencia, R es la constante molar de los gases (0,008314 kJ/mol K), T es la temperatura absoluta y E es la energía de activación del proceso de adsorción.
Resultados y discusión
Caracterización del adsorbente
En la Tabla 2 se encuentran tabulados los resultados de los análisis próximo y último de la cáscara de yuca modificada con ácido oxálico y sin modificar. Se puede observar que la cáscara de yuca sin modificar y modificada tienen un bajo contenido de humedad, lo que favorece la molienda. El contenido de azufre es bajo en ambas muestras, lo que sugiere que estos adsorbentes no presentan riesgos asociados con este elemento para el medio ambiente ni para la adsorción de azul de metileno. El aumento en el contenido de carbono y oxígeno en la cáscara de yuca modificada se atribuye a la adición de enlaces de grupo carboxilo que se dan en el proceso de esterificación, que es la finalidad de la modificación química con un ácido como el oxálico [22]. La lignina presente en la cáscara de yuca modificada fue de 7,9%. La densidad aparente tanto de la cáscara de yuca modificada se reportó en 0,22 mg/L. Estos datos característicos concuerdan con los datos reportados en [29].
Tabla 2 Resultados del análisis próximo y último y el contenido de lignina de la cáscara de yuca sin modificar y modificada con ácido oxálico.
Análisis de espectroscopia de infrarrojo con transformada de Fourier (FT-IR). La Figura 1 muestra los espectros FT-IR de la cáscara de yuca modificada y sin modificar. El espectro de la cáscara de yuca presenta un pico en 3408 cm-1 lo que indica la presencia de grupos carboxílicos O-H. Los picos observados entre 2922 cm-1 y 1645 cm-1 son producidos por los grupos alifáticos C-H y un tramo al C-O, estas bandas son normalmente encontradas en materia vegetal, debido a que estos grupos son los principales constituyentes de materiales lignocelulósicos como la celulosa y la hemicelulosa [30]. Los tres picos en 1734, 1688 y 1645 cm-1 son bandas de absorción de grupos carboxílicos con tramos de carbonilos (C-O) y de hidroxilos (O-H) los cuales están directamente ligados al proceso de adsorción [31]. El pico en 1558 cm-1 corresponde a la amida y en 1456 cm-1 al tramo simétrico de C=O. Los picos en 1373 cm-1 y en 1024 cm-1 son debido a la presencia de C-O de alcoholes y ácidos carboxílicos [8]. Por otro lado, el espectro de la cáscara de yuca modificada muestra cambios en algunos picos como el de 3417 cm-1 correspondientes a los grupos O-H y el de 1030 cm-1 de los ácidos carboxílicos. Dichos cambios en la posición de algunos picos significan que algunos grupos funcionales (-COOH y -OH) fueron exitosamente introducidos en la estructura celulósica de la cáscara de yuca después de la modificación química. Estos grupos funcionales (hidroxilos desprotonados y grupos carboxilos) son los responsables de la captura de azul de metileno en solución acuosa ya que funcionan como donadores de protones [32].

Figura 1 Espectros IR de la cáscara de yuca modifica (espectro negro) y cáscara de yuca sin modificar (espectro gris).
Determinación de sitios ácidos y básicos. Las curvas de titulación obtenidas por el método de Boehm permiten conocer la cantidad de sitios ácidos y básicos totales presentes en la cáscara de yuca modificada en miliequivalentes gramos (meq/g). Los resultados de los sitios ácidos y básicos fueron 4 y 0,91 meq/g respectivamente. La diferencia entre los sitios ácidos y básicos es de 3,0 (meq/g), esta valor es favorecedor para la biosorción de solutos cargados positivamente desde soluciones acuosas, como el azul de metileno.
pH en el punto de carga cero (PCC). El pHPCC de la cáscara de yuca fue de 6,37, lo que indica que la adsorción se favorece para pH mayores a este valor. El pHPCC de la cáscara de yuca modificada con ácido oxálico fue de 2,47. Esta disminución se puede atribuir a la modificación química que se realizó con el ácido oxálico, y favorece la adsorción de colorantes catiónicos como el azul de metileno en un rango mucho mayor y es congruente con reportes anteriores [33].
Efecto de las variables de estudio sobre la adsorción de azul de metileno
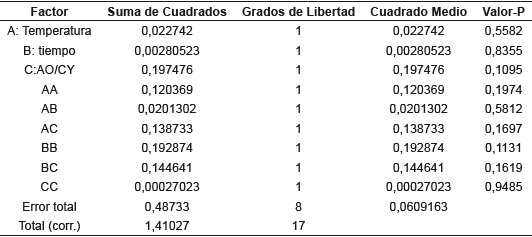
La Tabla 3 muestra el análisis de varianza (ANOVA) para la variable de respuesta: capacidad de adsorción Q en mg/g. La prueba de significancia estadística (Valor-P) indica que ninguna combinación de los factores (relación másica ácido/biomasa, temperatura y tiempo de modificación) inciden de manera significativa en la variable de respuesta. Esto es, los factores relación másica ácido/biomasa, temperatura y tiempo de modificación dentro del rango estudiado no afectan significativamente la capacidad de adsorción de azul de metileno.
Tabla 3 Análisis de varianza estadístico de los factores (relación másica ácido/biomasa, temperatura y tiempo de modificación) sobre la capacidad de adsorción de azul de metileno (ANOVA).
Así, cualquiera de las combinaciones es favorable para la adsorción, en todos los casos se obtuvieron remociones de más del 99% de azul de metileno de soluciones acuosas de 125 mg/L, como se resume en la Tabla 4. Resultados similares fueron reportados por [24] quienes trataron distintas biomasas térmicamente y obtuvieron también una remoción de más del 99% de azul de metileno de soluciones acuosas; no obstante, para estudios posteriores se seleccionó la combinación que resultó en una mayor capacidad de adsorción (24,82 mg/g). Las condiciones del experimento que resultó en la mayor capacidad de adsorción fueron 1,75 de relación ácido/biomasa, 50°C y 2 horas de reacción. Bajo las mismas condiciones, la cáscara de yuca sin modificar removió solo el 94,040% correspondiente a una capacidad de adsorción de 23,510 mg/g, esto es un hasta un 5,5% menos que con la cáscara de yuca modificada. Nuestros resultados sugieren que dentro de las condiciones de modificación estudiadas, la reacción de esterificación se lleva a cabo satisfactoriamente, originando biomasas modificadas con excelentes propiedades de adsorción del colorante azul de metileno.
Cinética de adsorción
Los datos de porcentaje de remoción utilizando la cáscara de yuca modificada con ácido oxálico, medidos a distintos tiempos bajo las mismas condiciones de temperatura y pH de dos soluciones de azul de metileno se muestran en la Figura 2.

Figura 2 Perfil cinético del porcentaje de remoción de azul de metileno a dos concentraciones iniciales distintas a pH 6 y 30 °C.
Para la solución de concentración inicial de 113 mg/L de azul de metileno se logró el equilibrio en un tiempo de 50 minutos. Por su parte, para la concentración menor (18 mg/L), el equilibrio se alcanzó en tan solo 15 minutos, observándose que, a mayor concentración de colorante, mayor tiempo se tarda en alcanzar el equilibrio. Además, los tiempos de remoción son bastante cortos, como se observa, la cantidad de azul de metileno removido incrementa rápidamente en los primeros diez minutos obteniendo porcentajes de remoción superiores al 95% lo cual concuerda con la literatura [34]. El aumento rápido en los primeros minutos puede deberse a una primera adsorción en la superficie y la segunda parte, que suele ser más lenta, puede atribuirse a mecanismos a nivel de poros; comportamientos similares fueron indicados por [35].
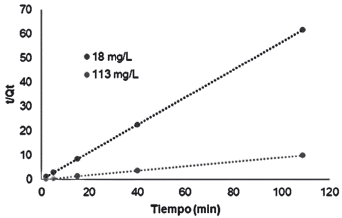
Los datos de capacidad de adsorción y concentraciones medidas a distintos tiempos fueron ajustados a los modelos cinéticos de pseudo primer y segundo orden. En la Tabla 5 se enlistan los parámetros de los modelos para dos concentraciones distintas de azul de metileno. Como se observa en la Tabla 5 y Figura 3, el mejor ajuste de los datos cinéticos se da con el modelo de pseudo segundo orden, con coeficiente de correlación de 1 para ambas concentraciones. Además, las capacidades de adsorción calculadas con este modelo coinciden con las capacidades obtenidas experimentalmente. Esto sugiere que el proceso de adsorción de azul de metileno con cáscara de yuca modificada con ácido oxálico está controlado por la adsorción química o quimisorción, involucrando fuerzas de atracción debidas a las valencias o intercambio de electrones entre el azul de metileno y los grupos funcionales en la superficie, principalmente grupos hidroxilo y carboxilo, de la cáscara de yuca modificada que se evidenciaron en la caracterización [2]. Esto indica posibles interacciones químicas entre los grupos hidroxilo y carboxilo cargados negativamente (-COO-) en la superficie del adsorbente con las moléculas de azul de metileno cargadas positivamente.
Tabla 5 Parámetros cinéticos de los modelos de pseudo primer y segundo orden para dos concentraciones diferentes de azul de metileno.

Equilibrio de adsorción
Los datos de capacidad de adsorción en el equilibrio a partir de diferentes concentraciones iniciales de azul de metileno logrados a diferentes temperaturas, bajo pH 6 fueron ajustados a los modelos de isotermas de Freundlich y Langmuir. Los parámetros para cada uno de los modelos se resumen en la Tabla 6.
Tabla 6 Parámetros de las isotermas Freundlich y Langmuir a 25, 35 y 45 °C asociadas al proceso de adsorción de azul de metileno con cáscara de yuca modificada.

Teniendo en cuenta los valores de los parámetros de Langmuir, se observa que los valores de capacidad máxima y la constante asociada a la energía de adsorción (KL) no son valores aplicables a la realidad física, por tanto, se puede concluir que este proceso de adsorción no se rige por los supuestos de homogeneidad en la superficie que establece Langmuir. Por otra parte, se observa que el coeficiente de correlación obtenido para el modelo de Freundlich es cercano a la unidad, además que los valores de n son menores a la unidad, y según la teoría de este modelo, valores del factor de heterogeneidad n menores que 1 favorecen la capacidad de adsorción multicapas.
Entonces, es válido afirmar que, el proceso de adsorción de azul de metileno con cáscara de yuca modificada, es un sistema de adsorción no lineal en superficie heterogénea en el cual la energía de la adsorción decrece exponencialmente cuando la cantidad de sitios activos del adsorbente disminuye [26]. El ajuste de los datos al modelo lineal de Freundlich se observa en la Figura 4.
Energía de activación del proceso de adsorción
El leve aumento que se observa en la capacidad de adsorción con aumentos de temperaturas en 10 °C en la Figura 4 puede atribuirse al incremento en la movilidad de una gran cantidad de iones de colorante en la reacción química que toma lugar entre los grupos funcionales del adsorbato y el adsorbente, que tiene un efecto de hinchamiento dentro de la estructura interna de la cáscara de yuca modificada, permitiendo que más moléculas de colorante logren penetrar la interfase sólido líquido 36]. Esta tendencia con la temperatura permite deducir que posiblemente el proceso de adsorción es de naturaleza química y endotérmica. El tipo de adsorción se puede indicar de acuerdo al valor de la energía de activación. El valor de la energía de activación calculado a partir de la pendiente de la gráfica que se muestra en la Figura 5, fue de 23,09 kJ/mol. El alto valor de esta energía corrobora que el proceso de adsorción implica fuerzas grandes típicas de las interacciones químicas entre los grupos funcionales de la superficie de la cáscara de yuca modificada y el azul de metileno, esto es, un proceso de quimisorción.
Conclusiones
En esta investigación se evaluó el potencial de la cáscara de yuca (Manihot esculenta) modificada con ácido oxálico para remover azul de metileno de soluciones acuosas. La introducción de grupos funcionales de ácidos carboxílicos en la superficie de la cáscara de yuca se logró con el tratamiento químico con ácido oxálico y se evidenció con el cambio de punto de carga cero del adsorbente y el espectro IR comparado con la cáscara de yuca sin modificar. Las condiciones de temperatura (40-60 °C), tiempo (1-3 h) y relación másica ácido oxálico/biomasa 1,5/2 en estos rangos no presentó afectación significativa en la capacidad de adsorción de azul de metileno según el análisis estadístico. Porcentajes de remoción de hasta 99,48 % fueron obtenidos para todas las condiciones de trabajo. La máxima capacidad de adsorción de azul de metileno con cáscara de yuca fue de 24,88 mg/g, modificada a 50°C por dos horas con 1,75 relación ácido oxálico/biomasa. Comparado con la cáscara de yuca, la capacidad de adsorción con la modificación aumentó en un 5 %. El proceso de adsorción resultó mejor ajustado al modelo de isotermas de Freundlich y al modelo cinético de pseudo segundo orden. La adsorción de hasta un 95% de azul de metileno se alcanzó en tan solo 15 minutos para concentraciones de 125 mg/L de colorante. La energía de activación del proceso de adsorción fue de 23,093 kJ/mol. El proceso de adsorción de azul de metileno con cáscara de yuca modificada puede describirse bien como un sistema de superficie heterogénea que implica fuertes interacciones químicas entre los grupos funcionales (principalmente enlaces carboxílicos) de la cáscara de yuca y el colorante.