Introdução
Materiais a base de celulose vêm sendo amplamente explorados devido à sua abundância, seu caráter renovável, dureza e baixa densidade. O número de trabalhos envolvendo o desenvolvimento de materiais contendo partículas nanocelulósicas tem aumentado expressivamente, indicando um crescente interesse em explorar a potencialidade de cargas celulósicas para o desenvolvimento de nanocompósitos, menos agressivos ao meio ambiente e, ao mesmo tempo, que apresentem boas propriedades mecânicas, térmicas e óticas [1]. A celulose é um homopolímero linear com unidade de glicose ligadas por ligações glicosídicas. É constituída por microfibrilas com diâmetro de tamanho nano e rodeadas por lignina e hemicelulose.
Os nanocristais de celulose (NCCs em português ou CNCs em Inglês), são os domínios cristalinos da celulose com aparência de grãos de arroz e tamanho em escala manométrica, de entre 5 a 20 nm de largura e 100 a 500 nm de comprimento [2]. Sua principal fonte de extração é a madeireira, da indústria de polpa e papel, contudo, pode ser extraída de outras fontes como sobras de madeira, bagaço de cana, cascas de coco e arroz e da biomassa decorrente da produção de óleo de soja e de palma [3].
Os CNCs são principalmente usados como reforço em nanocompósitos poliméricos por suas excepcionais propriedades mecânicas (modulo elástico e resistência à tensão), flexibilidade química e baixo custo, considerando a fonte de extração e o alto valor agregado ao produto final. A rota clássica de extração dos nanocristais é a hidrólise ácida (a 45 °C e 1 a 2 h de reação) com um único ácido (ácido sulfúrico) ou uma mistura de ácidos, envolvendo o ácido clorídrico e/ou ácido fosfórico. No entanto, as pesquisas buscam aprimoram os métodos de extração para uma produção mais eficiente e ambientalmente amigável dos CNCs. Por outro lado, busca-se uma maior pureza dos cristalitos, com faixa de distribuição granulométrica restrita e razão de aspecto uniforme.
Assim, métodos alternativos, como o patenteado por Leung et al.[5], são fundamentados no uso de uma solução aquosa de persulfato inorganico (preferívelmente Persulfto de Amônio, NH4S2O8 ou APS), e uma única etapa de disslução de lignina, hemicelulose, pectina e outros conteúdos da biomassa vegetal. Adicionalmente, a extração é realizada a temperaturas mais altas, entre 60 e 80 °C, podendo ser usada qualquer biomassa vegetal, a qual não precisa de pretratamento. Também, os CNCs produzidos contêm um indice de cristalinidade de até 20% maior do que o material celulosico precursor, no entanto, a cinética das reações de extração são muito mais lentas, implicando em tempos de processamento superiores a 10 h.
A fabricante CelluForce é líder na produção mundial de CNCs derivados da indústria madeireira, com 300 toneladas por ano e, de acordo com volume 253 da Revista Fapesp [3], esta produção é destinada para pesquisa, visando o desenvolvimento de produtos comerciais e aplicações para os CNCs. Considerando que, a tendência em matéria-prima para a extração dos CNCs são resíduos derivados da agroindústria (papel, álcool e agrofibras), e tendo em consideração as especiais aplicações onde os CNCs podem ser introduzidos, estima-se um grande auge do mercado (30%/ano), e que, o preço dos nanocristais de celulose poderá ser 20 vezes maior do que o da celulose. De acordo com Cidreira et al. [5], a celulose microcristalina (MCC) que é a forma purificada da celulose e, precursora dos CNCs pode ser encontrada comercialmente com o nome de Avicel PH-101 (CAS 9004-34-6) pelo custo de R$ 2696,00/kg [6].
O açaizeiro (Euterpe oleracea) é uma palmeira nativa da Amazônia, que ocorre em grandes extensões no estuário amazônico. A planta é utilizada de inúmeras formas: na ornamentação (paisagismo), na construção rústica (de casas e pontes), como remédio (vermífugo), na produção de celulose, na alimentação (polpa processada e palmito); na confecção de biojoias (colares, pulseiras etc.), ração animal; adubo e outros. O Estado do Pará é o principal produtor de açaí no Brasil, seguido do Amazonas e do Maranhão. O crescimento dos mercados da polpa processada desde o fruto tem aumentado o interesse no plantio dessa palmeira em áreas de terra firme, e especialmente nas degradadas [8].
Em relação à biomassa do açaí, de acordo com a Companhia Nacional de Abastecimento (CONAB), somente em 2017, a produção nacional de polpa de açaí atingiu as 219 855 toneladas, representadas no valor de R$ 596,8 milhões [8]. Desta produção, o Maranhão participou com 8,1%, posicionando-se em terceiro lugar no ranking de produção nacional. Considerando que 85% p do fruto é a biomassa residual, estudos aprofundados sobre o aproveitamento destes resíduos são de alta pertinência, quando se pensa no impacto ambiental pelo destino inadequado deles.
Como registrado por Almeida et al.[9], existem diversas aplicações para esta biomassa, na panificação, na fabricação de ração e na fitoterapia, e em particular, a fibra é usada para isolamento acústico, na indústria automobilística e na indústria cosmética. No entanto a maior parte deste material é descartado como rejeito orgânico. A biomassa do açaí (caroço e fibras) constitui um subproduto do processo de despolpamento. Pessoa et al. [10], registraram uma composição media da biomassa do açaí de 33% em peso de lignina, 33% de celulose, 37% de hemicelulose, 7% de material hidrossolúvel e 1% de organossolúveis, encontrados no conjunto fibra-caroço.
O cenário antes apresentado, evidencia uma alta pertinência de pesquisas abordando este assunto, tanto pela disponibilidade e acessibilidade da matéria prima (biomassa de açaí), como pela necessidade de consumo dos CNCs, de alto valor agregado derivados da mesma.
Dando continuidade aos estudos sobre valorização da biomassa, e na busca por metodologias de extração mais agradáveis ao ambiente, neste artigo são apresentados os desenvolvimentos até os dias atuais relacionados com a extração dos CNCs de biomassas lignocelulosicas, destacando a biomassa de açaí a partir do método de oxidação com Persulfato de Amônio.
Materiais e Métodos
Para a coleta das informações registradas neste artigo, foi utilizada como fonte principal a plataforma CAFÉ (Comunidade Acadêmica Federada) do portal de periódicos da Coordenação de Aperfeiçoamento de Nível Superior (CAPES). A plataforma é de acesso exclusivo das instituições de ensino e pesquisa do Brasil, e conta com um acervo de 45 mil títulos com texto completo em todas as áreas do conhecimento, 130 bases de dados referenciais e 12 bases de dados exclusivas de patentes, livros, enciclopédias e obras de referência, normas técnicas, estatísticas e conteúdo audiovisual. A busca pelas informações se fundamentou no período de 2010 a 2021, principalmente, não entanto patentes fundamentais e livros mais antigos, que registram os conceitos básicos sobre a oxidação de biomassa usando Persulfatos inorgânicos, também foram consideradas. As palavras chaves de busca das informações incluíram, principalmente: Ammonium persulfate oxidation, Acai berry residual biomass and Cellulose nanocrystals. No período de busca foram encontrados poucos trabalhos relacionados com a extração de nanocristais de celulose de biomassas derivadas da agroindústria pelo método de oxidação usando persulfato de amónio e, nenhum trabalho que registrasse a extração dos CNCs, desde a biomassa do açaí usando este método. Assim, as referências que mais elucidaram os conceitos e avanços no assunto podem ser destacadas: Leung et al. [4,11], Mascheroni et al. [12], Zhang et al.[13], Meng et al. [14] e nossas próprias experiências sobre o estudo desta biomassa, algumas já registradas em Zuniga et al. [15] e Cidreira et al.[5]. Por fim, para suportar esta revisão, alguns resultados experimentais preliminares sobre propriedades dos CNCs obtidos da biomassa de açaí pela oxidação APS e hidrólise ácida e, que estão em processo de análise para futuros registros foram são registrados aqui.
Resultados e analise Biomassa lignocelulósica
A biomassa lignocelulósica compreende os resíduos agroindustriais e a matéria orgânica proveniente diretamente de fontes naturais (animais, vegetais, industriais e florestais) ou resultantes de seu processamento. É destinada, principalmente, para a geração de fontes alternativas de energia [16]. Existem várias biomassas que são tradicionalmente usadas como fonte de energia mecânica, térmica e elétrica. Como recurso energético, a biomassa é classificada nas seguintes categorias: biomassa energética florestal, com seus produtos e subprodutos; biomassa energética agrícola, englobando as culturas agroenergéticas e os resíduos e subprodutos das atividades agrícolas, agroindustriais e da produção animal e rejeitos urbanos. Desde o ponto de vista ambiental, a partir do reaproveitamento e reciclagem desses resíduos podem-se diminuir os problemas resultantes de sua disposição inadequada na natureza, agregar valor aos subprodutos da agroindústria e valorizar os recursos naturais ou culturais de determinada região [17,18].
A biomassa lignocelulósica é constituída de estruturas duras e fibrosas, compostas principalmente pelos polissacarídeos de celulose e hemicelulose (aproximadamente 70% da massa seca), intercalados pela lignina, uma macromolécula composta de álcoois aromáticos [18]. A organização estrutural da parede celular da biomassa é composta por três camadas principais: a mais externa chamada lamela média, uma fina camada que mantém as células coesas e o tecido vegetal íntegro; a parede celular primária, depositada após a lamela média, sendo de grande importância para o acúmulo e controle do crescimento celular, e; por último e mais interna, a parede celular secundária responsável principalmente pela resistência mecânica da parede celular. A composição química dessa parede celular é composta pelas estructuras macromoleculares dos carboidratos (celulose e hemicelulose), da lignina e outros materiais em menor proporção como, ácidos graxos, amido, proteínas e outros contaminantes não identificados [19].
Os recentes avanços demonstram as utilidades da biomassa para a produção de biocombustíveis (etanol de primeira e segunda geração do bagaço de cana de açúcar) ou bioprodutos variados, também é muito utilizada nas biorrefinarias para a extração dos carboidratos de da lignina. Algumas biomassas tradicionais geram subprodutos específicos, como a casca de arroz, da qual se pode extrair glicose, sílica e sulfato de sódio, do bambu, para a produção de bioenergia, bioetanol e açúcares, e nos desenvolvimentos dos próprios autores, os caroços de açaí tem demonstrado altas potencialidades para a produção de energia, celulose e nanocristais [5,15,20].
Biomassa de açaí
O Açaí é uma palmeira típica da região da várzea amazônica cujo fruto, também nomeado açaí é popularmente consumido na forma de suco por possuir grande valor energético, alta concentração de fibra alimentar e excelentes propriedades antioxidantes. O crescimento da palmeira, ocorre espontaneamente no Brasil nos estados do Pará, Amazonas, Maranhão e Amapá. Desenvolve-se bem em condições de clima quente e úmido e não suporta períodos de seca prolongada [21].
Segundo Elarrat [22], uma característica importante para o aproveitamento desta palmeira é ser cespitosa, isso significa que ela consiga emitir brotações, ou perfilhos, que surgem na base da planta crescendo em touceiras, ou rebolada (na linguagem cabocla). Esta característica dá à planta uma grande capacidade de regeneração, facilitando a sua exploração de forma sustentável. A biomassa do açaí é decorrente do processo e despolpamento do fruto e está constituída pela semente (ou caroço) e a fibra, às quais se encontram fixadas ao redor do caroço, no mesocarpo do fruto. A desidratação do caroço facilita a remoção das fibras, inclusive com as mãos [23,24].
A Figura 1 apresenta o fruto do açaizeiro junto com a polpa ou suco extraído e a biomassa resultante, a qual constitui 85% da massa total do fruto. Pessoa et al.[10], registraram uma composição media da biomassa do açaí de 33% em peso de lignina, 33% de celulose, 37% de hemicelulose, 7% de material hidrossolúvel e 1% de organossolúveis, encontrados no conjunto fibra-caroço. Por outro lado, a Tabela 1, gerada de estudos dos próprios autores apresenta uma composição básica dos derivados da biomassa do açaí diferenciando a fibra e o caroço.
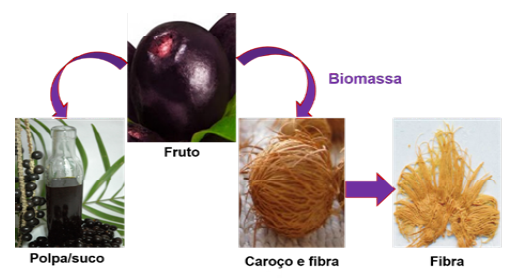
Figura 1 Fruto de açaí e sequencia de derivação da polpa e biomassa. Fonte: baseado em diversas imagens próprias e extraídas de wikipédia e de Pessoa et al. [10].
Tabela 1 Caracterização básica da biomassa lignocelulósica.
| Propriedade | Amostra (µm) | % (Valor médio) |
| Teor de umidade | Fibraa (500 ? φ ? 1000) | 4,56 (± 0,6420) |
| Caroçoa (2000 ? φ ? 4000) | 4,36 (± 0,3722) | |
| Extrativos totais | Fibraa (38 ? φ ? 500) | 13,56 (± 1,3859) |
| Caroçoa (2000 ? φ ? 4000) | 16,24 (± 0,8736) | |
| Lignina insolúvel | Fibrab (38 ? φ ? 500) | 45,63 |
| Caroçoa (2000 ? φ ? 4000) | 48,40 | |
| Teor de celulose | Fibrac (38 ? φ ? 250) | 52,56 |
| Caroçod (2000 ? φ ? 4000) | 21,91 | |
| Teor de lignina Kraft | Fibrab (250 ? φ ? 500) | 22,03 (0,030) |
| Caroçoa (2000 ? φ ? 4000) | 4,80 | |
| Cinzas totais | Fibraa (38 ? φ ? 250) | 3,168 (± 0,0762) |
| Caroçoa (2000 ? φ ? 4000) | 1,347 (± 0,0975) |
a: Amostra “In natura” lavada; b: Amostra sem extrativos; c: Amostra sem extrativos e deslignificada (Kraft); d: amostra deslignificada (Kraft).
Diferencias nas composições da biomassa podem ser atribuídas tanto ao genótipo e o período de colheita do fruto, como à metodologia adotada para a análise. Pinheiro et al.[25], reportaram porcentagens de umidade, determinados com balança específica a 160 °C (Shimadzu, MOC 63U) em torno de 10,5-12,0 % para a fibra e em torno de 10,2-11,8% para o caroço de açaí. Por outro lado, em Bufalino et al.[26], foram registrados teores de umidade, da fibra de açaí unida ao caroço bem mais altos (após a secagem a 105 °C durante 24 h), os quais oscilam entre 66,6 a 76,2% em base seca. Com respeito ao conteúdo de lignina insolúvel esta não difere, significativamente entre a fonte de extração, seja fibra ou caroço. Para fins comparativos, teores de lignina, reportados na literatura alternam entre: 33%, lignina Klason da fibra, segundo Pessoa et al.[10]; 35% lignina da fibra e 11% lignina do caroço, de acordo com Pinheiro et al.[25]. Da Tabela 1, pode-se observar que os maiores conteúdos de celulose pertencem à fibra, atingindo-se uma porcentagem de até 52,56%, comparado com o teor de celulose do caroço. Como referência, teores de celulose da biomassa residual de açaí foram reportados em torno de 33% [10] e 27% [20] na fibra e entre 44 a 47% no caroço de açaí [27,28]. Observa-se, por outro lado, que o maior conteúdo de lignina Kraft foi conseguido para a fibra, já para o caroço o conteúdo foi, em média 5 vezes menor. Estes valores estão atrelados aos valores registrados na literatura, assim, Mesquita [29] reportou uma porcentagem de 30,35% de lignina Kraft, entanto que Martins et al. (2008) encontraram 33% de lignina para a fibra do açaí (Euterpe oleracea). Por fim, os teores de cinzas encontrados estão dentro dos valores esperados para a biomassa não- madeireira. Em um estudo de Bufalino et al.[30] foram reportados valores de cinzas da fibra que recobre o caroço de açaí, entre 1,85 a 2,63% e do próprio caroço, entre 1,29 a 2,08. Por outro lado, em Pinheiro et al.[20], foram reportados valores de cinzas da biomassa residual de açaí coletada tanto na época de inverno como de verão que oscilaram entre 2,6 a 2,9 % para a fibra e entre 1,3 a 2,4% para o caroço.
Embora estudos da última década têm chamado a atenção pela valorização da biomassa do açaí, ela ainda é subutilizada. Após o despolpamento, a maior parte da biomassa é descartada em aterros sanitários e cursos de água causando poluição do solo e da água. Alguns animais peçonhentos se escondem nas pilhas de resíduos de açaí e seu odor desagradável são problemas adicionais. Logo, a qualidade de vida das populações locais poderia ser melhorada com o consumo e/ou comercialização de resíduos de açaí para a produção de energia [31,32]. Assim, o aproveitamento da biomassa residual do açaí mostra-se como uma alternativa para a redução do impacto ambiental, causado pelo elevado volume de resíduo gerado durante a sua produção, agregando valor à sua cadeia produtiva. Com esse aproveitamento pode-se obter materiais de maior valor agregado como os nanocristais de celulose.
Nanocristais de celulose
A celulose (C6H10O5)n é um polímero natural bastante atraente pelo alto potencial de substituição dos polímeros sintéticos em diversas aplicações. Consiste de um homopolissacarídeo linear cuja unidade repetitiva é a celobiose, que por sua vez é formada pela união de duas moléculas de glicose, através de ligações β-1,4 glicosídicas (vide Figura 2). Estas ligações proporcionam crescimento linear da cadeia macromolecular e, a consequência disto, a uma elevada massa molar, considerável grau de cristalinidade, e rigidez estrutural [33].
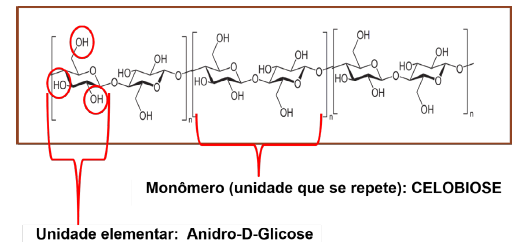
Figura 2 Organização estrutural do monômero Celobiose e unidade elementar Anidro-D-Glicose com grupos hidroxila na cadeia de celulose. Adaptada de Oliveira [1].
O arranjo linear das unidades de glicose resulta em uma distribuição uniforme de grupos hidroxila, o que permite a ocorrência de fortes interações de hidrogênio, que estabilizam seus arranjos cristalinos resultando em um polímero rígido [1]. A celulose é composta por regiões amorfas e cristalinas e, dependendo do tratamento e da fonte da celulose, o seu grau de cristalinidade varia [34].
Como observado na Figura 2, a estrutura da unidade elementar da celulose apresenta três hidroxilas livres, conferindo um caráter predominantemente hidrofílico à celulose. Por outro lado, elas também são responsáveis por interações de hidrogênio intra e intermoleculares, influenciando diretamente as propriedades da fibra [1]. Devido a essas ligações de hidrogênio há uma forte tendência da celulose a formar cristais que a tornam completamente insolúvel em água e na maioria dos solventes orgânicos [35].
Por sua vez, os nanocristais de celulose (CNCs) ou (NCCs) são nanoestruturas cristalinas da celulose estabilizadas por interações de ligações de hidrogênio complexas, e dispersadas em regiões amorfas da celulose [5,36].
Os nanocristais de celulose têm a aparência agulhada ou de grãos de arroz, por causa do afunilamento nas extremidades dos cristais, devido, provavelmente um resultado do processo de hidrólise ácida [37], porém com espessura cerca de 200 mil vezes menor e são considerados materiais mais nobres porque apresentam alta cristalinidade e resistência mecânica, com módulo elástico teórico semelhante ao do aço. Podem ter carga elétrica na superfície, e ainda apresentarem excelentes propriedades ópticas e eletrônicas devido às suas dimensões. Eles podem medir de 5 a 20 nm de largura e de 100 a 500 nm de comprimento com índice de cristalinidade (CRI) entre 54 - 88 % [38]. Os nanocristais de celulose (CNCs) são frequentemente referidos como microcristais, bigodes, nanocristais, nanopartículas, microcristalitos ou nanofibras [36].
Nanopartículas de celulose, incluindo nanofibras e nanocristais, podem ser obtidas a partir da hidrólise ácida ou enzimática da celulose [34]. Os CNCs são constituídos de domínios cristalinos de celulose que apresentam diferentes e interessantes propriedades mecânicas, óticas e térmicas quando comparados com as estruturas celulósicas de maior dimensão. Isso acontece porque, com a extração da celulose em escala nanométrica, a maioria dos defeitos associados à estrutura hierárquica de um organismo vegetal pode ser removida, produzindo a base de construção para a preparação de uma nova geração de materiais, como os compósitos baseados em celulose [37].
A fonte principal para a extração dos NCCs é a polpa do eucalipto, no entanto, nos últimos cinco anos fontes alternativas como fibras de origem lignocelulósica a exemplo do bagaço de cana- de-açúcar, cascas de coco e de arroz, algodão, e até de resíduos de madeira de reflorestamento, descartada pela indústria têm sido bem exploradas [38]. Os nanocristais são de origem renovável, leves e biodegradáveis, levando vantagem sobre outros materiais sintéticos derivados do petróleo [39].
Na ocorrência de obtenção de nanocristais a partir de materiais lignocelulósicos, alguns trabalhos com as fontes precursoras podem ser citados: Barros [33] extraiu CNCs a partir do resíduo de tecido de fibra de algodão tingido com corante índigo, com e sem a realização de pré-tratamento para remoção do corante. A partir de imagens microscópicas (MEV) foi comprovada a obtenção de nanocelulose do tecido de algodão tingido com corante de índigo, tanto pelo processo da hidrólise quanto pela via enzimática. O interessante do estudo foi a visualização de diversos formatos dos CNCs a depender da metodologia de extração, em formato de agulhas, pela hidrólise ácida e em formato de esfera, pela hidrólise enzimática. No estudo de Camargo [40], avaliou-se o bagaço de cana de açúcar para a produção de nanocristais de celulose a partir da hidrólise enzimática. O bagaço foi submetido a dois tipos de pré-tratamentos e, hidrolisado com duas diferentes cargas enzimáticas utilizando um extrato enzimático comercial. Os CNCs obtidos apresentaram formato de agulha com comprimentos entre 193 - 246 nm e diâmetros entre 17 - 30 nm. Por outro lado, no estudo de Sá [10], obteve-se, pela primeira vez CNCs a partir da hidrólise ácida (H2SO4) da folha do abacaxi. A partir da análise de difração de raios X, os autores encontraram características dos cristais extraídos relacionadas com as estruturas da celulose tipo 1. Dentre as principais aplicações dos CNCs destacam-se desde a fabricação de cosméticos como na embalagem de alimentos. Também, no reforço de materiais plásticos e de cimento, na fabricação de tintas, em sensores da indústria de petróleo e gás e na indústria eletroeletrônica. Por outro lado, na área biomédica, bem como na engenharia de tecidos os CNCs são usados em curativos especiais, próteses e na fabricação de dispositivos transportadores de fármacos [39,42]. Os formatos de aplicação são variados entre filmes, cápsulas, esferas e filamentos, os quais são construídos por meio de diferentes técnicas, aplicáveis à escala laboratorial como evaporação de solvente, filmes automontados e eletrofiação.
Metodologias de extração dos CNCs da biomassa lignocelulósica
De acordo com Czaikoski [43], as metodologias tradicionais de extração dos CNCs podem ser divididas em tratamentos químicos, mecânicos e de dissolução, que podem ser estabelecidos em etapas separadas, sequenciais ou por combinação. A escolha do modelo dependerá da diferença do material nanofibrilar, da matéria-prima celulósica, do pré-tratamento realizado e do processo de desintegração próprio.
O modelo tradicional de extração consiste de três etapas: a primeira é o pré-tratamento, isto é, quaisquer tratamentos prévios ao método de isolamento, que elimina os componentes amorfos das fibras como hemicelulose e lignina; A segunda etapa é a hidrólise parcial que é realizada por ácidos ou enzimas para quebrar a estrutura das fibras em cristais; A terceira etapa é a desintegração mecânica, realizado pelo uso de forças de cisalhamento. Após essas etapas, consegue-se obter suspensões coloidais de nanofibras em água, que são estabilizadas pelas cargas negativas dos grupos aniônicos introduzidos durante uma etapa de hidrólise parcial.
O pré-tratamento é de extrema importância, uma vez que havendo uma melhor remoção de hemicelulose e lignina o isolamento da celulose será mais efetivo. A metodologia mais usada consiste na imersão da biomassa em meio alcalino diluído, submetido à alta pressão e temperatura. Nele, as ligações de hidrogênio da estrutura da rede são quebradas, removendo certas quantidades dos componentes amorfos, facilitando a posterior etapa de hidrólise. Soluções de hidróxido de sódio em concentrações de 5% p/v são comumente usadas.
Na etapa de hidrólise as fibras são misturadas com soluções de ácidos fortes, como ácido sulfúrico, ácido clorídrico ou uma mistura de ambos sob condições controladas de temperatura e tempo. Resultante deste processo, as regiões amorfas entre as microfibrilas de celulose são destruídas liberando os bastões de CNCs [44]. O ácido sulfúrico é comumente utilizado por produzir suspensões mais estáveis, devido às cargas negativas que são introduzidas na superfície dos cristalitos extraídos. Como registrado em diversos trabalhos, as condições da hidrólise que resulta nos maiores rendimentos da extração, em diversas biomassas lignocelulósicas envolvem concentrações do ácido em solução aquosa em torno de 30 - 65 % p, temperatura de reação em torno de 45 °C e tempos de reação entre 20 min a 4 h, [14,15,43,45]. Após essa etapa, a suspensão resultante é diluída e submetida à centrifugação com posterior descarte do sobrenadante. O material é submetido a uma etapa de diálise contínua em água, usando para isto membranas seletivas de celulose regenerada que removem os íons sulfitos do ácido, alojados na superfície dos CNCs.
No tratamento mecânico é utilizada a força ultra- sônica (banho ou sonicador) para dispersar os nanocristais e manter a suspensão uniforme. Os CNCs obtidos pela hidrólise com H2SO4 apresentam menor estabilidade térmica, mas exibem maior dispersão, pois os grupos sulfatos inseridos na molécula provocam a catálise da degradação térmica da celulose e, ao mesmo tempo são responsáveis pela redução da capacidade de aglomeração dos cristais, devido à repulsão eletrostática. Já os CNCs obtidos com HCl apresentam maior estabilidade térmica e alta tendência a formar aglomerados, devido aos resíduos do cloreto presentes na cadeia serem facilmente removidos durante a etapa de lavagem [46].
Na busca pela valorização da biomassa, “métodos verdes”, isto é, aqueles que resultam em uma diminuição considerável de emissões para o ambiente, de ácidos fortes, economia de água e energia são bem valorizados. Entre eles podem são destacados a hidrólise ácida com ácidos orgânicos [47-49], a oxidação usando persulfato de amônio (APS), a hidrólise com agua subcrítica e supercrítica [50,51], a hidrólise enzimática [52], a oxidação mediada por TEMPO [5] e a desintegração mecânica [53]. Detalhamento sobre estas metodologias são registrados no trabalho de Cidreira et al. [5], assim na sequência, serão destacadas as particularidades da oxidação usando APS e alguns resultados obtidos sobre a biomassa de açaí.
Extração dos CNCs através da oxidação da biomassa usando persulfatos de amônio. A oxidação da biomassa, usando persulfatos inorgânicos é considerada uma rota “verde” de extração dos nanocristais de celulose, visto que, além de usar agentes de baixa toxicidade, alta solubilidade na água e baixo custo, pelo processo, é dispensado o prétratamento da biomassa (remoção de extrativos e branqueamento), o que resulta em um ganho adicional em economia de água e energia.
Tradicionalmente, os persulfatos inorgânicos como o Persulfato de Amônio ((NH4)2S2O8, CAS: 7727-54-0), misturado com ácidos e bases fortes (ácido clorídrico, ácido sulfúrico, hidróxido de sódio e hidróxido de potássio) têm sido usados como agentes oxidantes fortes para o isolamento da lignina de materiais lignocelulósicos [54,55]. No entanto, Leung et al. (2012) destaca que o material resultante deste processo não são os cristais d) e celulose, mas a celulose branqueada.
A metodologia, que usa somente o persulfato de amônio para a extração dos nanocristais de celulose, a qual nomearemos aqui “método APS”, foi descrita e patenteada por Leung et al. [4,11], e posteriormente verificada por vários pesquisadores [12,56], inclusive pelos autores deste artigo. O método APS implica no tratamento da biomassa, usando apenas o reagente APS em solução aquosa a temperaturas e tempos superiores a aqueles estabelecidos na hidrólise ácida. Sendo uma metodologia recente, os parâmetros experimentais devem ser estudados e ajustados para cada biomassa. A grande vantagem da técnica é que pode ser aplicada sobre qualquer biomassa lignocelulósica, tanto de origem madeireira ou de gramíneas, com teores de lignina de até 20%, como os resíduos agrícolas. Por outro lado, a biomassa residual não requer prétratamento, isto é não há necessidade de remoção de extrativos, dos carboidratos e da lignina que acompanham a celulose, o que implica em uma grande economia de recursos hídricos e energéticos.
De acordo com Mascheroni et al. [12], assim que o regente APS entra em contato com a água, acontecem dois processos simultâneos, um de hidrólise e outro de oxidação. Estes eventos são presentes tanto na superfície como no interior da fibra, onde os ions SO-4 e H2O2, liberados durantes as reações removem a lignina da superfície e penetram através do lúmen da fibra atacando a parte amorfa da celulose, deixando os CNCs expostos.
O mecanismo de reação do APS em agua, de Kolthoff e Miller [57] descreve a formação dos agentes atuantes no processo:
Estagio 1: Formação de ânions de bisulfato e oxigênio atômico. Consiste de uma reação não catalisada onde dois radicais libres de sulfatos se formam e rapidamente desaparecem quando reagem com a água:
Estágio 2: Formação de tetróxido de enxofre e anions de bisulfato (Etapa de hidrólise). Neste caso, a reação é catalisada pela própria acidez atingida durante a formação dos agentes (o pH cai drasticamente). Existe ruptura das ligações axissimétricas O - O para formar estes componentes:
Estágio 3: Formação de peroxido sulfúrico (Etapa oxidativa). A formação do peroxido sulfúrico dependerá da concentração do APS na mistura reacional. Se a concentração for menor de 0,5 M, formara-se ácido sulfúrico, e o processo de extração dos CNCs continuará conforme a metodologia convencional, tendo assim uma eficiência bem menor, visto que não houve prétratamento da biomassa. No entanto, Gall et al. [58] e Beer e Muller et al. [59] encontraram que quando a concentração de APS é superior a 0,5 M, o tetroxido de enxofre formado continua reagindo com a água para formar o peroxido sulfúrico ácido (H2SO5) o qual é um reconhecido e patenteado agente deslignificante [54]:
A Figura 3 (adaptada de Cidreira et al. [5]) esquematiza os eventos de transformação da biomassa assim que o reagente APS entra em contato, decompondo-se na solução aquosa, formando os peróxidos, atacando diretamente as microfibrilas de celulose, destruindo a fase amorfa e expondo os CNCs
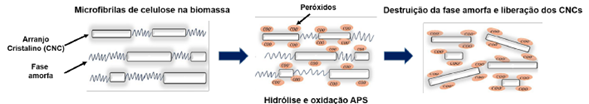
Adaptado de Cidreira et al. [5].
Figura 3 Representação esquemática do mecanismo de extração dos CNCs usando Persulfato de Amônio.
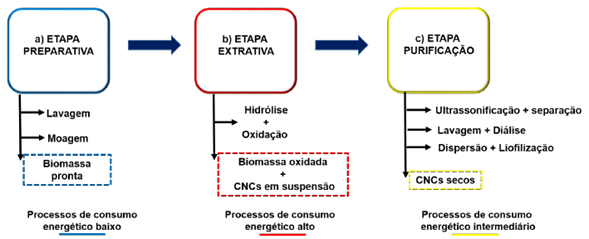
Experiências de extração de CNCs de biomassas lignocelulósica pelo método APS. Independentemente da origem da biomassa, o método APS se fundamenta nas etapas descritas na Figura 4: a) Etapa preparativa da biomassa; b) Etapa extrativa (ou oxidativa propriamente dita); c) Etapa de lavagem e purificação dos CNCs.
A etapa preparativa envolve a lavagem simples da biomassa para remoção dos açúcares e lipídeos decorrente da polpa (no caso da biomassa da agroindústria) e a moagem até a faixa granulométrica apropriada, o que irá depender do tipo de biomassa, entre 0,1 - 3 mm. A diferença da hidrólise ácida, esta etapa não implica na remoção previa dos extrativos orgânicos, da hemicelulose e da lignina da biomassa.
A etapa extrativa que envolve as reações químicas decorrentes do contato da biomassa com o agente APS em solução aquosa, catalisada pela temperatura, agitação e tempo de reação. Nesta etapa a fase amorfa da celulose é desintegrada liberando assim os arranjos cristalinos da mesma.
A etapa de purificação dos CNCs consiste na separação dos nanocristais da biomassa residual oxidada e da remoção dos íons sulfitos e óxidos depositados na superfície dos CNCs. Esta etapa é fundamental pois a eficiência da mesma impactará na qualidade e nas propriedades finais dos cristalitos e seu desempenho na aplicação
A depender da origem da biomassa, a etapa extrativa pode apresentar algumas variantes com respeito ao tempo necessário de reação, temperatura e concentração molar do APS em solução: Leung et al. [4], avaliaram o método APS com diversos materiais, os quais incluiram: celulose microcristalina Avicel PH102 da FMC Corp dos Estados Unidos, pó de celulose Whatman CFI (da Whatman Inc), linho e canas de linho (da Saskatchewan do Canadá), cânhamo de Quebec- Canadá, extrato de palha de tricale (da Agriculture and Afri-Food, Canadá que contém 54,5% de celulose, 12% de hemicelulose e 20% de lignina) e celulose bacteriana produzida na University of Western Ontario, Canada pelas bactérias gram- negativas Acetovacter xylinum BPR2001 (fibras de diâmetro 50 nm e grau de polimerização de 2.000 a 6.000). A biomassa como linho e cânhamo foi reduzida previamente em fragmentos de 2 - 3 mm de tamanho, na sequência, os autores misturaram a biomassa com a solução extrativa, na razão 0,1 g da biomassa em 10 mL de solução de APS de concentração 1 [M] e, aqueceram o sistema a 60 °C sob agitação vigorosa, durante 16 h. No caso da celulose bacteriana, o tempo de reação foi de 3 h. Ao término da reação, obteve-se uma suspensão branca sobrenadante, rica em CNCs e a biomassa residual precipitada no fundo, contendo também nanocristais ainda ligados. Procedeu-se com a separação da suspensão dos CNCs da biomassa residual com ciclos (4) de agitação/centrifugação/lavagem com agua ultrapura. Os autores observaram que tempos de reação prolongados e concentrações acima de 1 [M], conduziram a hidrólise excessiva o que diminuiu o rendimento dos CNCs. Por fim, após analises característicos que incluíram Microscopia de Força Atômica (MFA), Difração de raios X (PXRD), Espectroscopia de Fotoelétrons excitados por raios X (XPS) e a Espectroscopia de absorção no infravermelho (FTIR), os autores destacaram que os CNCs obtidos possuíam diâmetro inferior a 5 nm, especificamente, entre 3 - 4,9 nm, razão de aspecto L/D superior a 10, em torno de 12 a 60 um, índice de cristalinidade (CRI) entre 5 a 20% acima do índice de cristalinidade dos CNCs extraídos pela hidrólise ácida. Por outro lado, os CNCs obtidos foram mais uniformes, com uma distribuição de tamanho mais estreita e ainda de maior funcionalidade (acima de 8%) visto que a superfície resultou ativada com grupos funcionais carboxilados, o que facilita sua integração com outros materiais durante a formação de compósitos.
Mascheroni et al. [12], por sua vez extraíram CNCs de linter de algodão (da Innovhub, Itália) através de ambos os métodos, hidrólise ácida e APS. Os autores também trabalharam com um sistema reacional de concentração 1 [M] de APS onde foi introduzida a fibra a uma razão 10:1 g/L. A extração APS foi realizada a 75 °C, sob agitação constante por um período de 16 h, após o qual foi obtida a suspensão sobrenadante de CNCs. Na sequência, a suspensão contendo os CNCs foi separada da mistura através de 4 ciclos de agitação vigorosa (seja por banho ultrassom ou processador ultrassônico), lavagem com agua gelada e ultrapura e centrifugação, até que a suspensão atingiu o pH neutro (5 - 8), o qual é necessário para garantir sua completa dispersão no meio. Finalmente procederam a secagem dos CNCs via liofilização. Os autores recorreram às técnicas de Microscopia Eletrônica de Transmissão (MET) e Espalhamento Dinâmico da Luz (DLS) para definir a forma dos cristais e o tamanho, assim encontraram que, efetivamente estes possuíam forma de bastão, característicos dos nanocristais convencionais, e que a maior razão de aspecto (L/D) foi obtida para os CNCs extraídos pelo método APS (19,7 ± 8,0) ao invés de (16,4 ± 8,9), confirmado assim, o já reportado por Leung et al. [4]. Outro achado dos autores foi que não houve uma diferencia significativa na porcentagem de massa cristalina dos CNCs extraídos por ambos os métodos, neste caso, os valores, definidos pelas técnicas Difração de raios X (XRD), Ressonância Magnética Nuclear (RMN) e Espectroscopia de Infravermelho por Transformada de Fourier (FTIR) foram (62,6 ± 1,1)% para os CNCs_hidrólise ácida e (63,8 ± 1,2)% para os CNCs_APS. Também, os espectros FTIR dos autores registraram que os CNCs, extraídos pelo APS tinham grupos funcionais característicos dos grupos carboxílicos (C=O e COO-NH4+) o que indica o alto potencial de oxidação do método APS, o que, em consequência gerou uma energia livre de superfície 13,6% maior nos CNCs_APS em comparação com os CNCs_ hidrólise ácida. Assim os CNCs_APS tiveram mais facilidade de ancoragem com outros substratos durante a formação de compósitos. Em quanto ao rendimento da extração, os autores conseguiram extrair 34,4% de CNCs_APS e 53% de CNCs_ hidrólise ácida, e atribuíram esta diferença às condições da extração e ao processo de pós- tratamento da suspensão, também, foi colocada a possibilidade da ação continuada dos reagentes ácidos por um longo período de tempo, no método APS que pode causar a dissolução da celulose em cristalitos ou a formação de subprodutos [60]. Para avaliar a estabilidade térmica, os autores recorreram à Análise Termogravimétrica (TGA), a qual permitiu registrar que os CNCs pela hidrólise ácida tiveram menor temperatura de degradação e faixas de temperatura de degradação mais amplas em comparação com os CNCs_APS, o qual foi atribuído à introdução de grupos sulfatos e hidroxila na superfície das nanoparticulas durante a hidrólise ácida. Por fim, Mascheroni et al. [12], encontraram que os CNCs_APS tiveram melhor desempenho em aplicações de embalagem de alimentos produzidas com Politereftalato de etileno (PET), com propriedades de transparência, coeficiente de fricção, molhabilidade (wettability), ristalinidade dos filmes e resistência à água e ao oxigênio superior que com os filmes preparados com os CNCs obtidos da hidrólise ácida.
Zhang et al.[13], por outro lado, compararam os métodos de extração APS com a oxidação catalítica mediada pelo agente TEMPO e a hidrólise ácida, durante a extração de CNCs de sementes residuais de limão (Citrus limon), isto é a biomassa residual após a extração do óleo. Nesta oportunidade, foi realizado o prétratamento das sementes, pulverizando-as e realizando a remoção da hemicelulose e da lignina, de acordo com Dai et al. [61]. Posteriormente, a celulose seca de tamanho 149 μm foi submetida aos processos de extração dos CNCs. O processo de extração APS foi conduzido em condições similares a Mascheroni et al. [12], assim, foi mantida a proporção fibra/volume 10:1 g/L, a concentração de APS em 1 [M], a temperatura de 70 °C para um tempo de 14 h de reação. Ao término da reação, procedeu-se ao processo de separação, lavagem, diálise, dispersão e liofilização. Desta biomassa, os pesquisadores conseguiram extrair somente 13,03% de CNCs por esta metodologia, bem menor do que os 27,61% conseguido pela hidrólise ácida e 52,01% atingido pela oxidação TEMPO, os autores atribuiram o menor rendimento conseguido na oxidação APS às condições experimentais da extração, que no estudo não foram otimizadas [44]. Por outro lado, os autores destacaram as características, a seguir dos CNCs extraídos pelo método APS: que os CNCs apresentam grupos carboxílicos na superfície, resultantes da oxidação dos grupos hidroxila, o qual lhes comunicou maior estabilidade pela repulsão electrostática, como Leung et al. [11], registrou oportunamente; O alto índice de cristalinidade 74,40%, definido pela equação de Segal [62], para estes CNCs foi atribuído à maior decomposição da região amorfa da celulose durante a oxidação; Também, os nanocristais apresentaram maior estabilidade térmica (maior temperatura inicial e final de degradação, definida via TGA) e foi comprovada a sua aplicação na estabilização de emulsões Pickering, o qual foi atribuído ao maior índice de cristalinidade dos CNCs e ao menor comprimento dos mesmos 140 a 160 nm, visto que, em geral, entre menor o tamanho dos CNCs, mais fácil é a adesão das gostas de óleo para formar uma camada de emulsão, fazendo-a mais estável [63]. Desta forma os autores apontaram uma valiosa aplicação para os CNCs da semente de limão, como um potencial emulsificante “verde”, o qual pode ser utilizado nos processos de sínteses de polímeros via emulsão aplicados tanto para a área medica como alimentícia.
No nosso estudo, em andamento no Laboratório de Materiais Engenharia de Processos (LaMEP) da Coordenação de Engenharia Química da Universidade Federal do Maranhão (COEQ/ UFMA) as condições ótimas da extração foram estabelecidas com base em um planejamento estatístico, onde foi estudada a influência dos parâmetros experimentais sobre o rendimento da extração. Assim, realizando o processo de extração a uma razão 10:1 gfibra/L solução, a pressão atmosférica, em reator de 1 L com agitação contínua e banho de aquecimento controlado (como registrado na Figura 5), a influência da temperatura, concentração do reagente APS e tempo de reação sobre a porcentagem de CNCs extraídos foram avaliadas nas faixas de 60 - 80 °C, 0,5 - 2,0 [M] e 10 - 20 h, respectivamente. Um planejamento fatorial fracionário de resolução III com 3 pontos centrais (2k-1 + 3), totalizando 7 experimentos foi utilizado para o estudo [64], como registrado da Tabela 2. Como pode ser verificado, em nossa caracterização básica (Tabela 1), o conteúdo de celulose ? 52% p e de lignina ? 22 - 45% p da biomassa de açaí estudada (fibra do caroço de granulometria 38 ? φ ?250 μm) é comparável com aquelas biomassas para as quais o método de oxidação APS se mostrou eficiente [4]. Com o auxílio do software Statistica 7.0 (StatSoft) e os resultados de rendimento, obtidos nos experimentos foi possível visualizar três cenários de condições experimentais com desempenho suficiente para a extração dos CNCs: Cenário 1 (Figura 6a) para um tempo de reação de 10 h; Cenário 2 (Figura 6b) onde o tempo de reação é de 15 h e Cenário 3 (Figura 6c) onde o tempo de reação é de 20 h, onde, em todos os cenários houve variação da temperatura e concentração do reagente.

Figura 5 Montagem experimental para a extração dos CNCs pelo método APS. [1] Agitador; [2] Sistema reacional; [3] Banho de aquecimento.
Tabela 2 Rendimentos da extração dos CNCs da fibra de açaí pelo método APS.
| Experimento | T(°C) | C (M) | t (h) | Rendimento* da extração (% p) embase seca da fibra “in natura” |
|---|---|---|---|---|
| 1 | (-1) 60 | (-1) 0,5 | (+1) 20 | 35,72 |
| 2 | (-1) | (+1) 2,0 | (-1) 10 | 46,13 |
| 3 | (+1) 80 | (-1) | (-1) | 39,89 |
| 4 | (+1) | (+1) | (+1) | 45,47 |
| 5 | (0) 70 | (0) 1,25 | (0) 15 | 39,33 |
| 6 | (0) | (0) | (0) | 53,55 |
| 7 | (0) | (0) | (0) | 46,44 |
(*): Rendimentos calculados considerando diferença (massa da fibra residual - massa inicial seca)/ massa inicial seca. Os valores entre parêntesis (-1), (0) e (+1) representam, respectivamente os níveis mínimo, central e máximo das variáveis.
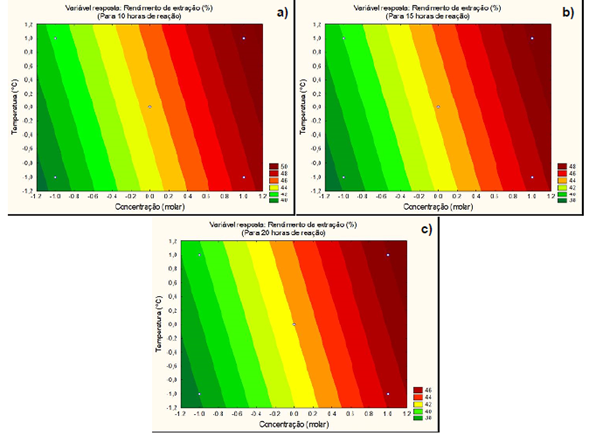
Figura 6 Gráficos de superfície de resposta mostrando a influência da concentração do reagente e da temperatura de reação para um tempo constante de 10 h, 15 h e 20 h, respectivamente. Os valores entre parêntesis (-1), (0) e (+1) representam, respectivamente os níveis mínimo, central e máximo das variáveis.
De acordo com os gráficos de superfície de resposta (onde os valores (-1), (0) e (+1) representam, respectivamente os níveis mínimo, central e máximo das variáveis), o maior rendimento da extração, em torno 50% foi obtido para a condição de C 2,0 [M], t de 10 h e T de 80 °C (Cenário 1). No entanto, pode-se observar que operando a uma temperatura menor (por exemplo 70 °C) e a partir da concentração no ponto central (1,25 M) para um tempo de reação um pouco acima de 10 h (Figura 6b e Figura 6c), atingem-se rendimentos próximos do máximo observado aqui 44 - 48 % p. É pertinente considerar esta avaliação, quando se pensa na economia do processo pelo menor consumo energético. Por outro lado, devem-se considerar as condições usadas em experiências sucedidas já reportadas como as de Leung et al. [4], Mascheroni et al. [12], Zhang et al. [13] para os quais foram recomendadas condições de operação entre 0,5 - 2,0 [M], 60 a 80 °C e 5 a 24 h para biomassas lignocelulósicas de origem das gramíneas. Desta forma, da análise dos perfis gerados neste estudo, recomenda-se a extração dos CNCs da biomassa de açaí (fibra), em aparelhagem experimental de bancada, de forma contínua nas condições: Concentração de 1,0 - 2,0 [M], tempo de reação de 10 - 12 h e Temperatura de 60 - 70 °C. A Figura 7 apresenta amostras dos CNCs purificados e secos extraídos a 60 °C, 70 °C e 80 °C com concentração constante de 1,25 [M] durante 12 h de reação. A Tabela 3 vem a complementar o resumo reportado em Zhang et al. [13], sobre as condições experimentais de extração de CNCs de acordo com o tipo de biomassa.

Figura 7 CNCs extraídos da fibra de açaí de granulometria (38 - 125) μm a 60 °C, 70 °C e 80 °C a 1,25 [M] durante 12 h, através do método APS.
Tabela 3 Condições de extração de CNCs e rendimento de acordo com o tipo de biomassa usando a oxidação APS.
| Biomassa | Conteúdo de celulose % p | Condições da extração recomendada | Rendimento % p | Referência |
|---|---|---|---|---|
| Pó de fibra de açaí (38- 250) μm | 52,56 | 1,25 [M]; 70 °C; 12 h | (44 - 46)* | Este estudo |
| Celulose da semente de limão (149) μm | 99 | 1,0 [M]; 75 °C; 14 h | 13,02# | Zhang et al. [13] |
| Linters de algodão (Innovhub) | 99 | 1,0 [M]; 75 °C; 16 h | 34,4 | Mascheroni et al. [12] |
| Linho e cana de linho (2000 - 3000) μm | - | 1,0 [M]; 60 °C; 16 h | 28 e 22, respectivamente | Leung et al. [4] |
| Polpa de madeira | - | 1,0 [M]; 60 °C; 16 h | 36 | Leung et al. [4] |
| Bagaço de cana de | - | 1,0 [M]; 60 °C; 16 h | 26,6 | Leung et al. [4] |
| Linters de algodão | 100 | 1,0 [M]; 60 °C; 16 h | 81 | Leung et al. [4] |
| Extrato de palha de | 54,50 | 1,0 [M]; 60 °C; 16 h | 31 | Leung et al. [4] |
(*): Rendimentos calculados considerando diferença (massa da fibra residual - massa inicial seca) / massa inicial seca. (#) Rendimento medido com base na massa inicial da celulose seca.
Por outro lado, embora a etapa de purificação dos CNCs envolve ciclos de lavagem e centrifugação, não há um número definido destes ciclos, pois dependerão do método de extração e reagente utilizado. O processo deve conduzir à remoção de impurezas dos reagentes e do ácido remanescente, o que leva à neutralização da suspensão dos cristalitos e a dispersão dos mesmos. De acordo com Meng et al. [14], mesmo que os íons sulfatos, formados durante a extração conduzam a formação de suspensões aquosas estáveis dos CNCs, estes grupos não devem estar presentes na superfície dos cristalitos, especialmente se estes são usados como reforço em compósitos, visto que os CNCs inseridos na matriz polimérica promoveriam uma baixa estabilidade térmica a altas temperaturas. Isto porque os grupos sulfatos, com o calor geram reações de desidratação da celulose e na sequência, diminuição do peso molecular, pela formação de cadeias curtas de celulose, resultando em energias de degradação térmicas bem baixas [65,67].
Para a purificação dos CNCs extraídos da biomassa do açaí pela oxidação APS, em particular foi definido um procedimento de separação e purificação, baseado nos procedimentos descritos em Zhang et al. [13], Jiang et al. [68] e Pinheiro et al. [25]. As etapas do procedimento são apresentadas, a seguir:
Etapa c.1. Cumprido o tempo da extração, deve- se adicionar água ultrapura gelada na mistura reacional com o intuído de interromper o avanço das reações. A consequência disto, formam-se duas faces, o precipitado constituído pela fibra residual e o sobrenadante que consiste da suspensão, rica em CNCs. É importante observar que em ambas as fases existe presença dos cristalitos, por isto, após a separação, ambas devem ser tratadas para promover a liberação dos CNCs.
Etapa c.2. Tratamento da suspensão. Foi seguida uma sequência de agitação em banho ultrassom por 15 min, para promover separação dos CNCs e posterior centrifugação por 10 min, a uma velocidade de 6.000 rpm, com o intuído de gerar duas fases, os CNCs no precipitado e as impurezas no sobrenadante. Retirou-se o precipitado (contendo os CNCs), o qual foi reservado para posterior diálise, entanto que o sobrenadante continuou a ser lavado agregando-se mais agua ultrapura para promover a precipitação dos CNCs ainda suspensos, adicionalmente verificou-se o pH da suspensão para o controle de neutralidade. O ciclo (agitação no banho ultrassom) ? (centrifugação) ? (separação das faces) continuou até que foi observado um valor de pH de 5,0, aproximadamente no sobrenadante (entre 5 a 6 ciclos de lavagem). Os CNCs, do precipitado obtido a cada sequência de lavagem foram dissolvidos em agua gelada e dispersos usando uma sonda ultrassónica por 5 min, posteriormente foram sujeitos a diálise em tubos de celulose regenerada com capacidade de separação de (cut off 12.000 - 14.000) Mw, durante 3 a 4 dias com troca contínua da agua de lavagem, a cada 2 h, conforme instruções do fabricante (Exemplos de marcas de membranas para tal proposito, disponíveis no mercado brasileiro são SERVA - SERVAPOR dialysis tubing, 44148.01 e INLAB - saco de diálise 133). Com a diálise, foi finalizada a purificação dos CNCs, atingindo-se um pH da suspensão entre 5,5 e 6,5. Após este processo, procedeu-se a secagem dos CNCs via liofilização. A Figura 8 apresenta a sequência do processo de purificação em imagens. Outros métodos de purificação dos CNCs podem envolver filtração, usando papel de filtro Whatman 541 ou filtros de microfibra de vidro, de acordo com o procedimento descrito por Lu e Hsieh [69], e Besbes, Alila e Boufi [70].
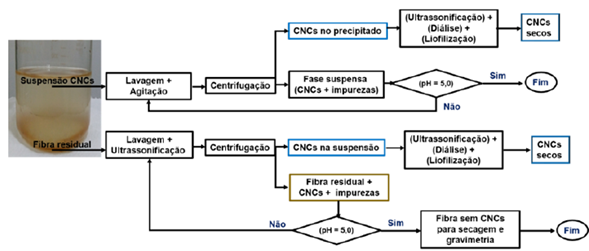
Figura 8 Processo de separação e purificação dos CNCs produzidos após a oxidação APS da biomassa de açaí.
Etapa c.3. Tratamento da fibra residual. Procedeu-se à lavagem da face concentrada em fibra residual, derivada da Etapa c.1, adicionando água destilada ou ultrapura gelada. Procedeu-se a agitação com sonda ultrassónica por 5 a 10 min para promover a liberação dos CNCs ainda aderidos às fibras. Procedeu-se à centrifugação suave a 3 500 rpm por 5 min e posterior separação do sobrenadante (contendo os CNCs) que continuaria para a posterior diálises e liofilização, como relatado na Etapa c.2. Repetiu-se a sequência (Ultrassonificação da fibra) ? (centrifugação) ? (separação da face suspensa) até o sobrenadante atingir o pH de 5.0. Comparado com o tratamento da suspensão (Etapa c.2) esta etapa deve ser bem mais rápida, isto é, com 2 a 3 ciclos de lavagem da fibra se consegue atingir o pH desejado, visto que a fase fibra não retém íons sulfitos. Por fim, a fibra residual completamente lavada, livre de CNCs foi seca em estufa a vácuo para contabilização dos rendimentos da extração.
Métodos de caracterização dos CNCs
A caracterização básica e especializada dos CNCs busca, principalmente avaliar a sua qualidade em termos de tamanho, razão de aspecto, pureza (íons residuais do processo de extração), dispersão e cristalinidade. Também, a depender destas propriedades, busca-se apontar aplicações, seja como reforço em compósitos poliméricos ou na formação de membranas carreadoras de remédios na área médica ou como agentes estabilizadores de emulsões poliméricas [5,13,25].
As metodologias de caracterização predominantes para a análise dos CNCs, independentemente da fonte e do método de extração devem incluir: Espectroscopia no Infravermelho por Transformada de Fourier (FTIR); Calorimetria Diferencial de Varredura (DSC); Analise Termogravimétrica (TGA); Difração de raios x (DRX); Microscopia Eletrônica de Transmissão (MET); Microscopia de Força Atômica (AFM); e Espectroscopia de Ressonância Magnética Nuclear (NMR). Por outro lado, metodologias alternativa como a análise reológica das suspensões têm cobrado força, toda vez que permitem complementar a caracterização, e em particular são mais acessíveis, rápidas e econômicas [15,71-74].
Espectroscopia FTIR. A estrutura molecular é responsável pelas diferentes propriedades moleculares, e por esta razão seu conhecimento é de grande importância. A espectroscopia vibracional constitui uma ferramenta poderosa para determinar grupos funcionais alojados na superfície do material, para identificar a conformação e estruturas de moléculas e para a obtenção do espectro vibracional completo da molécula, isto é a identificação de substâncias. Tradicionalmente, a espectroscopia FTIR, tem sido a técnica mais usada para a identificação de materiais poliméricos constituintes, por exemplo de embalagens plásticas, rígidas e flexíveis, organizados como monocamada ou com multicamadas [75].
Considerando que técnica permite identificar grupos funcionais presentes na superfície do material, a mesma tem sido de grande utilidade para confirmar a eficácia do prétratamento alcalino e do branqueamento, na remoção da lignina e de outros componentes estruturais, como hemicelulose e carboidratos de menor peso molecular, presentes nas fibras que serão submetidas a hidrólise ácida [76,78].
Considerando as particularidades das fibras, onde por um lado tem-se propriedades hidroscópicas e isolantes, e por outro lado, possui grupos funcionais orgânicos e inorgânicos, além da tecnologia convencional de análise, a tecnologia de Refletância Total Atenuada (ATR) é fundamental para a melhor visualização das bandas pertencentes às fibras in natura e pré-tratadas. Na tecnologia convencional, dois feixes de luz incidem por separado sobre a amostra, dissolvia em Brometo de Potássio KBr e, a depender da natureza e características dela serão absorvidas as frequências específicas de energia. No caso da tecnóloga ATR é dispensada a preparação da amostra, pois esta é colocada diretamente sobre um cristal opticamente denso com alto índice de refração. Desta forma o método busca aprimorar a transmissão visando obter espectros mais nítidos. Os equipamentos de detecção, em geral, operam e condições de Resolução 2 cm-1; Número de scans 40; Varredura 400 a 4000 cm-1; Apodização Happ-Genzel; amostra no formato de pastilha dissolvida em KBr (tecnologia convencional) ou pura, na análise por ATR.
No caso específico da análise de CNCs, Leung et al. [4], Mascheroni et al. [12] e Zhang et al. [13] usaram a técnica para identificar as bandas de absorção típicas dos CNCs extraídos de diversas fontes de biomassa, pela oxidação APS, como linho, linters de algodão e celulose da semente de limão, respectivamente. Também, os ensaios permitiram identificar o tipo de celulose predominante, como a Tipo Iα nos CNCs derivados da biomassa da agro-fibra e Tipo Iα na celulose bacteriana. Por outro lado, Pinheiro et al.[25] utilizou a técnica para detectar grupos funcionais característicos, na superfície dos CNCs após o tratamento com isocianato de octadecil, visando melhorar as propriedades reológicas e mecânicas dos seus nanocompósitos construídos com a matriz de poli(butileno adipado co-tereftalato).
Calorimetria Diferencial de Varredura (DSC) e Analise Termogravimétrica (TGA). São técnicas complementares que permitem avaliar a estabilidade térmica dos CNCs através do monitoramento da perda de massa e variação de fluxo de calor entre a amostra dos CNCs e uma amostra de referência, quando ambas são submetidas a um aquecimento ou resfriamento controlado, em ambiente oxidante (O2, ou CO2) ou inerte (N2, Árgon ou H2). Condições típicas da análise incluem uma varredura de temperatura desde 25 °C até 500 °C a uma velocidade de aquecimento de 10 °C/min. Em particular, análises de TGA e DSC simultâneas foram realizadas neste estudo nos CNCs extraídos por ambos os métodos, hidrólise ácida e oxidação APS, desde a fibra do caroço do açaí pré-tratada e in natura, respetivamente. Os testes, foram realizados em um analisador combinado DSC/TGA da NETZSCH (modelo STA 449C), pertencente ao Laboratório do Departamento de Física do IFMA-São Luis. As amostras foram aquecidas na faixa de 20 - 500 °C a uma velocidade de 10 K/min em atmosfera inerte. O tamanho da amostra oscilou em 5,3 mg. As Figuras 9 e 10 representam, respectivamente os termogramas DSC e TGA geradas das análises, e a Tabela 4 resume as características dos principais eventos térmicos visualizados.
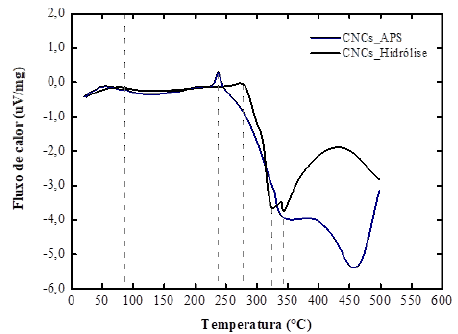
Figura 9 Comparação das curvas DSC dos nanocristais extraídos pela hidrólise ácida e pelo método APS.
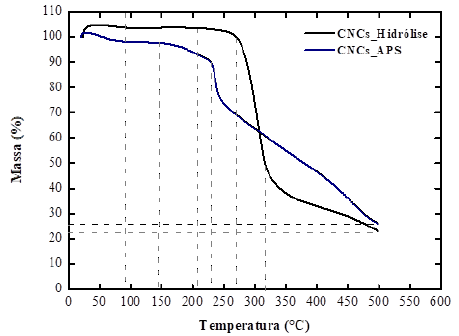
Figura 10 Comparação das curvas TGA dos nanocristais extraídos pela hidrólise ácida e pelo método APS.
Tabela 4 Resumo dos eventos térmicos observados das análises de DSC e TGA nos CNCs produzidos.
| Evento | CNCs_Hidrólise | CNCs_APS |
|---|---|---|
| Evaporação de unidade na superfície | 90 °C | 90 °C |
| Porcentagem de massa perdida pela evaporação | ~ 2,0% | ~ 2,0% |
| Temperatura inicial de degradação | 278,1 °C | 237,6 °C |
| Temperatura final de degradação | (317 - 325) °C | 343,0 °C |
| Pirólise dos nanocristais de celulose (evento exotérmico | (278,1 - 325) °C | (237,6 - 343,0) °C |
| Quebra de ligações glicosídicas, depolimerização e formação | (325 - 500) °C | (343 - 500) °C |
| de carbono residual | (endotérmico) | (exotérmico) |
| • Porcentagem de massa de material de carbono residual (Char residue) | 23,2% | 26,5% |
Como pode ser observado nas figuras ambas as amostras de CNCs exibem uma perdida de massa equivalente a 2,0 % devido aos efeitos de evaporação de umidade na superfície dos cristais. No intervalo de 100 - 200 °C é evidenciada a mobilidade molecular dos cristais (Transição vítrea) sem perda de massa. Na faixa de 230 - 340 °C, observa-se a maior perda de massa, caracterizada pela degradação da celulose (pirólise) e por fim, entre 325 - 500 °C aconteceram os fenômenos de depolimerização, onde são gerados componentes de baixo peso molecular, quebra de ligações glicosídicas e formação de material carbonáceo [13]. Mascheroni et al. [12] atribuíram a formação do carbono residual até os 500 °C aos grupos sulfatos presentes na superfície dos CNCs, principalmente quando extraídos pela hidrólise, também os autores relatam que a presença de grupos hidroxila e sulfatos conduzem a uma menor temperatura inicial de degradação e a faixas mais largas de degradação. Neste estudo em particular, os CNCs obtidos pelo método APS tiveram temperaturas menores de degradação, comparadas com as obtidas para os CNCs_ hidrólise, o que contradiz os resultados dos autores, no entanto, é pertinente lembrar que os CNCs_APS foram extraídos da biomassa sem prévio prétratamento, assim resíduos de açúcares, taninos e lipídeos, característicos do açaí podem estar acelerando a degradação, gerando também maiores resíduos carbonáceos. Por fim, se bem os termogramas DSC e TGA exibem tendências correspondentes até os 100 °C aproximadamente, é evidente que as pequenas diferenças observadas, a partir deste ponto se atribuem ao método de extração dos CNCs. Em particular, na fase final da degradação, até os 500 °C aconteceram reações de consumo de calor para os CNCs_hidrólise e liberação de calor para os CNCs_APS, o que pode ser atribuído aos reagentes utilizados e resíduos sobre os cristalitos.
Difração de raios X (DRX). Pela técnica é possivel quantificar o porcentual de cristalinidade dos CNCs. Esta se fundamenta no espalhamento coerente da radiação X, por estruturas organizadas (cristais), permitindo realizar estudos morfológicos em materiais, determinando sua estrutura cristalina e sua fração cristalina [79]. Assim, ao incidir um feixe de raios X em um cristal, o mesmo interage com os átomos presentes, originando o fenômeno de difração. A difração de raios X ocorre segundo a Lei de Bragg (Equação 1), a qual estabelece a relação entre o ângulo de difração e a distância entre os planos que a originaram, característicos para cada fase cristalina. Na Equação 1, n: número inteiro, λ é o comprimento de onda dos raios X incidentes, d é a distância interplanar e θ é o ângulo de difração [80]. Em geral, condições de operação para a definição da fração cristalina dos CNCs são de 45 kV e, os dados são adquiridos em uma escala 2Ɵ entre 5 - 40 °C. A partir das curvas de difração de raios X o grau ou fração cristalina é calculada da leitura das curvas de difração de raios X em função da razão da área cristalina com respeito a área total do difratograma. Jiang et al.[68], por exemplo encontraram picos de difração a 16,4 °C, 22,5 °C e 34,4 °C típicos da celulose Tipo I nos CNCs extraídos pela oxidação APS e pela hidrólise ácida de resíduo de papel de jornal. Também, os autores reconheceram a forma de ataque do ácido sulfúrico sobre a estrutura amorfa da celulose, calcularam a cristalinidade, o tamanho dos cristalitos e o espaçamento das células. Por fim avaliaram a pureza dos CNCs e concluíram que é possível extraí-los desta biomassa, com alta qualidade sem a necessidade de realizar destintamento prévio do papel.
Microscopia Eletrônica de Transmissão (MET). A Microscopia Eletrônica de Transmissão (MET) é uma técnica de alta resolução que permite a observação de aspectos microestruturais de amostras de diversos materiais. A morfologia interna e aspectos de estruturas cristalinas com dimensões de 0,1 mm - 0,3 nm podem ser analisadas com um aumento de 100x - 500000x [81]. Essa alta resolução é atingida porque ao invés de usar a luz visível, a MET utiliza um feixe de elétrons altamente energizados no vácuo. Como o elétron possui dimensões menores que o átomo, esse tipo de microscópio é capaz de mostrar detalhes em um nível subatômico, para isso, ele usa a intensidade de elétrons como intensidade luz com o auxílio de um computador que capta as imagens [82]. De acordo com Jr. [81] a operação do MET é iniciada com a geração de um feixe de elétrons que são acelerados em uma coluna de alto vácuo na direção da amostra. Em seguida, lentes eletromagnéticas e aberturas metálicas transformam o feixe de elétrons em um feixe monocromático que é focado sobre o material. Quando o feixe monocromático incide sobre a amostra, acontece diversos tipos de interações entre os elétrons incidentes e os elétrons do átomo do material como difração, absorção, mudança de fase e transmissão. Os elétrons transmitidos são focados por uma lente objetiva em uma imagem e contribuem para iluminação e resolução, já que o feixe de elétrons tem comprimento de onda da ordem de Angstrons. Já os elétrons que sofrem outros tipos de interação, como os difratados, são essenciais para dar contraste à imagem.
A técnica de MET pode ser utilizada para confirmar a existência de CNCs, estimar e quantificar a razão de aspecto e observar suas características estruturais [83]. Assim como em outros tipos de polímeros, a preparação de amostras de CNCs requer recobrimento metálico para melhorar o contraste da imagem porque o seu número atômico baixo dificulta o espalhamento de elétrons [84]. Suspensões de CNCs com concentração de 0,01 a 0,5 mg/mL devem ser empregadas para a caracterização com MET para garantir que os nanocristais possam ser observados individualmente [83]. Além disso, sonificação com ultrassom de ponta por 10 min é recomendado para melhor dispersão de NCCs. As dimensões dos nanocristais de celulose são afetadas por diversos parâmetros dos métodos de extração. Assim, a MET é uma técnica de caracterização poderosa para determinar as melhores condições de extração de acordo com a aplicação do nanomaterial.
Zhang et al. [85] avaliou a influência da concentração de persulfato de amônio (1, 1,5 e 2 M) nas dimensões de CNCs obtidos do bagaço de cana-de-açúcar branqueado. Com as imagens foi possível observar uma diminuição tanto no comprimento quanto no diâmetro dos CNCs com o aumento da concentração de reagente. Para a concentração de 1 M de persulfato de amônio o comprimento dos CNCs variou de 300 - 2200 nm e o diâmetro de 20 - 109 nm. Para concentração de 2 M foram obtidos CNCs com 140 - 500 nm de comprimento e 8 - 20 nm de diâmetro. Rohaizu e Wanrosli [86], também usaram MET para verificar se a oxidação com TEMPO seguida de sonificação produzia CNCs. As imagens revelaram que celulose nanocristalina com aspecto de bastão, com comprimento de 122 nm e largura de 6 nm, foi obtida após o tratamento de oxidação e sonificação. Uma das desvantagens relacionada a MET é o dano estrutural e químico causado pela incidência de elétrons altamente energizados. Quando o feixe de elétrons incidente sofre um espalhamento inelástico (com perda de energia), a estrutura cristalina pode ser danificada e a amostra pode não ser mais representativa do material de origem [82]. No entanto esse tipo de interação fornece informações importantes como estrutura interna e composição.
Microscopia de Força Atômica (MFA). A Microscopia de Força Atômica é uma técnica de varredura de força de alta resolução que permite obter informações da superfície de materiais em micro e nano-escalas em diferentes meios como ar, vácuo e líquido [81]. O princípio de operação da MFA consiste da aplicação de um cantilever, uma haste flexível com uma pequena agulha na dimensão de mícron capaz de interagir com a amostra por diferences forças [84]. A agulha do cantilever interage com a mostra e o cantilever deflete agindo como uma mola. O movimento do cantilever varia entre distâncias de mícron a 0,1, e com um sensor de deflexão assim, uma imagem não destrutiva da amostra é construída [87].
Os tipos de forças atrativas que aproximam a ponta do cantilever à amostra podem ser de natureza física, como capilaridade e interação de van der Waals, ou química, pela interação entre grupos funcionais da amostra. Já as forças repulsivas responsáveis pelo afastamento da agulha acontecem devido à interação coulômbica [81].
De acordo com Meyer [87], os dois tipos de operação da MFA podem dar diferentes informações sobre a amostra analisada. No modo contato, onde a agulha está a menores distancias em relação a amostra (na ordem de Angstrons), é possível obter imagens de alta resolução da topografia de superfície da amostra. Quando o microscópio atua no modo de não-contato, a distância entre o a agulha do cantilever e a amostra é da ordem de nanômetros, o que não fornece alta resolução, mas ainda mostra detalhes topográficos, distribuição de cargas e distribuição de filmes em líquidos.
A MFA é uma técnica importante para caracterização de NCCs, pois ela usa um método que não interfere na medição e que permite obter as dimensões representativas do material. Zhou et al. [88] caracterizou o comprimento e largura de NCCs da celulose microcristalina e da polpa de celulose branqueada extraídas pela oxidação com TEMPO. Neste trabalho foram utilizadas as imagens de altura obtidas com a MFA, onde a largura foi definida com a maior altura medida em cada nanocristal individual, utilizando o software NanoScope Analysis 1.70, e o comprimento foi mensurado pelo software ImageJ. Para obter dimensões representativas foram feitas entre 74 e 100 medições de largura e entre 640 e 817 medições de comprimento de independentes e diferentes nanocristais.
A partir das imagens MFA, Zhang et al. [13] determinaram os comprimentos médios dos CNCs obtidos pela oxidação TEMPO, oxidação APS e pela hidrólise ácida da celulose da semente de limão. Assim, os autores definiram comprimentos de 344,5 nm, 136,2 nm e 125,2 nm respectivamente.
Outra propriedade importante que pode ser obtida pela MFA é a rugosidade de filmes nanocompósitos com CNCs, que está relacionada com a dispersão dos nanomaterias na matrix polimérica. Deepa et al. [89], mostrou através da avaliação da rugosidade obtida pelas imagens de MFA que o tratamento de sonificação e oxidação com TEMPO de filmes com alginato e nanoceluloses melhora a dispersão dos NCCs, formando filmes mais homogêneos.
Espectroscopia de Ressonância Magnética Nuclear (RMN). A Espectroscopia de Ressonância Magnética Nuclear é uma técnica que fornece informações detalhadas de composição química e configuração e conformação de moléculas. Assim, ela fornece informação sobre as massas relativas do material cristalino e amorfo [12] Na RMN de próton (H+) a intensidade dos sinais pode ser relacionada diretamente com o número de núcleos de átomos presentes, o que permite uma análise quantitativa dos componentes. Já com a análise de RMN de 13C essa relação nem sempre é obedecida e a análise quantitativa é mais difícil. No entanto, as ressonâncias do 13C estão espalhadas em uma área muito maior, o que confere a essa técnica uma alta resolução. O princípio da RMN está baseado na característica de alguns núcleos de se alinharem a um forte campo magnético externo, causando alterações energéticas. Os sinais de ressonância são classificados de acordo com a sua intensidade, assim, sinais mais fortes indicam a presença em abundância de um componente na molécula, enquanto sinais mais fracos representam substâncias em menor concentração [90].
A análise de nanocristais de celulose é feita com os sinais gerados pelos carbonos C1, C4 e C6 da cadeia de celulose. O carbono C1 apresenta formas complexas de acordo com a fase cristalina em que se encontra, já os carbonos C4 e C6 se separam em duas distribuições referentes as partes cristalinas, entre 89 e 65 ppm, respectivamente e partes amorfas, entre 85 e 62 ppm, respectivamente [83]. Por outro lado, a modificação química de CNCs pode ser confirmada e quantificada pela técnica de RMN. Perez et al. [91] observou as mudanças apresentadas nos sinais dos carbonos C5 de 79,2 para 76,1 ppm e C6 de 60,8 para 175,3 ppm de amostras oxidadas em relação a amostras não- oxidadas, confirmando a introdução de grupos carboxílicos na superfície da cadeia de celulose. Como relatado anteriormente (item 3.4.1) Mascheroni et al.[12] não encontraram diferenças significativas no conteúdo de massa cristalina dos CNCs extraídos pela hidrolise ácida (62,6 %) e pela oxidação APS (63,8 %), em ensaios realizados a condições padrão de temperatura ambiente, em amostras de tamanho 100 mg pressurizadas dentro de um rotor de ZrO2 de 4 mm, obtendo os espectros de 13C a 150,9 MHz e H+ a 75,7 kHz durante 3,4 min e relaxação de 2 s.
Considerações finais
O aproveitamento da biomassa residual do açaí mostra-se como uma alternativa para a redução do impacto ambiental causado pelo elevado volume de resíduo orgânico decorrente do despolpamento do fruto. Por sua natureza lignocelulósica e pela alta produção e consumo do fruto, a biomassa residual do açaí tem enorme potencial para produzir celulose e seus nanocristais, uma vez que após o processo de despolpamento, em torno de 80% da massa do fruto é o resíduo gerado. Embora a extração pela hidrólise ácida seja a metodologia mais simples e econômica de operar, algumas desvantagens devem ser apontadas, tais como a corrosão dos equipamentos, devido à ação dos ácidos fortes, poluição ambiental e ainda a deposição de grupos sulfatos na superfície dos CNCs, que interferem na estabilidade térmica dos compósitos onde estes materiais participam.
Registros na literatura, e estudos dos próprios autores, conduzidos até os dias atuais, têm demonstrado que a metodologia de extração por oxidação, usando Persulfato de Amônio é mais eficiente, por ser ambientalmente amigável (não envolve ácidos fortes), requerer menor esforço energético (sem pré-tratamento da biomassa e uma única etapa de processo) e, principalmente porque as propriedades finais dos CNCs obtidos são superiores, tanto em índice de cristalinidade e massa cristalina extraída, como na razão de aspecto e estabilidade térmica. Embora a oxidação APS envolva maiores tempos de reação, temperaturas de processamento superiores e, ainda que, durante o processo são produzidos resíduos ácidos (ions sulfatos, sulfitos e bissulfatos) o processo é considerado dentro das metodologias “verdes” por ser mais sustentável, por usar menos solventes e ainda pela maior qualidade dos CNCs extraídos.
Por outro lado, a oxidação APS tem-se apresentado comercialmente mais viável para obter CNCs com uniformidade, cristalinidade aprimorada, com diâmetro menor e uniformes, com uma distribuição granulométrica restrita, a diferença dos processos convencionais que requerem técnicas de pós- separação para melhorar a uniformidade e, em termos gerais, a qualidade dos CNCs. Além disso, a extração com APS, tem produzido altos rendimentos e os CNCs resultantes possuem grupos carboxilados na superfície, com 8% ou mais de funcionalidade, tornando-os mais reativos e aprimorando sua flexibilidade e capacidade de processamento em compósitos. Em contraste, pela extração por hidrólise ácida são produzidos CNCs contendo apenas grupos hidroxila (quando o HCl é utilizado) ou apenas 2% de grupos sulfonila (quando H2SO4 é utilizado). A Tabela 5 oferece um comparativo das condições operacionais de cada metodologia permitindo visualizar as vantagens e desafios tecnológicos de cada uma.
Tabela 5 Revisão comparativa das condições operacionais de extração dos CNCs pela hidrólise ácida e oxidação APS.
| Critério | Hidrólise Ácida | Oxidação APS |
| Reagentes utilizados | Ácido Clorídrico (HCl), Ácido Sulfúrico (H2SO4), Hidróxido de Sódio (NaOH) e Ácido Nítrico (HNO3). | Preferencialmente persulfato de amônio ((NH4)2S2O8); ou ainda persulfato (K2S2O8) de potássio e persulfato de sódio (Na2S2O8) (ou uma mistura destes). |
| Pré-tratamento da biomassa | 1° etapa - Moagem e lavagem; 2° etapa - Renoção de extrativos totais; 3° etapa - Deslignificação alcalina; 4° etapa - Branqueamento; 5° etapa - Hidrólise Ácida. | Apenas uma etapa onde a acontece simultaneamente a dissolução de lignina, hemicelulose, pectina e outros conteúdos de biomassa vegetal |
| Temperaturas envolvidas | Lavagem e secagem: 70 °C; Deslignificação - dois ciclos de 127 °C Branqueamento: 70 °C Hidrólise ácida: em torno de 45 °C | Faixa de (60 - 80) °C |
| Tempos envolvidos | Moagem: 10 min; Lavagem: 2 h; Renoção de extrativos: 24 h; Deslignificação alcalina: 40 min cada ciclo; Branqueamento: 2 h Hidrólose ácida: (2 - 4) h Diálise - 3 dias; Dispersão dos nanocristais: 20 min | Entre (10 - 16) h |
| Características finais dos CNCs | Obtidos na faixa granulométrica 125- 250 µm, picos de reflexão para os valores de 2θ = 15.8°, 22.5° e 34,6° e cristalinidade de 45%. | Diâmetro médio na faixa de (3 - 7) nm e a razão de aspecto na faixa de (12 - 60), grau de oxidação variando de 0,01 a 0,20, e índice de cristalinidade (CrI) pode chegar acima dos 74%. |
Por fim, os resultados obtidos até a data, pelos próprios autores permitem concluir que nanocristais de celulose podem ser extraídos da fibra do caroço do açaí com características comparáveis com aqueles extraídos das biomassas de referência, por ambos os métodos de extração, hidrólise ácida e pela oxidação com o Persulfato de Amônio. Estes resultados estimulam o uso desta biomassa residual como uma nova fonte renovável para a produção dos CNCs, os quais possuem alta aplicabilidade como agente de reforço em nanocompositos, utilizados na área médica. Contudo, estudos aprofundados sobre a qualidade dos CNCs obtidos pela biomassa de açaí devem ser conduzidos, também, mesmo que a oxidação APS dispensa o prétratamento da biomassa antes da extração, (em termos de remoção de extrativos orgânicos, hidrossolúveis, hemicelulose e lignina), nesta pesquisa é recomentada a lavagem exaustiva da biomassa de açaí, com água a 70 °C até a remoção total dos taninos da fibra e, ainda, a remoção previa, ao menos dos extrativos e lipídeos, pois estes dificultam a ação dos sais inorgânicos que irão atuar sobre a celulose amorfa, expondo os nanocristais. Por outro lado, a pureza dos CNCs extraídos será superior, o que impactará grandemente na qualidade dos resultados das caracterizações posteriores.