Introducción
La neutropenia es uno de los eventos adversos más graves en los pacientes con neoplasias hematológicas y quimioterapia 1. La bacteriemia relacionada con neutropenia febril a menudo aumenta la morbilidad y la mortalidad relacionada con infección. En este contexto las fluoroquinolonas han sido extensamente estudiadas como profilaxis en los pacientes oncológicos, pero su uso rutinario continúa siendo controversial 2. La evidencia publicada ha proporcionado una base para la implementación de profilaxis antibacteriana con fluoroquinolonas para reducir la posibilidad de infección después quimioterapia mielosupresiva. Dos estudios doble ciego controlados con placebo, que incluyen 2325 pacientes, demostraron una reducción significativa en los eventos relacionados con las infecciones, buena tolerancia al tratamiento y la evidencia de costo-efectividad en pacientes con linfoma y cáncer sólido que recibían quimioterapia cíclica moderadamente mielosupresiva 3 y en pacientes con neoplasias hematológicas en quimioterapia a altas dosis 4. En el 2005 Reuter y col. evaluaron el impacto de la suspensión y reintroducción de la profilaxis con levofloxacino sobre la incidencia de eventos de fiebre, bacteriemia y mortalidad. El estudio concluyó que la profilaxis con fluoroquinolonas reduce la morbilidad global y la mortalidad por infección durante la neutropenia 5. Este estudio es probablemente el primero en sugerir que la profilaxis con fluoroquinolonas tiene un impacto significativo sobre la mortalidad secundaria a la infección. Un metaanálisis de 15 ensayos con profilaxis con fluoroquinolona versus placebo o ninguna intervención, reportó la reducción del riesgo de mortalidad por cualquier causa (riesgo relativo 0.52 [IC 95%, 0.35 a 0.77]), así como la mortalidad relacionada con fiebre 6.
La mayor preocupación en relación con el uso profiláctico de fluoroquinolonas es la aparición de bacterias resistentes. Se han reportado informes sobre cepas de Escherichia coli y Klebsiella pneumoniœ resistentes a fluoroquinolonas en los pacientes oncológicos 7,8; sin embargo, la relevancia clínica de este hallazgo no está clara. Bucaneve y col. observaron un aumento no significativo en la incidencia de bacteriemia por gramnegativos resistentes en los pacientes que recibieron levofloxacino, pero esto no afectó a los resultados como morbilidad o la mortalidad relacionada con la infección 4. En un estudio de casos y controles, Martino y col. evaluaron el impacto de la interrupción de la profilaxis con fluoroquinolonas, sobre la morbilidad de la infección. La suspensión de la profilaxis, produjo un incremento rápido de la tasa de infecciones por enterobacterias sensibles a fluoroquinolonas, con un impacto escaso sobre la morbilidad por infección 9. Estos datos sugieren que el beneficio de la profilaxis con fluoroquinolonas supera eventualmente el riesgo de aparición de resistencia.
En nuestra institución, la profilaxis con levofloxacino se utilizó en pacientes neutropénicos en quimioterapia, siguiendo los lineamientos emitidos por la National Comprehensive Cancer Network (NCCN) y las recomendaciones de las directrices de Infectious Diseases Society of America (IDSA) 10,11. La profilaxis se interrumpió en el 2012, el panel de expertos nacionales recomendó no efectuar profilaxis antibiótica con fluoroquinolonas 12. El argumento se sustentó en los datos de resistencia de Escherichia coli y de Klebsiella pneumoniae a las fluoroquinolonas a nivel local y nacional. En el 2009 los datos sobre resistencia a ciprofloxacina de Escherichia coli y Klebsiella pneumoniae en UCI y hospitalización en la cuidad de Bogotá, fueron 28.3 y 22.5% y 17.7 y 14.3%, respectivamente 13. La profilaxis se reinició en 2014 con el criterio de cumplir los estándares de guías internacionales y con el aval del comité de infecciones de la institución. El objetivo del estudio fue comparar la incidencia de neutropenia febril, infección documentada y muerte por infección, en una cohorte de pacientes adultos con neoplasias hematolinfoides en quimioterapia de alto riesgo, que reciben profilaxis antibiótica con levofloxacino, con un grupo de control histórico quienes no recibieron profilaxis, hospitalizados por el servicio hematología en un hospital de cuarto nivel.
Metodología
Se realizó un estudio de antes y después. Se analizaron datos de pacientes mayores de 18 años con neoplasias hematolinfoides, en quimioterapia de alto riesgo. Se revisaron los registros históricos de pacientes ingresados entre septiembre 2012 y agosto 2013, casos consecutivos identificados a través del registro estadístico del hospital según los códigos de CIE.10. Para este periodo, por protocolo del servicio ningún paciente recibía profilaxis con levofloxacino. Se excluyeron para el análisis siete casos de pacientes que habían recibido profilaxis con trimetoprim sulfametoxazol.
A partir de marzo 2014 se registraron los datos de pacientes con profilaxis con levofloxacino hasta noviembre del mismo año. Los pacientes con antecedente de hipersensibilidad a las fluoroquinolonas y aquellos tratados con terapia antibiótica por infección activa fueron excluidos. Según el protocolo institucional el día cinco del esquema de quimioterapia, los pacientes recibieron 500 mg de levofloxacino por vía oral, una vez al día. La profilaxis se administró hasta la recuperación de la neutropenia (definida como recuento el neutrófilos mayor de 500 mm3) y era suspendida si el paciente presentaba neutropenia febril o efectos secundarios asociados a la administración de levofloxacino tales como: reacción anafiláctica, compromiso neurológico, tendinitis asociada a quinolonas, anemia hemolítica, transaminitis, eritema multiforme, síndrome de Steven Johnson o neumonitis alérgica.
Se evaluaron las siguientes variables: edad, sexo, tipo de diagnóstico (leucemia linfoide aguda (LLA), leucemia mieloide aguda (LMA) síndrome mielodisplásico (SMD), linfoma no Hodgkin (LNH)), esquema de quimioterapia (inducción, consolidación, rescate), comorbilidades como enfermedad renal crónica (según KDOQI)14, uso de profilaxis antimicrobiana, reacciones adversas asociadas a la profilaxis, tiempo de duración de la profilaxis, duración de la neutropenia profunda. Los desenlaces de interés fueron neutropenia febril, aislamiento microbiológico, infección clínica identificada, duración de la hospitalización, estancia en la unidad de cuidados intensivos, mortalidad durante el evento agudo y resistencia a fluoroquinolonas.
Se definió neutropenia febril a la presencia de temperatura oral ≥ 38.3 °C o 38°C sostenida por una hora y el recuento de neutrófilos < 500 células/mL; bacteriemia, como la presencia de uno o varios gérmenes en al menos un hemocultivo o el aislamiento de un gram positivo en el caso particular de Staphylococcus coagulasa negativo, en dos o más hemocultivos. El sitio primario de infección y como probable causa del evento febril, como aquel evento considerado por el médico tratante, acompañado de signos o síntomas sugerentes de un foco infeccioso asociado a alteraciones de exámenes de laboratorio o estudios de imagen, confirmados o no por aislamiento de algún microorganismo en las muestras clínicas tomadas del sitio afectado. Se definió como muerte relacionada a la infección si se registró como causa de muerte en el certificado de defunción alguno de los siguientes términos: sepsis, sepsis severa o choque séptico.
Los pacientes fueron examinados en búsqueda de signos clínicos de infección o efectos secundarios asociados a levofloxacino. Diariamente se monitorizaron con hemograma y dos veces a la semana química sanguínea (transaminasas, bilirrubinas, nitrógeno ureico sanguíneo y creatinina). Si se documentaba neutropenia febril se obtenían muestras para cultivo microbiológico, al menos dos hemocultivos, obtenido de cada lumen del catéter venoso central (CVC) y uno periférico; si no era portador de CVC se obtenían dos hemocultivos por venopunciones diferentes. Un sistema automatizado de hemocultivos (BACTEC) se utilizó para cada prueba. Las susceptibilidades antibióticas se determinaron a partir de los puntos de interrupción estandarizada por el Instituto de Estándares Clínicos y de Laboratorio (CLSI). Otras muestras para análisis microbiológico se obtuvieron según el criterio del médico. La terapia antibacteriana empírica se inició según el protocolo institucional y se ajustó de acuerdo con el patrón de resistencia.
Análisis estadístico
La unidad de análisis fueron las admisiones hospitalarias, así, un paciente podía aportar información en uno o varios ingresos a quimioterapia, según el protocolo de quimioterapia (inducción, consolidación, rescate). Para el propósito del análisis el SMD y LMA quedaron en una sola categoría. Análisis descriptivo las variables cualitativas se presentan con frecuencias absolutas y relativas. Las variables cuantitativas se resumen con medidas de tendencia central y de dispersión. De manera exploratoria se comparó la proporción de neutropenia febril, infecciones documentadas y mortalidad intrahospitalaria descrita en la cohorte histórica con los datos de la cohorte prospectiva. Se realizó un análisis bivariado, se utilizó la prueba de Ji cuadrado o test exacto de Fischer para evaluar la asociación entre el uso de profilaxis antibiótica y los desenlaces de interés. Un valor p<0.05 se consideró estadísticamente significativo. Mediante análisis multivariado con método backward, se exploró la relación entre el uso de profilaxis antibiótica y cada uno de los desenlaces de interés: neutropenia febril, aislamiento microbiológico, infecciones clínicamente documentadas, muerte por infección. Los análisis se ajustaron por edad, diagnóstico, protocolo de quimioterapia, función renal y profilaxis antifúngica. Se reportan OR con intervalos de confianza de 95%. El análisis estadístico de la información se realizó en STATA 13®.
Resultados
Características generales de los pacientes
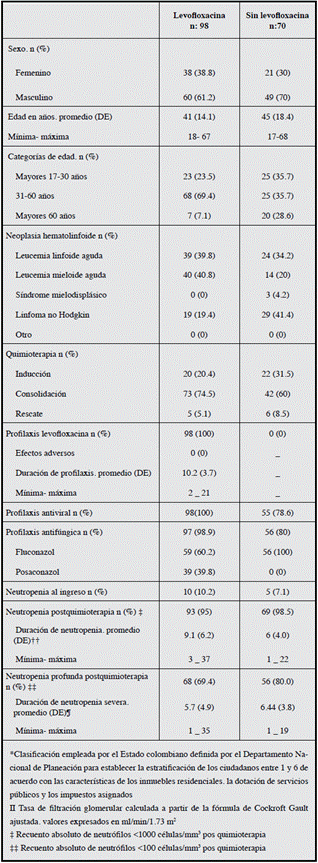
Un total de 168 admisiones hospitalarias fueron analizadas, 70 en la cohorte histórica y 98 en la cohorte expuesta, correspondientes a los ingresos a quimioterapia de 27 y 35 pacientes respectivamente. Las características basales se muestran en la Tabla 1. En el grupo que recibió profilaxis con levofloxacino la edad promedio 41.1 años (DE: 14,1), 60.2% hombres. A diferencia de la cohorte histórica, hubo más admisiones por leucemia aguda, LMA (40.8%) y LLA (39.8%). El 95% presentó neutropenia pos quimioterapia y 69,4% neutropenia profunda, la duración promedio 5.7 días (DE: 4.9). En todas las admisiones se administró profilaxis antiviral y en 98.9% profilaxis antifúngica (60.2% fluconazol y 39.8% posaconazol), en este segundo periodo como protocolo institucional se inició profilaxis con posaconazol en la inducción LMA, SMD de alto riesgo y protocolos de rescate. La duración promedio de la profilaxis con levofloxacino fue 10 días (DE: 3.7), no se documentaron efectos adversos relacionados con la administración de levofloxacino.
La edad promedio del grupo sin profilaxis era 45 años (DE: 18.4); siendo la mayoría hombres (70%). El diagnóstico de la enfermedad subyacente fue LNH 41.4%, seguido de LLA 31.2% y LMA 20%. El 60% de las admisiones hospitalarias fueron por quimioterapia de consolidación, 42% en inducción y sólo 8.5% rescate. El 80% presentó neutropenia profunda con una duración promedio 6.44 días (DE: 3.8). El 78.6% recibió profilaxis antiviral 7 y 98% profilaxis antifúngica.
Neutropenia febril
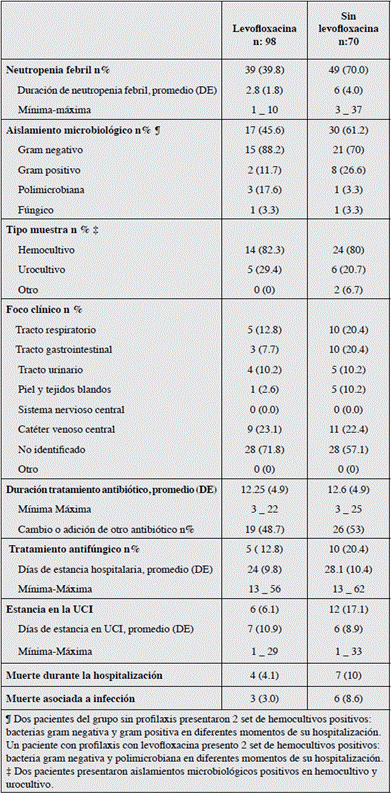
En 39.8% de las admisiones que recibieron profilaxis, se presentó neutropenia febril, en contraste con 70% del grupo sin profilaxis (p=<0.001). La duración promedio de la neutropenia febril fue 2.8 días (DE: 1.8) vs 6 días (DE: 4.0) para los que recibieron profilaxis y los que no recibieron levofloxacino respectivamente (p=<0.001). No se encontraron diferencias en los días de tratamiento antibiótico entre los dos grupos (p=0.9).
El cambio o adición de otro antibiótico se indicó en 48.7% del grupo con profilaxis en contraste con 53.7% quienes no recibieron levofloxacino (p=0.68). La media de la estancia hospitalaria fue 24 días (DE: 8.8) en el grupo de levofloxacino y 28.1 días (DE: 10.4) para el grupo sin profilaxis (p=0.008). La hospitalización en la unidad de cuidados intensivos fue menor en el grupo que recibió profilaxis con levofloxacino en comparación con el grupo sin profilaxis (6.1 vs 17.1, p=0.023).
La Tabla 2 presenta los resultados de los desenlaces clínicos. Se encontró asociación entre la administración de profilaxis con levofloxacino y la reducción de eventos de neutropenia febril OR=0.28 (IC 95% 0.14-0.54) datos crudos, el número necesario por tratar (NNT)= 3 (IC 95% 2-6). En el modelo ajustado por edad, diagnóstico, protocolo de quimioterapia y enfermedad renal crónica OR= 0.21 (IC 95% 0.10-0.43).
Aislamiento microbiológico
Se documentaron 17 (45.6%) aislamientos microbiológicos en los 39 eventos febriles (39.8%) en el grupo con levofloxacino y 30 (61.2%) aislamientos microbiológicos en los 49 eventos febriles (70%) en el grupo sin profilaxis (p= 0,049). Se presentó bacteriemia en 14 (82.3%) y 24 (80%) del grupo con levofloxacino y sin profilaxis respectivamente (p=0.844). En la Tabla 3 se describe la distribución de las bacteriemias y la resistencia bacteriana. Los gérmenes más frecuentemente aislados fueron bacilos gramnegativos, siendo el más frecuente Escherichia coli (14 aislados), seis en el grupo con levofloxacino y ocho en el grupo sin profilaxis. El 53 y 43.3% de las bacterias gramnegativas resistentes, se presentaron en el grupo con levofloxacino y sin profilaxis respectivamente (p=0.525). Dos episodios de bacteriemia por cocos grampositivos se encontraron en el grupo con profilaxis y siete episodios en el grupo sin profilaxis. Ocurrieron dos episodios de fungemia por Candida albicans, uno en cada grupo.
Infección clínicamente identificada
El número de infecciones clínicamente documentadas fueron 11/39 (28.2%) y 21/49 (42.8%) para el grupo con levofloxacino y sin profilaxis respectivamente (p=0.156). La infección asociada a catéter fue el foco de infección más frecuente en los dos grupos (Tabla 4). Se administró la terapia antibacteriana empírica de acuerdo con las directrices del protocolo. El régimen antibiótico inicial usado más frecuente consistía en monoterapia con un betalactámico antipseudomonas.
Mortalidad
La mortalidad 4.1 y 10% en el grupo con profilaxis y sin profilaxis respectivamente (p=0.12). La mortalidad relacionada a infección, se presentó en tres pacientes con levofloxacino en comparación con seis pacientes sin profilaxis (3 vs 8.6%, p=0.118) (Tabla 2). En el análisis multivariado no se encontró asociación entre el uso de profilaxis y la mortalidad por infección, OR 0.6 [IC 95% 0.14-2.44], datos ajustados por diagnóstico, protocolo de quimioterapia, edad y presencia de bacteriemia.
Discusión
Desde 1966, cuando Bodey y col cuantificaron el riesgo de infección asociado a neutropenia 15, se han realizado varios esfuerzos en desarrollar estrategias para prevenir la presencia de infecciones en pacientes con enfermedades hematológicas malignas que reciben protocolos de quimioterapia agresivos. El panel de NCCN recomienda profilaxis con fluoroquinolonas (se prefiere levofloxacino) en pacientes con duración prevista de neutropenia más de siete días (recuento absoluto de neutrófilos <100/ mcL) 10. Esto está de acuerdo con las recomendaciones de las recientes directrices de la IDSA para el uso de agentes antimicrobianos en pacientes neutropénicos con cáncer 11.
En 2005 se publicaron dos amplios estudios doble ciego, controlados con placebo, que sugirieron los beneficios de la profilaxis con levofloxacino en pacientes con neutropenia secundaria a la quimioterapia 3,4. El primer estudio fue realizado en 1565 pacientes con tumores sólidos y linfomas, con disminución en la incidencia de fiebre de 29% (p < 0.001), y el segundo estudio en 760 pacientes con leucemias agudas, tumores sólidos o linfomas con riesgo de neutropenia inducida por quimioterapia, con disminución en la incidencia de fiebre, de 20% (85% en el grupo placebo vs. 65% en el grupo de levofloxacino, p=0.001). Igualmente varios metaanálisis concluyen que el tratamiento profiláctico con levofloxacino es una manera eficaz y bien tolerada para prevenir episodios febriles y otros resultados relacionados con las infecciones relevantes en pacientes con cáncer, neutropenia profunda y prolongada 3,16,17. En nuestro estudio se encontró asociación entre la administración de profilaxis con levofloxacino y la reducción de eventos de neutropenia febril similar a lo reportado en la literatura internacional, es necesario considerar que los eventos relacionados con la infección en pacientes individuales durante varios ciclos no son independientes: factores del paciente, cambios en el tratamiento y la posible resistencia bacteriana que resulta del tratamiento antibacteriano en un ciclo anterior puede influir en el riesgo de infección y el efecto de la profilaxis en ciclos posteriores.
El conocimiento de los efectos de los antibióticos sobre la microbiota intestinal es parcialmente entendido hoy en día, dado que la flora intestinal por sí sola tiene capacidad de mantener potenciales patógenos bajo control. El uso de antibióticos genera entonces cambios no predecibles sobre la flora intestinal que en algunas ocasiones acarrea selección de gérmenes multidrorresistentes que pueden comportarse como flora colonizante transitoria y/o en circunstancias especiales ser fuente de infección en el contexto de huéspedes inmunosuprimidos 18. Este fenómeno no puede ser entendido como causa y efecto, existirán circunstancias favorecedoras y /o exposición de moléculas con mayor o menor potencial de selección de resistencia. En nuestro estudio no encontramos diferencias en la frecuencia de bacteriemias por gramnegativos ni aumento significativo en la tasa de resistencia bacteriana en el grupo que recibió profilaxis con levofloxacino. Diferentes autores han informado resultados opuestos. Gómez 19, analizó una población con alta resistencia a fluoroquinolonas y encontró una frecuencia similar de bacteriemias en pacientes en profilaxis con ciprofloxacino comparado con pacientes en el tiempo en que esta práctica se suspendió. Sin embargo, la resistencia a ciprofloxacino para Escherichia coli se incrementó de forma dramática en el grupo que recibió profilaxis de 12-87%. Verlinden y col 20 evaluaron el impacto clínico y microbiológico al descontinuar la profilaxis con fluoroquinolona en tres periodos consecutivos de ocho meses, no encontraron un aumento significativo en complicaciones infecciosas graves con la interrupción de la profilaxis. La incidencia global de bacteriemia no cambió, pero una mayor proporción de bacterias gramnegativas eran aisladas. Después de la interrupción de la profilaxis, la resistencia a fluoroquinolonas disminuyó 73.77.7%. Centros oncológicos de Europa han documentado un aumento marcado de las bacteriemias por gram negativos después de la interrupción de la profilaxis 21-23. Estos resultados sugiere que el aumento de la resistencia bacteriana, refleja la presión de los antibióticos sobre la flora endógena, lo cual es un fenómeno multiclonal y reversible, y no parece afectar de forma significativa los desenlaces clínicos. Esto nos indica que es mucha más compleja la relación del uso de antimicrobiano con el desenlace esperado de selección de colonizantes resistentes a antibióticos. Chong y cols 24 en una cohorte de 68 pacientes con neoplasias hematológicas, sometidos a quimioterapia con profilaxis con levofloxacino, tras desarrollar neutropenia no lograron demostrar un aumento significativo de Escherichia coli resistente en la microbiota fecal (11 vs 13 pacientes antes y después de la profilaxis respectivamente p=0.65) y la profilaxis en ciclos posteriores no indujo resistencia adicional a quinolonas en los pacientes con aislamiento de Escherichia coli. Si bien en nuestro estudio no encontramos este incremento en la resistencia, esto pudiera ser explicado por el corto periodo de seguimiento para ver reflejado este cambio en la susceptibilidad.
Una consideración importante es el aumento en la frecuencia de las infecciones por gram positivos en algunos ensayos con el uso de fluoroquinolonas, en especial estreptococos y estafilococos coagulasa negativa, probablemente por la falta de efectividad de fluoroquinolonas contra estos microorganismos 25,26. Sin embargo, no encontramos un incremento de las bacteriemias por gram positivos en el grupo con levofloxacino, situación similar para las candidemias.
La tasa histórica de mortalidad por infección en pacientes neutropénicos es de aproximadamente 5%. Los estudios realizados hasta antes de 2005, no habían demostrado mejoría en la supervivencia en los pacientes con profilaxis, sin embargo no se habían diseñado para contestar esa pregunta, principalmente por el número reducido de pacientes que incluían. El metaanálisis de Imran y col 27 informa que la profilaxis con una fluoroquinolona está asociado con un efecto favorable que implica una reducción en la mortalidad; sin embargo, sus resultados no alcanzaron significancia estadística (RR 0.76; IC 95% 0.54-1.08). La revisión actualizada de Cochrane 28 dirigida a evaluar el beneficio de la reducción de la mortalidad en comparación con placebo o ninguna intervención, concluyó que la profilaxis con antibióticos reducen significativamente el riesgo de muerte por todas las causas (46 ensayos, 5635 participantes; RR 0.66; IC de 95%: 0.55-0.79) y el riesgo de muerte relacionada con la infección (43 ensayos, 5777 participantes; RR: 0.61; IC 95% 0.48-0.77). En nuestro análisis no se logró mostrar un efecto benéfico de la profilaxis con levofloxacino en la mortalidad por infección, se requiere un estudio con un mayor tamaño de muestra para demostrar el efecto en este desenlace.
La literatura mundial ha demostrado la efectividad de profilaxis con levofloxacino en desenlaces como mortalidad relacionada con infección, es por esto que consideramos relevante el hallazgo de NNT de tres para prevenir un episodio de neutropenia febril, aunque este resultado ameritaría una comprobación en una cohorte de seguimiento más larga en nuestra población de estudio. Por otra parte aunque este diseño no pretende demostrar una diferencia en costos de atención es claro que este desenlace podría motivar un estudio que permitiera poner de manifiesto los beneficios en este punto, por cuanto demostrar un menor tiempo de neutropenia (2.8 vs 4 días), una menor estancia en la unidad de cuidados intensivos ( 17.1 vs 6.1%) podría reflejar además de disminución de costo cuantificables, una disminución potencial de exposición a diversos factores intrahospitalariamente que favorecerían un egreso más precoz.
Este estudio presenta limitaciones al ser un estudio cuasiexperimental que compara grupos "no equivalentes"; sin embargo, dado el tamaño de muestra requerido, este tipo de metodología permitía responder la pregunta planteada de forma más adecuada al contexto, los sesgos potenciales que son difíciles de controlar son respectivamente: efecto de regresión a la media y la evolución natural de la condición por cuanto en este tipo de estudios no se pueden obtener grupos homogéneos, y se limita a evaluar un desenlace antes y después de la introducción de la intervención que fue en este caso el uso en la cohorte prospectiva de levofloxacino profiláctica vs la suspensión de la misma en la cohorte histórica.
En conclusión, en este estudio, la profilaxis con levofloxacino mostró disminución de neutropenia febril, aislamientos microbiológicos, menor estancia hospitalaria y menor estancia en la unidad de cuidados intensivos. Según estos hallazgos, la profilaxis con levofloxacino, siempre y cuando el perfil de resistencia microbiológica local lo permita, podría ser propuesta como uso de rutina en los pacientes neutropénicos en quimioterapia de alto riesgo.