Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Química
Print version ISSN 0120-2804On-line version ISSN 2357-3791
Rev.Colomb.Quim. vol.34 no.1 Bogotá June 2005
Luisa Fernanda Navarrete 1 Liliana Giraldo, María Cristina Baquero 1 Juan Carlos Moreno 2
1 Departamento de Química. Facultad de Ciencias. Universidad Nacional de Colombia. Bogotá, Colombia. Correo electrónico: lgiraldogu@unal.edu.co, mcbaquero@unal.edu.co
2 Departamento de Química. Facultad de Ciencias. Universidad de los Andes, Bogotá, Colombia. Correo electrónico: jumoreno@uniandes.edu.co, Inavarre@uniandes.edu.co
RESUMEN
Se realizan lavados controlados durante diferentes periodos de tiempo, 6 y 12 horas, con soluciones diluidas de ácido sulfúrico, 2, 5 y 10%, sobre el precursor lignocelulósico cuesco de palma africana, consiguiendo reducir en más del 50% el contenido de cenizas de dicho material, en las que los componentes inorgánicos, principalmente elementos como hierro y aluminio, influyen notablemente en la reacción de gasificación con CO2 durante la activación física.
Se determinan las entalpías de inmersión en las muestras con mayor grado de activación con resultados que se encuentran entre el 2 y 10 J.g-1, y se comparan con los obtenidos para carbones activados resultantes de lavar el material de partida con agua en los mismos períodos de tiempo.
Palabras clave: carbón activado, cenizas, lavados ácidos, calorimetría de inmersión.
ABSTRACT
Controlled washings are made at different periods of time, 6 and 12 hours, with dilute sulfuric solutions 2, 5 and 10% on the lignocellulosic precursor shell of African Palm lowering 50% the ash content of the material.
The inmersion enthalpies are determined in the samples with greater degree of activation with results that are between 2 and 10 J.g-1 and are compared with those gotten for activated carbons resulting when the initial material are washed with water during similar periods.
Key words: activated carbon, ashes, acid washings, immersion calorimetry.
INTRODUCCIÓN
El carbón activado es un material carbonáceo y amorfo que presenta una alta porosidad y extensa área superficial interna, características que le confieren propiedades adsorbentes excepcionales que dependen en forma considerable del proceso de obtención que se realice al material precursor, el cual comprende básicamente dos etapas: carbonización y activación (1, 2).
La carbonización de materiales lignocelulósicos implica una serie de reacciones tales como depolimerización, craqueo y deshidratación de lignina y celulosa, en la que se retira la materia volátil liberando elementos –principalmente hidrógeno y oxígeno– en forma de alquitranes, quedando un esqueleto carbonoso con porosidad incipiente (3).
La activación física requiere altas temperaturas, generalmente mayores a 800 °C, en las que se abren los poros que eventualmente estaban cerrados o bloqueados, dando como resultado un carbón con una estructura porosa altamente desarrollada (4).
Cuando se obtiene un carbón activado, además de sus características texturales y de dureza, un parámetro que se debe considerar es su contenido de materia mineral, que debe ser lo menor posible. Sus componentes, principalmente óxidos de metales alcalino y/o alcalino-térreos, deben influir de forma significativa, modificando no sólo la velocidad de gasificación sino también el desarrollo y la formación selectiva de la porosidad (1, 5, 6). Ya que la materia mineral no contribuye notablemente al área superficial específica y a la porosidad, desde el punto de vista de aplicación se puede considerar como material inerte que decrece la adsorción por unidad de masa. Los carbones comerciales con bajo contenido de cenizas se preparan ya sea por lavado ácido o por una adecuada selección de la materia prima entre las que se encuentran los materiales lignocelulósicos.
En este trabajo se pretende reducir el contenido de cenizas mediante lavados controlados con soluciones diluidas de ácido sulfúrico, esperando que los componentes inorgánicos que contiene dicho material se solubilicen y puedan ser removidos y, de igual forma, determinar su cantidad. Para esto se analizan los contenidos de Na, K, Ca, Mg y Fe.
Un método adecuado para caracterizar la interacción superficial existente entre sólidos porosos y un líquido no reactivo es la calorimetría de inmersión. En esta técnica se determinan los efectos térmicos resultantes al sumergir un sólido en un líquido. La magnitud del calor generado se puede relacionar con una baja o alta producción de superficie de contacto, que es lo que se busca en el proceso de la activación (8, 9, 10). Por lo tanto se evalúa el efecto de los lavados realizados en la entalpía de inmersión de los carbones activados obtenidos en CCl4, que mide la interacción del líquido con la superficie del sólido.
METODOLOGÍA EXPERIMENTAL
Preparación de los carbones activados
Todos los carbones activados se obtienen a partir del mismo precursor, cuesco de palma africana, previamente reducido y tamizado a un tamaño entre 2,3-3,5 mm. Posteriormente se someten a lavados controlados con agua y con soluciones diluidas al 2, 5 y 10% de ácido sulfúrico durante 6 horas y 12 horas respectivamente.
Una vez lavado el material, se seca a 110 °C por un período de 72 horas y el material precursor se mantiene en un desecador hasta su utilización.
La carbonización se lleva a cabo a 600 °C en atmósfera de nitrógeno durante 2,5 horas en un horno vertical provisto de un controlador de temperatura Cole Parmer 89000-10, que permite ajustar la velocidad de calentamiento. Las condiciones de la carbonización son las siguientes: velocidad de calentamiento 10 °C min-1, flujo de nitrógeno 150-160 mL min-1.
Por último, se lleva a cabo la activación física de cada una de las muestras carbonizadas en atmósfera de CO2 hasta alcanzar una temperatura de 900 °C durante 1,5 horas. Las condiciones de la activación son las siguientes: velocidad de calentamiento 10 °C min-1, flujo de CO2 150-160 mL min-1.
Análisis de cenizas
Se pesan aproximadamente 2,000 g de las muestras previamente lavadas y secas y se llevan a la mufla a una temperatura de 800 ± 50 °C durante 17 horas. Concluido este tiempo se dejan enfriar a temperatura ambiente en un desecador. Las cenizas se pesan y se calcula el porcentaje de acuerdo con la norma ASTM D2866-83 (determinación del contenido total de cenizas en carbón activado) (11).
Análisis del contenido de metales en las cenizas
Para la determinación del contenido de metales en las cenizas resultantes del cuesco de palma africana, la muestra se somete a un ataque ácido de acuerdo con las normas ASTM D 3682-78 y D3683- 78 (12). Se utiliza un espectrofotómetro de absorción atómica Perkin Elmer Analyst 300, y se determinan: por absorción atómica Ca, Mg, y Fe y por emisión Na y K. Las soluciones estándar para las curvas de calibración se preparan a partir de soluciones patrón de 1000 mg L-1, con concentraciones de 0,2; 0,4; 0,6; 0,8 y 1,0 mg L-1. Se agrega 1,0 mL de solución de HF al 49% por cada 25 mL de solución y 12,5 mL de solución saturada de ácido bórico con lantano.
Calorimetría de inmersión
Para los carbones activados obtenidos que presentan mayor porcentaje de activación se determina la entalpía de inmersión en CCl4. Se pesan cantidades exactas entre 0,5000 y 1,0000 g de carbón activado que se colocan dentro de una canastilla, empleando como líquido de mojado CCl4 a 25,0 °C. Cuando el equipo alcanza la temperatura se inicia el registro de resistencia eléctrica que proviene de un termistor que actúa como termómetro por un periodo de aproximadamente 15 minutos, tomando lecturas de resistencia eléctrica cada 20 segundos. Se procede a realizar el contacto entre el sólido y el líquido, se registra el efecto térmico generado y se continúa con las lecturas de resistencia por aproximadamente 15 minutos más. Por último se calibra eléctricamente.
RESULTADOS Y DISCUSIÓN
Una vez se realizan los lavados con agua y soluciones de ácido sulfúrico al cuesco de palma africana, el material se somete a los procesos de carbonización y activación. Los resultados obtenidos en estas etapas se muestran en la Tabla 1 y, como se esperaba, se presentan pérdidas de peso del material sin lavar y del material previamente lavado, indicando la eliminación de componentes volátiles y alquitranes que causan un descenso notorio en la densidad de la muestra debido a la creación de cierta porosidad. En la Tabla 1 se presenta el tratamiento de lavado al que se somete el cuesco de palma africana, el porcentaje de pérdida de peso en la carbonización, el porcentaje de pérdida de peso en la activación y el porcentaje de producción global del sólido activado.
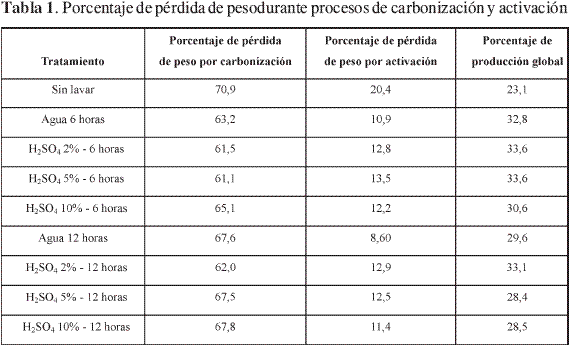
La pérdida de peso en la carbonización, obtenida para el precursor sin lavar, es del 70,9% y disminuye ligeramente cuando se le realizan lavados con agua, 63,2 y 67,9% para 6 y 12 horas respectivamente. Al someter el material a lavados con soluciones de H2SO4 de 2 y 5% el porcentaje de carbonización disminuye al nivel de 61% y vuelve a aumentar a 65% para la solución de ácido del 10%, en los lavados hechos durante 6 horas. Cuando el proceso se lleva a cabo durante 12 horas, el porcentaje de carbonización disminuye menos y se sitúa alrededor del 67% exceptuando el material que se lava con solución de H2SO4 al 2% para el que el porcentaje de carbonización es de 62%. A partir de estos resultados se puede observar que los lavados con agua y soluciones ácidas sobre el material precursor afectan el proceso de carbonización del mismo y, en general, hacen que se pierda menos material.
Con respecto al proceso de activación se observa que el porcentaje de ésta disminuye aproximadamente a la mitad, lo que demuestra un efecto catalizador de las cenizas. Así, para el precursor sin lavar se obtiene una activación del 20,4% y cuando se lava con agua se obtienen valores del porcentaje de activación del 10,9 y 8,60 para los períodos de lavado estudiados de 6 y 12 horas respectivamente; al lavar con las soluciones de ácido sulfúrico para los dos períodos de tiempo, los porcentajes de activación se encuentran alrededor de 12%, y como éste es un indicativo del grado de desarrollo de la porosidad, el resultado sugiere que el contenido de ceniza puede afectar la activación y por ende el desarrollo de porosidad.
En la activación, aunque se obtienen resultados muy cercanos, ésta se ve ligeramente afectada por la acción del lavado con ácido que permite liberar más material lignocelulósico. La muestra que menor pérdida de peso experimenta en la carbonización es la que mayor porcentaje de activación o burn-off presenta.
El rendimiento global en los procesos de carbonización y activación muestra que cuando el precursor no se somete a lavados la pérdida total de material es mayor, obteniéndose menos cantidad de material activado; con los lavados, en todas las condiciones estudiadas, se obtienen rendimientos en promedio de alrededor del 30%, siendo mayores para los tratamientos realizados a 6 horas.
Este rendimiento es similar al obtenido en ensayos anteriores realizados por este grupo con el mismo material precursor sin lavar (13). Briceño (14), en un trabajo en el que produce carbones activados con condiciones experimentales de carbonización y activación semejantes, reporta rendimientos globales máximos de 27%. El que los resultados del rendimiento aumenten con lavados del precursor tiene implicaciones económicos al obtener mayor cantidad de carbón activado; este efecto se logra con los lavados tanto en agua como con soluciones diluidas de ácido sulfúrico. Como el material mineral se ha retirado, la ausencia de éste se refleja en el peso final; así mismo, la ausencia de la materia mineral produce una menor activación (15).
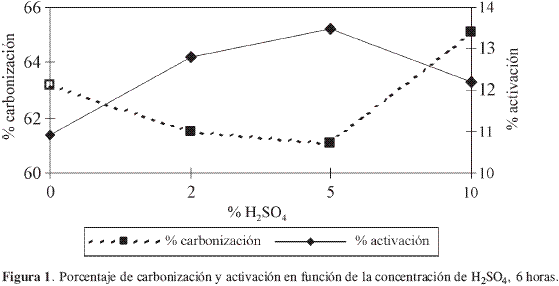
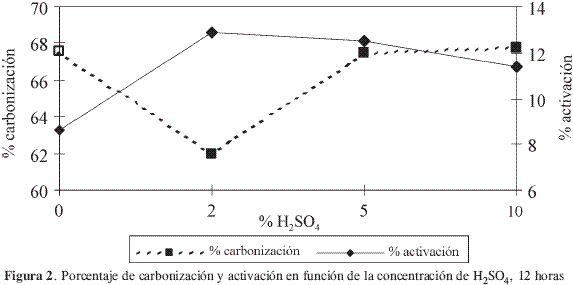
En las Figura 1 y Figura 2 se presenta el comportamiento de los porcentajes de carbonización y activación en función de la concentración de H2SO4; la Figura 1 corresponde a los lavados hechos durante 6 horas y la Figura 2 a los lavados hechos durante 12 horas. En las gráficas se observa cómo los carbones activados con mayor porcentaje de carbonización son los que presentan menor activación en los dos casos; sin embargo, para el material lavado a 6 horas la solución de ácido sulfúrico que más lo afecta es la de 5%, mientras que cuando se lava a 12 horas el tratamiento que más disminuye el porcentaje de activación es el de ácido sulfúrico al 2%.
En la Tabla 2 se presentan los resultados obtenidos para el contenido total de cenizas y el contenido de metales en las diferentes muestras de carbón activado obtenidos después de que el precursor se somete a los diferentes lavados con agua y con soluciones deH2SO4 . En la Tabla 2 la primera columna muestra el tratamiento realizado, la siguiente el porcentaje total de cenizas y en la restantes aparecen los contenidos de Na, K, Ca, Mg y Fe en cada muestra en mgg-1.
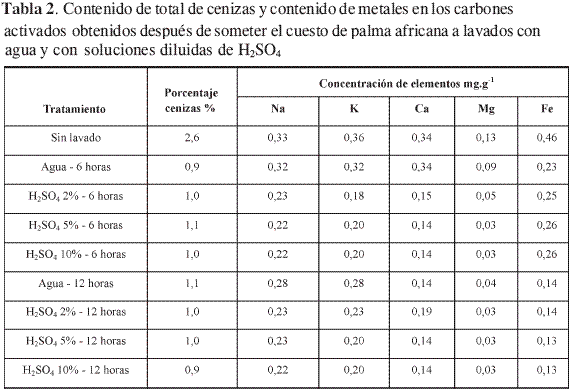
De los resultados obtenidos se puede observar el efecto de los diferentes lavados sobre el contenido de cenizas en el material precursor de los carbones activados. Se presenta una reducción considerable, poco más del 50% en el contenido de cenizas con respecto al material que no se ha lavado. La disminución de cenizas en el cuesco no es progresiva con respecto a la concentración del ácido, lo cual sugiere que la efectividad de los lavados tiene un límite, después del cual su acción permanece constante.
Se nota que el lavado retira material que es parte de las cenizas, razón por la cual suele realizarse este tratamiento sobre el material precursor (16). No se aprecia un efecto bien diferenciado de las distintas concentraciones del ácido sulfúrico; se sugiere en principio que esto puede deberse a que la concentración del ácido sulfúrico es muy débil como para atacar la matriz, por lo que se llevan a cabo lavados con concentraciones más altas, 15 y 20% durante 6 horas, dando resultados muy similares a los anteriores. Probablemente es el agua la que retira la mayor cantidad del material soluble y se aprecia un mínimo efecto del ácido. Lo que cabe esperar es una redistribución inorgánica y una mejor dispersión de la materia mineral en la matriz del carbón por el lavado ácido, que se nota en el grado de quemado en la activación. En la Figura 3 se presenta un diagrama de barras en el que se muestra el comportamiento del contenido total de cenizas en función del tratamiento de lavado; se presentan seis lavados con diferentes concentraciones en un periodo de 6 horas, y cuatro lavados hechos a 12 horas; en general, se llega a un porcentaje de cenizas que se encuentra alrededor del 1%.

Los resultados obtenidos para el contenido de los metales, Na, K, Ca, Mg y Fe en el cuesco de palma africana permiten ver que el contenido inicial de Na, K y Ca es similar y está alrededor de 0,30 mgg-1, es menor para el Mg de 0,13 mgg-1,mayor para el Fe de 0,46 mgg-1 y en general tales contenidos disminuyen con los lavados.
En la Figura 4 se presenta el contenido de Na para las diferentes muestras de material precursor en función de la concentración de H2SO4; en el punto marcado con –1 se coloca el contenido de Na para el material sin lavar y en el punto marcado con cero se coloca el contenido del metal cuando el cuesco se ha lavado con agua. Al lavar con agua se presenta una disminución en el contenido de cenizas tanto para 6 como para 12 horas, siendo mayor para este último; cuando se realizan los lavados con H2SO4 se observa una disminución del contenido de Na, a 0,22 mgg-1 con respecto a las muestras lavadas con agua, pero el efecto no varía con la concentración del H2SO4 ni con el tiempo de lavado.
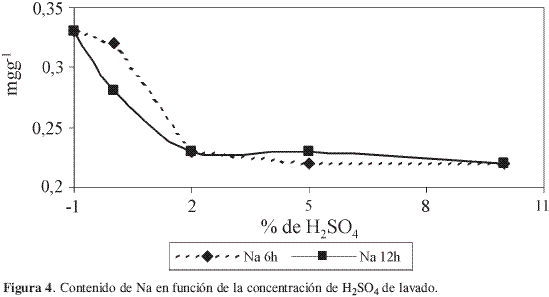
En la Figura 5 se muestra el comportamiento del contenido de K en función del tratamiento de lavado, la gráfica es similar a la que presenta el Na, es decir, se observa una disminución del contenido del metal cuando se lava con agua y al lavarlo con el H2SO4 a distintas concentraciones el contenido de K se mantiene alrededor de 0,20 mgg-1, tanto si el material se lava a 6 como a 12 horas.
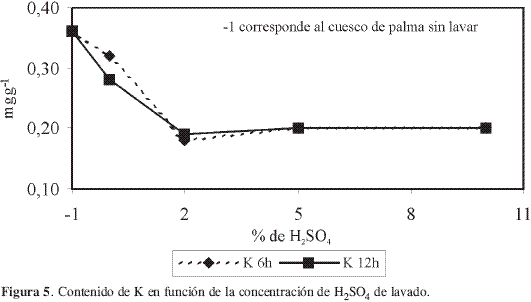
En la Figura 6 se presentan los resultados obtenidos para el contenido de Ca en las diferentes muestras. Inicialmente, al lavar el cuesco con agua a 6 horas no aparece disminución del contenido de este metal; al lavar con solución de H2SO4 al 2% el valor disminuye hasta 0,15 mgg-1 y se mantiene constante cuando se lava con las otras dos concentraciones para este tiempo. Cuando se realiza el lavado a 12 horas con agua el valor disminuye a 0,14 mgg-1 y se mantiene cuando se lava con H2SO4 a las tres concentraciones de trabajo, es decir, no se presenta una influencia del ácido sulfúrico para retirar Ca del cuesco.
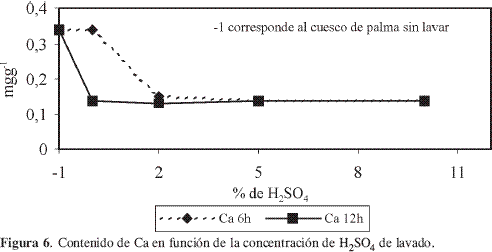
En la Figura 7 se muestran los resultados obtenidos en la disminución del contenido de Mg; como este metal se encuentra en menor cantidad en el cuesco su contenido desciende desde 0,13 a 0,03 mgg-1 con los lavados con H2SO4 al 5% a 6 horas y después se mantiene constante. Se puede decir que el contenido de Mg en el cuesco se lava casi totalmente al lavar con solución diluida, del 2% de ácido sulfúrico, durante 12 horas.

Por último, la Figura 8 muestra los contenidos de Fe para los diferentes tratamientos, se aprecia que la cantidad de Fe disminuye de 0,46 a 0,23 mgg-1 al lavar con agua a 6 horas; al lavar a este tiempo con soluciones ácidas en las concentraciones trabajadas, el contenido se mantiene. Al lavar el material con agua a 12 horas el contenido de Fe se reduce hasta 0,14 mgg-1 y después los lavados con soluciones ácidas no afectan dicho valor; en el caso del lavado del Fe es claro que la acción de remoción se debe al tratamiento con agua mostrando influencia importante del tiempo de contacto. La eliminación del Fe del material de partida para la obtención de carbones activados es interesante ya que se ha encontrado un efecto catalítico de este metal en el proceso de activación, así su presencia produce un aumento en la producción de porosidad (17).

La estructura porosa del carbón activado se desarrolla y modifica durante la activación, en la que debido a la pérdida selectiva de átomos de carbono se produce un aumento en la porosidad, la cual se ve afectada por varios factores, entre éstos la presencia de materia mineral en el material precursor (18). Una técnica útil para evaluar la superficie disponible de un sólido es la calorimetría de inmersión, que permite medir el cambio de entalpía que se produce por las interacciones energéticas entre el sólido y un líquido de mojado; por esta razón a los carbones activados obtenidos en este trabajo se les determina el calor de inmersión en CCl4 y los resultados se muestran en la Tabla 3.
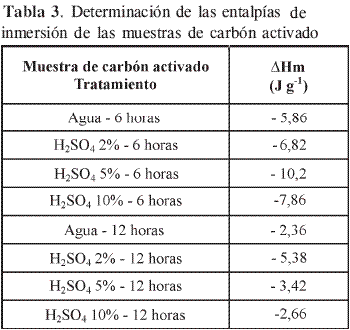
Se observan valores pequeños para la entalpía de inmersión que varían entre 2 y 10 J g-1. Estos resultados son concordantes con los porcentajes de activación encontrados e indican que se produce poca interacción entre el sólido, el carbón activado y el líquido de inmersión. Los resultados de las entalpías de inmersión corroboran que se presenta una activación mayor para las muestras lavadas con ácido sulfúrico al 5% por 6 horas y al 2%por 12 horas, si se compara con los carbones obtenidos a partir de precursor lavado con agua para los dos tiempos establecidos, para los cuales el calor de inmersión resulta menor en los dos casos.
CONCLUSIONES
Al realizar lavados con agua y soluciones diluidas de ácido sulfúrico se disminuye el contenido de cenizas en el cuesco de palma africana escogido como material precursor para la obtención de carbón activado.
Los lavados realizados afectan el proceso de carbonización al disminuir la pérdida de peso desde 70,9% en el cuesco sin lavar a 65% cuando se lava con soluciones de ácido sulfúrico durante 6 horas y 67% cuando se lava durante 12 horas.
El proceso de activación también se afecta con los lavados con las soluciones de ácido y disminuye la activación desde 20% para el material sin lavar a aproximadamente 13% para el material lavado tanto a 6 como a 12 horas.
El análisis de los elementos estudiados indica que éstos se retiran hasta un valor constante, que se alcanza con lavados con agua o con la solución al 2% de ácido sulfúrico y, en general, es suficiente el lavado a 6 horas. En el caso del Fe se observa una dependencia del tiempo de lavado.
Los resultados de la calorimetría de inmersión para los carbones activados obtenidos varían entre 2 y 10 Jg-1, y confirman que los carbones con mayor interacción energética son los lavados con ácido sulfúrico al 5%a 6 horas y al 2%a 12 horas, que presentan calores de inmersión de 10,2 y 5,38 Jg-1 respectivamente.
Agradecimientos Los autores agradecen a la División de Investigación Sede Bogotá, Universidad Nacional de Colombia, y al Convenio Marco entre la Universidad de los Andes y la Universidad Nacional de Colombia.
BIBLIOGRAFÍA
1. Rodríguez-Reinoso, F. (1997). Introduction to carbon technologies: Activated carbon. España. Universidad de Alicante, pp. 35-101. [ Links ]
2. Elliot, M. (1981). Chemistry of coal utilization. 2° supplementary. Ed. John Willey and Sons. New York, pp. 47-55. [ Links ]
3. Rodríguez-Valero, M. A.; Rodríguez-Escandell, M.; Molina-Sabio, M.; Rodríguez-Reinoso, F. (2001). CO2 activation of olive stones carbonized under pressure. Carbon, 39(2): 320-323. [ Links ]
4. Martín, M. J. (1990). Adsorción física de gases y vapores por carbones. Universidad de Alicante, España. pp. 10-15. [ Links ]
5. Rodríguez-Reinoso, F. (1991). Fundamental Issues in Control Gasification Reactivity. Lahaye and P. Ehrburger (eds.). Kluwer Academic Publishers. Netherlands. pp. 533-571. [ Links ]
6. Morgan, M.; Jenkins, R.; Walter, P. (1981). Inorganics constituents in American lignites. Fuel, 60, 189-193. [ Links ]
7. Linares-Solano, A.; Martín-Gullon, J.; Salinas-Martínez de Lecea, C.; Serreno-Talavera, B. (2000). Activated carbons from bituminous coal: effect of mineral matter content. Fuel 79, 635-643. [ Links ]
8. Silvestre-Albero, J.; Gómez, C.; Sepúlveda- Escribano, A.; Rodríguez- Reinoso, F. (2001). Characterization of microporous solids by inmersion calorimetry. Colloids and surfaces A 187, 151-165. [ Links ]
9. Stoeckli, F.; Slasli, A.; Hugi- Cleary, D.; Guillot, A. (2002). Microporous and Mesoporous Materials, 51, 197-202. [ Links ]
10. Moreno J. C.; Giraldo L. (2001). Aplicación de la técnica calorimétrica en la determinación del calor de inmersión de carbón activado. Noticias Químicas 23(75): 16. [ Links ]
11. American Standard Test Method. Total ash content of activated carbon. Philadelphia: ASTM, 1988. p. 370: il. (D2866-83.). [ Links ]
12. American Standard Test Method. Major and minor elements in coal and coke ash by atomic absorption. Philadelphia: ASTM, 1983. pp. 464-469: il. (D3682-78). [ Links ]
13. Informe final del proyecto de investigación "Preparación de carbones activados a partir de residuos lignocelulósicos". Universidad Nacional de Colombia, Departamento de Química, 2002. [ Links ]
14. Briceño, N. (2002). Caracterización de carbones activos obtenidos de cuesco de palma africana por activación con dióxido de carbono. Trabajo de grado. Departamento de Química. Universidad Nacional de Colombia. Bogotá. [ Links ]
15. Rodríguez-Reinoso, F.; Molina- Sabio, M. (1992). Activated carbons from lignocellulosic materials by chemical and/or physical activation on overview. Carbon. 30 (7): 1111-1118. [ Links ]
16. Rodríguez-Reinoso, F.; Molina- Sabio, M. (1998). Carbones activados a partir de materiales lignocelulósicos. Química e Industria. 45(9): 563-571. [ Links ]
17. Hastaoglu, M.; Hassam, M.; Berruit, F. (1988). Assement of catalytic effect of iron on carbon gasification using a gas-solid reaction model. Fuel 67, 1482-1489. [ Links ]
18. Marsh, H.; Rodríguez-Reinoso, F. (2000). Sciences of carbon materials. Universidad de Alicante. Alicante, España. p. 40. [ Links ]














