Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Colombiana de Química
versão impressa ISSN 0120-2804versão On-line ISSN 2357-3791
Rev.Colomb.Quim. v.36 n.2 Bogotá jul./dez. 2007
HIDROGENACIÓN DE CITRONELAL SOBRE CATALIZADORES DE Ir/TiO2/SiO2
HYDROGENATION OF CITRONELLAL OVER Ir/TiO2/SiO2 CATALYSTS
HIDROGENAÇÃO DE CITRONELAL EM CATALISADORES Ir/TiO2/SiO2
Hugo A. Rojas1, Gloria del Carmen Borda1, Patricio Reyes2, José J. Martínez1,3, Jesús S. Valencia3, José L. García-Fierro4
1 Escuela de Química, Facultad de Ciencias, Universidad Pedagógica y Tecnológica de Colombia, Av. Norte, Tunja, Colombia. hrojas_sarmiento@hotmail.com
2 Facultad de Química, Universidad de Concepción, Casilla 160-C, Concepción, Chile.
3 Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia, sede Bogotá, Bogotá, Colombia.
4 Instituto de Catálisis y Petroleoquímica, CSIC, Catoblanco, 28049, Madrid, España.
Recibido: 16/03/07 – Aceptado: 23/08/07
RESUMEN
En este trabajo se estudió la hidrogenación selectiva de citronelal sobre sistemas de Ir/TiO2, Ir/SiO2, e Ir soportado en óxidos mixtos (Ir/TiO2-SiO2) reducidos a 473 y 773 K. Se analizó el efecto de la adición de TiO2 al soporte y de las temperaturas de reducción de los catalizadores para evaluar el posible efecto de especies TiOx parcialmente reducidas, sobre la actividad y selectividad de la reacción. Los sólidos resultantes se caracterizaron por quimisorción de hidrógeno a temperatura ambiente, adsorción de nitrógeno a 77 K, DRX, TEM y XPS. Los resultados indican que los catalizadores reducidos a alta temperatura (HT: 773 K) favorecen la producción del alcohol insaturado debido al efecto de interacción fuerte metal-soporte conocido como SMSI. Los catalizadores reducidos a baja temperatura (LT: 473 K) llevan a la ciclización del anillo produciendo isopulegol. Estos catalizadores mostraron una alta actividad y una menor selectividad hacia el alcohol insaturado.
Palabras clave: hidrogenación de citronelal, TiO2/SiO2, catalizadores de Ir, interacción fuerte metal-soporte.
ABSTRACT
Catalytic hydrogenation of citronellal over Ir/TiO2, Ir/SiO2, and Ir supported on mixed oxides (Ir/TiO2/SiO2) reduced at 473 y 773 K was studied. The effects of the partially reducible support species, the reduction temperatures (473 K or 773 K) and the successive TiO2 addition were analyzed. The catalysts were characterized by H2 chemisorption at room temperature, N2 adsorption at 77 K, XRD, TEM and XPS. The results showed that the high temperature reduction treatment (HT: 773 K) favored the production of the unsaturated alcohol, which can be explained in terms of the so-called strong metalsupport interaction (SMSI) effect. Catalysts reduced at low temperature (LT: 473 K) mainly led to a cyclization reaction producing isopulegol. These catalysts showed high activity but low selectivity to the unsaturated alcohol.
Key words: citronellal hydrogenation, TiO2/SiO2 support, Ir catalysts, strong metal support interaction (SMSI).
RESUMO
Nesse trabalho, foi estudada a hidrogenação seletiva do citronelal em catalisadores Ir/TiO2, Ir/SiO2 e Ir suportado em óxidos mistos (Ir/TiO2-SiO2) reduzidos a 473 e 773 K. Foi analisado o efeito da adição da TiO2 no suporte e das temperaturas de redução dos catalisadores para evaliar o possível efeito das espécies TiOx parcialmente reduzidas, sobre a atividade e seletividade da reação. Os sólidos resultantes foram caracterizados por quimisorção de hidrogênio a temperatura ambiente, adsorção de nitrogênio a 77 K, DRX, TEM e XPS. Os resultados indican que os catalisadores reduzidos a alta temperatura (HT: 773 K) favorecem a produção do álcool insaturado pelo efeito da interação forte metal-suporte conhecido como SMSI. Os catalisadores reduzidos a baixa temperatura (LT: 473 K) conduzen para a ciclização do anel produzindo isopulegol. Esses catalisadores mostraram uma alta atividade e uma baixa seletividade para álcool insaturado.
Palavras-chave: hidrogenação de citronelal, TiO2/SiO2, catalisadores do Ir, interação forte metal-suporte (SMSI).
INTRODUCCIÓN
Los óxidos binarios de Ti–Si son materiales interesantes desde diversos puntos de vista; el coeficiente de expansión térmica de estos óxidos no varía en un amplio rango de temperatura, lo cual los hace candidatos adecuados en catálisis (1); exhiben propiedades ácidas y pueden ser usados como catalizadores ácidos, en especial en reacciones de deshidratación. Su uso se ha extendido a la fotocatálisis y a reacciones de oxidación. Además, el efecto de interacción fuerte metal-soporte (SMSI) que presenta la titania (TiO2) (2) y la posibilidad de obtener este tipo de soporte con alta área superficial hacen que los óxidos mixtos de Ti–Si muestren un gran potencial (3). Sin embargo, son escasos los trabajos reportados respecto a su uso como soporte, particularmente en reacciones de hidrogenación selectiva (4-6), en especial de moléculas insaturadas con grupos carbonilo. El interés que despierta el uso de este tipo de soportes en estas reacciones es la posibilidad de aumentar la selectividad hacia la hidrogenación del grupo carbonilo con relación a otro tipo de grupos funcionales, debido a la SMSI que logra activar selectivamente el grupo C=O para producir alcoholes insaturados ampliamente usados en la química fina. Uno de los pocos trabajos reportados que pone en evidencia el efecto SMSI en óxidos mixtos de Ti-Si lo realizó P. S. Kumbhar (6) con catalizadores de Ni/SiO2-TiO2 en reacciones de hidrogenación de acetofenona.
La distribución de titania sobre diferentes óxidos inertes se ha efectuado por varios procedimientos tal como se ha descrito en distintos trabajos (7-13). Los óxidos TiO2 depositados sobre la superficie de SiO2 han sido menos investigados; estos se preparan por impregnación (7-11), deposición química de vapor y precipitación. La impregnación requiere el anclaje de un precursor altamente reactivo (alcóxido metálico) en los grupos hidroxilos de la superficie de la sílice. Las condiciones de síntesis determinan la homogeneidad de la dispersión de la titania sobre la sílice. Sin embargo, es común encontrar dos tipos de especies de Ti sobre la sílice: 1. especies de TiOx altamente dispersas en la superficie de la sílice por medio de enlaces Ti–O–Si y 2. cristalitos de TiO2 (9, 13). Se considera que a bajas concentraciones de TiO2 los iones Ti pueden considerarse como especies aisladas e inmovilizadas en la matriz de la sílice. La porosidad, tamaño y morfología de los poros de la sílice pueden influir sobre el máximo recubrimiento alcanzado por el precursor (11); de igual forma una alta concentración de hidroxilos y bajas temperaturas son condiciones ideales para lograr la cobertura de monocapa en óxidos soportados de SiO2/TiO2. Esto ha sido verificado por medidas espectroscópicas de UV–Vis en reflectancia difusa (DRS) y espectroscopía Raman mediante el consumo de silanoles (Si–OH) durante la deposición de óxido del titanio en el soporte de sílice (14). Srinivasan et ál. (11) encontraron que en sílice no porosa (Stoeber sílica) se lograba una máxima dispersión de TiO2 (3,0 Ti/nm2 de sílice). Sin embargo, Gao et ál. (14) demostraron que la dispersión puede llegar hasta 4,0 Ti/nm2 al controlar adecuadamente las variables de preparación. El tiempo de reacción, tamaño, reactividad del precursor y ausencia de agua fisisorbida se cuentan como las principales variables en la preparación de óxidos soportados de Ti-Si (3). Estas variables determinan si la unión química de los grupos hidroxilos superficiales con precursores de Ti es monofuncional (una molécula de precursor por grupo OH), bifuncional (una molécula de precursor por dos grupos OH) o en algunos casos trifuncional. El tiempo de reacción es un parámetro experimental importante ya que su magnitud se relaciona con el grado de enlace entre el precursor y los grupos hidroxilo, especialmente aquellos menos reactivos. El efecto estérico de los grupos alquílicos de los precursores de titania impide que reaccionen grupos hidroxilos poco accesibles. Por otra parte, la ausencia de agua fisisorbida en la superficie de la sílice asegura que los grupos silanoles estén disponibles en la reacción y así se evita la hidrólisis del precursor de Ti, que al formar agregados de TiO2 cristalino pueden perderse en la remoción del solvente o en una etapa posterior.
En este trabajo se estudia la hidrogenación de citronelal sobre catalizadores de Ir/TiO2, Ir/SiO2 e Ir soportado en óxidos mixtos (Ir/TiO2/SiO2), para la obtención de citronelol, un intermediario valioso en la producción de fragancias y feromonas (15). Los catalizadores se redujeron a 473 y 773 K con el fin de analizar el efecto del soporte parcialmente reducido y así lograr la activación del grupo carbonilo del citronelal para obtener selectivamente el alcohol insaturado.
Ciertos catalizadores convencionales a partir de Fe, Ni, Pd ocasionan la formación de productos saturados, debido a que las moléculas orgánicas interaccionan fácilmente con la superficie de los metales. Esto podría explicarse desde el punto de vista de la termodinámica, ya que es más favorable la hidrogenación del doble enlace C=C (590 kJ mol-1) que el enlace C=O (728 kJ mol-1). Sin embargo, en la hidrogenación selectiva hacia el grupo carbonilo los catalizadores convencionales no son los más adecuados. Gallezot et ál. (16) afirman que los metales del grupo VIII con mayor ancho de banda δ serán más selectivos hacia el enlace C=O, siendo el orden de selectividad SC=O Os>Ir>Pt>Ru>Rh. Catalizadores de Ir han demostrado una alta selectividad hacia el alcohol insaturado en la hidrogenación de aldehídos α, β-insaturados (17-20), pero no se ha reportado su uso en la hidrogenación de citronelal.
PARTE EXPERIMENTAL
Preparación de catalizadores
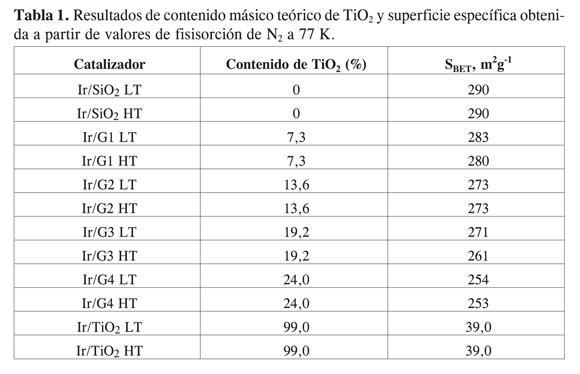
Se prepararon catalizadores de Ir soportados sobre SiO2 (Grace Davidson SBET = 280 m2g-1), TiO2 (BASF D-11-11 SBET = 39 m2g-1) y óxidos mixtos de TiO2/SiO2. Los óxidos mixtos se obtuvieron previamente por anclado de isopropóxido de titanio (Aldrich 98%) sobre sílice (10). Para ello, una solución de isopropóxido de titanio en tolueno (Aldrich 99%) se adicionó en proporción de 1 mmol por gramo de sílice previamente secada al vacío a 423 K. La mezcla resultante se mantuvo durante 16 h bajo agitación vigorosa, en reflujo y atmósfera inerte (nitrógeno); posteriormente se filtró con lavados sucesivos de tolueno y éter etílico. El sólido resultante (G1) se secó al vacío durante 5 h a 423K. Una parte del material obtenido se impregnó con una solución de H2IrCl6 para obtener el catalizador Ir/G1. Otra parte del óxido mixto SiO2/TiO2 (G1) se enriqueció con TiO2, siguiendo el procedimiento de reflujo, secado y calcinación para obtener el soporte G2. De igual forma se obtuvieron los soportes G3 y G4. En la Tabla 1 se indica el contenido teórico de TiO2 para cada uno de los soportes obtenidos.
El componente metálico se depositó por impregnación del soporte (sílice, titania u óxido mixto) a partir de una solución acuosa de H2IrCl6 en cantidad adecuada para generar un 1% en peso de iridio. Los sólidos se redujeron durante dos horas en H2 a 473 K (LTR: baja temperatura de reducción) y 773 K (HTR: alta temperatura de reducción) previo a su caracterización o empleo catalítico (17-21).
Caracterización y evaluación catalítica
El área superficial (SBET) se determinó a partir de isotermas de adsorción de nitrógeno a 77 K en un equipo Micromeritics ASAP 2010. El análisisTEMse realizó en un microscopio Jeol modelo JEM-1200 EXII. Los difractogramas de rayos X se obtuvieron en un difractómetro Rigaku usando un filtro de Ni y la radiación CuKá con λ = 1,504 Å.
Se evaluó la capacidad de la monocapa de hidrógeno quimisorbido en el metal, CH2 (moléculas de hidrógeno por gramo de catalizador) a partir de la extrapolación a presión cero de la parte lineal de la isoterma de quimisorción de hidrógeno, asumiendo un coeficiente estequiométrico de 1, entre átomos de hidrógeno y átomos de Ir; la superficie metálica y la dispersión se evaluaron según fórmulas establecidas (22). El valor de dispersión permite conocer los números de sitios activos del catalizador y, por tanto, expresar los valores de actividad catalítica en TOF (Turnover Frequency) o moléculas transformadas por sitio activo por segundo.
Los ensayos catalíticos se realizaron en un reactor tipo STR operado a 0,62 MPa de H2 y 363 K. La reacción se mantuvo en una agitación constante de 1000 rpm y tamaños de partículas menores de 100 µm, lo que permite asegurar que no existen limitaciones de transferencia de masa. El análisis de reactivos y productos se efectuó por cromatografía de gases utilizando un equipo de GC Varian 3400 y una columna HP–Wax (30mx 0,53mmx 1,0 µm) la cual se mantuvo isotérmicamente a 423 K. Las temperaturas del inyector y del detector fueron de 473 K. Como gas de arrastre se empleó helio a un flujo de 1,0 cm3min-1.
Para evaluar los datos catalíticos la conversión se definió como el número de moles de citral transformado respecto del número de moles de citral alimentado por 100, y la selectividad se definió como la cantidad molar de producto de interés formado respecto de la cantidad total de moles de productos por 100. De igual manera se evaluó la actividad inicial y TOF calculado considerando una isoconversión al 10%. La actividad se expresó como las µmoles de citronelal convertidas por segundo y gramo de catalizador.
RESULTADOS Y DISCUSIÓN
Caracterización de los catalizadores
En la Tabla 1 se presentan los resultados de área superficial y % teórico de TiO2 para cada uno de los sólidos estudiados. Se observa que los catalizadores de Ir/TiO2 (LT y HT) tienen baja área superficial en comparación con el catalizador Ir/SiO2(LT y HT) debido a que la sílice es un soporte que posee mayor porosidad que la titania. En los óxidos de TiO2/SiO2 usados como soportes un incremento en la cantidad de titania provoca una disminución de la superficie del sólido; esta situación corresponde a un recubrimiento progresivo de la sílica por parte del óxido de titanio (7). Aunque aparentemente la presencia de pequeñas cantidades de TiO2 en SiO2 no altera drásticamente el área superficial de la sílice, este efecto se observa sólo a elevados contenidos de Ti. Una disminución similar en el área superficial de óxidos soportados de TiO2/SiO2 ha sido reportada por Kumbhar et ál. (6) y Castillo et ál. (7, 8), quienes explican este fenómeno como el resultado de una obstrucción de poros, debido a la sinterización de TiO2 a altas temperaturas de calcinación (1088 K); sin embargo, en el presente estudio se aplican temperaturas de calcinación (673 K) y de reducción (773 K) menores, por lo que este efecto puede no estar presente.
En la Tabla 2 se muestra la relación H/Ir, las superficies metálicas por gramo de metal y el tamaño de cristal metálico estimado por TEM. La relación H/Ir se determinó por medidas de quimisorción de H2; estos resultados indican que la razón H/Ir es relativamente baja para los catalizadores soportados en SiO2 y TiO2 y considerablemente superior en el caso de soportar el iridio en óxidos mixtos, lo cual sugiere la creación de otros sitios de anclaje del precursor metálico. Se puede observar que una alta relación H/Ir presenta consecuentemente una gran superficie metálica por masa de metal. En la serie Ir/G HT se observa que a medida que aumenta el enriquecimiento por TiO2 la variación en la razón H/Ir, comparada con la serie Ir/G LT, disminuye drásticamente; esta misma relación es muy marcada para el catalizador Ir/G4 HT; esto se explica en virtud del cubrimiento de las partículas de Ir por especies TiOx generadas por el conocido efecto SMSI (17-20), lo cual está de acuerdo con las observaciones de Hoffmann et ál. (10) en catalizadores de Pt/SiO2/TiO2, quienes encontraron, con el uso de DRIFTS, un fuerte efecto SMSI al cuarto ciclo de impregnación de TiO2, es decir, a contenidos elevados de TiO2.
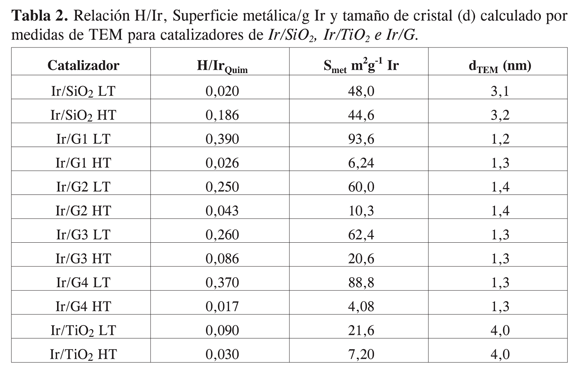
La disminución observada en la razón H/Ir no puede atribuirse a un efecto de la dispersión, pues prácticamente no hay cambios en el tamaño de cristal de Ir al comparar catalizadores reducidos a baja o alta temperatura, como lo demuestran los resultados de TEM. Sin embargo, los tamaños de cristal metálico calculados a partir de los resultados de quimisorción para la serie HT son sustancialmente mayores que los observados por TEM; este comportamiento se explica por la presencia del efecto SMSI mencionado (17-20), por lo que estos valores no tienen mayor sentido y usualmente no son reportados para catalizadores en estado SMSI; por lo tanto, en este trabajo solo se presentan los tamaños de partícula metálica obtenidos por TEM.
Las especies de iridio tienden a permanecer más dispersas en los soportes mixtos, especialmente en aquellos con mayor contenido de titania (Figura 1); se han encontrado resultados similares para catalizadores de Co/TiO2/SiO2 (5). La distribución de tamaño obtenida para los catalizadores Ir/G es muy estrecha y el diámetro promedio de partícula se encontró cercano a 1,3 nm para la mayoría de este tipo de catalizadores. Para catalizadores soportados en SiO2 o TiO2 las partículas de iridio tienden a aglomerarse con una distribución de partícula más ancha, especialmente en TiO2; incluso se detectan partículas metálicas de alrededor de 10 nm en este soporte. Los resultados obtenidos para sílice indican que una elevada área superficial podría resultar en una mejor distribución, pero no garantizar una buena dispersión.

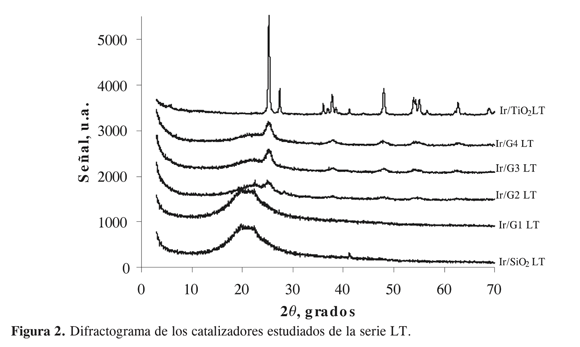
En la Figura 2 se presentan los patrones de difracción de rayos X de los catalizadores estudiados. El catalizador Ir/ SiO2 presenta sólo una señal en 2θ≈40º, que posiblemente corresponde a la presencia de cristalitos de Ir; esta señal también aparece en el catalizador Ir/TiO2, que son los únicos catalizadores cuyo tamaño de cristal es algo más elevado y detectable por esta técnica, aunque se sabe que, por difracción de rayos X, concentraciones del orden del 1% son el límite de detección (22). El difractograma obtenido para el catalizador soportado en titania indica picos característicos de anatasa. En el caso de los catalizadores soportados en óxidos mixtos TiO2/SiO2, para el de menor contenido de TiO2, el difractograma corresponde al de un sólido amorfo, lo que indica que el TiO2 se encuentra altamente distribuido sobre el soporte. Puede observarse que la intensidad de los picos característicos para ambos soportes cambia con base en las relaciones de titania y sílice. Al aumentar el contenido de TiO2 progresivamente, se detectan reflexiones típicas de la titania en su fase anatasa, y se muestran bandas anchas que caracterizan a especies de pequeño tamaño de cristal; las señales crecen en intensidad y se hacen un poco más agudas a mayores contenidos de TiO2, lo que sugiere un incremento en el tamaño de los cristales.
El ambiente químico, la coordinación y la dispersión relativa del iridio sobre la superficie del óxido soportado SiO2/TiO2, como del titanio sobre la superficie de la sílice, se evaluaron por XPS. La Tabla 3 resume las energías de enlace de Si 2p, Ti 2p3/2, Ir 4f7/2 para los catalizadores estudiados. Los valores de energía de enlace para Si 2p y Ti 2p3/2 fueron de 103,4 y 458,5 eV, respectivamente. Con respecto al pico de Ir 4f7/2 se obtuvo un valor de 60,2 eV que corresponde a especies reducidas del metal (18). Luego de la adición de Ti sobre la sílice se detecta un ligero incremento en la energía de enlace, hecho que sugiere la presencia de una fracción de especies de Irä+ generadas por la transferencia electrónica entre el titanio parcialmente reducido y las partículas de iridio (16-18).
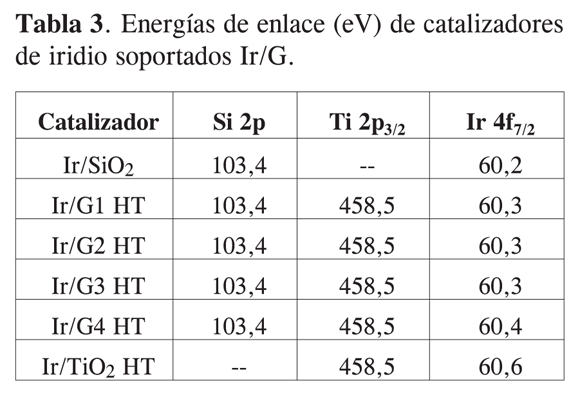
La energía de enlace para el pico de Ti 2p3/2 (458,5 eV) obtenido para estos catalizadores se asigna a iones Ti4+ en una coordinación octaédrica como en la fase anatasa, según los resultados reportados por Mariscal et ál. (23), quienes han determinado que la energía principal de enlace del pico de Ti 2p3/2 puede descomponerse en dos contribuciones: una cercana a 458,5 eV, asignada al ión Ti4+ en coordinación octaédrica, similar a la fase anatasa del TiO2, y otra cercana a 460,0 eV, asociada al ión Ti4+ en coordinación tetraédrica dentro de la estructura de la sílice. A medida que la carga de titania aumenta, la energía de enlace del pico de Ti 2p3/2 permanece constante, infiriendo que la titania no se deposita en forma de una monocapa superficial, sino que está formada de aglomerados (clusters) de anatasa que surgen en los procesos de calcinación y/o de reducción.
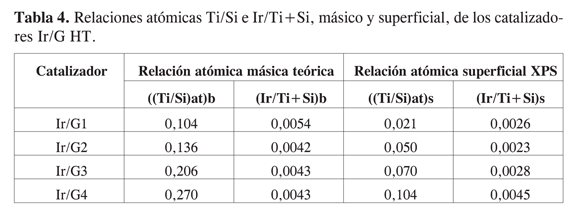
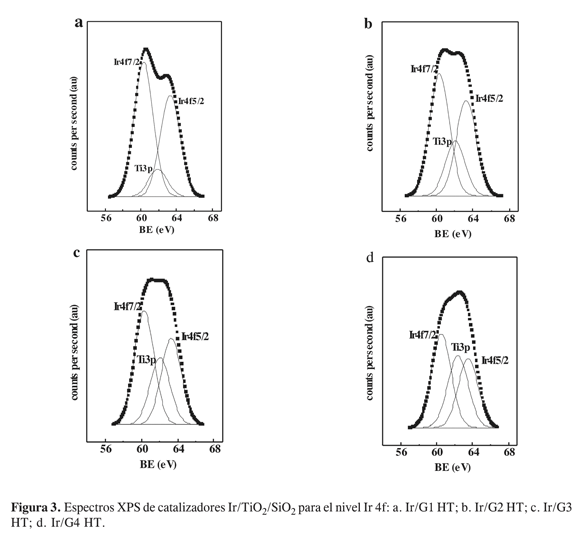
La Tabla 4, resume las relaciones atómicas másicas teóricas y superficiales obtenidas por XPS de Ti/Si e Ir/(Ti+Si). Puede observarse que la relación másica teórica ((Ti/Si)at)b es mucho más alta que la relación Ti/Si superficial (Ti/Si)at)s. Esto sugiere que, aunque la superficie de estos sólidos es mayor, puede ocurrir una segregación parcial de cristales de TiO2, posiblemente en forma de agregados (clusters) como aparece confirmado en la literatura (7). Con respecto a la relación de Ir/(Ti+Si), no hay una diferencia significativa debido a que el tamaño de partícula metálica y el área superficial son similares, con una fuerte caída en el área a un elevado contenido de Ti. Los aglomerados de TiO2 contribuyen a la obstrucción de poros, con una consecuente disminución del área superficial, como se indica en los resultados de SBET (Tabla 1). Al observar el espectro XPS (Figura 3), para los catalizadores de Ir/G HT, el pico de Ti 3p aparece entre las señales de Ir 4f7/2 e Ir 4f5 /2; es interesante observar la contribución de esta banda respecto a los componentes de Ir; la situación indica una posible migración de especies TiOx sobre la superficie de la sílice, fenómeno que se acentúa con el incremento de la carga de TiO2.
Actividad catalítica
La evolución de la conversión total de citronelal con el tiempo de reacción para las series estudiadas se muestra en las Figuras 4a y 4b. En general, se puede observar una alta conversión en los catalizadores estudiados para ambas series. La velocidad es mayor durante la primera hora de reacción y luego se destaca una disminución en la pendiente. Los catalizadores de Ir/TiO2 e Ir/SiO2 reducidos a baja temperatura (LT) presentan baja actividad; el catalizador Ir/TiO2 LT es el menos activo, esto se atribuye a su menor cantidad de centros activos (mayor tamaño de cristal metálico). Para la serie de catalizadores Ir/G LT se presenta un incremento en la actividad a medida que se aumenta el contenido de TiO2, hasta llegar a un máximo en el catalizador Ir/G2 LT, que se explica por la generación de sitios diferentes de anclaje del precursor que conducen a un aumento de la dispersión, situación que se traduce en una disminución del tamaño de cristal. A contenidos superiores de TiO2 se produce un cubrimiento mayor de los cristales, lo que provoca una disminución de la capacidad hidrogenante de los catalizadores, tal como se muestra en la Figura 4a para catalizadores Ir/G3 LT e Ir/G4.
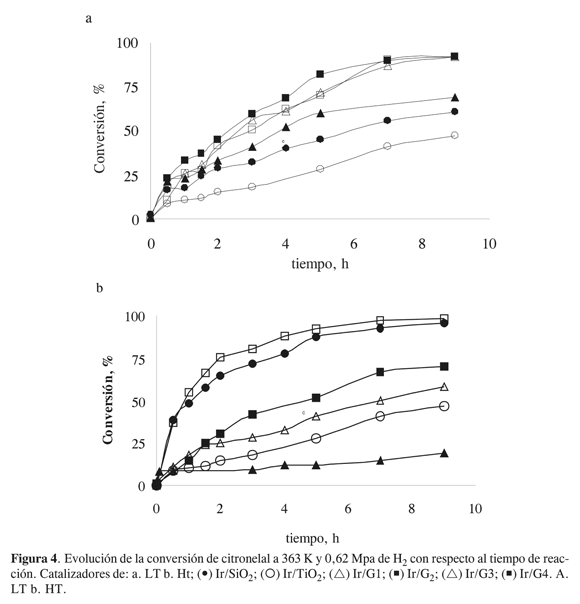
Para los catalizadores a alta temperatura el sólido de mayor actividad es Ir/TiO2, lo cual puede explicarse como una consecuencia del efecto SMSI que experimenta el TiO2, el cual no está presente en su contraparte LT (17-20). Los catalizadores soportados en óxidos mixtos HT presentan un comportamiento similar respecto de su actividad, como puede verse en la Figura 4b. Sin embargo, el catalizador Ir/G4 con mayor contenido de TiO2 presenta un incremento considerable en su actividad. La causa de este comportamiento reside en el mayor enriquecimiento de TiO2, con lo cual se logra un mayor efecto SMSI; esta observación concuerda con los hallazgos descritos por Hoffman et ál. (15).
En la Tabla 5 se comparan los niveles de conversión a las 3 h de reacción, actividad inicial y actividad por sitio (TOF) a un 10% de conversión sobre los catalizadores HT y LT. Los valores de actividad inicial y TOF para los catalizadores LT permiten corroborar la tendencia observada en los valores de conversión, es decir, un máximo para Ir/G2 LT por efecto de generación de algunos sitios interfaciales muy activos (efecto SMSI). Para los catalizadores Ir/G3 e Ir/G4 LT se presenta una caída en actividad inicial y TOF debido probablemente a exceso de TiO2 por cubrimiento de los sitios activos. Por otra parte, para los catalizadores Ir HT no se observan cambios significativos en el valor de actividad inicial y TOF y, comparados con el comportamiento del catalizador Ir/TiO2 HT con la excepción del sólido Ir/G4 HT, que presenta valores considerablemente superiores. Esto puede interpretarse tomando en consideración que en los sistemas de bajo contenido de TiO2 el anclaje de especies TiOx al soporte es relativamente fuerte y su migración es relativamente difícil. En el catalizador Ir/G4 HT, su contenido de Ti es superior, se forman cristalitos de TiO2 anatasa, y es más fácil la migración de especies TiOxsobre los cristalitos de Ir (10), lo que permite generar especies de Ir que son muy eficientes en la polarización del enlaceC=O(17-21); de esta forma se genera un catalizador activo y selectivo.

En la Tabla 6 se resume la selectividad observada hacia los productos obtenidos para los catalizadores estudiados. Para la serie HT las sustancias mayoritarias corresponden a productos de hidrogenación del enlace carbonilo y del doble enlace carbono–carbono; es decir, citronelol y 3,7-dimetil octanal, respectivamente. La hidrogenación total de estos productos permite la formación del alcohol saturado, 3,7-dimetil octanol.

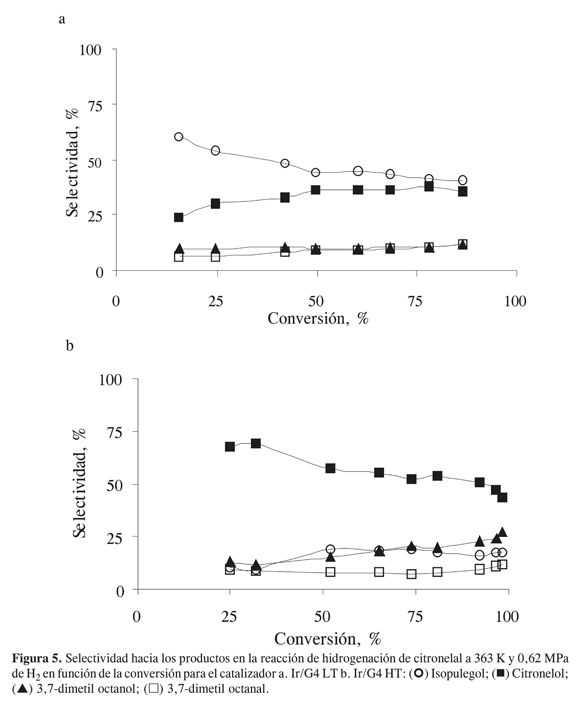
El 2–isopropenil–5–metil ciclohexanol (isopulegol) es el resultado de la ciclización del anillo, lo que ocurre principalmente en catalizadores reducidos a baja temperatura. Puede entonces observarse que la selectividad es dependiente del efecto del soporte. En catalizadores donde se presenta un marcado efecto SMSI se favorece la producción del alcohol insaturado, como se observa en catalizadores Ir/TiO2 HT e Ir/G4 HT, respectivamente (Figura 5), con lo cual la producción de citronelol es dependiente del contenido de Ti en el catalizador. La producción del isopulegol se asocia a la presencia de sitios Brönsted, en la forma establecida por Milone et ál. (15).
CONCLUSIONES
La deposición de TiO2 sobre sílice logró presentar una alta área superficial que se disminuye gradualmente con el enriquecimiento de TiO2 debido a la formación de aglomerados de TiO2, especialmente en forma de anatasa. El tratamiento en atmósfera reductora influye drásticamente en el comportamiento de selectividad obtenido, mas no en su actividad; así, los catalizadores reducidos a alta temperatura (HT: 773 K) favorecen la producción del alcohol insaturado (citronelol) debido al efecto conocido como SMSI (disminución de las propiedades de quimisorción y presencia de sitios Irä+), fenómeno que es evidente a altas cargas de titania. Los catalizadores reducidos a baja temperatura (LT: 473 K) favorecen la isomerización del citronelal hacia isopulegol, un proceso que ocurre principalmente sobre el soporte. La alta actividad mostrada por los catalizadores se debe en parte a la generación de nuevos sitios interfaciales y a la adecuada distribución del metal lograda sobre los óxidos mixtos de TiO2/SiO2.
AGRADECIMENTOS
Los autores agradecen a Colciencias y a la Dirección de Investigaciones (DIN) de la UPTC, Tunja, Colombia, por el apoyo otorgado al proyecto Colciencias- 1109-05-17865.
REFERENCIAS BIBLIOGRÁFICAS
1. Stakheev, A. Y.; Shpiro, E. S.; Apijok, J. XPS and XAES study of TiO2-SiO2 mixed oxide system. J. Phys. Chem. 1993. 97 (21): 5668-5672. [ Links ]
2. Tauster, S. J.; Fung, S. C.; Garten, R. L. Strong metal-support interactions. Group 8 noble metals supported on titanium dioxide. J. Am. Chem. Soc. 1978. 100 (1): 170-175. [ Links ]
3. Gao, X.; Wachs, X. E. Titania-silica as catalysts: molecular structural characteristics and physico-chemical properties. Catal. Today. 1999. 51 (2): 235-254. [ Links ]
4. Grzechowiak, J. R.; Szyszka, I.; Rynkowski, J.; Rajski, D. Preparation, characterization and activity of nickel supported on silica-titania. Appl. Catal. A: General. 2003. 247 (2): 193-206. [ Links ]
5. Jongsomjit, B.; Wongsalee, T.; Praserthdam, P. Catalytic behaviors of mixed TiO2-SiO2 supported cobalt Fischer-Tropsch catalysts for carbon monoxide hydrogenation. Mat. Chem. Phys. 2006. 97 (1): 343-350. [ Links ]
6. Kumbhar, P. S. Nickel supported on titania-silica: preparation, characterization and activity for liquid-phase hydrogenation of acetophenone. Appl. Catal. A: General. 2002. 96 (2): 241-252. [ Links ]
7. Castillo, R.; Koch, B.; Ruiz, P.; Delmon, B. Influence of the amount of titania on the texture and structure of titania supported on silica. J. Catal. 1996. 161 (2): 524-529. [ Links ]
8. Castillo, R.; Koch, B.; Ruiz, P.; Delmon, B. Influence of preparation methods on the texture and structure of titania supported on silica. J. Mater. Chem. 1994. 4: 903-906. [ Links ]
9. Capel-Sánchez, M. C.; Campos- Martin, J. M.; Fierro, J. L. G. Influence of the textural properties of supports on the behaviour of titanium- supported amorphous silica epoxidation catalysts. J. Catal. 2005. 234 (2): 488-495. [ Links ]
10. Hoffman, H.; Staudt, P.; Costa, T.; Moro, C.; Benvenutti, E. FTIR study on the electronic metal support interactions on platinum dispersed on silica modified. Surf. Interface Anal. 2002. 33: 631-633. [ Links ]
11. Srinivasan, S.; Datye, A. K.; Smith, M. H.; Watchs, I. E.; Peden, C. H. P. Interaction of titanium isopropoxide with surface hydroxyls on silica. J. Catal. 1994. 145 (2): 565-573. [ Links ]
12. Mohamed, M. M.; Salama, T. M.; Yamaguchi, T. Synthesis, characterization and catalytic properties of titania- silica catalysts. Colloids Surf. A: Physicochem. Eng. Aspects. 2002. 207 (1-3): 25-32. [ Links ]
13. Montes, M.; Getton, F. P.; Vong, M. S. W.; Sermon, P. A. Titania on silica. A comparison of sol-gel routes and traditional methods. J. Sol-Gel Sci. & Techn. 1997. 8 (1-3): 131-137. [ Links ]
14. Gao, X.; Bare, S. R.; Fierro, J. L. G.; Banares, M. A.; Wachs, I. E. Preparation and in-situ spectroscopic characterization of molecularly dispersed titanium oxide on silica. J. Phys. Chem. B. 1998. 102 (29): 5653-5666. [ Links ]
15. Milone, C.; Perri, A.; Pistone, A.; Neri, G.; Calvagno, S. Isomerization of (+) citronellal over Zn(II) supported catalysts. Appl. Catal. A: General. 2002. 233 (1-2): 151-157. [ Links ]
16. Gallezot, P.; Richard, R. Selective hydrogenation of aldehidos ,-insaturados. Catal. Rev. Sci. Eng. 1998. 40 (1-2): 81-126. [ Links ]
17. Rojas, H.; Borda, G.; Reyes, P.; Martínez, J.; Valencia, J. XX Simposium Iberoamericano de Catalise. Resumos dos trabahlos, 2006. p. 261. [ Links ]
18. Reyes, P.; Rojas, H.; Pecchi, G.; Fierro, J. L. G. Liquid-phase hydrogenation of citral over Ir-supported catalysts. Appl. Catal. A: General. 2002. 248: 59. [ Links ]
19. Reyes, P.; Rojas H.; Fierro, J. L. G. Kinetic study of liquid-phase hydrogenation of citral over Ir/TiO2 catalysts. Appl. Catal. A: General. 2003. 248 (1-2): 59-65. [ Links ]
20. Reyes, P.; Rojas, H.; Fierro, J. L. G. Effect of Fe/Ir ratio on the surface and catalytic properties in citral hydrogenation on Fe-Ir/TiO2 catalysts. J. Mol. Catal. A: Chem. 2003. 203 (1-2): 203-211. [ Links ]
21. Marzialetti, T.; Fierro, J. L. G.; Reyes, P. Iridium supported catalyst for enantioselectivite hydrogenation of 1-phenyl-1,2-propanedione: The effects of the addition of promoter and the modifier concentration. Catal. Today. 2005. 107-108: 235-243. [ Links ]
22. Rojas, H. Hidrogenación de citral sobre catalizadores de Ir e Ir-Fe, Ir-Ge. Tesis de doctorado. Universidad de Concepción, Chile. 2003. [ Links ]
23. Mariscal, R.; López-Granados, M.; Fierro, J. L. G.; Sotelo, J. L.; Martos, C.; Grieten, R. van. Morphology and surface properties of titania- silica hydrophobic xerogels. Langmuir. 2000. 16 (24): 9460-9467. [ Links ]














