Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Química
Print version ISSN 0120-2804On-line version ISSN 2357-3791
Rev.Colomb.Quim. vol.36 no.3 Bogotá Sep./Dec. 2007
ESTUDIO DRX EN MATERIALES CATALIZADORES Cu-Ni-SiO2 PARA HIDROGENACIÓN DE ACEITE DE SOYA. DESARROLLO DE ESTRUCTURA CRISTALINA Y ACTIVIDAD CATALÍTICA
DRX STUDY IN CATALYSTS MATERIAL Cu-Ni-SiO2 FOR HYDROGENATION OF SOY OIL. DEVELOPMENT OF CRYSTALLINE STRUCTURE AND CATALYTIC ACTIVITY
ESTUDO DRX EM MATERIAIS CATALISADORES Cu-Ni-SiO2 PARA HIDROGENACIÓN DE AZEITE DE SOYA. DESENVOLVIMENTO DE ESTRUTURA CRISTALINA E ATIVIDADE CATALÍTICA
Gloria I. Cubillos1, Jesús A. García1, Carlos A. Delgado1, Liliana Giraldo1
1 Departamento de Química, Facultad de Ciencias. Universidad Nacional de Colombia. gcubillos@unal.edu.co, jagarcia06@gmail.com, carlosnatalejo@yahoo.com, lgiraldogu@unal.edu.co
Recibido: 13/07/07 – Aceptado: 28/11/07
RESUMEN
Para buscar elementos experimentales que soporten la hipótesis según la cual se forman estructuras cristalinas Cu-Ni o, eventualmente, Cu-Ni-SiO2 en la síntesis de catalizadores para la hidrogenación de aceite de soya, se prepararon mezclas de estos tres materiales a partir de sales de los metales con sílice (aerosil). Se calcinaron a 270 °C y se redujeron a 330 °C en atmósfera de hidrógeno. En los materiales reducidos se estudió el difractógrama de RX en el rango 37 a 53°, y se comparó con el difractograma de aleaciones Cu-Ni –en las cuales se conoce la formación de cristales mixtos–, y con los difractogramas de los elementos puros Cu y Ni. Los resultados muestran señales de difracción diferentes a las señales de los componentes puros. La actividad catalítica se muestra diferente en los materiales que presentan distorsión en su estructura cristalina.
Palabras clave: difracción de RX, fases cristalinas, sinergia de Cu sobre Ni-SiO2, catalizador bimetálico Ni-Cu- SiO2, hidrogenación de aceite de soya, estructura cristalina.
ABSTRACT
Looking for experimental facts that support the hypothesis of formation of Cu-Ni or Cu-Ni-SiO2 crystals formation hypo- thesis in the syntesis of catalytic materials for soja oil hydrogenation, different mixtures of the metals nitrates with SiO2 (aerosil), were prepared and calcined at 270 oC, then reduced in hydrogen atmosphere at 330 oC. RX Diffraction registers of the prepared materials, Ni-Cu alloys, Ni and Cu pure metals, show that differences in diffraction signal in prepared materials exist with respect to pure metals. The catalytic activity show differences too.
Key words: Sinergy, Ni-Cu-SiO2 sinergic effects, bimetallic catalyst, soja oil hydrogenation.
RESUMO
Para procurar elementos experimentais que suportem a hipótese segundo a qual se formam estruturas cristalinas Cu-Ni ou eventualmente Cu-Ni-SiO2 na síntese de catalisadores para a hidrogenación de azeite de soya, prepararam-se misturas destes três materiais a partir de sais dos metais com sílice (aerosil). Se calcinaron a 270 °C e se reduziram a 330 °C em atmosfera de hidrogênio. Nos materiais reduzidos se estudou o difractógrama de RX na casta 36 a 53 graus, e se comparou com o difractógrama de ligas de metais Cu-Nem, nas quais se conhece a formação de cristais mistos, e com os difractógramas dos elementos puros Cu e Nem. Os resultados mostram que se apresentam sinais de difracção diferentes aos sinais dos componentes puros. A atividade catalítica se mostra diferente nos materiais que apresentam distorção em sua estrutura cristalina.
Palavras-chave: sinergia, sinergia Ni-Cu-SiO2, catalisador bimetálico, hidrogenación de azeite de soya.
INTRODUCCIÓN
El níquel soportado sobre sílice continúa siendo uno de los catalizadores más empleados en los procesos de hidrogenación (1). En un trabajo precedente se logró establecer que la actividad catalítica del níquel soportado sobre sílice puede ser influenciada favorablemente por el cobre en el proceso de hidrogenación de aceite de soya (2). Se contaba con la evidencia reportada por Bond. G. C. (3-4) en 1962, trabajo en el cual la hidrogenación de benceno sobre una aleación níquel-cobre muestra un incremento en la actividad de hidrogenación cuando el material aleado contiene un 25% de cobre, y con el trabajo reportado por Kang y cols. (5) sobre catalizadores Ni-Cu soportados sobre gama alúmina, donde se encontró que la presencia de cobre en el catalizador no solo cambia la actividad, sino que incrementa la selectividad en la hidrogenación del butadieno hacia 1-buteno.
Otros trabajos recientes con catalizadores bimetálicos muestran cómo la actividad del catalizador esta íntimamente relacionada con las propiedades fisicoquímicas del material y con la sinergia que se presenta entre los átomos metálicos directamente expuestos sobre la superficie (6-10); sin embargo, también debe considerarse que dentro del proceso de síntesis de los catalizadores se generan variaciones geométricas en los sitios activos, responsables del cambio en la actividad intrínseca de los átomos superficiales del metal (6), y posiblemente se presenta la formación de estructuras cristalinas que podrían ser las causantes de la variación en las propiedades de un catalizador determinado (7). En el presente trabajo se muestra la correlación entre la estructuracristalina desarrollada en los materiales catalizadores, y la actividad catalítica en la reacción de absorción de hidrógeno por parte del aceite de soya para dar productos hidrogenados como se mostró en un trabajo anterior (2).
MATERIALES Y MÉTODOS
Se sintetizaron cinco mezclas catalizadoras con los tres componentes, Ni-Cu-SiO2, por el método de coprecipitación (11-14) de los dos metales. La síntesis de los nitratos se realizó a partir de la reacción de ácido nítrico concentrado RA, con níquel electrolítico RA y cobre en polvo HopKin & Williams, cada metal del 99,9% de pureza. Las soluciones de cada uno de los nitratos se mezclaron sobre sílice tipo aerosil. Las mezclas preparadas se homogeneizaron por 8 horas y se secaron por convección con aire caliente a 60 °C. Se calcinaron durante 12 horas en un horno eléctrico controlado para mantener 270 °C, obteniéndose el material que se denominó precatalizador; cada uno de los precatalizadores se redujo en atmósfera de hidrógeno a 330 °C durante 25 horas, generando los materiales catalizadores.
Las concentraciones se programaron manteniendo la relación en peso Ni/SiO2 0,5 constante. La relación de moles de metal nCu/(nNi+nCu) se programó para obtener valores en un rango de 0 a 1.
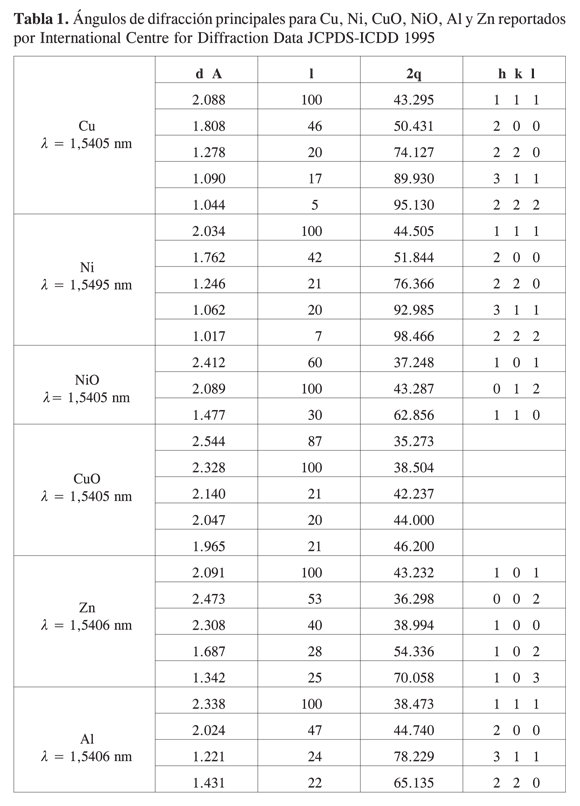
Con los materiales calcinados y los productos reducidos se realizó un estudio de difracción de rayos X (DRX) en un difractómetro JEOL DX-60S (15-16), utilizando filtro de níquel y radiación K (λ=1.5418 Å) de Cu, a una velocidad de 0,5° (2θ) por minuto, con una resolución de 0,25θ. El análisis se realizó sobre los catalizadores en polvo cubiertos con aceite para prevenir la oxidación. Se empleó como patrón de difracción níquel electrolítico en lámina y cobre en polvo del 99,9% de pureza (HopKin & Williams Ltda.)
Para juzgar la actividad generada en los distintos materiales se realizó una serie de procesos de hidrogenación de aceite de soya (AS) en las mismas condiciones de presión y temperatura con cada uno de los catalizadores sintetizados en el equipo descrito en la referencia 17. El nivel de actividad de cada uno se evaluó con base en el consumo de hidrógeno, en las condiciones de reacción descritas y discutidas en la referencia 2.
Para realizar el análisis comparativo de los resultados, los materiales sintetizados se identificaron con la siguiente nomenclatura: el número 5 se refiere a la relación Ni/SiO2 0,5 en peso. Las letras C (cobre), N (níquel) y S (sílice), van seguidas de un número que indica el porcentaje de moles de metales y, por último, se escribe entre paréntesis la temperatura a la cual se realizó la reducción. Por ejemplo: 5NSC30(330) identifica un material con relación Ni/SiO2 0,5 en peso y fracción molar 0,3 de Cu (nCu/(nCu+nNi)), reducido a 330 °C.
RESULTADOS Y ANÁLISIS
Caracteristicas de los absorbentes
Se evaluó el perfil de los difractogramas patrón de cobre y níquel, y sus diferencias con respecto a especies para las cuales se cuenta con la evidencia de cristales mixtos (aleaciones) (18). Se tomaron difractogramas de los patrones, dos aleaciones diferentes, y de los catalizadoresen las mismas condiciones de operación: 40KV, 40mA, ganancia 32 y constante de tiempo 1.
Los difractogramas de la Figura 1 muestran una buena resolución de la señal correspondiente a los ángulos de Ni y Cu cuando se encuentran separados o mezclados (ver Tabla 1). Los hombros que aparecen a la izquierda de cada una de las señales de difracción de mayor intensidad para el níquel, se deben a la distorsión generada por el movimiento de planos producto del trabajo mecánico, ya que se trata de una lámina de níquel; en el cobre en polvo están ausentes.
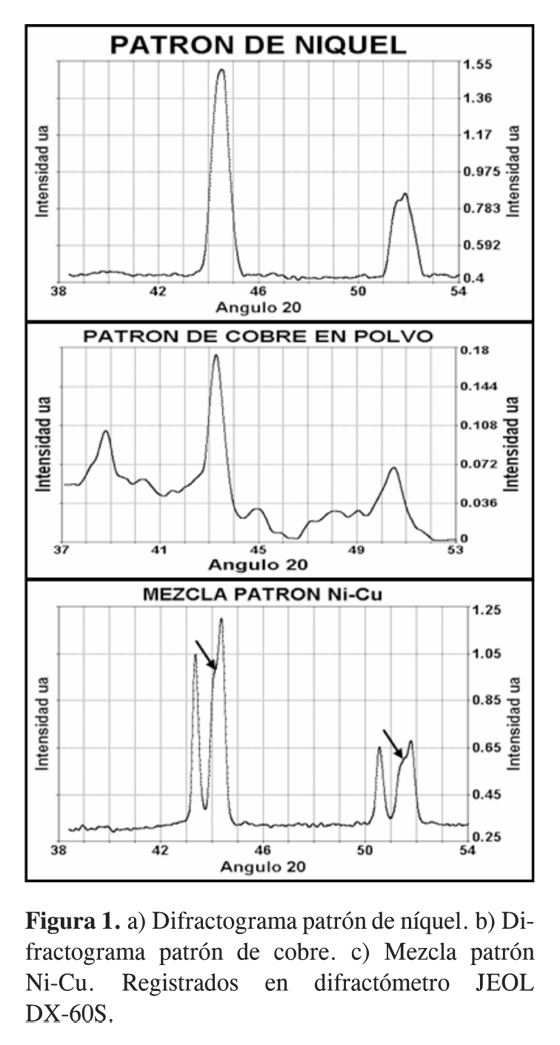
Si se forman cristales mixtos Ni-Cu en las mezclas catalizadoras, la distancia interplanar se incrementa y, por tanto, deben observarse señales de difracción hacia ángulos menores a los reportados para los metales puros, lo que se evidencia a partir de la Ley de Bragg.
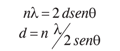
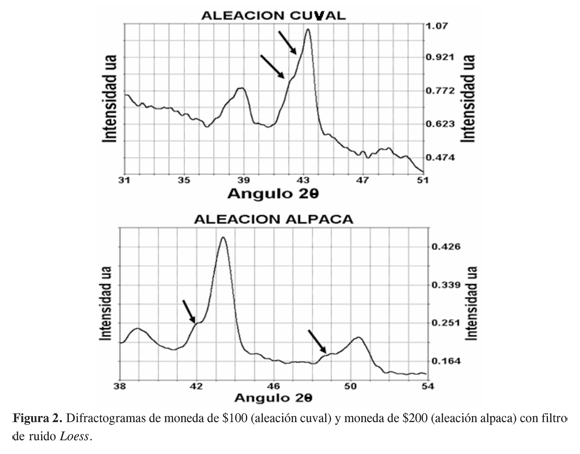
Para confirmar la hipótesis planteada se realizó un estudio DRX de las aleaciones utilizadas para acuñar las monedas de la República de Colombia, de las cuales se conoce la existencia de cristales mixtos, y cuya composición en cinc, cobre y níquel fue amablemente suministrada por el Banco de la República.
Las señales de difracción de mayor intensidad para cada uno de los metales presentes en cada aleación aparecen en la Tabla 1. Puede notarse cómo la señal de difracción de intensidad 100 para los planos (1 1 1) del cobre coincide con la de la misma intensidad para el Zn en la aleación alpaca y, eventualmente, con la de NiO si estuviese presente, dentro de un rango de dispersión de ± 0,1°. Lo mismo sucede para la aleación cubal, la señal que aparece a 2θ 38.504 para el CuO es muy cercana a la del aluminio (38.46), de tal manera que el equipo no permite resolverlos. Por tanto, los hombros que aparecen en la Figura 2 a la izquierda de la difracción principal (43.295) del cobre en las dos aleaciones estudiadas (ver flechas) son ocasionados posiblemente por la distorsión generada en la estructura cristalina debida a la formación de cristales mixtos. En las mismas condiciones de análisis se registró eldifractograma de los precatalizadores y catalizadores sintetizados.
Los precatalizadores no mostraron señales de difracción diferentes a las de losóxidos de cobre y níquel.
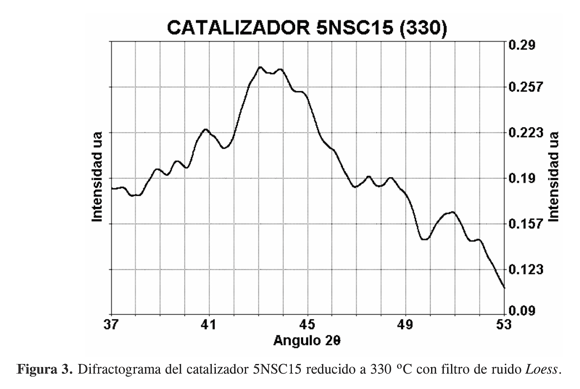
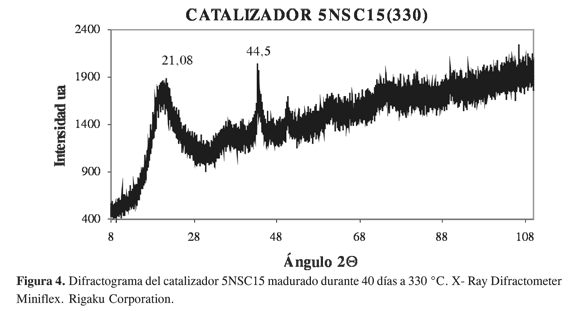
Para el catalizador 5NSC15(330) (Figura 3), se observa que se trata de un material con cristales muy gruesos en cuyo espectro de difracción no es posible asignar, en forma segura, las señales de los componentes, por tanto lo podemos considerar como un material amorfo. Este catalizador se sintetizó seis veces porque a pesar de tener una composición muy similar a catalizadores muy activos, resultó inactivo en el proceso de hidrogenación de AS; el DRX de uno de ellos que se sometió a maduración por cuarenta días a la temperatura de reducción aparece en la Figura 4. Se observa que después del proceso de maduración aparece una cristalización incipiente.
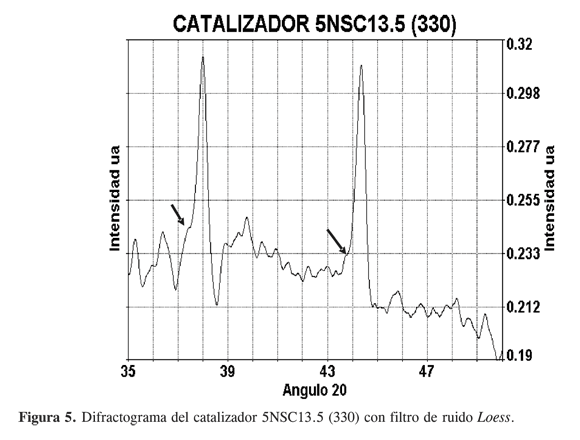
El catalizador 5NSC13.5 (330), de composición muy cercana al anterior, presenta una buena cristalización como se aprecia en el perfil de los picos de difracción relativamente estrechos de la Figura 5; la señal que aparece a 44,5° 2θ, corresponde a la difracción para los planos con índices de Miller (1 1 1) de níquel, y presenta un hombro en 43,9. El otro pico de difracción presente en 38,0 también presenta un hombro en 37,4. En los dos casos la diferencia entre el pico de mayor intensidad y su hombro es de 0,6, lo que nos conduciría a proponer la formación de un cristal mixto Ni-Cu como causante de la distorsión dentro de la estructura cristalina. La señal que aparece a 38,0 es cercana a la de intensidad 100 para el CuO (38,5), sin embargo, la ausencia del pico de intensidad 87, que debe aparecer en 35,237 para el mismo óxido (ver Tabla 1), y la diferencia de 0,5° 2θ con respecto al obtenido experimentalmente para el patrón de CuO, nos lleva a concluir que se trata de una estructura cristalina diferente al óxido de cobre.
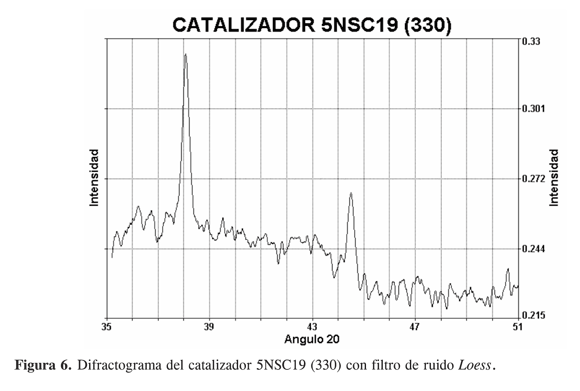
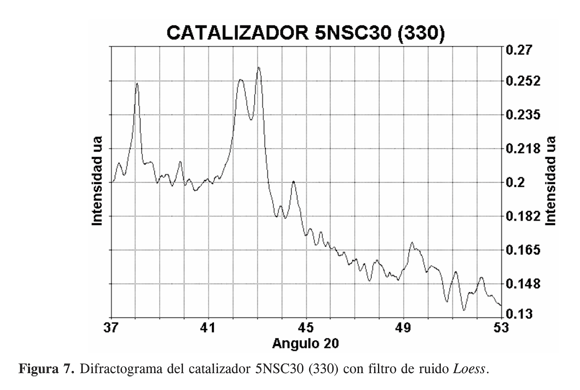
Estas dos señales, con simetría similar, aparecen en los catalizadores 5NSC19(330) y 5NSC30(330) aunque con intensidades relativas diferentes (Figuras 6 y 7, respectivamente). El catalizador 5NSC30(330), tiene además dos señales de mayor intensidad en 42,3 de una estructura no asignada, y en 43,1 de cobre distorsionado, este conjunto de señales indica una buena cristalización del material (Figura 7).
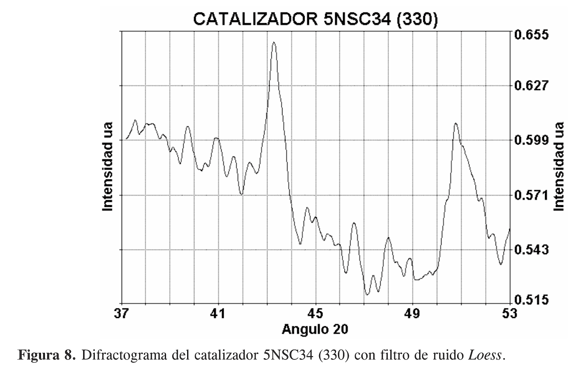
El catalizador 5NSC34(330) (Figura 8) presenta dos señales de difracción en 43,3 y 50,8 con intensidad máxima, pertenecientes al cobre confirmado por el hombro en 50,4, la segunda corresponde a una estructura diferente no asignada. En la primera, por deconvolución de los picos, se puede diferenciar un hombro en 42,8, relacionado posiblemente con una distorsión en la estructura cristalina del cobre, y en el segundo pico se aprecian dos hombros en 50,4 de cobre y 51,8 de níquel.
Se encontró que aquellos catalizadores que desarrollan una estructura cristalina definida presentan mayor actividad frente a la hidrogenación de AS, que aquellos que no desarrollan tal estructura.
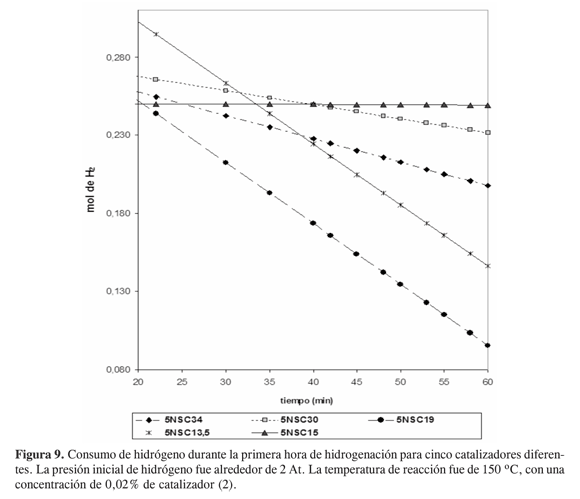
Los catalizadores 5NSC13.5 y 5NSC19, con diferente composición pero estructura cristalina semejante, se caracterizan por tener una actividad muy similar en el proceso de hidrogenación. El catalizador 5NSC15, con composición más cercana al 5NSC13.5, no presentó actividad alguna en el proceso de hidrogenación en comparación con los anteriores, este resultado se confirmó seis veces en síntesis diferentes. Los catalizadores restantes, 5NSC30 y 5NSC34, tienen actividad catalítica intermedia, como se presenta en la tendencia de actividad correspondiente al consumo de hidrógeno (Figura 9).
La ausencia de actividad catalítica, simultáneamente con la ausencia de estructura cristalina en la muestra 5NSC15, en la serie que tiene como única diferencia el contenido de cobre, indica que se ha formado otra u otras fases sólidas en ese punto de composición, distintas a los otros miembros de la serie, y que no presentan actividad catalítica en la hidrogenación de AS.
CONCLUSIONES
Los resultados experimentales muestran que los materiales sintetizados con composición variable de Cu, Ni y SiO2, desarrollan diferentes estructuras cristalinas según la composición, y diferencias en la actividad catalítica. El estudio de rayos X de los materiales sintetizados muestra unalto grado de cristalinidad en los catalizadores 5NSC13.5, 5NSC19 y 5NSC30, que se caracterizan también por presentar dos picos simétricos claramente definidos en 38,1 y 44,5. La aparición de señales de difracción hacia ángulos ligeramente inferiores de los característicos de cobre y níquel puros corresponde al incremento de la distancia interplanar dentro de la estructura cristalina, tal como se puede deducir a partir de la Ley de Bragg y, por tanto, indican la presencia de un tipo de distorsión dentro de la estructura original, posiblemente debido a la formación de un cristal mixto Ni-Cu. Los resultados de las pruebas de hidrogenación de aceite de soya (AS) indican que existe una correlación entre el desarrollo de estructura cristalina en el catalizador y su actividad catalítica, y que puede darse la aparición de fases sólidas diferentes no cristalinas que tampoco son activas catalíticamente. Se considera importante este resultado en cuanto que hasta ahora no se ha propuesto la estructura cristalina del catalizador como un elemento que determine la actividad del mismo.
REFERENCIAS BIBLIOGRÁFICAS
1. Krompiec, S.; Mrowiec-Bialon, J.; Skutil, K.; Dukowicz, A.; Pajak, L.; Jarzebski, A. B. Nickel-alumina composite aerogel catalysts with a high nickel load: a novel fast sol-gel synthesis procedure and screening of catalytic properties Journal of Non-Crystalline Solids. 2003. 315: 297-303. [ Links ]
2. Cubillos, G. I. Estudio de la sinergia del sistema cobre, níquel, sílice en la hidrogenación de aceite de soya. Tesis de maestría, Facultad de Ciencias, Departamento de Química, Universidad Nacional de Colombia. Bogotá. 2004. [ Links ]
3. Bond, G. C. The twelve-The hydrogenation of Acetylenic Compounds and Diolefins. En: Catalysis by Metals. Academic Press. London and New York. 1962. pp. 281-309. [ Links ]
4. Bond, G. C. The thirteen-The hydrogenation of Aromatic and Heterocyclic Compounds. En: Catalysis by Metals. Academic Press. London and New York. 1962. pp. 311-334. [ Links ]
5. Kang, M.; Song, M. W. et al. g Alumina Supported Cu-Ni Bimetallic Catalysts: Characterization and Selective Hydrogenation of 1,3-Butadiene. The Canadian Journal of Chemical Engineering. 2002. 80: 63-70. [ Links ]
6. Martin, G. A.; Dalmon, J. A. Benceno Hydrogenation over Nickel Catalysts at Low and High Temperatures: Structure- Sensitivity and Copper Alloying Effects. Journal of Catalysis . 1982. 75: 233-242. [ Links ]
7. Jens, S.; Johannes, A. P. Gelten and Stig Helveg. Sintering of nickel catalysts: Effects of time, atmosphere, temperature, nickel-carrier interactions, and dopants Applied Catalysis A: General. 2006. 309: 237-246. [ Links ]
8. Gaigneaux, E. M.; Abdel Dayem, H. M.; Godard, E.; Ruiz, P. Dynamic phenomena and catalytic reactivities of oxide surfaces. Applied Catalysis A: General. 2000. 202: 265-283. [ Links ]
9. Pyatnitsky, Y.; Ilchenko, N. Some kenetic of unsteady - state partial oxidation reactions. Dinamic processes on metal oxide surfases. Catalysis Today. 1996. 32: 21-28. [ Links ]
10. Gil, A.; Ruiz, P.; Delmon, B. Effect of the support and added oxides on the bistability observed in the oxidative dehydrogenation of 2- propanol over copper- supported catalysts. Catalysis Today. 1996. 32: 185-191. [ Links ]
11. Acevedo, M. A. Estudio de la relación Ni/SiO2 en un catalizador de alta actividad para la hidrogenación de aceites. Tesis. Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia. Bogotá. 1989. [ Links ]
12. Schwarz, J. A. Methods for preparation of Catalytic Materials. American Chemistry Society. 1995. 95: 477-510. [ Links ]
13. Gates, B. C. Methods for preparation of Catalytic Materials. American Chemistry Society. 1995. 95: 511-522. [ Links ]
14. Trujillo, A. Búsqueda de un método de obtención de un catalizador Ni-SiO2 de alta actividad en la hidrogenación de aceites a partir de ferroníquel. Tesis. Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia. Bogotá. 1988. [ Links ]
15. Jeol. X ray spectrometer System JSX-60S Series pp 1-4. [ Links ]
16. Jenkins, R.; Snyder, R. Introduction to X-ray powder diffractometry. John Wiley & Sons. INC. New York. 1996. [ Links ]
17. García, J. A., De Milleri, P. A semiautomatic batch reactor for the study of vegetable oil hydrogenation. Instrumentation Science & Tecnology. 1999. 27: 335-341. [ Links ]
18. Losana, L.; Ferrer, J. M. Metalurgia. Manuel Marín. Barcelona. 1951. pp. 38-39. [ Links ]














