Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Química
Print version ISSN 0120-2804On-line version ISSN 2357-3791
Rev.Colomb.Quim. vol.38 no.2 Bogotá May/Aug. 2009
ESMECTITA PILARIZADA CON Al-Ce, MODIFICADA CON ÓXIDO DE POLIETILENO. EMPLEO COMO SOPORTE CATALÍTICO PARA EL NÍQUEL
Al-Ce PILLARED SMECTITE MODIFIED WITH POLYETHYLENE OXIDE. USE AS NICKEL CATALYTIC SUPPORT
ESMECTITA PILARIZADA COM Al-Ce MODIFICADA COM ÓXIDO DE POLIETILENO, UTILIZADA COMO UN SUPORTE CATALITICO PARA O NIQUEL
Carlos Enrique Daza, Fabián Puentes, Sonia Moreno, Rafael Molina1
1 Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia, sede Bogotá. Bogotá, Colombia. Autor para correspondencia: ramolinag@unal.edu.co
Recibido: 14/02/09 - Aceptado: 10/08/09
RESUMEN
Se modificó una esmectita natural con soluciones mixtas de Al-Ce en presencia de un tensoactivo de tipo no iónico (óxido de polietileno). La intercalación se llevó a cabo asistida por ultrasonido para favorecer la homogenización de la mezcla y la difusión de especies hacia la interlámina del mineral. Se estudió el efecto de la relación tensoactivo-arcilla y la potencialidad de estos materiales como soportes catalíticos para el níquel. Los análisis termogravimétricos indicaron que la descomposición del tensoactivo se da a 500 °C. Los espectros DRIFT y DRX sugieren que la incorporación del tensoactivo se presenta en la superficie externa del mineral, el cual fue pilarizado. El aumento en la cantidad de tensoactivo causó pérdida de cristalinidad del material. La presencia del tensoactivo induce la formación de mesoporos. Los TPR-H2 indicaron que la modificación en presencia del tensoactivo favorece la reducibilidad del Fe del mineral. Se identificaron diferentes especies reducibles de Ni sobre la superficie del soporte, evidenciándose un aumento en la interacción níquel-soporte y en la reducibilidad a 700 °C con H2 puro para los catalizadores obtenidos a partir de los materiales modificados con tensoactivo. Se obtuvieron catalizadores con buena distribución del níquel en la superficie, tamaños de cristalitos menores de 10 nm y estabilidad térmica limitada. Los catalizadores modificados con tensoactivos soportados sobre arcillas presentaron mejores actividades catalíticas en el reformado de metano con CO2 a 700 °C (WHSV =60Lg-1h-1) con menores niveles de formación de coque.
Palabras clave: esmectita, tensoactivo, soporte catalítico, níquel.
ABSTRACT
A natural smectite was modified with Al-Ce solutions in the presence of Non-ionic surfactant (polyethilene oxide). The intercalation was carryingoutby ultrasound assistance in order to promote homogenization of the slurry and the diffusion of species into the lamellar space of mineral clay. The effect of surfactant-clay ratio and the potential of these solids like nickel catalytic supports were investigated. Thermogravimetical analysis indicated that the surfactant decomposition it is completed at 500 °C. DRIFT and XRD spectra suggest that the incorporation of the surfactant is on the external surface of clay and that the mineral was pillared. The increase in the surfactant ratio causes a lose of cristallinity material. The presence of surfactant induced mesoporous formation in the material. TPR-H2 indicated that the modification in presence of surfactant promotes the reducibility of Fe in the mineral. Several Ni reducible species on the support surface were identified. The interaction Ni-support and the reducibility with pure H2 at 700 °C were increased when the mineral clay was modified with the surfactant. Catalysts with good nickel distribution, particle size under 10nm and thermal stability limited was obtained. Ni-Catalyst supported on surfactant modified clays showed the best catalytic performance in the CO2 reforming of methane at 700 °C (WHSV =60Lg-1h-1) whit the lowest coke formation.
Key words: smectite, surfactant, catalytic support, nickel.
RESUMO
Uma esmectita natural foi modificada pelo meio de uma mistura com uma solução de Al-Ce, na presença de um surfactante do tipo nonionic (óxido de polietileno). A intercalação foi realizada assistida por ultra-som para facilitar a homogeneização da mistura e da difusão das espécies no espaço interlamelar da argila mineral. Nós estudamos o efeito do peso argila-surfactante e as potencialidades destes materiais como suporte para os catalisadores do níquel. A análise termogravimétrica indicou que a decomposição da superfície é completa a 500 °C. Espectros DRIFT e DRX sugerem que a incorporação do surfactante ocorre preferencialmente na superfície externa da argila e que foi modificada pelo meio dum processo do pilarização. O aumento da quantidade de surfactante provoca uma perda de cristalinidade do material. A presença da surfactante induziu a formação do mesoporous no material. O TPR-H2 mostrou que a mudança na presença do surfactante favorece a redução do Fe neste mineral. Também foi possível a identificação de uma formação de espécies reduzíveis do níquel na superfície do meio que. Encontraram-se um aumento do níquel-suporte a interação e reducibilidad em 700 °C com H2 puro para os catalisadores feitos de materiais com superfície modificada. Catalisadores foram obtidos com boa distribuição de níquel na superfície, e tamanho do cristal menores de 10nm e estabilidade térmica limitada. O catalisador suportado em argila modificada com surfactante mostrou melhor atividade catalítica na reforma do metano a 700 °C (WHSV =60Lg-1h-1) com baios níveis de formação de coque.
Palavras-chave: esmectita, surfactante, suporte catalítico, níquel.
INTRODUCCIÓN
Los minerales arcillosos son materiales muy interesantes como soportes catalíticos debido a su gran abundancia, bajo costo y propiedades particulares (1). La modificación de estos minerales mediante intercambio con polihidroxocationes inorgánicos de mayor tamaño y posterior calcinación, genera materiales con especies estables y altamente distribuidas del óxido metálico, incrementando el espaciado interlaminar del mineral y creando una nueva estructura porosa (1, 2). Los polihidroxocationes de aluminio se han convertido en la especie modificante más ampliamente estudiada (1-4), sin embargo, se conocen métodos que involucran la intercalación con especies mixtas con otro catión de transición que presente propiedades catalíticas o promotoras específicas (1). En especial, el cerio se ha empleado como componente de varios sistemas catalíticos en reacciones de oxidación puesto que posee la capacidad para cambiar fácilmente de estado de oxidación, mejora la dispersión metálica, aumenta la estabilidad térmica de los soportes, promueve la oxidación-reducción de metales nobles y acumula y libera oxígeno en la superficie (5-8).
La síntesis de arcillas modificadas asistida por ultrasonido, ha sido reportada como un método que se caracteriza por presentar efectos positivos en la disminución de tiempo en el procedimiento, la difusión de especies hacia el espacio interlaminar, la homogenización de la mezcla y el aumento en la estabilidad térmica del material resultante (9, 10).
Por otra parte, el empleo de tensoacti-vos de tipo no iónico ha permitido la modulación de la porosidad de los minerales arcillosos modificados (11, 12). La ventaja de este método es que el tamaño del poro es controlado por el tamaño de los agregados conformados por los tensoactivos permitiendo una amplia versatilidad en el método (11, 12). Igualmente, se ha reportado que el tamaño de los poros del material final depende directamente de la cantidad de tensoactivo adicionada en la suspensión. Dicha metodología se ha empleado en la obtención de soportes catalíticos con alta estabilidad térmica y grandes áreas superficiales (13).
Se han reportado diversos trabajos sobre la modificación de esmectitas con ten-soactivos no iónicos para la obtención de soportes catalíticos, específicamente para el níquel, empleando diferentes tipos de tensoactivos y soluciones modificantes de varios metales, y obteniendo materiales de tipo mesoporoso con elevada área superficial y altas dispersiones del níquel luego de su impregnación vía húmeda (14, 15). Igualmente, los catalizadores presentan altas actividades catalíticas en la reacción de reformado de metano con CO2 y moderadas desactivaciones por coquización (13).
El principal objetivo del presente trabajo es evaluar la viabilidad de la obtención de soportes catalíticos para el níquel, promovidos con cerio, para el reformado de metano con CO2, a partir de la modificación de una esmectita natural en presencia de óxido de polietileno (Tergitol l5-S-9) y ultrasonido, sistema que hasta el momento no ha sido estudiado. Se presentan los resultados de la síntesis y la caracterización estructural, textural y morfológica de los soportes y catalizadores y laevaluacióncatalíticaenelreformadode metano con CO2 a 700 °C (WHSV =60 Lg-1h-1) en donde se estudia el efecto de la relación tensoactivo/arcilla.
MATERIALES Y MÉTODOS
Material de partida
El material empleado es un mineral arcilloso esmectítico clasificado como montmorillonita tipo chamber, proveniente del departamento del Tolima (Colombia), previamente caracterizado, cuya composición química es 58,91% de SiO2, 15,40% de M2O3, 5,79% de FeO3, 1,13% de Na2O, 2,83% de CaO y 2,73% de MgO (16). Se empleó la fracción con tamaño de agregado menor a 50 μm obtenida por sedimentación vía húmeda, siguiendo la ley de Stokes. El material de partida se intercambió dos veces con NaCl 1 M empleando una relación de 20 mLg-1 a temperatura ambiente por un periodo de 24 h. Se realizaron lavados con agua destilada y secado a 60 °C.
Síntesis de los soportes catalíticos
La solución modificante se preparó a partir de una solución comercial de clorhidrato básico de aluminio 0,1 M y Ce(NO3)3.6H2O. La sal de cerio se disolvió en la solución de aluminio manteniendo una relación molar Ce/(Al + Ce) igual a 10%. Posteriormente, la mezcla se maduró durante 2 h a 60 °C.
El mineral intercambiado con sodio se dispersó en agua destilada en presencia de cantidades determinadas y variables de óxido de polietileno (Tergitol 15-S-9), y se agitó vigorosamente durante 24 h a temperatura ambiente. La solución modificante se adicionó gota a gota sobre la suspensión del mineral arcilloso (20 meqg-1) bajo agitación a 80 °C con envejecimiento durante 2 h. Luego, la suspensión se sometió a ultrasonido durante 300 minutos (90W, 47kHz) a temperatura ambiente. El sólido se separó por decantación y fue secado a 80 °C. El material resultante se calcinó a 500 °C durante 4 h, para lo cual, la temperatura se incrementó a una rampa de 10 °Cmin-1 con isoterma durante 15 minutos cada 100 °C (14, 15). Posteriormente, los materiales se lavaron con agua destilada y se secaron a 100 °C durante 12 h. Los sólidos fueron denominados SAX, en donde X corresponde a la relación en masa tensoactivo-arcilla, con valores entre 0,0 y 2,0.
Síntesis de los catalizadores
Los catalizadores fueron preparados por el método de impregnación húmeda empleando Ni(NO3)2.6H2O como sal precursora y 10% en peso de Ni. Los sólidos se calcinaron a 500 °C durante 4 h empleando una rampa de 10 °Cmin-1. Los catalizadores obtenidos se denominaron NiSAX.
Caracterización
Los análisis termogravimétricos se realizaron en un equipo TA-Instrument 2950 con una precisión de ± 0,001 mg, bajo atmósfera de aire a 100 mL/min y una rampa de calentamiento de 10 °Cmin-1.
Los espectros DRIFT se tomaron en un equipo Magna IR 560 Nicolet a temperatura ambiente y sin ningún tratamiento previo.
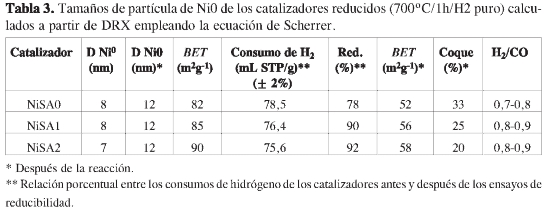
Los patrones de DRX en polvo se llevaron a cabo en un equipo Bruker AXS, modelo D8 Advanced, equipado con ánodo de cobre. Los tamaños promedio de partícula fueron calculados usando la ecuación de Scherrer: D = kλ/βCosθ, donde D es el tamaño de partícula, λ es la longitud de la radiación empleada, k es una constante geométrica, β es el ancho a altura media de la señal expresado en radianes y θ el ángulo de difracción (17).
Las áreas superficiales BET se midieron por adsorción de N2 a 77 K usando un equipo Micromeritics ASAP 2000.
Los perfiles de TPR-H2 se tomaron en un equipo Chembet 3000 Quantachrome, equipado con un detector de conductividad térmica, siguiendo metodologías ya reportadas . Las muestras (< 250 μm) fueron previamente desgasificadas a 400 °C por 1 h en flujo de Ar y reducidas con una rampa de calentamiento de 10 °C/min, empleando 10% (v/v) H2/Ar a 30 mL/min. Los ensayos se realizaron bajo condiciones que garantizaron resultados libres de los efectos de las variables de operación en la forma y temperatura máxima de los perfiles de reducción (18, 19). Los pretratamientos sobre los catalizadores se realizaron a 700 °C durante 1 h con un flujo de H2 puro de 30 mLmin-1 y una rampa de calentamiento de 10 °Cmin-1. El enfriamiento se realizó con flujo de Ar de 30 mLmin-1. Se realizaron ensayos de TPR-H2 bajo las condiciones antes mencionadas.
Los análisis de microscopía electrónica de barrido (SEM) se llevaron a cabo en un equipo FEI Quanta 200 provisto de un sistema de microanálisis por energía dispersiva (EDX).
Evaluación catalítica
Los ensayos catalíticos se realizaron utilizando 50 mg del sólido en polvo. Los catalizadores fueron reducidos a 700 °C (rampa de 10 °Cmin-1) con H2 puro (30 mLmin-1) durante una hora. El reactor se alimentó con una mezcla 5/5/40 CH4/ CO2/N2 y flujo de 50 mLmin-1. Los gases de salida fueron analizados por dos cro-matógrafos conectados en línea, equipados con detectores de conductividad térmica. Con el primer cromatógrafo se determinaron CH4 yCO2, los cuales fueron separados por medio de una columna Carboxen 1006 (He: 25 mLmin-1). La relación H2/CO se determinó empleando el segundo cromatógrafo, el cual fue equipado con un tamiz molecular (Ar: 25 mLmin-1).
RESULTADOS Y DISCUSIÓN
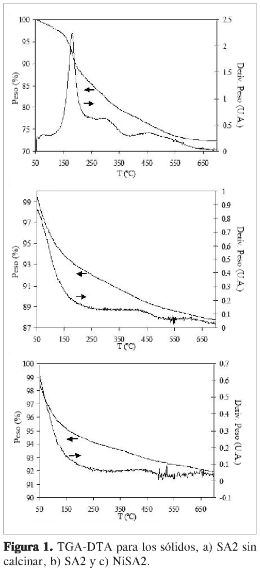
El termograma del sólido SA2 sin calcinación presenta diferentes eventos térmicos (Figura 1). El primero de ellos ocurre entre 150 y 240 °C correspondiente a una pérdida de peso de 12.5%. Este evento ha sido asignado a la pérdida de agua fisiadsorbida y simultánea deshidroxilación parcial de los polímeros catiónicos incluidos en el espacio interlaminar del mineral (20). Sin embargo, también se ha reportado que la descomposición y desorción del tensoactivo comienza a suceder cerca de los 200 °C, y que la cantidad de agua fisiadsorbida es mínima, debido a la naturaleza hidrofóbica de la superficie (21). En la región entre 250 y 550 °C ocurren dos eventos térmicos que corresponden a una pérdida de peso de 15,1 y 27,5% respectivamente, y resultan de la combinación de una deshidroxilación completa de los polímeros catiónicos para generar óxidos, la deshidroxilación de las láminas del mineral y la descomposición completa de los residuos carbonáceos producto de la descomposición de la molécula orgánica (20).
El termograma para el soporte SA2 luegodelacalcinacióna500 °C durante4 h registra una pérdida de peso de 11,8% por debajo de los 200 °C, la cual puede asignarse a la desorción de moléculas de agua fisisorbidas en las láminas del mineral o en los pilares a causa de la rehidratación del material (20). El termograma para el catalizador NiSA2 es similar al del soporte SA2, y muestra una pérdida de peso de 8,2%. En ambos casos, la región por encima de los 250 °C presenta pérdidas de masa causadas por la deshidroxilación parcial del mineral, las cuales son considerablemente bajas debido a la calcinación de los materiales. Los resultados indican que no hay presencia de residuos carbonáceos en los soportes ni en los catalizadores.
De esta manera, los análisis termograviméticos señalan que los procesos de calcinación elegidos para la síntesis de los materiales, son los adecuados para generar la descomposición completa tanto de la materia orgánica proveniente del tensoactivo, como de los nitratos provenientes de la sal precursora de Ni.
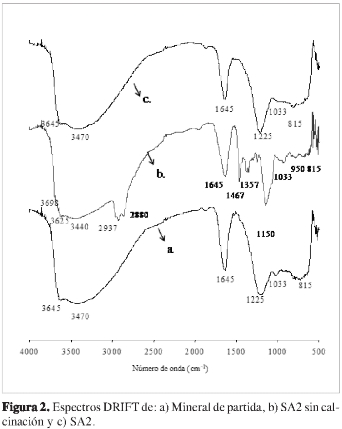
La Figura 2 registra los espectros DRIFT para el soporte SA2, antes y después de la calcinación, y para el catalizador NiSA2. Cada uno de los espectros DRIFT presenta señales características del mineral de partida. En efecto, en el espectro del sólido SA2 sin calcinación, se registra la señal a 3 625 cm-1 correspondiente a estiramientos de grupos -OH estructurales, la cual es típica de esmectitas con alto contenido de Al en la capa octaédrica (22-24). En el caso de los sólidos SA2 y NiSA2, se observa un ligero corrimiento de las señales correspondientes a grupos -OH estructurales hacia 3 645 cm-1. Este desplazamiento puede estar relacionado con la transformación térmica del material y con la formación de nuevos grupos hidroxilo en los óxidos interlaminares (22-24).
Las señales a 3 440 y 1 645 cm-1 corresponden al agua adsorbida mientras que la señal a 1 033 cm-1, al estiramiento asimétrico de los enlaces O-Si-O (22-24). Se ha reportado que el desplazamiento de la señal a 1 033 cm-1 hacia valores mayores, está relacionado con la formación de los pilares en el espacio interlaminar del mineral (22-24). Sin embargo, en los resultados del presente estudio no se observa un corrimiento considerable de esta señal, sino una disminución de su intensidad, luego del proceso de modificación, lo cual se explica por la deshidroxilación parcial de la estructura del mineral. De la misma manera, la señal a 1 150 cm-1 para el material sin calcinación, se desplaza a 1 225 cm-1 en los sólidos SA2 y NiSA2, lo cual ha sido previamente asignado a la formación de un nuevo enlace M(IV)-O- Al entre el pilar y las capas tetraédricas del mineral arcilloso (22).
La banda localizada a 950 cm-1 en el soporte SA2 sin calcinar (deformaciones AlAlOH), no se observa en los espectros de los sólidos SA2 y NiSA2, debido posiblemente a la deshidroxilación de la arcilla. Por otra parte, en los tres sólidos se observa una banda a 815 cm-1 asignada a estiramientos asimétricos AlFeOH en la capa octaédrica del mineral, la cual no sufre cambios significativos luego del proceso térmico (23).
Por otro lado, en el espectro para el soporte sin calcinación, pueden apreciarse bandas características del tensoactivo adsorbido en la superficie del mineral arcilloso. Así, las bandas a 2 937 y 2 880cm-1 corresponden a vibraciones -CH2 asimétricas y simétricas respectivamente, mientras que las señales a 1357 y 1467cm-1 se asignan a deformaciones asimétricas y simétricas de los enlaces C-H en los grupos R-CH3 (25). Se ha considerado que estas señales podrían estar ausentes debido a las interacciones ion-dipolo entre los grupos hidroxilados del tensoactivo y los cationes de intercambio de la arcilla, cuando la molécula orgánica se encuentra en la cavidad interlaminar de la esmectita (11). Este aspecto sugiere que la incorporación del tensoactivo en nuestros materiales se da preferencialmente en la superficie externa de la arcilla, y que esta interacción puede darse mediante enlaces de hidrógeno entre los grupos -OH superficiales del mineral y terminales del tensoactivo.
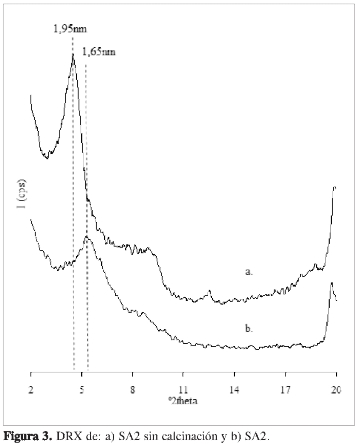
La Figura 3 registra los patrones de DRX para el sólido SA2 antes y después de la calcinación. La línea d001 (1,95 nm) para el material sin calcinar, es típica de esmectitas intercaladas con policationes de Al que luego de la calcinación generan los pilares de Al2O3 (1-3). Se ha reportado la síntesis de arcillas con pilares mixtos de Al-Ce que presentan espaciados basa-les hasta de 2,57 nm luego de la calcinación a 500 °C (26). En el presente trabajo se observa que luego de la calcinación la línea d001 se desplaza hasta 1,65 nm indicando la formación del pilar de Al probablemente "adornado" o dopado con óxidos de Ce (5, 27).
Los resultados de DRX sugieren que la incorporación del tensoactivo se da en la superficie externa de la arcilla debido a que no se observan cambios en la línea d001 que indiquen la formación de agregados micelares de gran tamaño en los espacios interlaminares, lo que está de acuerdo con los resultados de espectroscopía DRIFT.
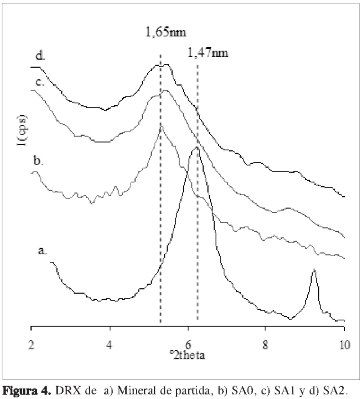
La Figura 4 registra los patrones de DRX para la serie de arcillas modificadas con diferentes cantidades de tensoactivo. Los resultados indican que todos los sólidos fueron modificados vía pilarización, puesto que se observa un corrimiento en el espaciado basal de 1,40 nm (mineral arcilloso de partida) a 1,65 nm en los materiales modificados (28, 29). La línea d001 para las arcillas modificadas es menos intensa que para la arcilla natural, debido a la pérdida de agua de los espacios interlaminares y a la inserción de pilares ligeramente irregulares en tamaño.
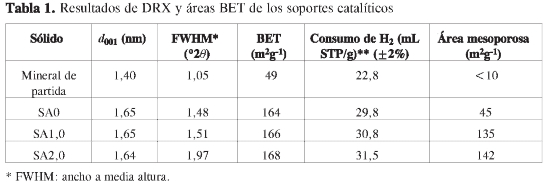
La Tabla 1 presenta en detalle los resultados de los patrones de DRX para los soportes catalíticos. Se evidencia que los espaciados interlaminares de los materiales son menores a los que generalmente se reportan para sistemas similares (entre 1,7 y 1,85 nm) (1-3). Esta característica se debe principalmente al tratamiento térmico de calcinación que se realiza sobre los sólidos (500 °C durante 4 h), más severo que los tradicionalmente usados (400 °C durante 2 h).
Por otra parte, los anchos de las líneas d001 para los materiales modificados con óxido de polietileno son ligeramente mayores en comparación con el sólido que se modificó en ausencia de tensoactivo (material SA0). Algunos autores han señalado la relación entre el ancho a altura media y
la distribución de pilares en el espacio interlaminar del mineral modificado (2, 4). De esta manera, se puede sugerir que la modificación en presencia de óxido de polietileno causa un detrimento en la cristalinidad de los materiales, siendo más evidente el efecto con mayores cantidades de ten-soactivo (material SA2).
Como puede observarse en la Tabla 1, el área superficial del mineral arcilloso de partida se incrementó de 49 m2g-1 a 164-168 m2g-1, indicando la formación de una nueva estructura porosa. Es ampliamente conocido que la formación de microporos en los espacios interpilares contribuye en mayor extensión al área superficial total, mientras que los mesoporos formados entre agregados laminares contribuyen en menor proporción (1-3).
Sin embargo, aplicando diferentes procedimientos de modificación con tensoactivos, se han reportado materiales con áreas superficiales superiores a las de los materiales obtenidos en el presente trabajo (13). Estas diferencias probablemente son el resultado tanto del método de modificación como de la naturaleza del mineral arcilloso de partida.
Las áreas superficiales BET para los sólidos SA0, SA1 y SA2, registran valores muy similares entre sí, lo cual no permite establecer correlaciones y tendencias. Como se sugirió, la adsorción del tensoactivo en el método asistido con ultrasonido ocurre preferencialmente en la superficie externa del mineral y no en los espacios interlámina e interpilar, siendo estos últimos los de mayor aporte en el área superficial. No obstante, como se puede observar, los materiales modificados con tenso-activos son mayoritariamente mesoporosos (82% del area total); dichos mesoporos son formados por los agregados conformados por el tensoactivo entre las agrupaciones de láminas de la arcilla que son eliminados mediante la calcinación del sólido (1-3).
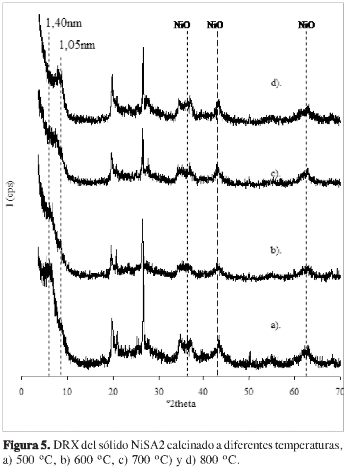
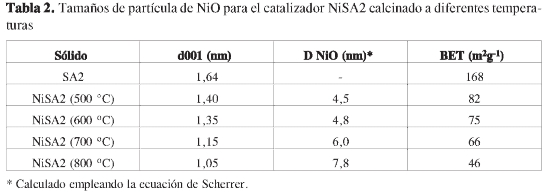
La Figura 5 registra los patrones de DRX para el material SA2 impregnado con 10% Ni, calcinado a 500 °C (NiSA2) y sometido adicionalmente a diferentes temperaturas de calcinación durante 2 h. La Tabla 2 resume los resultados de los difractogramas mencionados y del área BET determinada. En primer lugar, se aprecia que luego de la impregnación con níquel y de la calcinación del soporte catalítico, el espaciado basal se desplaza de 1,64 nm a 1,40 nm y se evidencia una pérdida en la intensidad de la reflexión, como resultado del proceso térmico aplicado para la descomposición del precursor. La calcinación del catalizador NiSA2 a diferentes temperaturas, causa un descenso progresivo en la línea d001 hasta registrar un valor de 1,05 nm a 800 °C, lo que indica el colapso del espacio interlaminar del mineral.
Por otra parte, los tamaños de partícula del NiO calculados con la ecuación de Scherrer, evidencian la formación de nanopartículas en la superficie del soporte. En el análisis de los tamaños de partícula, la interferencia provocada por la presencia de señales de minerales contaminantes en el soporte, puede causar desviaciones de los valores que, a su vez, pueden provocar grandes diferencias en las determinaciones. Es posible asumir que en todos los casos, dichas incertidumbres son las mismas para cada material. Los procesos térmicos aplicados a los materiales, causan un aumento en el tamaño de los agregados de NiO; sin embargo, la sinterización no es dramática hasta 800 °C, en donde se registran tamaños de partícula de 7,8 nm. Esto indica buena estabilidad de los agregados de níquel en la superficie de estos materiales.
Como puede observarse en la Tabla 2, luego de la impregnación con Ni el área superficial del material SA2 disminuye de 168 a 82 m2g-1, debido a la formación de agregados de NiO en la porosidad del sólido y al proceso térmico de descomposición del precursor. A mayor temperatura de calcinación, se observa un descenso progresivo del área superficial, lo cual se relaciona directamente con los cambios cristalográficos observados en la fase esmectítica que son evidentes en la Figura 5.
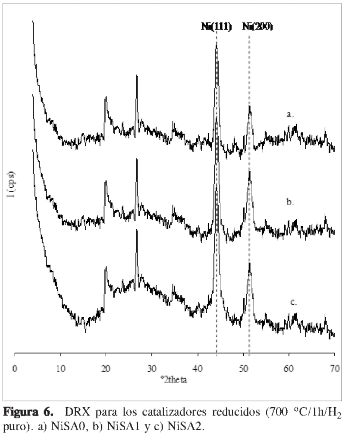
En la Figura 6 se registran los patrones de DRX para los catalizadores reducidos a 700 °C durante una hora con H2 puro, donde se evidencian solamente las reflexiones características del Ni0 y la ausencia de formación de otro tipo de fases cristalinas. Igualmente, se puede apreciar que en estos materiales la línea d001 prácticamente desaparece luego del proceso de reducción, sugiriendo una pérdida total de la cristalinidad de la fase esmectitas.
En la Tabla 3 se reportan los tamaños del cristalito metálico para los catalizadores reducidos calculados con la ecuación de Scherrer, lo cual revela la formación de nanopartículas de Ni de tamaños menores que io nm. Los catalizadores cuyo soporte fue sintetizado con tensoactivo (NiSA1 y NiS A2) presentan tamaños de partícula ligeramente inferiores al catalizador NiSAo, sugiriendo un efecto positivo. Anteriormente, se han reportado tamaños de partícula mayores (12-18 nm) y tendencias similares conrespecto a la cantidad de tensoactivo .
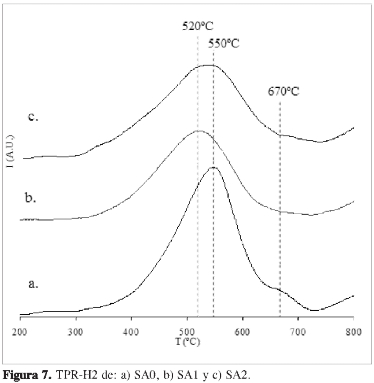
La Figura 7 ilustra los perfiles de TPR-H2 para los soportes catalíticos modificados con diferentes cantidades de óxido de polietileno. Como puede observarse, se registra un pico de máxima reducción entre 520 y 550 °C correspondiente a la reducción de óxidos de hierro depositados en la superficie externa de las láminas del mineral arcilloso (31). En el caso de los soportes catalíticos sintetizados con mayores cantidades de tensoactivo, el desplazamiento en las temperaturas de reducción de 550 a 520 °C sugiere que el tensoactivo favorece la accesibilidad a los óxidos de hierro, causando una disminución en su temperatura de reducción, lo cual podría estar relacionado con el tamaño de los aglomerados cristalinos y su morfología. En la Tabla 1 se registran los consumos de hidrógeno para los soportes catalíticos, en donde es posible observar que los materiales modificados con Al-Ce presentan valores ligeramente superiores al mineral natural, lo cual indica la contribución de la reducción del Ce incluido. Sinembargo, puedenotarsequelacontri-bución más importante en la reducción del soporte corresponde al Fe que naturalmente se encuentra decorando las láminas exteriores del mineral.
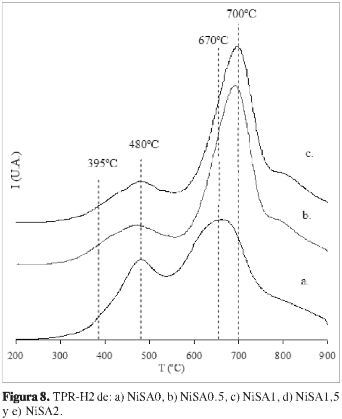
Los perfiles deTPR-H2paraloscatali-zadores impregnados con 10% nominal de Ni (Figura 8), evidencianla formación de especies reduci-bles de níquel con diferentes ambientes químicos. Como es de conocimiento general, la naturaleza heterogénea de la superficie de las arcillas naturales modificadas implica las diferentes localizaciones que puede adoptar el níquel cuando es impregnado (1). Los perfiles registran en todos los casos, dos picos principales de formas asimétricas con temperaturas de máxima reducción en 480 °C y 670-700 °C respectivamente, con consumos de hidrógeno independientes de las variables de síntesis (Tabla 3) lo cual es coherente con otros reportes (32). Las temperaturas de máxima reducción se encuentran por encima de la correspondiente al NiO, lo cual, bajo las condiciones de los ensayos realizados aquí, es de 400 °C, sugiriendo la formación de especies de níquel que presentan interacción con el soporte. De esta manera, es posible clasificar los tipos de especies reducibles en aquellas con interacciones Ni-superficie débiles (~480 °C) y con interacciones fuertes (~700 °C y hombro en ~800 °C).
Es posible asociar los perfiles de reducción del níquel para estos materiales con el ambiente químico del metal. Los tipos de especies reducibles de baja interacción pueden relacionarse con aquellos clústeres de NiO formados en la superficie externa del mineral, es decir, sobre las láminas y/o sobre los agregados de óxidos, principalmente de Fe, deposita dos sobre dichas láminas. Por su parte, las especies reducibles de alta interacción pueden relacionarse con clústeres de NiO formados en los espacios interlámina e in-terpilar y con especies de NiO que decoran los pilares de Al2O3. Debido a la mi-croporosidad de los intersticios inter-lámina e interpilar, es muy factible que los clústeres formados allí, sean de menor tamaño que los formados en la superficie externa.
Adicionalmente, es posible observar en la Figura 8 que el perfil para el sólido NiSA0 presenta señales más anchas que el resto de la serie de sólidos sintetizados. El pico correspondiente a especies reducibles de mayor intensidad en el sólido NiSA0, presenta una menor temperatura de reducción que el resto de la serie de materiales, indicando que para los soportes sintetizados en presencia de tensoactivos, se generan especies de NiO cuyas interacciones con la superficie son más fuertes. Por otra parte, para el sólido NiSA0 se observa una mayor intensidad en el pico a 480 °C, lo cual sugiere la formación de una mayor cantidad de especies de baja interacción. Igualmente, es posible apreciar que para los sólidos NiSA0 y NiSA 0.5, la formación de NiO libre (pico observado a 395 °C) se desfavorece con mayores cantidades de tensoactivo.
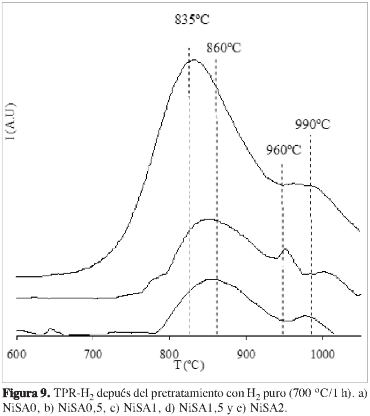
Con el objetivo de evaluar la reducibilidad de los catalizadores, se realizaron perfiles de TPR-H2 sobre los materiales reducidos previamente a 700 °C con H2 puro durante una hora (Figura 9). En primer lugar, se observa que la reducibilidad de los catalizadores bajo estas condiciones es parcial, puesto que solamente parte de las especies de alta interacción Ni-superficie son reducidas. Los perfiles de los sólidos pre-reducidos se caracterizan por picos entre 840 °C-860 °C y entre 940 °C-960 °C. En comparación con los materiales sin pretratamiento, las temperaturas de reducción son mayores sugiriendo que la formación de nanopartículas de Ni0 en la superficie del material y/o el cambio en la cristalinidad del sólido, dificultan la reducción del NiO que continúa anclado en los sitios de alta interacción con la superficie. De acuerdo con los valores determinados (Tabla 3), puede observarse claramente que la reducibilidad del níquel es mayor en el caso de los soportes catalíticos sintetizados en presencia del tensoactivo (entre 90 y 92%).
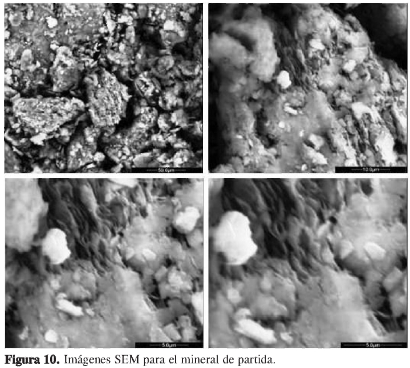
En las Figuras 10, 11, 12 y 13 pueden apreciarse las micrografías SEM del mineral arcilloso de partida y de los sólidos SA0, SA2 y NiSA2 respectivamente. En el caso del mineral arcilloso de partida, se observan aglomerados de tamaños mayores a 50 μm, compuestos por empaquetamientos compactos de hojas, lo cual es típico de los minerales laminares como las esmectitas. Igualmente, se observan cristales de tamaños menores que 10 μm embebidos en los cristales laminares, los cuales pueden corresponder a impurezas mineralógicas como el cuarzo y otros. Para los sólidos SA0 y SA2 se observa una morfología completamente diferente a la del mineral de partida. En primer lugar, se observan aglomerados de tamaños inferiores en donde es clara la formación de hojuelas de tamaños por debajo de 5 μm, las cuales florecen como esponjas en partículas primarias entre 10 y 20 μm. Estos cristales tipo hojuelas presentan asociaciones desordenadas tipo borde-borde y cara-borde y son el resultado de apilamientos cara-cara de láminas pi-larizadas, tal como lo indican los resultados de DRX (33).
Los sólidos SA0 y SA2 presentan morfologías similares compuestas por apilamientos de hojuelas, sin embargo, es posible apreciar que el sólido SA2 presenta hojuelas de menores tamaños, lo cual puede deberse a la formación de agregados de tensoactivo entre cristales durante la síntesis que impiden la cohesión y el crecimiento de aglomerados de mayor tamaño durante la calcinación, generando un efecto "molde" de la molécula orgánica, en cuanto al tamaño de los cristalitos laminares y a la formación de mesoporos observada (11).
El sólido NiSA2 presenta una morfología compuesta por partículas aglomeradas de tamaños superiores a 50 μm. No se observa el ordenamiento antes visto en las hojuelas y es clara la mayor rugosidad y el cambio de morfología causado por el proceso y el recubrimiento con NiO, eventos que van en detrimento de la cristalinidad de la fase esmectítica como se observó por DRX. El mapeo químico realizado por EDX sobre la muestra NiSA2 evidenció la buena distribución del níquel tanto en aglomerados de tamaños grandes como en partículas primarias de tamaños pequeños.
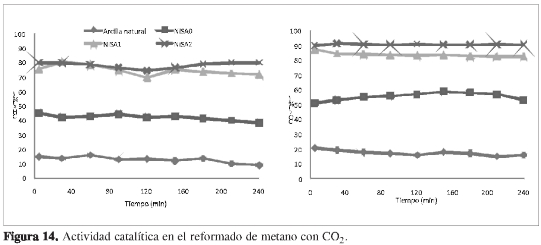
En la Figura 14 se registran las curvas de conversión en el reformado de metano con CO2 a 700 °C (WHSV = 60Lg-1h-1) para los catalizadores NiSAO, NiSAl y NiSA2. Los catalizadores soportados sobre minerales modificados presentan mejores actividades catalíticas que aquel sólido en donde el Ni es soportado sobre la arcilla natural, lo cual es debido a la estabilidad térmica y la porosidad que confiere al material la metodología de modificación. Dentro de ellos, los materiales modificados con tensoactivos son los mejores, registrando conversiones entre 70 y 80% de CH4 y 85 y 90% de CO2.Seha reportado que la distribución mesoporosa de los catalizadores, favorece el acceso y la distribución de especies activas sobre el soporte lo cual se correlaciona con los resultados encontrados en el presente trabajo (13, 18, 30).
Igualmente, se puede observar que las conversiones de CO2 son ligeramente superiores a las de CH4, lo cual indica la presencia de la reacción inversa de desplazamiento agua-gas que conduce a la formación de vapor de agua como subproducto (14, 15). No obstante, la selectividad del proceso es alta y las relaciones H2/CO que se obtienen se encuentra entre 0,7 y 0,9 (Tabla 3), las cuales son adecuadas para aplicaciones posteriores del gas de síntesis.
La cantidad de coque formada fue determinada luego de la reacción mediante TGA (Tabla 3), evidenciándose que los catalizadores modificados con tensoactivos registran menores niveles de formación de coque, lo cual guarda directa correlación con las actividades catalíticas. Se determinó que el coque formado se quema a temperaturas entre 600 y 650 °C, lo que sugiere que mayoritariamente son formados filamentos de carbono de acuerdo con lo reportado en la literatura (14, 15).
Después de la reacción, los catalizadores evidencian una pérdida de área BET entre 33 y 35% respecto al catalizador sin reducir, y mínimos niveles de sinterización de la fase metálica (Tabla 3), lo que indica la alta estabilidad de los catalizadores, los cuales, pese a la formación de coque reportada, no evidenciaron desactivación bajo las condiciones empleadas.
CONCLUSIONES
Se obtuvieron soportes catalíticos para el níquel a partir de la modificación de una esmectita natural con policationes de Al-Ce en presencia de óxido de polietileno y ultrasonido. El método de modificación genera materiales pilarizados con espaciados basales promedio de 1,65 nm. La adsorción del tensoactivo mediante el método con ultrasonido, se da preferencialmente en la superficie externa del mineral, lo cual afecta la morfología, la cristalinidad y el tamaño de los agregados laminares.
Se generan nanopartículas de NiO, las cuales se distribuyen homogéneamente en la superficie y se disponen en ambientes químicos de baja y alta interacción. Los catalizadores evidencian la pérdida de área superficial en función de la temperatura, lo que indica limitada estabilidad térmica hasta los 800 °C, cuando ocurre el colapso de la fase esmectítica sin sinterización notable de las partículas de NiO.
La reducibilidad de los catalizadores a 700 °C con H2 puro es mayor para los materiales sintetizados en presencia del tensoactivo. La reducción de los materiales genera tamaños de cristalito de níquel menores que 10 nm y pérdida de la cristalini-dad de la fase esmectítica.
Los catalizadores soportados sobre arcillas, modificados con tensoactivos, presentaron mejores actividades catalíticas en el reformado de metano con CO2 a 700 °C (entre 70 y 80% de CH4y 85 y 90% de CO2) con menores niveles de formación de coque, mínimos niveles de sinterización y relaciones H2/CO entre 0,7 y 0,9.
AGRADECIMIENTOS
Carlos Daza agradece a Colciencias por la beca para sus estudios de doctorado. Los autores agradecen al profesor Gerardo Rodríguez del departamento de ingeniería química de la Universidad Nacional de Colombia, por la realización de los ensayos catalíticos en la reacción de reformado de metano con CO2. Se agradece el soporte financiero de los proyectos DIB-Universidad Nacional de Colombia Código Hermes 10272 y 10289.
REFERENCIAS BIBLIOGRÁFICAS
1. Gil A.; Gandía, L. M.; Vicente, M. A. Recent advances in the synthesis and catalytic applications of pillared clays. Catal. Rev.-Sci. Eng. 2000. 42: 145-212. [ Links ]
2. Moreno, S.; Gutiérrez, E.; Álvarez, A.; Papayannakos, N. G.; Poncelet, G. Al-pillared clays: from lab syntheses to pilot scale production characterisation and catalytic properties. Appl. Catal. A. 1997. 165: 103-114. [ Links ]
3. Salerno, P.; Asenjo, M. B.; Mendioroz, S. Influence of preparation method on thermal stability and acidity of Al-PILCs. Thermochimica Acta. 2001. 379: 101-109. [ Links ]
4. Selvaraj, S.; Mohan, B. V.; Krishna, K. N.; Prakash, B. S. J. Pillaring of smectites using an aluminium oligomer: a study of pillar density and thermal stability. Appl. Clay Sci. 1996. 10: 439-450. [ Links ]
5. Carriazo, J. G.; Centeno, M. A.; Odriozola, J. A.; Moreno, S.; Molina, R. Effect of Fe and Ce on Al-pi-llared bentonite and their performance in catalytic oxidation reactions. Appl. Catal. A. 2007. 317 (1): 120-128. [ Links ]
6. Wang, S.; Lu, G. Q. Role of CeO2 in Ni/CeO2-Al2O3 catalysts for carbon dioxide reforming of methane. Appl. Catal. B. 1998. 19 (3-4): 267-277. [ Links ]
7. Wang, W.; Stagg-Williams, S. M.; Noronha, F. B.; Mattos, L. V.; Passos, F. B. Partial oxidation and combined reforming of methane on Ce-promoted catalysts. Catal. Today. 2004. 98 (4): 553-563. [ Links ]
8. Yao, H. C.; Yao, Y. F. Y. Ceria in automotive exhaust catalysts : I. Oxygen storage. J. Catal. 1984 . 86 (2): 254-265. [ Links ]
9. Katdare, S. P.; Ramaswamy, V.; Ramaswamy, A. V. Factors afecting the preparation of alumina pillared montmorillonite employing ultraso nics. Micro. Meso. Mat. 2000. 37: 329-336. [ Links ]
10. Pérez, A.; Centeno, M. A.; Odriozola, J. A.; Molina, R.; Moreno, S. The effect of ultrasound in the synthesis of clays used as catalysts in oxidation reactions. Catal. Today. 2008. 133-135: 526-529. [ Links ]
11. Alexandre, M.; Dubois, P. Polymer-layered silicate nanocomposites: preparation, properties and uses of a new class ofmaterials. Mat. Sci. Eng. 2000. 28: 1-63. [ Links ]
12. Zhu, H. Y.; Ding, Z.; Lu, C. Q.; Lu, G. Q., Molecular engineered porous clays using surfactants. Appl. Clay Sci. 2002. 20: 165-175. [ Links ]
13. Hao, Z.; Zhu, H. Y.; Lu, G. Q. Zr-Laponite pillared clay-based nickel catalysts for methane reforming with carbon dioxide. Appl. Catal. A. 2003. 242(2): 275-286. [ Links ]
14. Daza, C. E.; Kiennemann, A.; Moreno, S.; Molina, R. Dry reforming of methane using Ni-Ce catalysts supported on a modified mineral clay. Appl. Catal. A: Gen. 2009. 364 (1-2): 65-74. [ Links ]
15. Daza, C. E.; Kiennemann, A.; Moreno, S.; Molina, R. Stability of Ni-Ce catalysts supported over Al-PVA modified mineral clay in dry reforming of methane. Energy and Fuels. 2009. 23, 3497-3509. [ Links ]
16. Laguna, O. Efecto del contenido esmectítico en procesos de pilarización de minerales arcillosos provenientes de la coordillera Central de Colombia. Tesis de Maestría en Química, Universidad Nacional de Colombia, Bogotá, Colombia, 2007. [ Links ]
17. Ertl, G.; Knozinger, H.; Weitkamp, J. Handbook of heterogeneous catalysis. Vol. 2. Weinheim, Germany: Wiley-VCH. 1997. p. 447. [ Links ]
18. Molina, R.; Poncelet, G. [alpha]-alumina-supported nickel catalysts prepared from nickel acety-lacetonate: a TPR study. J. Cat. 1998. 173 (2): 257-267. [ Links ]
19. Monti, D. A. M.; Baiker, A. Temperature-programmed reduction. Parametric sensitivity and estimation of kinetic parameters. J. Catal. 1983. 83 (2): 323-335. [ Links ]
20. Valverde, J. L.; Cañizares, P.; Sun-Kou, M. R.; Molina, C. B. Enhanced thermal stability of Al-pi-llared smectites modified with Ce and La. Clays Clay Minerals. 2000. 48: 424-432. [ Links ]
21. Moronta, A.; Iwasa, N.; Fujita, S. I.; Shimokawabe, M.; Arai, M. Nickel catalysts supported on MgO/smectite-type nanocomposites for methane reforming. Clays clays minerals. 2005. 53 (6): 622-630. [ Links ]
22. Kloprogge, J. T.; Frost, R. L.; Fry, R. Infrared emission study of the thermal transformation mechanism of Al13-pillared clay. Analyst. 1999. 124: 381-384. [ Links ]
23. Madejova, J. FTIR techniques in clay mineral studies. Vib. Spec. 2003. 31: 1-10. [ Links ]
24. Madejova, J.; Bujdak, J.; Janek, M.; Komadel, P. Comparative FT-IR study of structural modifications during acid treatment of dioctahedral smectites and hectorite. Spectrochimica Acta A. 1998.54: 1397-1406. [ Links ]
25. Mandalia, T.; Berga, F. Organo clay mineral-melted polyolefin nanocomposites effect of surfactant/CEC ratio. J. Phys. Chem. Solids. 2006. 67 (4): 836-845. [ Links ]
26. Booij, E.; Kloprogge, J. T.; Veen, J. A. R. V. Large pore REE/Al pillared bentonites: preparation, structural aspects and catalytic properties. Appl. Clay Sci. 1996. 11 (2-4): 155-162. [ Links ]
27. Carriazo, J. G.; Martínez, L. M.; Odriozola, J. A.; Moreno, S.; Molina, R.; Centeno, M. A. Gold supported on Fe, Ce, and Al pillared bento-nites for CO oxidation reaction. Appl. Catal. B. 2007. 72 (1-2): 157-165. [ Links ]
28. Hernando, M. J.; Pesquera, C.; Blanco, C.; González, F. Increase in thermal stability of the texture in montmorillonites pillared with aluminum/ cerium polyoxocations. Langmuir. 2002: 5633-5636. [ Links ]
29. Hernando, M. J.; Pesquera, C.; Blanco, C.; González, F. Synthesis, characterization and catalytic properties of pillared montmorillonite with aluminum/cerium polyoxycations. Chem. Mat. 2001. 13: 2154-2159. [ Links ]
30. Wang, S.; Zhu, H. Y.; Lu, G. Q. Preparation, characterization, and catalytic properties of clay-based nickel catalysts for methane reforming. J. Colloid Int. Sci. 1998. 204: 128-134. [ Links ]
31. Belver, C.; Bañares-Muñoz, M. A.; Vicente, M. A. Fe-saponite pillared and impregnated catalysts I. Preparation and characterisation. Appl. Catal. B. 2004. 50: 101-112. [ Links ]
32. De Lucas, A.; García, P. B.; Garrido, A.; Romero, A.; Valverde, J. L. Catalytic synthesis ofcarbonnanofibers with different graphene plane alignments using Ni deposited on iron pillared clays. Appl. Catal. A. 2006. 301 (1): 123-132. [ Links ]
33. Alexandre, M.; Dubois, P. Polymer-layered silicate nanocomposites: preparation, properties and uses ofa new class ofmaterials. Mat. Sci. Eng. R. 2000. 28 (1-2): 1-63. [ Links ]