Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Colombiana de Química
versión impresa ISSN 0120-2804versión On-line ISSN 2357-3791
Rev.Colomb.Quim. v.39 n.2 Bogotá mayo/ago. 2010
CAPTURA DE CO2 MEDIANTE TRANSPORTADORES SÓLIDOS DE OXÍGENO
CO2 CAPTURE BY CHEMICAL LOOPING COMBUSTION
CAPTAÇÃO DE CO2 A TRAVÉS DE TRANSPORTADORES SÓLIDOS DE OXIGÊNIO
Carmen R. Forero1,2, Juan Adánez3, Pilar Gayán3, Luis F. de Diego3, Francisco García-Labiano3, Alberto Abad3
1 Escuela de Ingeniería de Recursos Naturales y del Ambiente, Universidad del Valle, Calle 100 No. 100-00,25360, Cali, Colombia.
3 Departamento de Energía y Medioambiente, Instituto de Carboquímica(CSIC), Miguel Luesma Castán, 4, 50018, Zaragoza - España.
Recibido: 18/12/09 - Aceptado: 30/08/10
RESUMEN
La evaluación de transportadores de oxígeno (TO), basados en CuO y NiO sobre Al2O3 y preparados por impregnación, se llevó a cabo en una planta piloto de dos lechos fluidizados interconectados de 500 Wte, donde se utilizaron tanto metano como gas de síntesis como gas combustible. Además, se estudió el efecto de diferentes impurezas presentes en el gas combustible como azufre o hidrocarburos ligeros en la eficacia de combustión del proceso y en el comportamiento de los TO. Los resultados obtenidos mostraron que ambos TO son adecuados para la captura de CO2 mediante transportadores sólidos de oxígeno en el proceso de combustión de metano, gas de síntesis o metano con impurezas como hidrocarburos ligeros o azufre en el gas.
Palabras clave: captura de CO2, cobre, níquel, transportadores de oxígeno, combustión.
ABSTRACT
NiO and CuO based oxygen carriers (OCs) supported on Al2O3 prepared by impregnation were selected for its evaluation in a continuous pilot plant of 500 Wth of two interconnected fluidized beds, where both methane and syngas were used as fuel gas. In addition, the effect of possible impurities in the fuel gas such as sulphur compounds and other hydrocarbons in the combustion efficiency of the process and the behaviour of the OCs were studied. Based on these results, it can be concluded that both OCs are suitable for a chemical looping combustion (CLC) process with methane, syngas and methane with impurities such as light hydrocarbons or sulphur.
Key words: CO2 capture, chemical looping combustion, copper, nickel, oxygen carriers.
RESUMO
A avaliação das transportadoras de oxigênio (TOs), baseados em CuO e NiO sobre Al2O3 e preparados por impregnação, foi testada em uma planta piloto de dois leitos fluidizados de 500 Wte interligados, utilizando-se o metano como gás de síntese e como combustível. Além disso, foi estudado o efeito de diferentes impurezas presentes no gás combustível como enxofre o hidrocarbonetos ligeros na eficiência de combustão do processo e no comportamento dos TOs. Os resultados mostraram que ambos TOs são adequados para a captura de CO2 por transportadores de oxigênio sólido no processo de combustão de metano, gás de síntese ou metano com presença de impurezas como enxofre ou hidrocarbonetos ligeros e gases.
Palavras-chave: captação de CO2, cobre, níquel, transportadores de oxigênio, combustão.
INTRODUCCION
La captura y el almacenamiento de CO2 (CAC) constituyen un proceso que involucra la separación del CO2 emitido por la industria y fuentes relacionadas con la energía, su transporte a un lugar de almacenamiento y su aislamiento de la atmósfera a largo plazo. Este proceso de CAC se está convirtiendo en una de las opciones de mitigación del cambio climático, en lo que se refiere a la estabilización de las concentraciones atmosféricas de gases de efecto invernadero. La combustión indirecta con transportadores sólidos de oxígeno está considerada como una alternativa eficiente energéticamente para la captura CO2, ya que es una tecnología con separación inherente del CO2 (1). Los transportadores de oxígeno (TO) transfieren el oxígeno del aire al combustible evitando el contacto directo entre ellos. El proceso se lleva a cabo en dos reactores interconectados, uno de reducción y otro de oxidación, entre los cuales circula el sólido de manera cíclica. En el reactor de reducción se produce la reacción del gas combustible con el óxido metálico [ecuación 1] produciendo CO2 y H2O. Tras la condensación del H2O, se genera una corriente pura de CO2, no siendo necesaria una energía adicional para la separación del CO2 de los humos de combustión, como sucede en el proceso convencional.
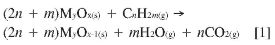
En el reactor de oxidación se produce la regeneración del óxido metálico con aire mediante la ecuación [2].
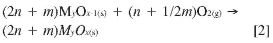
La reacción neta es:
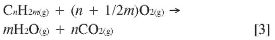
La reacción en el reactor de reducción es endo o exotérmica, dependiendo del metal empleado. En el reactor de oxidación siempre es exotérmica. Sin embargo, la cantidad total de calor generada en los dos reactores del proceso de combustión con TO es la misma que en un combustor tradicional, y además consideraciones termodinámicas muestran que la destrucción de exergía en este sistema es mucho más baja produciendo un aumento en la eficiencia energética neta (2). El combustible puede ser tanto gaseoso (gas natural, gas de síntesis, etc.) como sólido (carbón, coque de petróleo, etc.).
Un factor clave para el éxito del desarrollo de este proceso es el transportador sólido de oxígeno (TO), puesto que tiene que cumplir unos requisitos sin los cuales el sistema no sería operativo. Estas características son principalmente: reactividad elevada y mantenida a través de los ciclos para reducir la cantidad de sólido en cada reactor; resistencia al desgaste; reacción selectiva a CO2 y H2O, y resistencia a la deposición de carbono para aumentar la capacidad de captura; no presentar problemas de defluidización o aglomeración, y tener una elevada capacidad de transportar oxígeno para reducir la cantidad de sólido en circulación. Además, se requiere que el TO sea seguro medioambientalmente, fácil de preparar y abundante para reducir su coste.
Se han propuesto muchos tipos de transportadores de oxígeno como posibles candidatos para la combustión con transportadores sólidos (3), pero en general se componen de una fase activa (óxido metálico) encargada de transportar el oxígeno, y una fase inerte que opera a modo de soporte aportando resistencia física y superficie para distribuir la fase activa. Como fases activas se han propuesto óxidos de níquel, hierro, manganeso, cobalto y cobre, entre otros, y como fases inertes ZrO2, TiO2, Al2O3, sepiolita, kaolin y diversos aluminatos. Las proporciones entre fase activa e inerte, el método de preparación, las condiciones y el combustible utilizados para estudiar las propiedades del transportador de oxígeno en concreto han dado lugar a un alto número de trabajos en la literatura (3-8).
El grupo de Combustión y gasificación del Instituto de Carboquímica (ICB) ha centrado su investigación en el desarrollo de TO, tanto desde el punto de vista de la preparación de materiales, como de la investigación básica sobre su comportamiento y caracterización físico-química. Además, ha realizado experimentos de combustión en plantas piloto de 500 Wte y 10 kWte en continuo para demostrar la viabilidad técnica de este nuevo proceso.
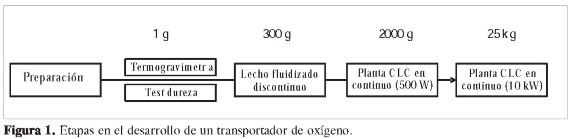
La Figura 1 muestra de forma esquemática el proceso de desarrollo de un TO, así como la cantidad de material necesario en cada etapa. La primera etapa en el desarrollo de un TO consiste en la elección de un óxido metálico, un soporte y un método de preparación (coprecipitación, mezcla másica y extrusión, impregnación, precipitación-deposición, etc.) adecuados (9, 13). La primera selección de un TO se realiza con base en la reactividad del TO en las reacciones de reducción-oxidación determinadas por termogravimetría y la resistencia mecánica determinada con las pruebas de dureza. En una segunda etapa, se realizan experimentos en lecho fluidizado discontinuo, que permiten conocer el desgaste del TO en condiciones similares a las de operación en continuo, la posible aglomeración del material y la distribución de productos en la combustión. Para conocer el comportamiento del TO durante largos periodos de tiempo, se realizan experimentos en una planta de 500 Wte, que consiste en dos lechos fluidizados interconectados que pueden operar a diferentes temperaturas (14-20). En esta planta se puede analizar también el efecto sobre el TO de las impurezas presentes en el gas combustible como H2S o hidrocarburos ligeros. Además, el ICB dispone de una planta de 10 kWte que realizó 200 h de operación en continuo con un TO de cobre con excelentes resultados (21, 22).
Actualmente se están desarrollando transportadores de oxígeno basados en CuO y en NiO preparados por impregnación sobre alúmina. El objetivo de este trabajo es presentar los principales resultados que se han obtenido en cuanto al comportamiento de estos transportadores en la planta piloto de 500 Wte utilizando diferentes gases combustibles, y el efecto que posibles impurezas en el gas combustible -como compuestos de azufre o hidrocarburos ligeros- tienen en la eficacia de combustión del proceso.
MATERIALES Y MÉTODO
Transportadores de oxígeno
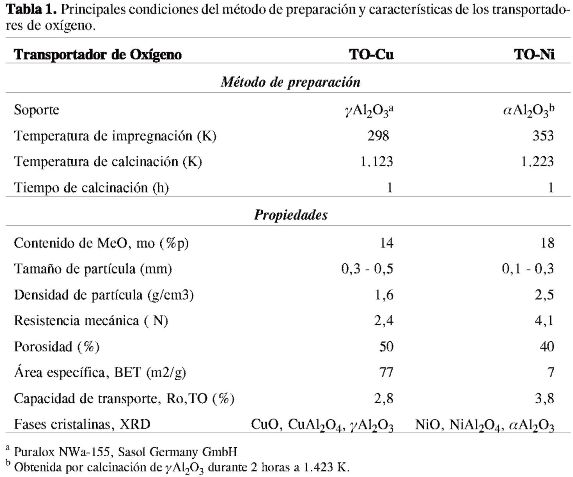
En trabajos previos se determinaron el efecto que el método de preparación, el contenido de metal y el tipo de soporte tenían sobre la reactividad, la distribución de productos, la velocidad de atrición y la aglomeración en el TO (9-13). Estos estudios permitieron seleccionar dos transportadores basados en cobre (TO-Cu) y níquel (TO-Ni) preparados por impregnación seca sobre alumina (Al2O3) con adecuadas características para el proceso. Las principales condiciones del método de preparación y las características de los dos TO se muestran en la Tabla 1.
Planta experimental para la captura de CO2 mediante TO (500 Wte)
Una vez seleccionados y caracterizados los TO, se prepararon en cantidad suficiente para usarlos en una planta piloto de 500 Wte trabajando en continuo durante un alto número de horas (~ 120 h). En esta planta se analizó el efecto que las diferentes condiciones de operación tienen sobre la eficacia de combustión del proceso.
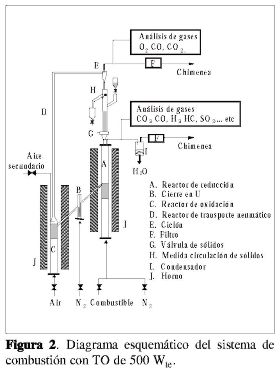
La Figura 2 muestra un diagrama esquemático de la planta piloto diseñada y construida en el Instituto de Carboquímica (ICB-CSIC) para llevar a cabo el proceso de combustión con captura de CO2. La planta se compone principalmente de dos reactores de lecho fluidizado, el de reducción (RR) y el de oxidación (RO), interconectados entre sí por un reactor de cierre en U; un reactor de transporte neumático que conduce los sólidos del RO al RR; un ciclón para recoger los sólidos transportados por el reactor de transporte neumático; una válvula de control de sólidos para regular el caudal de TO circulante y un filtro para recoger los sólidos finos no recogidos por el ciclón.
En esta planta se puede modificar el caudal de sólidos en circulación mediante la válvula de sólidos instalada (G) manteniendo constante el resto de condiciones de operación, como el caudal de combustible o la cantidad de aire suministrado. Además, es posible medir dicho caudal de circulación de sólidos directamente (H) por pesada.
El RR (A) y el RO (C) son lechos fluidizados de 0,05 m de diámetro interno con una zona de precalentamiento para el combustible o el aire y una altura de lecho de 0,1 m. El reactor de transporte neumático (D) es de 0,02 m de diámetro interno y 1 m de altura. En el RR se produce la combustión del combustible empleando el oxígeno suministrado por el TO, dando CO2 y H2O. Las partículas reducidas del TO pasan al RO (C) para su regeneración, a través del cierre en U (B) para evitar la mezcla del combustible con el aire. Los finos generados durante el proceso por fragmentación o desgaste son retenidos a la salida de los gases de cada reactor mediante un filtro (F).
La planta dispone de herramientas de medición y control del sistema. El flujo de los gases de alimentación se mide con controladores de flujo másico para cada gas. Las condiciones de operación se miden en continuo mediante una serie de termopares y transductores de presión situados en diferentes puntos de la planta. Las temperaturas del RR y del RO se controlan de forma independiente mediante dos hornos (J). Los gases de salida del RR y del RO se llevan a diferentes analizadores de gas en línea para conocer su composición. A la salida del RR se mide la concentración de CO, CO2 y CH4 mediante un detector NDIR, y la concentración de H2 mediante un detector de conductividad térmica. A la salida del RO se mide la concentración de O2, CO y CO2 con un analizador paramagnético y NDIR respectivamente.
Condiciones de experimentación
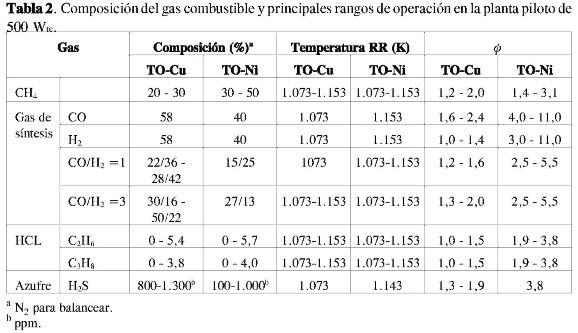
El comportamiento de cada uno de los transportadores usados en esta investigación (TO-Cu, TO-Ni) se analizó empleando diferentes gases combustibles. Así, se utilizó CH4 puro, CO puro, H2 puro, mezclas CO/H2, CH4 con hidrocarburos ligeros (C2H6, C3H8) o CH4 con sulfuro de hidrógeno (H2S) para estudiar el efecto del tipo de gas combustible y de las impurezas del gas sobre la eficacia de combustión y el comportamiento del TO. Las principales condiciones de operación empleadas en cada caso se resumen en la Tabla 2.
El inventario total de sólidos en el sistema se mantuvo entre 1,1-1,3 kg. Las condiciones de operación seleccionadas fueron diferentes para los dos TO debido a las características de los materiales. La velocidad del gas de entrada en el RR fue de 0,14 m/s para TO-Cu (dp = 0,3-0,5 mm, p = 1,6 g/cm3) y de 0,1 m/s para el TO-Ni (dp = 0,1-0,3 mm, p= 2,5 g/cm3). La temperatura en el RO se mantuvo constante e igual a 1.223 K en todos los experimentos, excepto en los de CH4 con H2S para el TO-Cu, en el cual se trabajó a 1.173 K. La temperatura en el RR se varió entre 1.073 y 1.153 K tanto para el TO-Ni como para el TO-Cu. Para analizar el efecto de la relación molar MeO/combustible, se variaba la cantidad de combustible alimentado, manteniendo constantes el caudal total y la circulación de sólidos (en el caso del CH4 porcentajes entre el 20 y el 30% para el TO-Cu, y entre el 30 y el 50% para el TO-Ni, siendo el resto N2). En los experimentos, para analizar el efecto de la composición del gas (gas de síntesis) y del azufre, se variaba la relación molar MeO/combustible modificando la apertura de la válvula de sólidos y, por tanto, del caudal de circulación (valores entre 7 y 10,5 kg para el TO-Cu, y entre 3-14 para el TO-Ni).
El comportamiento de la planta piloto se evaluó respecto a la eficacia de combustión, ηc, calculada a partir de los valores de los gases de salida del RR según la ecuación [4].
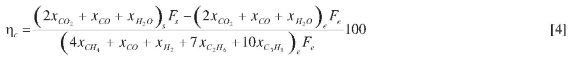
donde Fe es el flujo molar de la corriente de gases de entrada al RR, Fs es el flujo molar de la corriente de gases de salida del RR y x¡ es la fracción molar del gas i.
El valor de esta eficacia muestra si la operación del sistema está cerca o lejos de la combustión completa del combustible (CO2 + H2O), es decir ηc = 100%.
Además, esta eficacia de combustión se evalúa en función de una relación molar MeO/combustible, Φ, definida por la ecuación [5] como:

donde FMeO es el flujo molar de óxido metálico que entra al RR, Fcomb es el flujo molar de entrada de combustible en el RR y b es el coeficiente estequiométrico del combustible empleado calculado como:
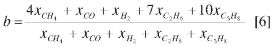
Un valor de Φ = 1 corresponde al caudal molar estequiométrico de óxido metálico necesario para oxidar completamente el combustible a CO2 y H2O.
RESULTADOS Y DISCUSIÓN
Para analizar la influencia de las condiciones de operación (TRR y Φ), la planta piloto estuvo operando durante más de 100 h en caliente con cada uno de los TO. En cada condición experimental estudiada, el sistema se mantuvo estable durante al menos /-1 h. Las temperaturas de los reactores se mantuvieron estables, así como la circulación de sólidos. Los resultados experimentales se obtuvieron primero analizando las características de los dos TO preparados, y segundo estudiando el efecto que la relación molar MeO/combustible tiene sobre la eficacia de combustión cuando se utilizan los dos transportadores de oxígeno en la planta piloto de 500 Wte en la combustión con diferentes gases combustibles e impurezas: combustión de metano, combustión de gas de síntesis (mezcla de CO/H2), combustión de metano con presencia de etano o propano y combustión de metano con presencia de H2S para ambos TO.
Características de los TOs basados en CuO y MO
En la Tabla 1 se pueden observar las principales propiedades de los dos TO empleados en este estudio. El TO-Ni posee una mayor capacidad de transportar oxígeno debido al mayor contenido de MeO; tanto el área específica como la porosidad son menores debido a que el soporte empleado se prepara por sinterización de y Al2O3 a alta temperatura y la calcinación del impregnado también se lleva a mayor temperatura. Las diferencias en densidad se deben tanto a la cantidad y diferencia de MeO como al soporte. En cuanto a las fases cristalinas, se puede establecer que en ambos transportadores el metal está presente como óxido y como aluminato. La resistencia mecánica es mayor en el TO-Ni debido a las etapas de sinterización tanto del soporte como del impregnad; sin embargo, ambos valores son suficientemente altos para la fluidización.
Combustión de CH4
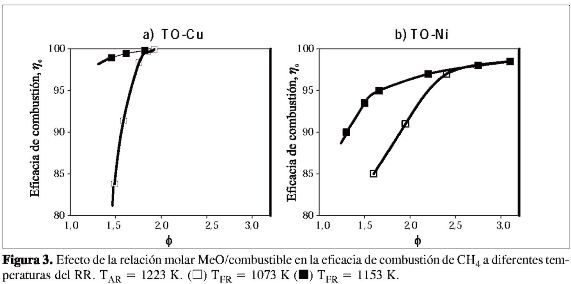
Para determinar el comportamiento de los TO de Cu y Ni en la combustión con metano se realizaron varios experimentos a diferentes TRR, concentraciones de metano y caudales de circulación de sólidos (Tabla 2). La Figura 3 presenta las eficacias de combustión obtenidas en función de § a diferentes temperaturas del RR con el TO-Cu (Figura 3a) y el de TO-Ni (Figura 3b). Como se puede ver, es posible convertir todo el metano alimentado cuando se utiliza un TO-Cu. Cuando se utiliza un TO-Ni existen limitaciones termodinámicas que impiden la combustión completa del metano a CO2 y H2O, debido a la existencia de pequeñas cantidades de CO e H2 en las condiciones de equilibrio. Eficacias de combustión cercanas al equilibrio (99,5 %) se alcanzaron con relaciones de Φ mayores a 3 cuando se utilizó el TO-Ni. Con el TO-Cu se obtuvo combustión completa de metano con relaciones mayores de 1,5 a 1.153 K. Con ambos TO se halló un importante efecto de la temperatura del RR. Cuanto mayor era la temperatura de operación, eran necesarios menores § para alcanzar altas eficacias de combustión debido a la mayor reactividad del TO. Cabe señalar que las conversiones máximas de metano se obtienen con menores relaciones Me/combustible cuando se emplea el TO-Cu. Esto se debe a su mayor reactividad, ya que por análisis termogravimétrico se encontró que todo el cobre de la partícula es igual de activo para la reacción con metano. Sin embargo, en el TO-Ni parte del Ni impregnado forma aluminatos (ver fases XRD, Tabla 1) cuya reactividad con metano es mucho menor que la del óxido (14).
Combustión de gas de síntesis
Para analizar el efecto de diferentes variables de operación (composición, relación molar MeO/combustible y temperatura) en la combustión de gas de síntesis sobre la eficacia de combustión, se realizaron diferentes pruebas en la planta piloto utilizando el TO-Cu y el TO-Ni según se muestra en la Tabla 2. Se usaron relaciones molares de CO/H2 entre 1 y 3, puesto que son las típicas obtenidas en los gasificadores comerciales. Además, se utilizaron H2 y CO puros para comparar. Las composiciones del gas de síntesis alimentadas al reactor cumplían el equilibrio WGS (reacción de intercambio) en las diferentes relaciones utilizadas.
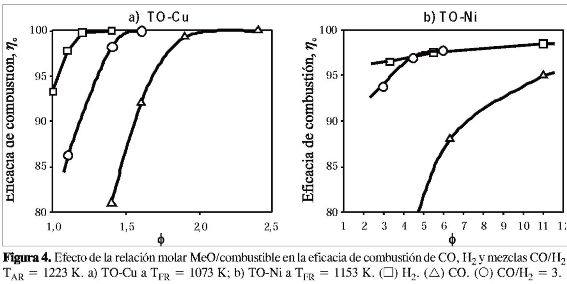
La Figura 4a presenta el efecto de § sobre la eficacia de combustión para una relación CO/H2 igual a 3, y utilizando H2 y CO puros a una temperatura del RR de 1.073 K cuando se usó el TO-Cu. Se observa que el gas de síntesis puede convertirse totalmente con Φ > 1,5. Para el H2 se necesitan menores relaciones para obtener combustión completa. Sin embargo, las eficacias de combustión son mucho menores cuando se utiliza CO como gas combustible. Estos resultados concuerdan con los encontrados en TGA, donde la reactividad del TO era mayor cuando se utilizaba H2 en vez de CO.
La Figura 4b muestra la eficacia de combustión en función de Φ cuando se utilizaron H2 puro, CO/H2 = 3 y CO puro a TRR = 1. 153 K con un TO-Ni. Cuando se usó un TO-Ni, se obtuvieron resultados similares a los encontrados con el TO-Cu, las mayores eficacias se obtuvieron con H2 y las menores con CO, siendo necesarias relaciones de MeO/combustible mayores de 12 para obtener eficacias adecuadas cuando se utilizaba CO puro. Con el TO-Ni eran necesarios valores de Φ mayores que con el TO-Cu para conseguir conversiones elevadas próximas a las del equilibrio. Estos TO-Ni tienen unas limitaciones termodinámicas que hacen que sólo se puedan alcanzar eficacias máximas del 99,2% con COy99,4% conH2.
Hay que señalar que las eficacias de combustión encontradas fueron muy similares para las dos relaciones de gas de síntesis utilizadas tanto para el TO-Ni como para el TO-Cu, teniendo en cuenta la alta concentración de CO existente en la relación CO/H2 = 3. Estos resultados se explican por el papel que la reacción WGS presenta en el mecanismo global de la reacción de combustión del gas de síntesis en un proceso con transportadores sólidos de oxígeno (15, 16). Debido a que los TO-Cu y TO-Ni son más reactivos con el H2 que con el CO, la velocidad de desaparición del H2 es mayor y, por tanto, desplaza el equilibrio WGS a la formación de más H2 y CO2, incrementando así la desaparición del CO.
Efecto de la presencia de hidrocarburos (C2H6, C3H8) en la combustión de CH4
La tecnología de captura de CO2 mediante transportadores sólidos de oxígeno fue desarrollada para la combustión de gas natural o de gas de síntesis obtenido de la gasificación de carbón. Sin embargo, los gases industriales y de refinerías contienen cantidades variables de hidrocarburos ligeros (C2 - C5) que pueden llegar a oscilar entre el 10 y el 30%. La posible presencia de estos hidrocarburos en el gas combustible puede afectar la reactividad del TO y el transporte y almacenamiento de CO2 si estuvieran presentes en los gases de combustión. Por ello se estudió el efecto que tenía la presencia de cantidades variables de etano y propano en el gas combustible (CH4) sobre la eficacia de combustión, distribución de productos, deposición de carbono y aglomeración, utilizando un TO-Cu y otro de Ni. Las condiciones experimentales se muestran en la Tabla 2. La composición de la mezcla de gas se eligió para mantener el mismo consumo de O2 que cuando se utilizaba solo metano (17, 18).
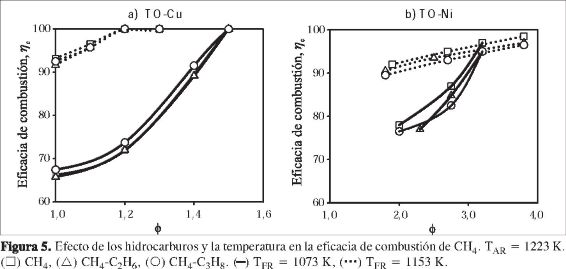
La Figura 5 presenta el efecto de la temperatura en el RR y la relación molar Φ en la eficacia de combustión para diferentes mezclas de hidrocarburos. Como se puede observar, la presencia de C2H6 o C3H8 no afecta significativamente el comportamiento de los TO, obteniéndose resultados similares al CH4 sin hidrocarburos ligeros. Por tanto, con el TO-Cu (Figura 5a) se pueden obtener conversiones completas del gas combustible para Φ mayores de 1,2 trabajando a 1.153 K. Con el TO-Ni (Figura 5b), conversiones cercanas al límite termodinámico se obtienen a valores de Φ mayores de 3,5. Además, en la Figura 5 se puede ver el importante efecto de la temperatura del RR para las diferentes mezclas y TO. Para obtener combustiones máximas del gas se necesitan mayores valores de Φ cuanto menor es la temperatura de operación en el RR. Sin embargo, hay que recalcar que en ningún caso se detectaron hidrocarburos inquemados a la salida del RR. Las pérdidas de eficacia de combustión se deben a aumentos de las concentraciones de CO, H2 o CH4 (sólo en el caso de TO-Cu) a la salida del RR, pero no a la presencia de etano o propano sin quemar. Además, se halló que era posible evitar la deposición de carbono sobre el TO operando a TRR = 1.153 K o Φ > 1,5 con el TO-Cu, y en ninguna situación se detectaron problemas de aglomeración o desactivación del TO con ninguno de los TO.
Efecto del azufre en la combustión deCH4
Además de la presencia de hidrocarburos ligeros en el gas combustible, otras impurezas como el azufre en forma de H2S pueden estar presentes en los combustibles gaseosos. El gas natural puede contener pequeñas cantidades de H2S (~20 ppm) pero el gas de refinería puede contener hasta 800 ppm o incluso hasta 8.000 en el caso del gas de síntesis sin tratar. El diseño y la operación de las plantas industriales de combustión con transportadores sólidos de oxígeno podrían verse afectados por la presencia de compuestos de azufre por varias razones: desde el punto de vista operativo, el comportamiento del TO podría ser afectado por la formación de compuestos que pueden causar su desactivación y, por tanto, la disminución de la eficacia de combustión del proceso. La formación de algunos sulfuros de bajo punto de fusión podría causar aglomeración de los TO, y esto afectaría la circulación de sólidos entre los reactores. En estos casos sería necesaria la desulfurización del combustible antes de su uso en el proceso. Por tanto, se estudió el efecto que tiene la presencia de H2S en el gas combustible (CH4) sobre la eficacia de combustión y el comportamiento del TO en la planta piloto utilizando las diferentes condiciones experimentales que se muestran en la Tabla 2, tanto para el TO-Ni como para el TO-Cu (19, 20).
Las especies termodinámicamente posibles en un proceso de combustión con TO dependen del metal utilizado, el gas combustible y las condiciones de operación (temperatura, concentraciones de H2S, etc). En un TO-Cu, la formación de sulfuros es termodinámicamente posible cuando se trabaja en condiciones de relación molar MeO/combustible subestequiornétricas, independientemente de la temperatura y la concentración de H2S. En condiciones de operación por encima de la relación estequiométrica, el azufre se liberará como SO2 en el RR. Por el contrario, el TO-Ni puede formar sulfuros en el RR cuando se utilizan gases con altas concentraciones de H2S (>600ppm) o temperaturas del RR por debajo de 1.153 K. Los experimentos realizados en la planta piloto para analizar el efecto del H2S en la eficacia de combustión, se seleccionaron basándose en estudios termodinámicos previos (19, 20).
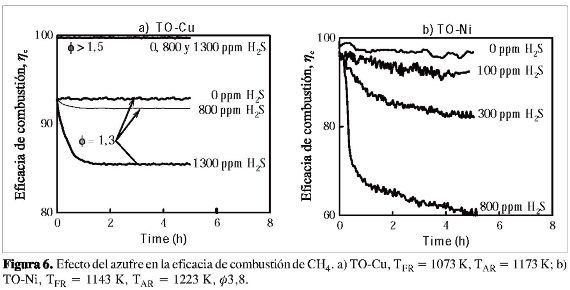
En la Figura 6a y 6b se muestran las eficacias de combustión en función del tiempo cuando se variaba la concentración de H2S para unas condiciones de operación determinadas. Se encontró que el TO-Cu puede trabajar con elevadas concentraciones de H2S sin que la eficacia se vea afectada utilizando relaciones Φ> 1,3. Balances de materia de S en el sistema mostraron que el azufre alimentado era liberado en forma de SO2 en el RR en más de un 95%. Cuando las condiciones de operación eran cercanas a la relación estequiométrica (Φ < 1,3), la presencia de H2S afectaba la eficacia de combustión debido a la formación de Cu2S en el TO. En estas condiciones, la reactividad del TO-Cu disminuía y el azufre se acumulaba en el sólido.
Con el TO-Ni se halló que la eficacia de combustión se veía afectada fuertemente cuanto mayor era la concentración de H2S utilizada, aunque este efecto era despreciable cuando la concentración de H2S era <100 ppm. Parte del azufre alimentado era liberado en el RO como SO2, y el resto del S se acumulaba en el sólido en forma de sulfuros y sulfatos causando una desactivación del TO-Ni. No obstante, se encontró que el TO-Ni podía recuperar su actividad inicial después de algún tiempo sin alimentación de H2S.
Desde el punto de vista ambiental, el azufre liberado en el RO debe cumplir la normativa existente en cuanto a emisiones para combustibles gaseosos (35 mg/Nm3 para plantas > 50 MWte). Si el azufre es liberado como SO2 en el RR, las impurezas como SOx, NOx, etc., tienen un gran potencial de interacción en la compresión, en el transporte y en el almacenamiento de CO2 y debería eliminarse del mismo.
Hay que señalar que no se observaron problemas de aglomeración durante toda la experimentación con ninguno de los TO.
CONCLUSIONES
Se encontró que con ambos TO se podían alcanzar las conversiones máximas posibles de metano con valores de Φ > 1,5 para el TO-Cu y de Φ > 2,5 para el TO-Ni. Además, tanto la temperatura del RR como la relación molar MeO/combustible tenían un efecto muy importante sobre la eficacia de combustión para ambos TO. Con el TO-Cu son necesarias menores relaciones MeO/combustible que con el TO-Ni para obtener combustiones completas del gas.
Ambos TO presentaban las mayores eficacias de combustión con el H2 y las menores con el CO. Además, se encontró que la composición del gas de síntesis tenía poco efecto sobre la eficacia de combustión, siendo estos valores altos y similares para las relaciones CO/H2 = 1 y 3. Esto era debido al importante papel que desempeña la reacción de WGS en la reacción de combustión del CO presente en el gas de síntesis.
La presencia de hidrocarburos ligeros (C2H6 y C3H8) en el gas combustible (CH4) no presentó problemas de operación con ninguno de los TO, siendo posible la combustión completa de los mismos en condiciones similares a las encontradas para el CH4.
Con el TO-Cu se advirtió que la presencia de H2S no afectaba la eficacia de combustión del proceso si se trabajaba con Φ > 1,5. El azufre alimentado al sistema era liberado en el RR en forma de SO2. Sin embargo, cuando se analizó el efecto de dicha impureza con el TO-Ni, se encontró que afectaba la reactividad del TO debido a la formación de sulfuros, y por tanto disminuía la eficacia de combustión. La pérdida de reactividad dependía de la concentración de H2S alimentada, aunque para concentraciones de H2S < 100 ppm la pérdida de eficacia era despreciable. El azufre alimentado al sistema se distribuía entre el SO2 liberado en el RO y el acumulado en forma de sulfuros y sulfatos en el sólido. Por consiguiente, combustibles con contenidos de azufre bajos (<100 ppm) podrían usarse en un proceso de combustión con captura de CO2 con estos TO-Ni.
Después de más de 100 h de operación en caliente con cada uno de los TO, no se observaron problemas de aglomeración o de atrición con ninguno de los dos TO. Por tanto, de acuerdo con los resultados obtenidos, ambos TO son adecuados para un proceso de captura de CO2 con transportadores sólidos en la combustión de metano o gas de síntesis y ante la presencia de impurezas como hidrocarburos ligeros o azufre en el gas.
REFERENCIAS BIBLIOGRÁFICAS
1. Kerr, H. R. Capture and separation technologies gaps and priority research needs. En: Thomas, D., Benson, S. (Eds.). Carbon Dioxide Capture for Storage in Deep Geologic Formations-Results from the CO2 Capture Project, Vol. 1. Oxford, UK, Elsevier Ltd. 2005. (Chapter 38). [ Links ]
2. Anheden, M.; Svedberg, G. Exergy analysis of chemical-looping combustion systems. Energy Convers. Mgmt. 1998.39(16-18): 1967-1980. [ Links ]
3. Mattisson, T.; Zafar, Q.; Johansson, M.; Lyngfelt, A. Chemical-looping combustion as a new CO2 management technology. First Regional Symposium on Carbon Management, Dhahran, Saudi-Arabia, May 22-24, 2006. 19 p. [ Links ]
4. Ishida, M.; Jin, H. A novel chemical-looping combustor without NOx formation. Ind. Eng. Chem. Res. 1996. : 2469-2472. [ Links ]
5. Ishida, M.; Jin, H.; Okamoto, T. A fundamental study of a new kind of medium material for chemical-looping combustion. Energy & Fuels. 1996. 10: 958-963. [ Links ]
6. Mattisson, T.; Järdnäs, A.; Lyngfelt, A. Reactivity of some metal oxides supported on alumina with alternating methane and oxygen-Application for chemical-looping combustion. Energy & Fuels. 2003. 17: 643-651 [ Links ]
7. Lyngfelt, A.; Thunman, H. Construction and 100 h operational experience of a 10-kW chemical-looping combustor. En: Thomas, D., Benson, S. (Eds.). Carbon Dioxide Capture for Storage in Deep Geologic Formations-Results from the CO2 Capture Project, Vol. 1. Oxford, UK, Elsevier Ltd. 2005. (Chapter 36). [ Links ]
8. Adánez, J.; García-Labiano, F.; de Diego, L. F.; Gayán, P.; Abad, A.; Celaya, J. Development of oxygencarriers for chemical-looping combustion. En: Thomas, D., Benson, S. (Eds.). Carbon Dioxide Capture for Storage in Deep Geologic Formations-Results from the CO2 Capture Project, Vol. 1. Oxford, UK, Elsevier Ltd. 2005. (Chapter 34). [ Links ]
9. Gayán, P.; de Diego, L. F.; García-Labiano, F.; Adánez, J.; Abad, A.; Dueso, C. Effect of support on reactivity and selectivity of Ni-based oxygen carriers for chemical-looping combustion. Fuel. 2008. 87: 2641-2650. [ Links ]
10. Gayán, P.; Dueso, C.; Abad, A.; Adánez, J.; de Diego, L. F.; García-Labiano, F. NiO/Al2O3 oxygen carriers for chemical-looping combustion prepared by impregnation and deposition-precipitation methods. Fuel. 2009. 88: 1016-1023. [ Links ]
11. Adánez, J.; de Diego, L. F.; García-Labiano, F.; Gayán, P.; Abad, A. Selection of oxygen carriers for chemical-looping combustion. Energy & Fuels. 2004. 18(2): 371-377. [ Links ]
12. de Diego, L. F.; García-Labiano, F.; Adánez, J.; Gayán, P.; Abad, A.; Corbella, B. M.; Palacios, J. M. Development of Cu-based oxygen carriers for chemical-looping combustion. Fuel. 2004. 83: 1749-1757. [ Links ]
13. de Diego, L. F.; Gayán, P.; García-Labiano, F.; Celaya, J.; Abad, A.; Adánez, J. Impregnated CuO/ Al2O3 oxygen carries for chemical-looping combustion: avoiding fluidized bed agglomeration. Energy & Fuels. 2005. 19: 1850-1856. [ Links ]
14. Adánez, J.; Dueso, C.; de Diego, L. F.; Garcia-Labiano, F.; Gayán, P.; Abad, A. Methane combustion in a 500 Wth chemical-looping combustion system using an impregnated Ni-based oxygen carrier. Energy & Fuels. 2009. 23: 130-142. [ Links ]
15. Forero, C. R.; Gayán, P.; de Diego, L. F.; Abad, A.; Garcia-Labiano, F.; Adánez, J. Syngas combustion in a 500 Wth chemical-looping combustion system using an impregnated Cu-based oxygen carrier. Fuel Processing Technology. 2009. 90: 1471-1479. [ Links ]
16. Dueso, C.; Garcia-Labiano, F.; Adánez, J.; de Diego, L. F.; Gayán, P.; Abad, A. Syngas combustion in a chemical-looping combustion system using an impregnated Ni-based oxygen carrier. Fuel. 2009. 88: 23572364. [ Links ]
17. Adánez, J.; Dueso, C.; de Diego, L. F.; Garcia-Labiano, F.; Gayân, P.; Abad, A. Effect of fuel gas composition in chemical-looping combustion with Ni-based oxygen carriers. 2. Fate of light hydrocarbons. Ind. Eng. Chem. Res. 2009.48 (5): 2509-2518. [ Links ]
18. Gayán, P.; Forero, C. R.; de Diego, L. F.; Abad, A.; Garcia-Labiano, F.; Adánez, J. Effect of gas composition in chemical-looping combustion with copper based oxygen carriers: Fate of light hydrocarbons. Int. J. Greenhouse Gas Control. 2010. 4: 13-22. [ Links ]
19. Garcia-Labiano, F.; de Diego, L. F.; Gayan, P.; Adanez, J.; Abad, A.; Dueso, C. Effect of fuel gas composition in chemical-looping combustion with Ni-based oxygen carriers. 1. Fate of sulfur. Ind. Eng. Chem. Res. 2009. 48 (5): 2499-2508. [ Links ]
20. Forero, C. R.; García-Labiano, F.; de Diego, L. F.; Gayan, P.; Adanez, J.; Abad, A. Effect of gas composition in chemical-looping combustion with copper based oxygen carriers: Fate of sulfur. Int. J. Greenhouse Gas Control. 2010. 4: 762-770. [ Links ]
21. Adanez, J.; Gayan, P.; Celaya, J.; de Diego, L. F.; Garcia-Labiano, F.; Abad, A. Chemical-looping combustion in a 10 kW prototype using a CuO/Al2O3 oxygen carrier: effect of operating conditions on methane combustion. Ind. Eng. Chem. Res. 2006. 45: 6075-6080. [ Links ]
22. de Diego, L. F.; García-Labiano, F.; Gayan, P.; Celaya, J.; Palacios, J. M.; Adanez, J. Operation of a 10 kWth chemical-looping combustor during 200 h with a CuO-Al2O3 oxygen carrier. Fuel. 2007. 86: 1036-1045. [ Links ]