Introducción
En la actualidad, se producen en el Ecuador 32'528.428 cajas de banano (Musa paradisiaca) de exportación según A.E.B.E [1]. Esto le otorga al país una posición privilegiada dentro del sector bananero mundial como productor potencial de banano. Sin embargo, se estima que de esta producción el 7% se considera desecho, ya que, al no cumplir con los debidos requisitos para ser empacado y comercializado, se convierte en un residuo [2]. Por lo anterior, se han buscado nuevas alternativas biotecnológicas para la optimización de estos desechos con el objetivo de disminuir el impacto ambiental generado por estos.
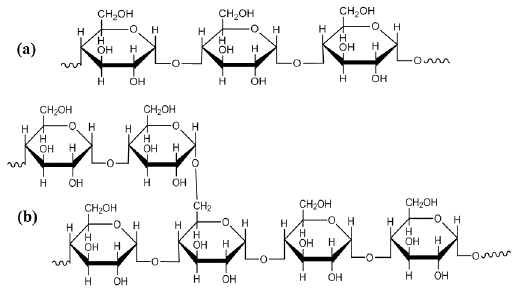
El banano, cuando está en estado inmaduro, puede llegar a alcanzar una cantidad de 70% de almidón [3], fuente importante para la elaboración de nuevos biopolímeros biobasados. Viloria et al. [4] explican que el almidón está constituido por dos polisacáridos muy importantes: la amilosa, conformada por cadena lineal de unidades glucosidicas entre 200 y 2500 unidades y la amilopectina, conformada por una estructura ramificada que se une mediante el enlace α (1-6) de cada 10 unidades lineales de la glucosa (ver Figura 1).
El almidón que es obtenido de desechos agrícolas y de plantas sirve para producir polímeros biodegrables y pueden ser mezclados con bioplásticos, lo que produce una descomposición para la generación de abono orgánico útil para el suelo [5]. Hay que considerar que la adición de este tipo de polímeros naturales en dosificación con otros de tipo sintético provoca un aumento en la degradabilidad de la matriz polimérica y que, en algunos casos como la combinación del almidón en un 30% con el polietileno de baja densidad, ha provocado que la matriz sea considerada como un material parcialmente biodegradable [6]. Según el trabajo realizado por Rodríguez [7], la mezcla de los biopolímeros y los polímeros sintéticos dan como resultado nuevos materiales con mejores o iguales propiedades térmicas y mecánicas que la matriz polimérica original y se evidencian importantes reducciones en el costo. Cayuela et al. [8] muestran que los biopolímeros son alternativas ambientalmente seguras, debido a que ayudan a reducir la dependencia del petróleo.
Actualmente, las investigaciones están enfocadas en el desarrollo de nuevos materiales biodegradables dosificados con polisacáridos obtenidos de fuentes renovables y que en medio de compostaje se comportan totalmente como biodegradables [9]. Adicional a esto, dentro de estas investigaciones es importante mantener o mejorar las propiedades mecánicas y térmicas de los materiales desarrollados. Para la producción de nuevos polímeros dosificados con fibras naturales hay que considerar, como se mencionó antes, el precio de producción a nivel industrial: la materia prima renovable y la cantidad de energía necesaria para producirlos [10].
Por otro lado, los polímeros termoplásticos constituyen el 80% de la producción total de plásticos. Sin embargo, el porcentaje de reciclaje de estos plásticos es muy bajo [11]. Actualmente, los polímeros termoplásticos han sido objeto de estudio en dosificaciones con fibras naturales, esto debido a sus buenas propiedades térmicas y mecánicas. La gran mayoría de los termoplásticos son poco biodegradables. En el trabajo realizado por Cepeda et al. [12] se indica que estos polímeros sintéticos a menudo son dosificados con fibras naturales. Se recalca que estos polímeros derivados del petróleo, aunque poseen una baja estabilidad y una liberación de tóxicos perjudiciales al ser humano, poseen una gran estabilidad mecánica en mezcla con otros polímeros naturales.
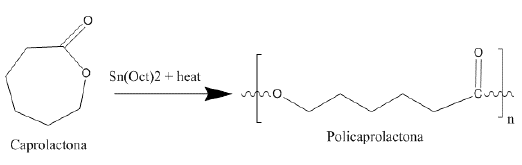
Uno de los polímeros termoplásticos de gran uso en la actualidad por su compatibilidad con polímeros lignocelulósicos es el policaprolactona (PCL). Según Barney [13], el PCL es un polímero sintético biodegradable con una estructura lineal (ver Figura 2). Posee una buena resistencia química al agua, a aceites, a solventes e, incluso, al cloro, además de tener un punto de fusión de alrededor de 58 a 60 °C.
El PCL es un polímero producido por síntesis química a partir de fuentes petroquímicas, con características especiales y, debido a su biodegradabilidad, es útil para la mezcla con fibras naturales [14]. Hay que considerar que en el área biomédica se utiliza este polímero como matriz de liberación de medicamentos. Su degradabilidad se basa, principalmente, en que su grupo éster puede hidrolizarse y convertirse en oligómeros de bajo peso molecular y llegar a ser metabolizado por microorganismos como fuente de carbono [15]. Debido a sus características térmicas tales como su baja temperatura de fusión (≈ 60 °C), su temperatura de transición vítrea (≈ -60 °C) y su cristalinidad (≈ 50%), estas pueden modificarse por medio de dosificaciones con otros polímeros degradables con el objetivo de aumentar estos parámetros [16]. Adicional a esto, el PCL tiene una estructura uniforme por lo que es fácilmente miscible con otros polímeros, mejorando así su cristalinidad y sus propiedades [13].
Lorenzo et al. [13] afirma que la incorporación de un agente compatible en la matriz polimérica de PCL mejora las propiedades mecánicas y además ayuda a optimizar el desempeño de esta matriz, sin verse afectada de forma negativa la biodegradabilidad del mismo, debido a la interacción que existe entre las dos fases.
Al modificar un almidón, este tendrá una mayor estabilidad a condiciones extremas de procesamiento y, por lo tanto, sus propiedades funcionales se ven mejoradas notablemente [14]. Los almidones acetilados son usados en la industria debido a que el almidón nativo no tiene la capacidad de resistir a procesos de alto esfuerzo, como por ejemplo procesos de corte y temperatura, debido a su inestabilidad [20].
Teniendo en cuenta lo anterior, la presente investigación tiene como propósito estudiar las dosificaciones de PCL con el almidón extraído y modificado de la cascara de banano a través de un análisis diferencial de barrido (DSC, por sus siglas en inglés) y conocer cómo influye la adición de este polisacárido en la matriz termoplástica. Para esto, se estudiarán los parámetros térmicos tales como: la temperatura de transición vítrea (Tg), temperatura de fusión (Tm) y el calor entálpico (ΔΗ). Lo anterior tiene como objetivo demostrar cuál es el comportamiento de estas dosificaciones en función de sus transiciones térmicas (Tg y Tm) y analizar cuál es el grado de reticulación (cristalinidad) de estos nuevos biopolímeros, para así establecer la mejor dosificación considerando sus transiciones térmicas.
Materiales y métodos
La materia prima para la obtención del almidón fue extraída de las cáscaras de banano (Musa paradisiaca). Se recolectaron 3000 g de cáscaras de banano en estado de residuo de una zona en la ciudad de Machala (Ecuador). A partir de estas cáscaras se procedió a la extracción del almidón y la determinación del rendimiento por el método planteado.
Extracción del almidón
El procedimiento para la extracción del almidón se realizó mediante una metodología propuesta por Montoya et al. [21] con unas ligeras modificaciones. Allí se explica el proceso para la extracción por un método seco, el cual se detalla a continuación.
Método seco para la extracción
- Selección de las cáscaras: En esta operación se desecharon las cáscaras en mal estado.
- Lavado de las cáscaras: Se realizó con agua fría, junto a un cepillo se procedió a eliminar todas las impurezas (polvo, basuras, pajas, etc.).
- Licuado: Consistió en licuar las cáscaras para reducir su tamaño.
- Secado: El precipitado se secó en un desecador marca Memmert a una temperatura de 105 °C durante 8 h.
- Licuado: Se procedió nuevamente a licuar para reducir la compactación de la masa obtenida.
- Tamizado: Se procedió a desintegrar todos los grumos formados durante el proceso desecado mediante seis tamices de diferente tamaño 20, 40, 60, 80, 100 y 120 micras.
- Almacenado: Se colocó la muestra de interés dentro de una funda hermética.
Blanqueamiento del almidón extraído
El blanqueamiento del almidón se realizó con una solución de hipoclorito de sodio al 10%, la cual se calentó previamente en un vaso de precipitados. Posterior a ello, se colocó el almidón y se mantuvo a una temperatura de 70 °C durante un periodo de dos horas con agitación constante. Luego de ello se lavó la misma con agua destilada obteniendo de esta manera un pH final entre 7,5 y 9. Seguidamente, se filtró con ayuda de una bomba, para luego secar durante un periodo de 24 h en una estufa marca Memmert a 35 °C.
Análisis proximal químico
Para establecer cuáles son las cualidades del almidón extraído, se procedió a realizar el análisis proximal químico donde se determinaron parámetros como: la humedad, temperatura de gelatinización y complejo yodo-almidón.
Determinación de la humedad
Para la determinación del porcentaje de humedad, se empleó la NORMA INEN 1462. [22] "cereales y productos de cereales. Determinación del contenido de humedad". Inicialmente se estabilizó la estufa durante 45 min para alcanzar la temperatura de trabajo (105-130 °C). Posterior a ello, se pesaron 2 g de muestra y se llevaron a la estufa marca Memmert a 130 °C durante un periodo de una hora. Una vez enfriada la muestra, se reportó el residuo de almidón como cantidad de sólidos totales y pérdida de peso como humedad.
Determinación de la temperatura de gelatinización
Para la determinación de este parámetro se empleó el procedimiento aplicado por Granados et al. [23]. Para ello, se preparó una suspensión de almidón al 5% y se colocó a baño maría a 85 °C con agitación constantemente. Luego, se introdujo un termómetro a la suspensión y de esta manera se leyó la temperatura a la cual la suspensión se estabiliza cambiando su aspecto y comienza el hinchamiento de los gránulos causando una polimerización al momento de la gelatinización, lo que aumenta su peso por la retención de agua en forma de gel.
Complejo yodo-almidón
La prueba del complejo del yodo se realizó aplicando el procedimiento realizado por García [24] con unas ligeras modificaciones. Para este análisis se colocaron 5 mL de la solución de almidón soluble al 1% en un tubo de ensayo. Luego, se agregaron 3 gotas de solución de yodo al 0.1 N. Se calentó el tubo directamente a la llama del mechero, hasta que se tornara de color claro. Posterior a ello, se expuso el mismo tubo en agua fría y se tomó el tiempo que tardaba en regresar a su coloración inicial.
Análisis de azúcares reductores
El método para la determinación de amilosa establecido por Hoover y Ratnayake [25] permitió determinar los porcentajes de la relación amilosa/ amilopectina en la muestra. Para ello se pesaron 100 mg de muestra en un frasco volumétrico de 100 mL. Se agregó 1 mL de etanol al 95 % v/v y 9 mL de hidróxido de sodio 1N. Se dejó reposar a 20 °C entre 18 y 24 h. Posteriormente, se aforó en un matraz de 100 mL con agua destilada. En un balón de aforo de 100 ml se colocaron 50 mL de agua destilada, 5 mL de la preparación inicial, 1 mL de ácido acético 1 N y 2 mL de solución de yodo al 2 %. Se mezcló y se aforó. Al finalizar, se almacenó la muestra en la oscuridad durante 20 min para leer la densidad óptica en un espectrofotómetro UV-visible marca JENWAY a una longitud de onda de 620 nm.
Acetilación del almidón
Para la acetilación del almidón se procedió según el método realizado por Sánchez [26]. Este consistió en tomar 50 g de almidón y adicionar 100 mL de agua destilada, conformándose una suspensión uniforme con ayuda de un agitador. Posteriormente se introdujo en un baño frio a una temperatura de 15 °C. Seguidamente, se ajustó el pH entre 8.0 - 8.5 de la suspensión con una solución de NaOH al 3%. Se adicionó el anhidro acético, a volúmenes de 5, 10 y 15mL con el objetivo de obtener diferentes grados se sustitución. Posterior a esto, se dejó reaccionar el sistema por 10 min más y se adicionaron 10 mL de HCL 0,5 N para disminuir el pH hasta 4.0 - 4,5 lavando este almidón 3 veces con agua destilada. La muestra se centrifugó a 2500 rpm por 20 min y se realizó un último lavado con etanol absoluto y nuevamente se centrifugó a 2500 rpm por 10 min más. El secado de la muestra sometida se realizó en una estufa marca Mammert a una temperatura de 40 °C por 12 h.
Formulación
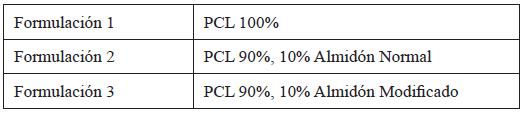
Se realizó una dosificación entre el almidón normal, el modificado y el polímero PCL, para posteriormente determinar el grado de reticulación (durante el proceso de solidificación) que posee el almidón dosificado con un plástico derivado de un hidrocarburo. La Tabla 1 muestra las distintas dosificaciones.
Análisis de espectroscopia infrarrojo (IR)
El objetivo de realizar el análisis IR fue determinar la estructura del almidón extraído. Esto se realizó en un intervalo de longitud desde 4400 hasta 515 cm-1, y en unidades de absorbancia de un espectro infrarrojo FTIR "WQF 510".
Análisis diferencial de barrido (DSC)
Este análisis permite conocer la cantidad de calor absorbido o desprendido por una sustancia cuando es sometida a una temperatura constante, además de poder observar sus transiciones térmicas en un determinado tiempo o cuando es calentada o enfriada a una velocidad determinada y en un cierto rango de temperatura [27]. En este análisis se obtuvo información sobre la temperatura de fusión, temperatura de transición vítrea y su calor entálpico de cada una de las dosificaciones. Para ello se tomaron aproximadamente 10 mg de muestra exponiéndola a temperaturas de calentamiento desde -35 °C hasta 220 °C. Luego, un enfriamiento desde 220 °C hasta -35 °C y, finalmente, un recalentamiento de -35 °C hasta 220 °C de manera sincronizada.
Resultados y discusión
Rendimiento de la extracción del almidón
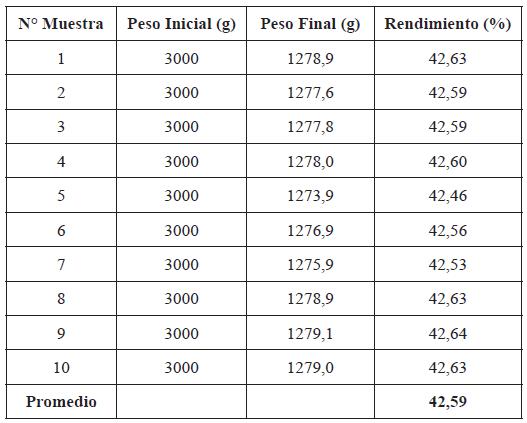
Como parte de la extracción del almidón está la cuantificación del rendimiento del proceso aplicado, esto con el único objetivo de comprobar que la extracción ha sido eficaz en términos de cantidades. Se determinó el rendimiento de la metodología realizando el proceso a 10 muestras con el objetivo de tener o establecer un resultado representativo del proceso propuesto implementado, como se muestra en la Tabla 2. Allí se pueden observar los pesos iniciales y finales de cada muestra (M). A partir de estos valores se obtuvo un rendimiento promedio del 42,59%, lo que indica que el método propuesto para la extracción del almidón ha tenido un resultado aceptable.
Análisis proximal químico
En el análisis químico realizado se obtuvieron algunos datos importantes para cada uno de ellos.
Determinación de la humedad
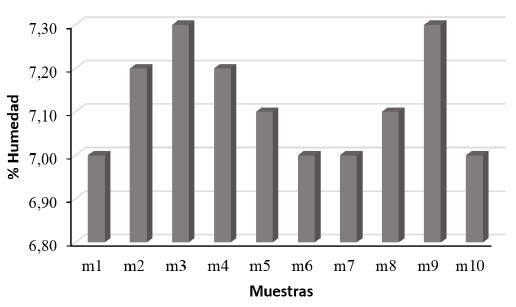
En la Figura 3 se observan los resultados del análisis de la humedad, donde se aprecia que el promedio aproximado general es del 7%. Es importante conocer este dato, ya que la cantidad de agua presente en el almidón influye en la reticulación de la matriz polimérica dosificada. La destructuración no se ve afectada debido a que la humedad no es demasiada alta [5].
Determinación de la temperatura de gelatinización
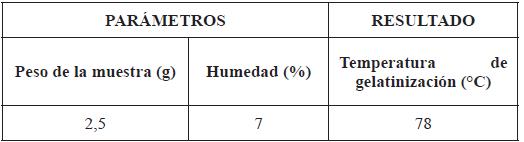
En la temperatura de gelatinización se obtuvo un valor de 78 °C, lo que significa que la absorción de agua es algo considerable en las zonas de los gránulos donde es accesible. Sin embargo, esta temperatura nos indica que el hinchamiento de las partículas comienza a considerarse relativamente alto. En la Tabla 3 se presentan las condiciones del análisis, en las que se puede observar una temperatura relativamente alta de 78 °C. Este valor obtenido nos indica que el almidón extraído puede usarse en materiales donde sean necesarias temperaturas no muy altas, ya que esto representa una mayor estabilidad del gránulo interno del almidón y esto evidencia una mayor cristalinidad en el interior [28].
Complejo yodo -almidón
El objetivo de la determinación del complejo de almidón mediante la prueba de yodo es determinar el grado de hidrolisis del almidón mediante la formación y deformación de los complejos de coordinación formados entre el yodo y el almidón. Al hacer reaccionar el yodo con el almidón se forma una solución colorida, la cual se debe a la formación de un complejo de coordinación entre las micelas de almidón y de yodo.
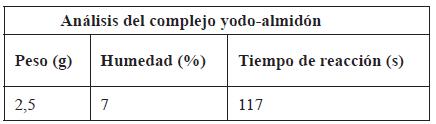
Este color disminuye cuando la temperatura aumenta, hasta desaparecer por completo, y se intensifica al bajar nuevamente la temperatura. En esta reacción el yodo se introduce en las espiras (espacios vacíos de un polisacárido) de la molécula del almidón modificándolo y así provocando un color púrpura, indicando su presencia; mientras mayor sea la concentración de almidón de una muestra, menor tiempo tarda en tomar dicha coloración. La reacción tuvo una duración de 117 segundos, además de considerar otros parámetros como el peso y la humedad inicial (ver Tabla 4).
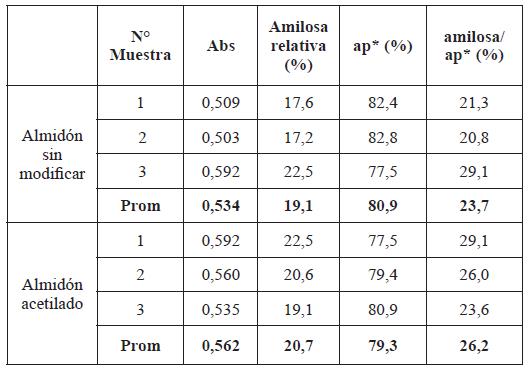
En la Tabla 5 se aprecia la relación de amilosa-amilopectina presente en las muestras de almidón. Esta relación indica el tipo de almidón obtenido ya que se pueden clasificar en diferentes grupos: los almidones cerosos que contienen muy poca cantidad de amilosa son alrededor del 1%; los almidones normales contienen entre 15-30% de amilosa y los almidones altos en amilosa contienen 50% o más de este polímero natural. En los resultados obtenidos podemos decir que la muestra trabajada es de almidón normal ya que los valores oscilan entre el 19 y 20 % para el almidón sin modificar y de igual manera para el almidón modificado. Entre los factores que influenciaron este resultado se consideran la alta cantidad de humedad (alrededor del 58%) del banano del cual se obtuvo el almidón y una moderada madurez.
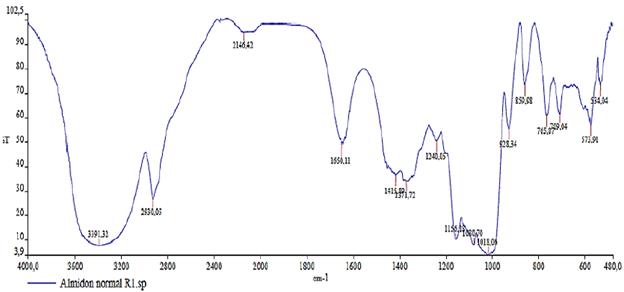
Análisis de espectroscopia infrarrojo (IR)
En la Figura 4 se aprecia el espectro IR del almidón sin modificar extraído del proceso planteado. Se puede observar que existe un pico a una longitud de onda de 3391 cm-1 lo que significa la tensión de un grupo hidroxilo (OH) y un grupo C-H a una banda de 2930 cm-1, debido a la vibración de tensión del grupo mencionado, mientras que se observa un pico en 1650 cm-1 que proviene del agua intramolecular contenida en el almidón (vibración por flexión del grupo O-H).
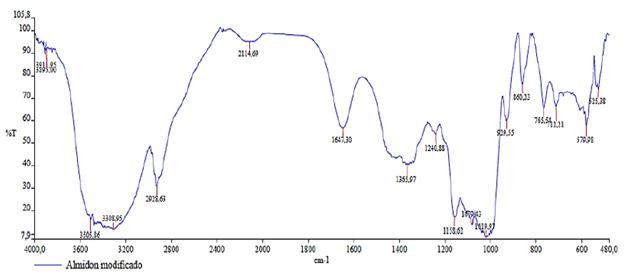
La Figura 5 pertenece al espectro IR del almidón modificado que se realizó mediante el proceso de acetilación. Allí se observa una ligera disminución en las señales correspondientes a las vibraciones por estiramiento del grupo hidroxilo comprendido en el rango de 3000 hasta 3900 cm-1 y, además, se observan vibraciones por flexión alrededor de 1647 cm-1 de los grupos -OH. Esto es debido a los estiramientos de los enlaces intermoleculares del grupo hidroxilo de la molécula, es decir, se remplazaron los grupos -OH de la molécula de almidón por grupos acetilos, proporcionándole un efecto esférico a las vibraciones por flexión. De acuerdo a lo anterior, se puede señalar que la acetilación efectuada a las muestras fue efectiva.
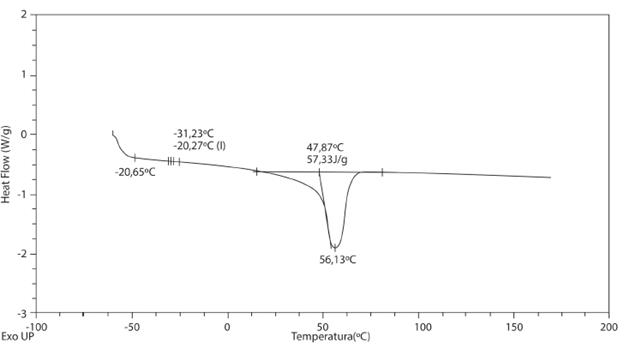
Análisis diferencial de barrido
Se realizó el presente análisis con la finalidad de obtener información acerca de la reticulación de la mezcla entre el PCL y el almidón sin modificar y modificado. En la Figura 6 se observa el análisis DSC del PCL sin dosificar. En la figura se observa un punto de fusión y una temperatura de = 56 °C. En la literatura revisada [29] se encuentra una temperatura aproximada de =60 °C, siendo valores aproximados.
Posteriormente, se realizó el análisis DSC del PCL dosificado con el almidón sin modificar en un 10% en peso. En este primer análisis (ver Figura 7), se observa que la dosificación (al 10%) logra tener una temperatura de fusión de 64 °C variando con la temperatura de fusión del PCL sin dosificar que es de 57 °C (ver Figura 6). Sin embargo, su temperatura de transición vítrea comienza alrededor de =31 °C y termina a=10 °C (ver Figura 7). Esto evidencia una rotación de la cadena polimérica alrededor de los enlaces por lo que se ve una modificación de su temperatura de transición vítrea.
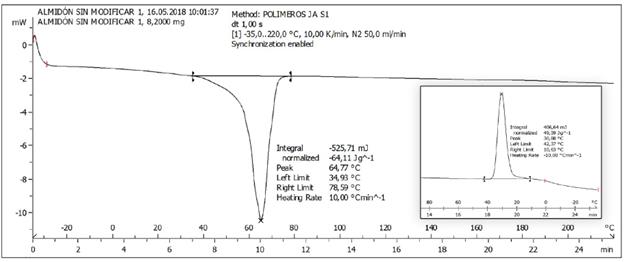
Figura 7 Curvas de calentamiento y enfriamiento (Análisis DSC del PCL dosificado en un 10 % con almidón sin modificar).
En la Figura 8 se observa el DSC de la dosificación del PCL con el almidón extraído, en el cual se observa que la dosificación logra tener una temperatura de transición de =66,4 °C variando con la temperatura de fusión del PCL sin dosificar. Esto se debe al tamaño de la partícula añadido a la matriz polimérica y al grupo acetilo reaccionado en el almidón. A pesar de ello, en este análisis se tiene una máxima temperatura de transición vítrea aproximadamente de =33 °C (ver Figura 8), lo se debe al movimiento de rotación de la cadena polimérica que es muy baja. Como se aprecia en las figuras, no existe una significante variación de temperaturas entre las dos dosificaciones en comparación con el PCL sin dosificar, a excepción de las temperaturas de transición vítrea que son diferentes.
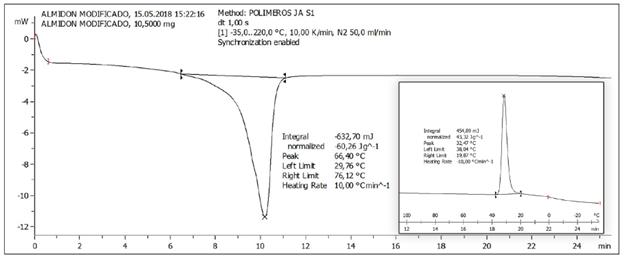
Figura 8 Curvas de calentamiento y enfriamiento (Análisis DSC del PCL dosificado con el almidón modificado en un 10%).
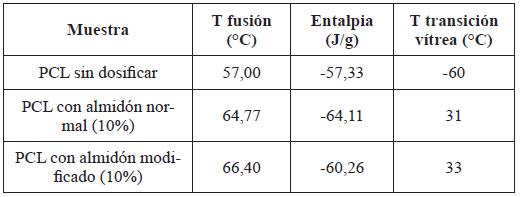
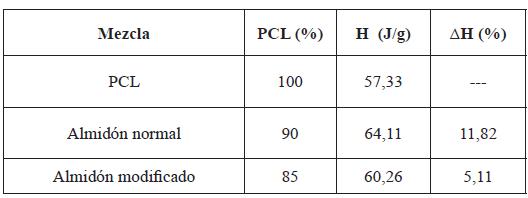
En la Tabla 6 se presenta un resumen de los análisis DSC del PCL con el almidón sin modificar y modificado, visualizando que existe un incremento en las temperaturas de fusion hasta 9 °C tanto para el almidón sin modificar, como para el modificado. Esto indica que la adición de este polisacárido mejora las propiedades térmicas de la matriz polimérica.
Evaluación de la reticulación del PCL en dosificación con el almidón
Para estudiar la reticulación que se produjo entre el PCL y el almidón sin modificar y modificado, se calculó y comparó el grado o fracción de cristalinidad en función de la cantidad de energía desprendida (exotérmica) ocurrida en la primera curva (reacción de curado) de calentamiento a través del análisis DSC a cada una de las mezclas (almidón modificado y sin modificar). Este calor desprendido por las muestras es proporcional al área (H) de la curva y esta área es correspondiente a la masa cristalizada. En la Tabla 7 se observan los porcentajes de reticulación de cada dosificación, donde la mezcla con el almidón sin modificar tiene el mayor grado de reticulación (11,82%). Esto implica que la adición de este polisacárido aumentó la difusividad de la matriz polimérica incrementando la movilidad de los agentes de relleno [30].
Se presentan en la Tabla 7 los calores de fusión de las mezclas del PCL con el almidón normal y modificado. Se observa que existe un incremento alrededor del 12% en el calor de fusión del polímero PCL + el almidón sin modificar, en comparación con el polímero PCL sin adicionar ningún agente. De igual manera, existe un incremento del 5% en el calor de fusión del polímero PCL + el almidón modificado en contraste con el PCL sin mezcla.
Al analizar estos resultados se evidencia que el almidón actúa como un tipo de agente reticulante aumentando la reticulación de la matriz polimérica hasta un H de 64,11 J/g. Sin embargo, en lo que respecta a la mezcla del PCL con el almidón modificado, se observa que existe un incremento de su calor de fusión de 60,26 J/g, lo que indica que el almidón modificado no es un buen agente reticulante para la matriz polimérica.
Conclusiones
En el presente trabajo de investigación se realizó el estudio comparativo de una dosificación entre un polímero termoestable como es el caso del PCL, el almidón extraído de los desechos del banano (cáscara) al 10% en peso y con almidón modificado mediante acetilación igualmente al 10% en peso. En el método de extracción realizado se evidenció que la cantidad de amilosa obtenida fluctúa entre 19 y el 20%, por lo que podemos considerar que el almidón está clasificado como "normal". En cuanto a las dosificaciones de este almidón con el PCL se observó que existe un incremento en la temperatura de fusión de la mezcla polimérica de 9 °C (desde 57 °C para el PCL sin dosificar hasta un 67 °C para las dosificaciones), lo que indica que el almidón adicionado actúa de una manera positiva en el aumento de dicha temperatura. Sin embargo, en la reticulación de cada una de las dosificaciones se observó que el grado de reticulación del almidón sin modificar con el PCL presenta el mayor porcentaje (12%), lo que indica que este tipo de almidón sin modificar actúa como un buen agente reticulante, esto en comparación con el PCL sin dosificar. Finalmente, podemos decir que la adición de este tipo de polisacárido en un porcentaje del 10% (sin modificar, preferiblemente) modifica las propiedades térmicas del PCL de una manera positiva y además su comportamiento cristalino.