Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Agronómica
Print version ISSN 0120-2812
Acta Agron. vol.61 no.4 Palmira Oct./Dec. 2012
1Ingeniera Agroforestal, estudiante de Maestría en Fitopatología, Universidad de Caldas, Manizales, Caldas, Colombia. 2Ing. Agr., Magister en Fitopatología. Profesor Auxiliar, Departamento de Producción Agropecuaria, Facultad de Ciencias Agropecuarias, Universidad de Caldas, Manizales, Caldas, Colombia. 3Ing. Agr., Ph.D. Profesor Asociado, Universidad Nacional de Colombia, sede Palmira/Centro Internacional de Agricultura Tropical – CIAT, Colombia.
*Autor para correspondencia: oscar.guzman@ucaldas.edu.co; †roalorpaz@hotmail.com; ‡jaocampop@unal.edu.co
Los nematodos fitoparásitos son una de las mayores limitantes en la fruticultura tropical causando grandes pérdidas económicas por la reducción de los rendimientos. En Colombia no existe información respecto a estos parásitos que afectan el cultivo del maracuyá y es necesario generarla para crear estrategias de manejo. El objetivo del estudio fue identificar y cuantificar los nematodos fitoparásitos presentes en plantas de maracuyá de la Colección Nacional, conformada por 28 accesiones de diferentes procedencias establecida en la Granja Luker en Palestina, Caldas (Colombia), a 1058 m.s.n.m., 5° 4' 13.2" N y -75° 41' 7.7" O, 23 °C, 2250 mm/año y 75% de HR. La recolección de las muestras se realizó en la zona de plateo de cada planta hasta 60 cm de profundidad. En cada accesión se tomaron tres muestras de 100 g de raíces funcionales y 100 g de suelo. La extracción de nematodos de raíces y suelo se realizó con base en el principio de flotación en azúcar. Para los datos se desarrolló un análisis univariado con la estimación del promedio, el coeficiente de variación, el análisis de varianza y prueba de Tukey al 5%, para establecer las diferencias entre accesiones. Se recuperaron nematodos de siete géneros, Helicotylenchus, Rotylenchulus, Radopholus, Meloidogyne, Tylenchus, Aphelenchoides y Trichodorus. Las especies con mayor frecuencia en las accesiones, tanto en raíces como en suelo, fueron Helicotylenchus dihystera, Rotylenchulus reniformis y Radopholus similis con 100, 75 y 61%, respectivamente. Se encontraron 11, 8 y 16 accesiones de maracuyá sin parasitismo de los géneros Radopholus, Rotylenchulus y Meloidogyne, respectivamente. Dentro de éstas, sobresalen las accesiones AntFla03 y CauFla01 por sus características agronómicas, las cuales constituyen un reservorio genético para programas de fitomejoramiento en la búsqueda de resistencia o tolerancia a nematodos fitoparásitos que involucren hibridación o injertación.
Palabras clave: Colombia, fitonematodos, Helicotylenchus, maracuyá, nematodos de las plantas, Passiflora edulis, Radopholus similis, Rotylenchulus.
Plant parasitic nematodes are one of the major constraints in tropical fruit causing great economic losses by reducing yields. In Colombia there is not information dealing with the production systems about these parasites affecting passion fruit cultivation so, it is necessary to generate information for management strategies. The aim of this study was to identify and quantify plant parasitic nematodes present in the National yellow passion fruit Collection consisting of 28 accessions from different origin and established in the farm Luker in Palestina (Caldas), Colombia. Sample collection was carried out in the root area of each plant at a depth of 60 cm in each accession. Three samples of 100 g of functional root system and 100 g of soil were taken. The extraction of root and soil nematodes was based on the flotation principle of nematodes in sugar. For data an univariate analysis with the estimated average, the coefficient of variation, analysis of variance and Tukey test at 5%, to establish the differences among accessions was performed. Results showed seven kinds of soil and root phytonematodes: Helicotylenchus, Rotylenchulus, Radopholus, Meloidogyne, Tylenchus, Aphelenchoides and Trichodorus. The species most frequently found in root and soil of accessions were Helicotylenchus dihystera, Rotylenchulus reniformis and Radopholus similis with 100, 75 and 61%, respectively. Results showed 11, 8 y 16 accessions without parasitism of the genera Radopholus, Rotylenchulus and Meloidogyne, respectively. Among these, accession AntFla03 and CauFla01 were outstanding due to their agronomic characteristics which constitute a gene pool for breeding programs in search for phytoparasitic nematode resistance or tolerance that involve hybridization or grafting.
Key words: Colombia, Helicotylenchus, maracuyá, Passiflora edulis, phytonematodes, plant nematodes, Radopholus similis, Rotylenchulus.
El maracuyá (Passiflora edulis f. flavicarpa Degener) es económicamente la principal especie del género Passiflora L. Se encuentra distribuida en zonas tropicales desde el nivel del mar hasta 1350 m.s.n.m. Es una especie originaria de la región amazónica y descrita en la isla de Hawaii (EE.UU) en 1932 por Degener, desde donde se difundió a otros países tropicales del mundo (Degener, 1932; Morton, 1967; Ulmer, 2004; Ocampo y Urrea, 2012). En Colombia fue introducido a comienzos de 1960, en el departamento del Valle del Cauca, y actualmente es el tercer productor mundial con cerca de 6000 ha cultivadas, después de Brasil y Ecuador (Jaramillo et al., 2009). En el país la producción de maracuyá es aproximadamente de 92,000 t (Agronet, 2012) y se concentra en los departamentos de Huila con 1234 ha y 18,838 t, Meta con 759 ha y 15,452 t y Valle del Cauca con 641 ha y 12,012 t. El 75% de la producción nacional se exporta a países europeos como jugo concentrado y el resto se comercializa como fruta fresca en mercados locales (Isaac, 2009). La fruta de maracuyá ha conquistado los mercados internacionales por su aroma, sus características organolépticas y sus propiedades medicinales (Yockteng et al., 2011). La planta crece en suelos de texturas franca a franca-arenosa, con una profundidad mínima de 60 cm, ricos en materia orgánica, bien drenados y con un pH entre 5.5 y 7.5 (García, 2002; Lima y Cunha, 2004). Prefiere zonas con precipitaciones entre 800 a 1500 mm/año, temperatura de 20 a 25 °C y humedad relativa menor de 80% (Fischer et al., 2009; Ocampo et al., 2012).
El cultivo de maracuyá es afectado por hongos, bacterias, virus y nematodos fitoparásitos, lo que reduce la producción hasta en 50% y ocasiona grandes pérdidas económicas para los productores. El aumento en la incidencia y severidad de plagas como las moscas del ovario o del botón floral, Dasiops gracilis, D. enedulis y D. yepezi, y enfermedades como secadera o marchitez vascular por Fusarium oxysporum f. sp. passiflorae, Schlecht, bacteriorsis o mancha de aceite, Xanthomonas campestris pv. passiflorae Pereira, roña, Cladosporium cladosporioides Fresen, virus del mosaico de la soya, Soybean mosaic virus SMV y los nematodos fitoparásitos como Meloidogyne spp., Rotylenchulus spp. y Helicotylenchus spp., ocasionan presión fitosanitaria (Lozano, 2008; Castaño, 2009; Hernández et al., 2011), incrementan el deterioro del cultivo y aumentan la demanda por tratamientos químicos, en contra de la salud humana y del medio ambiente (Guerrero- López y Hoyos-Carvajal, 2011; Villegas et al., 2012). Los nematodos en este cultivo han sido poco estudiados y los diagnósticos fitosanitarios por parte de los productores consisten en observación visual que muchas veces se confunde con deficiencias de elementos nutritivos.
Los nematodos son filiformes de tamaño microscópico (300 a 1000 µm de largo x 15 a 35 µm de ancho) que habitan en el suelo (Agrios, 2005; Luc et al., 2005). Los nematodos fitoparásitos ocasionan daños internos o externos en las raíces de las plantas, al momento de alimentarse por medio de su estilete y algunos pueden ocasionar agallas o nudos como los del género Meloidogyne spp. o estar asociados con hongos del suelo como Fusarium spp. (Mai et al., 1996; Siddiqi, 2000; Fischer et al., 2010).
En un estudio realizado en los departamentos del Valle del Cauca, Cauca y Caldas, Sánchez et al. (1993) registraron nueve géneros de nematodos fitoparásitos que afectan el cultivo de maracuyá; entre estos, Rotylenchulus reniformis Lindford y Oliveira presentó la mayor frecuencia en el suelo (72%) y en las raíces (25%) cuando se compararon con Helicotylenchus sp., Tylenchorhynchus sp. y Meloidogyne sp. que no superaron 19%. En un estudio similar, Suárez et al. (1994) observaron que R. reniformis es el nematodo con mayor incidencia en los cultivos de maracuyá de la zona central de Venezuela (Aragua, Barinas, Carabobo y Miranda), cultivo en el cual ocasiona una reducción en la emisión de raíces de las plantas y un amarillamiento general del follaje.
En condiciones de laboratorio, Suárez et al. (2002) encontraron que este mismo nematodo disminuye el peso aéreo y de raíces de maracuyá y se reproduce 2.5 veces más respecto al inóculo inicial. Otros estudios en maracuyá y gulupa (P. edulis Sims) mostraron a Meloidogyne incognita (Kofoid y White) Chitwood, M. javanica (Treub) Chitwood y Helicotylenchus dihysteroides Siddiqi como nematodos que destruyen el sistema radicular (Suárez et al., 1994; Sikora y Fernández, 2005; Lozano, 2008). Entre los nematodos fitoparásitos, los formadores de agallas pertenecientes al género Meloidogyne son considerados los de mayor importancia económica por los daños que causan en vegetales, frutales, ornamentales y arvenses (Agrios, 2005). En este género existen más de 89 especies nominales, no obstante, M. incognita, M. javanica, M. arenaria (Neal) Chitwood y M. hapla (Chitwood) son las causantes de grandes pérdidas económicas en áreas agrícolas en el mundo (Rodríguez-Kábana y King, 1987; Cia y Salgado, 2005; Sikora y Fernández, 2005; Fischer et al., 2010).
En Colombia son escasos los estudios relacionados con nematodos fitoparásitos en las especies cultivadas del género Passiflora L. y especialmente en maracuyá. Debido a la importancia del cultivo para el país, el efecto de estos nematodos en el sistema radicular y la parte aérea de la planta, al igual que la oportunidad de explorar el componente genético como una estrategia de manejo, el objetivo de este trabajo fue identificar y cuantificar los nematodos fitoparásitos presentes en la Colección Nacional de Maracuyá establecida en la Granja Luker en Palestina (Caldas), bajo el proyecto de investigación Aprovechamiento de la diversidad del maracuyá, la gulupa y la granadilla para mejorar y diversificar los sistemas de producción en Colombia – Ministerio de Agricultura y Desarrollo Rural - MADR, como contribución al conocimiento de los problemas sanitarios de este cultivo y de la fruticultura colombiana en general.
La investigación se realizó en la granja Luker, ubicada en la vereda Santágueda del municipio de Palestina, Caldas (Colombia), a 1058 m.s.n.m., 5° 4' 13.2" N y -75° 41' 7.7" O. La temperatura promedio es de 23 °C, la precipitación anual de 2250 mm, la humedad relativa de 75% y el brillo solar promedio diario de 6 h. Los suelos son altos en materia orgánica, con textura franco arenosa y pH 6.8 (Aristizábal, 2002).
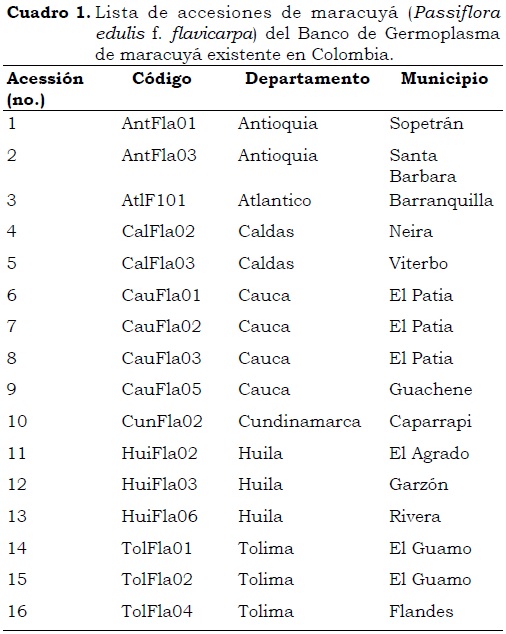
El banco de germoplasma de maracuyá, establecido en la granja Luker en octubre del 2009, está constituido por 28 accesiones de diferentes procedencias (Cuadro 1). El arreglo espacial de la colección es bloques al azar con dos repeticiones y una unidad experimental de 5 plantas con un sistema de espaldera sencilla, a una distancia de siembra de 3 x 3 m.
Para el ensayo, las muestras fueron recolectadas de la zona de plateo de cuatro plantas de cada una de las 28 accesiones. Las muestras se tomaron en hoyos rectangulares de 40 cm de lado y 60 cm de profundidad, se recolectaron tres muestras de 100 g de las raíces funcionales y 100 g de suelo, que fueron depositadas en bolsas plásticas transparentes debidamente rotuladas con el código de la accesión, antes de ser enviadas para procesamiento y análisis al Laboratorio de Fitopatología del Departamento de Producción Agropecuaria de la Universidad de Caldas.
La extracción de nematodos de raíces y suelo se realizó siguiendo el principio de flotación de estos en azúcar (Jenkins, 1964; Araya et al., 1995). Para el efecto, las raíces fueron lavadas con agua corriente, se pesaron y cortaron en trozos de 30 g antes de ser licuadas a alta velocidad por 30 s en una licuadora Osterizer, con 500 ml de agua. La solución del licuado fue depositada en un tamiz de 250 µm colocado a su vez sobre un tamiz de 25 µm. La muestra fue lavada con agua a presión para generar desprendimiento de los nematodos, y el material remanente en el tamiz de 25 µm fue depositado en tubos de 30 ml que se centrifugaron a 3800 r.p.m. durante 5 min. A continuación, se eliminó el sobrenadante y se adicionó una solución de sacarosa al 50% para repetir la centrifugación. Los nematodos flotantes en la solución de sacarosa se depositaron en el tamiz de 25 µm para lavar la sacarosa con agua corriente a baja presión, y finalmente tomar 20 ml de agua con nematodos en una caja Petri. La extracción de nematodos del suelo se hizó de manera similar, pero con omisión del procedimiento de licuado
.Las muestras obtenidas fueron trasferidas a cajas Petri que contenían 36 cuadrantes de 6 x 6 cm y se extrapoló con base en una muestra de 100 g de raíces o suelo. Se seleccionaron al azar tres cuadrantes y se cuantificó el número de nematodos en cada uno de ellos con uso de un microscopioestereoscopio.
Para la identificación de fitonematodos se tomaron 20 nematodos de cada caja Petri y con la ayuda de una aguja de disección se montaron en un porta-objetos con una gota de agua para su observación al microscopio compuesto de luz (Nikon, 40X). La identificación de los géneros y especies se realizó con las claves taxonómicas de Siddiqi (2000), figuras publicadas por Mai et al. (1996), los descriptores de nematodos fitoparásitos del C.I.H. (1972-1977), y de acuerdo con la experiencia del segundo coautor de la presente investigación.
Para los datos se realizó un análisis univariado con la estimación del promedio, el coeficiente de variación, el análisis de varianza y prueba de Tukey al 5%, para establecer las diferencias entre accesiones. Para el desarrollo de las estadísticas se tuvo en cuenta un valor de 100% de frecuencia, cuando una especie de nematodo fitoparásito se encontró en el total de las cuatro muestras. Los análisis se realizaron con el programa estadístico SAS versión 8.1 (Statistical Analisys Software, 2000).
Identificación de nematodos fitoparásitos
En las 28 accesiones de maracuyá evaluadas fueron identificados siete géneros de nematodos fitoparásitos: Rotylenchulus spp., Helicotylenchus spp., Radopholus spp., Meloidogyne spp., Tylenchus spp., Aphelenchoides spp. y Trichodorus spp. Estos géneros pertenecen principalmente a la clase Secernentea, orden Tylenchida, familias Hoplolaimidae, Pratylenchidae, Meloidogynae, Tylenchidae y Aphelenchidae, respectivamente (Mai et al., 1996; Siddiqi, 2000; Perry et al., 2009). El género Trichodorus spp. pertenece a la clase Adenophorea, orden Dorylaimida, familia Trichodoridae (Mai et al., 1996).
Poblaciones de los nematodos fitoparásitos Rotylenchulus reniformis y Helicotylenchus dihystera
En estos géneros, el mayor número de individuos en 100 g fue encontrado en las muestras de raíces, con valores desde 1 en la accesión Bavaria hasta 181 en CunFla02 para Rotylenchulus, y desde 77 en TolFla04 hasta 337 en CalFla03, con un coeficiente de variación (CV) de 8.3% (Cuadro 2 y Cuadro 3). Las accesiones que presentaron las mayores poblaciones de Rotylenchulus spp. en 100 g de raíces se encontraron en el departamento de Cauca en las accesiones CaulFla01, Caul- Fla02, CaulFla03 y CaulFla05, Antioquia en AntFla01 y AntFla03, Huila en HuiFla02, HuiFla03 y HuiFla06; Cundinamarca en CunFla02; y Caldas en CalFla02 y CalFla03. En el caso del género Helicotylenchus spp. todas las accesiones presentaron poblaciones que variaron entre 77 y 337/100 g de raíces en las accesiones TolFla04 y CalFla03, respectivamente (Cuadro 3, Figura 1).
En las muestras de suelo, las poblaciones totales de ambos géneros de nematodos fueron inferiores a las encontradas en las raíces (Cuadro 3), con un promedio de 252, un rango 103 a 400 nematodos/100 g y un CV de 14.6%. Los valores mínimos de poblaciones se presentaron en las accesiones TolFla01, TolFla02, TolFla04 y TolFla07 en el Tolima, y en todas las accesiones evaluadas en el Valle del Cauca (Cuadro 3).
Helicotylenchus spp., con 100% de incidencia, un promedio de 214 nematodos/100 g de raíces y 98 nematodos/100 g de suelo fue el género que se observó con mayor frecuencia en las muestras (Cuadro 3). Rotylenchulus spp. con 75% fue el segundo género más abundante (Cuadro 3, Figura 1). Sánchez et al. (1993) en cultivos de maracuyá comerciales en los departamentos del Valle del Cauca, Cauca y Caldas hallaron que R. reniformis fue la especie más frecuente con 72% y 25% en suelo y raíces, respectivamente, seguida de Helicotylenchus spp. con una presencia en suelo de 19% y 0.6% en raíces.
Se debe mencionar que Rotylenchulus spp. no se encontró en las accesiones TolFla02, Tol- Fla04, TolFla07, ValFla01; ValFla03; ValFla04, ValFla09; ValFla10 y Bavaria, lo que permite sugerirlas como posibles reservas genéticas, con potencial de resistencia a los nematodos identificados en el presente estudio.
Los bajos coeficientes de variación (CV) encontrados (< 35%) muestran una baja dispersión de los datos de poblaciones de nematodos en cada accesión y representación de los géneros en cada una de ellas (Cuadro 3). Los coeficientes de determinación (R2) obtenidos variaron entre 0.70 y 0.99, lo que sugiere una distribución homogénea de los valores en cada accesión en relación con el promedio (n.p.) además de interacción entre la presencia de los diferentes géneros de nematodos con cada accesión (Cuadro 2).
Poblaciones de Meloidogyne spp. y Radopholus similis
Radopholus similis presentó una frecuencia de 61%, con valores entre 73 y 190 individuos/ 100 g de raíces para las accesiones CauFla03 y ValFla08, respectivamente (Cuadro 3). El género Meloidogyne spp. presentó frecuencias de 43 y 39% en suelo y raíces, con valores entre 18 y 180 individuos por muestra (suelo y raíces) en la accesión AntFla03 (Cuadro 3). Así mismo, Meloidogyne spp. no se registró en las accesiones AtlFla01, CalFla02, CauFla01, CauFla03, CauFla05, CunFla02, HuiFla02, HuiFla03, HuiFla06, TolFla01, TolFla02, VaLFla04, VaLFla05, VaLFla06, VaLFla07 y VaLFla08 (Cuadro 3).
El-Borai y Duncan (2005) encontraron que los nematodos reniformes R. reniformis y del nudo radical, M. incognita, M. javanica y Meloidogyne spp. afectan la longevidad de la planta de maracuyá y limitan su producción de frutos con gran daño económico. Así mismo, R. reniformis fue detectado en 84% de los muestreos realizados en las islas Fiji (Oceanía) con densidades de 36,000 nematodos en 200 cm3 de suelo. En Belice y Brasil, R. reniformis se ha hallado asociado con el sistema radicular de maracuyá (Bridge et al., 1996; Sharma et al., 2000).
Sikora y Fernández (2005) observaron que los nematodos formadores de nudos M. incognita, M. javanica, R. reniformis y H. dihysteroides, ocasionan deformaciones en las raíces, debilitan las plantas, producen clorosis y muerte descendente. Las heridas en el sistema radicular favorecen la necrosis por penetración de otros patógenos naturales presentes en el suelo.
La presencia de R. similis (Figura 1) es el primer registro del nematodo barrenador en plantas de maracuyá en Colombia, con una frecuencia de 61% en las 28 accesiones evaluadas. Esta especie se alimenta principalmente de raíces y cormos de banano y plátano, y afecta el crecimiento y desarrollo de estos cultivos, con pérdidas en producción entre 20 y 80% (Guzmán-Piedrahita, 2011). Milne y Keetch (1976) consideran que el maracuyá es un cultivo de rotación en Suráfrica que se utiliza para el manejo de R. similis, el cual no infecta a P. edulis f. edulis (gulupa) y P. edulis f. flavicarpa (maracuyá).
Los nematodos fitoparásitos Tylenchus, Aphelenchoides y Trichodorus se hallaron con una frecuencia de 100%, 71% y 4%, respectivamente. Este último únicamente se vio en la accesión CalFla03 con 60 individuos en las muestras de raíces, lo que contrasta con los resultados de Sánchez et al. (1993), quienes observaron en menores porcentajes Pratylenchus spp., Tylenchorhynchus spp., Aphelenchus spp., Criconemella spp., Hoplotylus spp., y Xiphinema spp. en cultivos de maracuyá en los departamentos del Valle del Cauca, Cauca y Caldas. Las diferencias pueden ser debidas principalmente a la forma de uso del suelo, a los hospedantes presentes antes de establecer el cultivo y a las condiciones ambientales.
Las diferencias entre las poblaciones de nematodos en el Banco de Germoplasma de Maracuyá en relación con los hallazgos en otros estudios se explican por la variabilidad genética existente en el banco, el cual está compuesto por accesiones de diferentes orígenes geográficos del país. Variabilidad representada por accesiones más tolerantes o susceptibles a los nematodos fitoparásitos, que se pueden considerar como un reservorio genético para la selección asistida de genotipos superiores (élite) y que contribuyen a la solución de la problemática con estos microorganismos y a mitigar las pérdidas económicas de los productores. La no presencia (0) de nematodos fitoparásitos en las raíces de algunas accesiones sugiere una aparente tolerancia a estos organismos y pueden considerarse como genotipos superiores.
Esta resistencia genética como estrategia para el manejo de enfermedades se puede evaluar en condiciones de almácigos, con el propósito de comprobar las ventajas de estos materiales.
- Los resultados determinaron la presencia de siete géneros de nematodos fitoparásitos en las 28 accesiones de maracuyá evaluadas, tanto en las muestras de suelo como en raíces. Son nematodos asociados principalmente con especies de los géneros Helicotylenchus spp. y Rotylenchulus spp., con una incidencia entre el 100% y el 75%, respectivamente.
- La presencia y el número de nematodos fitoparásitos dispuestos en el germoplasma estudiado, permiten concluir que hay una variabilidad genética en las accesiones de maracuyá en cuanto a la susceptibilidad o tolerancia a estos organismos. A su vez, la metodología empleada en esta investigación es sugerida para posteriores estudios en la identificación y cuantificación de nematodos en el cultivo de maracuyá.
- El estudio identificó las accesiones Ant- Fla03, CalFla03, CauFla01, CauFla02 y HuiFla06 con tolerancia a uno o dos de los géneros Helicotylenchus spp., Rotylenchulus spp. y Meloidogyne spp. reportados en esta investigación. La aparente tolerancia a nematodos reportada en algunas accesiones es fundamental para procesos de fitomejoramiento en el maracuyá, en la búsqueda de cultivares más tolerantes a estos problemas fitosanitarios que permitan un mejor desarrollo del cultivo y una reducción de los tratamientos químicos para su control.
El primer y segundo autor agradecen al Programa de Maestría en Fitopatología de la Facultad de Ciencias Agropecuarias de la Universidad de Caldas, por facilitar las instalaciones del laboratorio de Fitopatología para los análisis de raíces y suelo. El tercer autor agradece al Centro de Bio-Sistemas de la Universidad Jorge Tadeo, por la coordinación y apoyo del proyecto financiado por el Ministerio de Agricultura y Desarrollo Rural de Colombia – MADR Aprovechamiento de la diversidad del maracuyá, la gulupa y la granadilla para mejorar y diversificar los sistemas de producción en Colombia, y a la empresa Casa Luker por el establecimiento y mantenimiento de la Colección Nacional de Maracuyá durante el desarrollo de esta investigación.
Agrios, G. 2005. Plant Pathology. 5ed. Nueva York. Elsevier Academic Press. 922 p. [ Links ]
Agronet. 2012. Ministerio de Agricultura y Desarrollo Rural de Colombia. Análisis-Estadísticas, Maracuyá. Disponible en: http://www.agronet.gov.co [Fecha revisión: 25 de marzo de 2012] [ Links ]
Araya, M.; Centeno, M.; y Carrillo, W. 1995. Densidad poblacional y frecuencia de los nematodos parásitos de banano (Musa AAA) en nueve cantones de Costa Rica. Corbana 20(43):6 - 11. [ Links ]
Aristizábal, J. 2002. Estimación de la tasa de fijación de carbono en el sistema agroforestal nogal cafetero (Cordia alliodora) - Cacao (Teobroma cacao L.) - Plátano (Musa paradisiaca). Corporación Colombiana de Investigación Agropecuaria (Corpoica) - Casa Luker. Trabajo de Pregrado. Universidad Distrital Francisco José de Caldas. Bogotá D.C. 125 p. [ Links ]
Bridge, J.; Hunt, D. J.; y Hunt, P. 1996. Plant parasitic nematodes of crops in Belize. Nematropica 26:111 – 119. [ Links ]
Castaño, J. 2009. Enfermedades importantes de las pasifloráceas en Colombia. En: Miranda, D.; Fischer, G.; Carranza, C.; Magnitskiy, S.; Piedrahita, W.; y Flórez, L. E. (Eds.). Cultivo, poscosecha y comercialización de las pasiforáceas en Colombia: maracuyá, granadilla, gulupa y curuba. Ruben's Impresores Eds. Bogotá, Colombia. Pp. 223 – 244. [ Links ]
Castillo, J. A. 2004. Variación de la erodabilidad y aplicación de la ecuación universal de pérdida de suelo (USLE) en los Andes colombianos. Tesis Doctoral. Universidad Nacional de Colombia sede Palmira. Palmira, Valle, Colombia. 50 p. [ Links ]
Cia, E.; y Salgado, C. L. 2005. Doenças do algodoeiro (Gossypium spp.). En: Kimati, H.; Amorin, L.; Rezende, A. M.; Bergamin Filho, A.; y Camargo, E. A. (Eds.). Manual de fitopatología. 4. Ed. São Paulo. Agronômica Ceres. Pp. 41 – 52. [ Links ]
Commonwealth Institute of Helminthology, CIH. 1972-1977. Descriptions of Plant-parasitic Nematodes. Commonwealth Agricultural Bureaux. Peter´s Street, St. Albans, Herts., England. Sets 1 - 7. [ Links ]
Degener, O. 1932. Flora Hawaiiensis. Family 344. Hesperomannia lydgatei. Published privately, 2 p. [ Links ]
El-Borai, F. E.; y Duncan, L. W. 2005. Nematode parasites of subtropical and tropical fruit tree crops. En: Luc, M.; Sikora, R. A.; y Bridge, J. (Eds.). Plant parasitic nematodes in subtropical and tropical agriculture. 2nd Edition. Chap. 2. Pp. 478 - 479. [ Links ]
Fischer, G.; Casierra, F.; y Piedrahita, W. 2009. Ecofisiología de las especies pasifloráceas cultivadas en Colombia. En: Miranda, D.; Fischer, G.; Carranza, C.; Magnitskiy, S.; Piedrahita, W.; y Flórez, L. E. (Eds.). Cultivos, poscosecha y comercialización de las pasifloráceas en Colombia: Maracuyá, granadilla, gulupa y curuba. Soc. Col. Cien. Hort. Pp. 45 – 67. [ Links ]
Fischer, I. H.; Bueno, C. J.; Marchi-Garcia, M. J.; y Marques De Almeida, A. 2010. Reação de maracujazeiro- amarelo ao complexo fusariose-nematoidede galha. Acta Sci. Agron. 32(2):223 - 227. [ Links ]
García, M. 2002. Guía técnica cultivo de maracuyá amarillo. Centro Nacional de Tecnología Agropecuaria y Forestal (CENTA). El Salvador. 31 p. [ Links ]
Guerrero-López, E.; y Hoyos-Carvajal, L. 2011. Buenas prácticas agrícolas (BPA) con énfasis en el manejo integrado de plagas y enfermedades de gulupa (Passiflora edulis Sims). Universidad Nacional de Colombia, MADR y Fondo de Fomento Hortifrutícola. 43 p. [ Links ]
Guzmán-Piedrahita, O. A. 2011. El nematodo barrenador (Radopholus similis [Cobb] Thorne) del banano y plátano. Rev. Luna Azul 33:137 - 153. [ Links ]
Hernández, L. M.; Castillo, C. F.; Ocampo, J.; y Wyckhuys, K. 2011. Guía de identificación de las principales plagas y enfermedades del maracuyá, la gulupa y la granadilla. Centro Bio-Sistemas Universidad Jorge Tadeo Lozano, Centro Internacional de Agricultura Tropical (CIAT), Palmira, Colombia. 60 p. [ Links ]
Isaac, M. 2009. Mercados nacionales e internacionales de las frutas pasifloráceas. En: Miranda, D.; Fischer, G.; Carranza, C.; Magnitskiy, S.; Piedrahita, W.; y Flórez, L. E. (Eds.). Cultivos, poscosecha y comercialización de las pasifloráceas en Colombia: maracuyá, granadilla, gulupa y curuba. Soc. Col. Cien. Hort. Pp. 327 – 343. [ Links ]
Jaramillo, J.; Cárdenas, J.; y Orozco, J. 2009. Manual sobre el cultivo del maracuyá (Passiflora edulis) en Colombia. Corporación Colombiana de Investigación Agropecuaria (Corpoica). Palmira, Colombia. 80 p. [ Links ]
Jenkins, W. R. 1964. A rapid centrifugal flotation technique for separating nematodes from soil. Pla. Dis. Rep. 48:692. [ Links ]
Lima, A. De A.; y Cunha, M. A. 2004. Da maracujá: producao e qualidade na passicultura. Cruz de Almas: Embrapa Mandioca e Fruticultura. 113 p. [ Links ]
Lozano, M. 2008. Manual del manejo preventivo de la Secadera (Fusarium sp.) en el cultivo del maracuyá. Corporación Colombiana de Investigación Agropecuaria, CORPOICA, C.I. Nataima. Huila, Colombia. 76 p. [ Links ]
Luc, M.; Sikora, R.; y Bridge, J. 2005. Plant parasitic nematodes in subtropical and tropical agriculture. 2nd. Edition. 871 p. [ Links ]
Mai, W.; Mullin, P.; y Lyon, H. 1996. Plant parasitic nematodes. A pictorical key to genera. Fifth edition. Comstock Publishing Associates. A Division of Cornell University Press. 277 p. [ Links ]
Milne, D. L.; y Keetch, D. P. 1976. Some observations on the host plant relationships of Radopholus similis in Natal. Nematropica 6:13 - 17. [ Links ]
Morton, J. 1967. Yellow passionfruit ideal for Florida home gardens. Proc. Florida State Hortic. Soc. 80:320 - 330. [ Links ]
Ocampo, J.; y Urrea, R. 2012. Recursos genéticos y mejoramiento de la gulupa. En: Ocampo, J. y Wyckhuys, K. (Eds.). Tecnología para el cultivo de la gulupa (Passiflora edulis f. edulis Sims) en Colombia. Centro de Bio-Sistemas Universidad Jorge Tadeo Lozano, Centro Internacional de Agricultura Tropical (CIAT) y Ministerio de Agricultura y Desarrollo Rural (MADR), Bogotá, Colombia. Cap. 3:16 - 22. [ Links ]
Ocampo, J.; Posada, P.; Medina, J.; y Jarvis, A. 2012. Zonificación agroecológica y efecto del cambio climático en el cultivo del maracuyá (Passiflora edulis f. flavicarpa Degener) en Colombia. 58th Annual Meeting of the Interamerican Society for Tropical Horticulture – ISHS y VI Congreso de la Sociedad Peruana de Horticultura. Lima – Perú, del 3 al 6 de noviembre de 2012. Pp 41. [ Links ]
Perry, R.; Moens, M.; y Starr, J. 2009. Root knot nematodes (Cabi). 480 p. [ Links ]
Rodríguez-Kábana, R.; y King, P. S. 1987. La naranjilla y la maracuyá como hospederos de nematodos de la soya. Nematropica 17:171 - 177. [ Links ]
Sánchez, M. Y.; Manyoma, L.; y Varón, F. 1993. Identificación y parasitismo de nematodos asociados con maracuyá (Passiflora edulis Sims). Fitopatología Colombiana 17(1):12 - 20. [ Links ]
SAS INSTITUTE, STAT. 2000. Guide for personal computers. Version 8.1. SAS Inst., Cary, NC, USA. 1028 p. [ Links ]
Sharma, R. D.; Junqueira, N. T. V.; y Gomes, A. C. 2000. Reaction of passionfruit genotypes to the Reniform nematode, Rotylenchulus reniformis. Nematologia Brasileira 25: 211–215. [ Links ]
Siddiqi, R. 2000. Tylenchida: Parasites of plants and insects. CAB International. Londres. 864 p. [ Links ]
Sikora, R. A.; y Fernández, E. 2005. Nematode parasites of vegetables. In: Luc, M.; Sikora, R. A.; y Bridge, J. (Eds.). Plant parasitic nematodes in subtropical and tropical agriculture, CAB International, Wallingford, Reino Unido. Chap. 9:319 - 392. [ Links ]
Suárez, Z.; González, M. S.; Rosales, L. C.; y Tellechea, V. 1993. Alteraciones histológicas en Passiflora edulis f. sp. flavicarpa inducidas por Rotylenchulus reniformis. Fitopatología Venezolana 6:11 - 14. [ Links ]
Suárez, Z.; González, M. S.; y Tellechea, V. 1994. Distribución geográfica y daño causado por Rotylenchulus reniformis en Venezuela. Resúmenes XXVI Reunión Anual de la Organización de Nematólogos de los Trópicos Americanos, Honduras. Pp. 23. [ Links ]
Ulmer, T. 2004. Passiflora. Passions flowers of the world. Portrand, Oregon. Timber Press. 430 p. [ Links ]
Villegas, B.; Ocampo J.; y Castillo, C. 2012. Principales enfermedades en el cultivo de gulupa y su manejo. En: Ocampo, J. y Wyckhuys, K. (Eds.). Tecnología para el cultivo de la gulupa (Passiflora edulis f. edulis Sims) en Colombia. Centro Bio- Sistemas de la Universidad Jorge Tadeo Lozano, Centro Internacional de Agricultura Tropical CIAT y Ministerio de Agricultura y Desarrollo Rural (MADR) Bogotá, Colombia. Cap. 9: 54 - 65. [ Links ]
Yockteng, R.; Coppens, G.; y Souza, T. 2011. Passiflora. In: Chittaranjan Kole (Ed.). Wild crop relatives: genomic and breeding resources. Tropical and Subtropical Fruits. Springer Verlag, Berlin, Heidelberg. Chap. 7:129 - 171. [ Links ]













