Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Agronómica
Print version ISSN 0120-2812
Acta Agron. vol.61 no.4 Palmira Oct./Dec. 2012
1Bióloga, Grupo de investigación BIOPLASMA-UPTC. Escuela de Ciencias Biológicas. Facultad de Ciencias Básicas. Universidad Pedagógica y Tecnológica de Colombia. Tunja, Boyacá, Colombia. 2Bióloga, M.Sc., Docente Departamento Biología y Microbiología, Universidad de Boyacá. Tunja, Boyacá, Colombia. 3Dr. Biología, Profesor Titular Escuela Ciencias Biológicas, Director Grupo BIOPLASMA-UPTC, Universidad Pedagógica y Tecnológica de Colombia. Tunja, Boyacá, Colombia. *Autor para correspondencia: jocpach@gmail.com; †dianapcaro@yahoo.com; ‡sandraer22@hotmail.com; ††leidyrache@yahoo.com
En Colombia los estudios para establecer métodos modernos de propagación y selección de materiales vegetativos de uchuva (Physalis peruviana) son escasos; por tanto, es necesario explorar técnicas alternativas como la aplicación de radiación ionizante, la cual permite ampliar la variabilidad genética, obtener plántulas con características fenotípicas favorables y contribuir al mejoramiento de la productividad. Con el objeto de inducir alteraciones cromosómicas, yemas axilares de P. peruviana cultivadas en medio MS suplementado con 0.1 mg/lt de BA y 0.05 mg/lt de AIB fueron irradiadas con 50, 100, 200 y 300 Grays (Gy) de radiación gamma. El experimento se llevó a cabo utilizando un diseño completamente al azar, con cinco tratamientos, cada uno con 30 unidades experimentales. Después de nueve subcultivos (ciclos de multiplicación de 30 días cada uno), los microtallos regenerados de yemas irradiadas presentaron menor viabilidad que los regenerados de yemas no irradiadas. Las plántulas regeneradas de yemas irradiadas con 100 Gy presentaron mayor porcentaje de enraizamiento, longitud del tallo y número de hojas; la dosis de 300 Gy inhibió el desarrollo de tallos y primordios radicales, aunque los explantes permanecieron viables. En células de ápices radicales tomados de plántulas regeneradas de yemas irradiadas se observaron puentes en anafase y telofase, cromosomas rezagados y cromosomas aislados, siendo mayor la frecuencia de los cromosomas rezagados. El mayor porcentaje de células con alteraciones cromosómicas se cuantificó en ápices radicales de plántulas regeneradas de yemas irradiadas con 200 Gy. En invernadero, 86 – 93.8% de plántulas regeneradas de yemas irradiadas y no irradiadas fueron viables.
Palabra clave: Alteraciones cromosómicas, cultivo in vitro, plántulas, Physalis, radiación gamma, radiación ionizante, uchuva.
In Colombia, studies carried out to establish modern methods for propagation and selection of plant of cape gooseberry (Physalis peruviana) are scarce so, it is necessary to explore alternative techniques such as the application of ionizing radiation, which enables greater genetic variability and to obtain seedlings with phenotypic characteristics that could be beneficial to contribute to improve productivity. To induce chromosomal alterations, axillary buds of P. peruviana with 50, 100, 200 and 300 Gy of gamma radiation were irradiated and were cultured in MS medium supplemented with BA 0.1 mg·L-1 plus IBA 0.05 mg·L-1. The experiment was conducted using a complete random design, five tests each with thirty experimental units were carried out. After nine subcultures (9 multiplication cycles, 30 days each), regenerated shoots of irradiated buds presented smaller viability than the regenerated non irradiated buds. The regenerated plantlets buds irradiated with 100 Gy had higher rooting percentage, shoot length and number of leaves; the dose of 300 Gy inhibited the development of shoots and roots, although the explants remained viable. In cells taken from radical tips of regenerated plantlets of irradiated buds were observed bridges in anaphase and telophase, laggards and isolated chromosomes, being higher the frequency of laggard chromosomes. The higher percentage of cells with chromosomal alterations was quantified in radical tips of regenerated plantlets of buds irradiated with 200 Gy. In greenhouse, 86-93.8% of regenerated plantlets of irradiated or not buds were viable.
Key words: Cape gooseberry, chromosomal alterations, gamma radiation, in vitro culture, ionizing radiation, Physalis, plantlets.
La uchuva (Physalis peruviana L.) ocupa el segundo lugar entre los frutos exportados desde Colombia (Flórez et al., 2000). La aplicación de métodos alternativos de propagación y selección es una opción para mejorar la calidad de los frutos y alcanzar buena aceptación por los consumidores. En las últimas décadas han surgido nuevas técnicas para el estudio y manipulación de materiales vegetales, lo que posibilita el mejoramiento genético de fenotipos que favorecen la producción de frutos de mejor calidad.
La uchuva se propaga por métodos sexual y asexual, siendo el primero el más utilizado; no obstante para la producción de plántulas utilizables en el establecimiento de plantaciones comerciales no es el método más aconsejable, ya que la variabilidad genética de las plantas de origen sexual puede incidir negativamente en caracteres importantes como la productividad (Almanza, 2000).
Las técnicas in vitro se utilizan en programas de producción y ofrecen ventajas para la obtención de mutaciones. En estos programas, células meristemáticas o tejidos y células mitóticamente activas pueden ser propagadas en condiciones in vitro, estableciendo cadenas proliferativas, lo que significa que los microtallos axilares producidos a partir del cultivo de células meristemáticas o yemas son subdivididos en porciones apicales y segmentos nodales que sirven como explantes secundarios para continuar la propagación, con el fin de preparar suficiente cantidad de material que puede ser sometido a tratamientos mutagénicos (Suprasanna et al., 2008). La inducción de mutantes por medio de radiación ionizante es ampliamente propuesta para el mejoramiento de plantas productivas (Lu et al., 2007). Esta radiación produce alteraciones de tipo estructural, fenotípico y de comportamiento en células, tejidos, órganos y plantas completos (Cervantes et al., 1996). Estas mutaciones permiten ampliar la variabilidad genética y facilitan la selección de plantas con características mejoradas, las cuales pueden favorecer la producción de frutos con mejor aceptación.
Los patrones de crecimiento y productividad de las plantas pueden ser fácilmente modificados por agentes mutagénicos (Raghava y Raghava, 1989). Además del descubrimiento de los rayos X y el uso de las radiaciones ionizantes como los rayos gamma y los neutrones, se han establecido metodologías para inducir variaciones útiles en el mejoramiento de cultivos (Fuchs et al., 2002).
La radiación puede inducir inestabilidad genómica en células, la cual es transmitida a su progenie a través de generaciones de replicación celular con efectos genéticos en generaciones posteriores tales como mutaciones y aberraciones cromosómicas (Little, 2006). En este sentido se debe tener en cuenta que la exposición a altas dosis de radiación puede inducir varios eventos mutacionales por célula, con el riesgo creciente de que una mutación favorable sea acompañada por cambios genéticos no deseables (Otahola et al., 2001). Fuchs et al. (2002), Lu et al. (2007) Hung y Johnson (2008), Suprasanna et al. (2008), Yamaguchi et al. (2009) y Rodríguez (2004) realizaron estudios citogenéticos enfocados en la caracterización cariotípica y la inducción de cambios cromosómicos numéricos en P. peruviana y otras especies.
El objetivo de la presente investigación fue inducir cambios morfológicos y citogenéticos con empleo de rayos gamma aplicados a yemas axilares de microtallos de uchuva (P. peruviana) y evaluar los caracteres de interés que pueden favorecer la producción de frutos de mejor calidad.
El trabajo se realizó en el Laboratorio de Cultivo de Tejidos Vegetales, Bioplasma, de la Universidad Pedagógica y Tecnológica de Colombia (UPTC), Tunja.
Selección de material vegetal
En huertos comerciales del municipio de Arcabuco (Boyacá) (5°42'20" N, 73°25'59" O; a una altura de 2739 m.s.n.m., con temperatura media de 15°C y precipitación media de 1781.3 mm), se seleccionaron plantas sanas de uchuva y con buena producción de frutos, de las cuales se tomaron rebrotes basales de 10 cm de longitud que se envolvieron en papel húmedo para transportarlos al laboratorio en bolsas plásticas.
Asepsia superficial de rebrotes
Los rebrotes se dividieron en segmentos nodales, se enjuagaron con agua destilada más Tween 20 (Merck), (0.25 ml/100 ml) durante 5 min y agitación constante. Luego se sumergieron en etanol a 70% durante 15 s y se sumergieron en hipoclorito de sodio (NaOCl) al 1.05% p/v durante 30 min, antes de enjuagarlos tres veces con agua destilada estéril.
De los segmentos nodales asépticos se separaron las yemas axilares y se cultivaron durante 30 días en medio MS (Murashige y Skoog, 1962) complementado con agar (oxoid) 6500 mg/lt, BA (6-bencilaminopurina) 0.1 mg/lt y AIB (Ácido-3-indolbutírico) 0.05 mg/ lt. El pH de los medios se ajustó a 5.6 con NaOH ó HCl 1N y se esterilizaron en autoclave a presión de 1 kg/cm2 y 121 °C durante 20 min. Los cultivos se incubaron en cuarto de crecimiento a 23 ± 1 °C con luz continua (70 - 80 µmol/m2) suministrada por tubos fluorescentes Sylvania de 75 Watt. Una vez se desarrollaron los microtallos, se dividieron en segmentos nodales los cuales se utilizaron para establecimiento de cadenas proliferativas.
Exposición de yemas axilares a rayos gamma
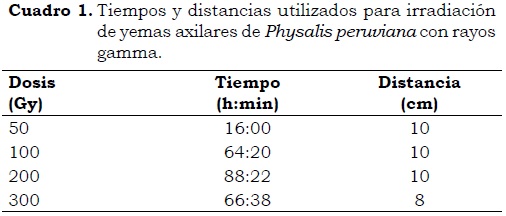
En total se tomaron 150 segmentos caulinares nodales con una yema axilar, procedentes de microtallos mantenidos en cadenas proliferativas que fueron sometidos a diferentes dosis de rayos gamma producidos por una fuente de 60Co ubicada en la UPTC. Las dosis de radiación que se aplicaron a los explantes fueron de 50, 100, 200 y 300 Gy según tiempos y distancias requeridos para la aplicación de los rayos gamma que aparecen en el Cuadro 1. En cada dosis de radiación se expusieron 30 yemas axilares. Durante el proceso de irradiación los explantes se mantuvieron en placas Petri con medio de cultivo MS.
Regeneración de plántulas a partir de yemas irradiadas
Los segmentos nodales con las yemas irradiadas se cultivaron en medio MS durante nueve subcultivos de 30 días cada uno, al término de los cuales los microtallos desarrollados se utilizaron para establecer cadenas proliferativas. Después del primero y noveno subcultivos se realizaron observaciones macro-morfológicas relacionadas con viabilidad, enraizamiento, longitud de tallos, número y forma de hojas en plántulas regeneradas en las cadenas proliferativas de materiales irradiados y no irradiados, además, se tomaron raíces para observación y análisis cromosómico.
Endurecimiento de plántulas
En esta fase, las plántulas regeneradas en las cadenas proliferativas de materiales irradiados y no irradiados, obtenidas después del noveno subcultivo, fueron transferidas a invernadero, previa eliminación con agua corriente del agar adherido a las raíces. Posteriormente las plántulas fueron transferidas a vasos plásticos con sustrato compuesto por suelo, arena y cascarilla de arroz en proporción 2:1:1, respectivamente.
Alteraciones cromosómicas en células de ápices radicales
Las observaciones de cromosomas se desarrollaron siguiendo el protocolo propuesto por Rodríguez (2004) y modificado por Díaz et al. (2008). La verificación de la presencia de alteraciones cromosómicas se realizó en ápices radicales de plántulas provenientes de yemas irradiadas y no irradiadas del noveno subcultivo (270 días después de irradiadas las yemas). Para cada observación en cada tratamiento se recolectaron entre 2 y 4 raíces de 1 a 3 cm, entre las 14:00 y 16:00 horas y de cada una de ellas se separaron los ápices que medían 4 - 5 mm.
Los ápices radicales aislados se enjuagaron con agua destilada y se sumergieron en una solución de colchicina a 0.5% durante 5 h a 4 °C. Después se enjuagaron con agua destilada e inmediatamente se sumergieron en solución Farmer (etanol 96%:ácido acético glacial, 3:1) durante 24 h a 4 °C. Los ápices radicales que no se utilizaron inmediatamente fueron conservados durante 30 días en etanol a 70% y 4 °C.
Posteriormente, los ápices radicales fueron sometidos a la acción de una mezcla enzimática compuesta por celulasa (3%), pectinasa (1.5%) y macerozima (1.0%) mantenida en tubos de ensayo en condiciones de oscuridad, a 37 °C durante 25 min en baño maría. Para interrumpir la acción enzimática, los ápices fueron enjuagados con agua destilada antes de separar la zona meristemática (1 - 2 mm) que fue colocada en un portaobjeto con la adición de 2 gotas de orceina acética al 2% durante 25 min.
Los ápices meristemáticos coloreados fueron flameados ligeramente, se colocó un cubreobjetos sobre ellos y con una barra de goma se propinó un golpe seco sobre los tejidos; luego, con ayuda de papel absorbente, se tomó la placa entre el pulgar y el índice para ejercer presión sin deslizar las láminas y finalmente se selló con barniz transparente. Para seleccionar placas con buena dispersión celular, la observación se hizo en microscopio con objetivo 25X y las observaciones posteriores para análisis de cromosomas con objetivos de 50X y 100X. Para los registros fotográficos se utilizó un microscopio Carl Zeiss, Jena Jenamedz, con objetivos de 50X y 100X, proyectivos de 16X y 20X y una cámara digital Kodak easy c533 de 5.0 mega píxeles.
Análisis estadístico
En total se realizarón cinco tratamientos (0, 50, 100, 200, 300 Gy), cada uno con 30 unidades experimentales. Los datos de enraizamiento in vitro se expresan como porcentajes de explantes enraizados después del primero y el noveno subcultivos. Los datos de hojas/ explante y longitud de tallo fueron analizados mediante Andeva, con un nivel de confiabilidad de 95%. Para los factores que resultaron estadísticamente significativos se realizó la prueba DHS (diferencia honestamente significativa). Los datos fueron procesados con el paquete estadístico Statgraphics Plus versión 2.0 (1996). La longitud del tallo se midió sobre papel milimetrado estéril. Para identificar la presencia de alteraciones cromosómicas se observaron en total 100 placas; cada una contenía una raíz donde se observaron 10 campos. Los datos se expresaron como porcentaje total de células que presentaron alteraciones y de células que revelaron una alteración específica con respecto al número de células en división por tratamiento.
Asepsia superficial de rebrotes
El protocolo utilizado para la asepsia de los segmentos nodales procedentes de rebrotes tomados de plántulas en campo permitió recuperar un 73% de explantes asépticos, con eliminación de contaminantes superficiales, lo que permitió la propagación in vitro de los segmentos nodales y posterior obtención de las yemas que fueron irradiadas. Protocolos de asepsia similares para establecimiento in vitro de cultivos fueron utilizados en especies del género Physalis, utilizando NaOCl en P.peruviana (Díaz et al., 2008) y en P. ixocarpa (Ramírez y Ochoa, 1991; Contreras y Almeida, 2003) y cloruro de mercurio (HgCl2) en P. pubescens (Rao et al., 2004) como agente desinfectante.
El cultivo en medio MS de yemas axilares, tomadas de los segmentos nodales de rebrotes de plantas de campo, facilitó el desarrollo de los microtallos utilizados para el establecimiento de cadenas proliferativas, con subcultivos cada 30 días. Díaz et al. (2008) encontraron un desarrollo favorable de yemas de P. peruviana cultivadas en medio MS con BA y AIB.
Regeneración de plántulas a partir de yemas irradiadas
A pesar de las precauciones de asepsia mantenidas durante el cultivo, traslado y exposición de los explantes a la fuente de 60Co, algunas de las yemas irradiadas resultaron contaminadas con hongos y/o bacterias; además de la contaminación, la exposición a la radiación contribuyó a la muerte de algunas yemas. Las yemas irradiadas con 300 Gy no desarrollaron tallos ni primordios radicales y después de tres subcultivos murieron. Según Fuchs et al. (2002) los rayos gamma, por ser un tipo de radiación ionizante, tienen una alta capacidad de penetración y su acción letal en las células se mide como pérdida de la actividad mitótica, que ocurre a causa de las aberraciones cromosomales. En este sentido, uno de los más importantes y difíciles aspectos de radio-protección es establecer límites entre dosis de radiación altas y bajas (Zaka et al., 2002). Desde luego, el establecimiento de un límite es un tema controversial debido a que depende en gran medida de la sensibilidad de cada especie, individuo y aun del tipo de tejido o célula. Raghava y Raghava (1989) consideran que dosis altas de radiación inhiben la síntesis de reguladores de crecimiento. La reducción en la supervivencia de explantes al aumentar la dosis de radiación fue de la forma siguiente: con 50 Gy la viabilidad fue 60%, con 100 Gy 73%, con 200 Gy 10% y con 300 Gy 0%, observándose que en dosis bajas (50 Gy) y altas (200 y 300 Gy) disminuyó la viabilidad. La baja respuesta de regeneración a altas dosis de radiación puede ser atribuida al efecto tóxico de la radiación gamma sobre las células embriogénicas u organogénicas y a la pérdida de competitividad de esas células y sus progenies (Suprasanna et al., 2008). Los resultados obtenidos concuerdan en parte con lo observado en Narcissus tazetta var. chinensis (Lu et al., 2007), Wasabia japonica (Hung y Johnson, 2008) y Chrysanthemum morifolium (Yamaguchi et al., 2009), en los cuales se encontró que dosis de radiación altas pueden causar altas frecuencias de mutaciones pero baja proporción de regenerantes en cultivo in vitro. Además, los autores establecieron que la probabilidad de la reducción de la supervivencia se debe a que los callos y tejidos in vitro son mucho más sensibles a los tratamientos con radiación y por tanto, requieren dosis muy bajas (5-15 Gy) comparado con la dosis requerida para semillas o bulbos (Lu et al., 2007).
Las plántulas regeneradas de yemas irradiadas y no irradiadas presentaron diferentes respuestas rizogénicas. Durante el primer subcultivo, se observó respuesta rizogénica en dos tratamientos –microtallos desarrollados a partir de yemas no irradiadas e irradiadas con 50 Gy– encontrando 65% y 3.3% de explantes con desarrollo radical, respectivamente. En el noveno subcultivo se observaron respuestas rizogénicas en todos los tratamientos, siendo mayor en plántulas regeneradas de yemas expuestas a 50 Gy y de yemas no irradiadas (100 y 96% respectivamente) (Cuadro 2). En este mismo subcultivo se observaron diferencias (P < 0.05) en el número de hojas presentes en plántulas regeneradas de yemas irradiadas y no irradiadas, con un promedio de 3.7 hojas/explante en el tratamiento de 100 Gy (Cuadro 2).
En todos los subcultivos las plántulas regeneradas de yemas irradiadas mostraron tallos más cortos (1.8 - 2.2 cm) en comparación con los de plántulas no irradiadas, no obstante en el noveno subcultivo las plántulas presentaron tallos de longitudes diferentes en un rango 2.99 - 7.8 cm (Cuadro 2). Resultados similares a los encontrados en este estudio se hallaron en Cicer (Toker et al., 2005), Wasabia japonica (Hung y Johnson, 2008) y caña de azúcar (Suprasanna et al., 2008); sin embargo, contrastan con los de Rekha y Langer (2007) en Artemisia pallens quienes registraron menor longitud de tallos en los controles que en plantas irradiadas. Es posible que el aumento en la longitud de los microtallos de plántulas inducido por bajas dosis de rayos gamma (50 y 100 Gy) sea el resultado del efecto promotor de estas dosis, que inducen la síntesis de auxinas y otros reguladores y consecuentemente activan puntos dormantes de crecimiento (Otahola, 1999; Wi et al., 2007).
Las diferencias en los porcentajes de enraizamiento entre los tratamientos, así como entre el promedio de hojas/explante y la longitud del tallo al finalizar el noveno subcultivo, se deben a la inhibición o estímulo de los procesos fisiológicos y bioquímicos de la radiación ionizante, lo cual depende de la dosis aplicada (Raghava y Raghava, 1990).
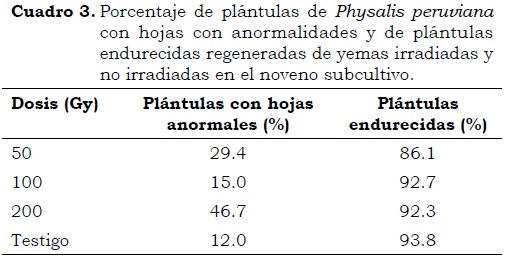
Las plántulas regeneradas de yemas irradiadas y no irradiadas presentaron hojas con formas ovalada, alargada, acorazonada deforme y fusionada, y bordes lisos y ondulados (Foto 1). El mayor porcentaje (47%) de plántulas con hojas anormales se observó en el tratamiento con 200 Gy, mientras que en los tratamientos con 50 y 100 Gy y sin irradiar, el porcentaje de plántulas con hojas anormales fue de 29%, 15% y 12%, respectivamente (Cuadro 3). Hung y Johnson (2008) encontraron variaciones similares de forma y tamaño en hojas irradiadas de Wasabia japonica.
Endurecimiento de plántulas
Después de 90 días del inicio del ensayo se encontraron entre 86.18% y 92.3% de plántulas endurecidas, procedentes de yemas irradiadas y 93.8% de plántulas de yemas no irradiadas (Cuadro 3). Estos valores coinciden con los de Hung y Johnson (2008), quienes en invernadero encontraron en W. japonica entre 72% y 92% de endurecimiento en plantas de esta especie sometidas a radiación gamma.
Alteraciones cromosómicas en células de ápices radicales
Algunas células de los ápices meristemáticos presentaron alteraciones cromosómicas en diferentes fases del ciclo, principalmente en anafase, puentes y cromosomas rezagados (Foto 2a y Foto 2c); en telofase, puentes (Foto 2b) y en metafase y anafase cromosomas aislados (Foto 2d). Las alteraciones cromosómicas durante la anafase indican que la radiación influye especialmente en la función del huso mitótico. Los puentes generalmente son debidos a la formación de cromosomas dicéntricos originados por intercambio entre cromosomas después del rompimiento de la doble hebra de ADN (Zaka et al., 2002). Según Little (2006) el rompimiento de dicha hebra se considera como una lesión característica, responsable de los efectos biológicos de la radiación ionizante. En los estudios de Zaka et al. (2002) con P. sativum se encontraron puentes y cromosomas rezagados durante la anafase y la telofase.
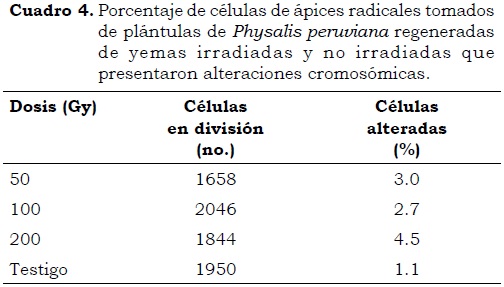
En el Cuadro 4 se incluyen los porcentajes de células que mostraron alteraciones con respecto al número de células en división, encontrando el mayor porcentaje (4.5%) de células alteradas en las procedentes del tratamiento con 200 Gy y el menor (2.7%) en el tratamiento con 100 Gy. Esto demuestra que a medida que aumenta la dosis de radiación crece la presencia de células con alteraciones hasta cierta dosis, en la cual se observa un efecto letal en las células; en este estudio el efecto letal se presentó con dosis de 300 Gy. resultados similares fueron obtenidos por Zaka et al. (2002) quienes establecieron una relación lineal para las variables dosis-efecto que muestra un incremento en la presencia de aberraciones cromosómicas, de acuerdo con el aumento en la dosis de radiación. Los bajos porcentajes (2.7-4.5) de células alteradas observados en este trabajo con respecto a los obtenidos en el estudio de Zaka et al. (2002) (15% en dosis de 2 Gy y 20% en dosis de 3-10 Gy), posiblemente fueron debidos a la diferencia en dosis de radiación utilizadas, a la sensibilidad de cada especie, al tipo de tejidos y/o células de cada tejido sometidas a irradiación. Además, es posible que sólo una pequeña proporción de aberraciones cromosómicas durante las primeras mitosis hayan aparecido en las células irradiadas que han conservado su habilidad de división, mientras que la restante se encuentra integrada en el genoma y se expresa gradualmente durante las siguientes divisiones celulares (Zaka et al., 2002).
Dentro de los tratamientos, las alteraciones cromosómicas más frecuentes (1.0, 1.5 y 0.2%) (Cuadro 5) fueron cuantificadas en células de yemas tratadas con dosis de 200 Gy, donde se presentaron puentes tanto en anafase como en telofase y cromosomas aislados, respectivamente. La frecuencia más alta (1.9%) de cromosomas rezagados se encontró en las células de yemas tratadas con 100 Gy. Por otro lado, se cuantificaron frecuencias similares de alteraciones cromosómicas en yemas no irradiadas y en dosis de 100 Gy para puentes en anafase (0.4%), en 50 Gy para puentes en telofase (0.2%) y en 50 y 100 Gy para cromosomas aislados (0.1%). Fuchs et al. (2002) consideran que cuando se aplican agentes mutagénicos físicos o químicos a material de propagación sexual o asexual, se observa una relación directa entre la dosis y la tasa de mutación, pero también es notable una relación similar entre la dosis y el daño celular. Esto concuerda con los resultados obtenidos en el presente trabajo, ya que se evidenció una relación similar o directamente proporcional, así, a mayor dosis de irradiación mayor daño celular, inclusive la dosis de 300 Gy causó muerte celular. En este sentido, Otahola et al. (2001) indican que en exposiciones crecientes a radiación gamma, la frecuencia de mutaciones generalmente aumenta y la sobrevivencia disminuye. Según Kovács y Keresztes (2002) cuando la radiación ionizante es absorbida por materiales biológicos, existe la posibilidad de que ésta actúe directamente sobre puntos específicos en la célula; así mismo, consideran que la radiación puede interactuar con átomos o moléculas en la célula, particularmente agua, produciendo radicales libres que pueden difundirse y dañar componentes importantes de la misma célula.
En general, en células de yemas no irradiadas las frecuencias de las alteraciones fueron bajas con respecto a las cuantificadas en células procedentes de yemas irradiadas (Cuadro 5 y Foto 2). La presencia de alteraciones en células procedentes de materiales no irradiados podría ser considerada como un efecto de mutación espontánea. Según Poehlman y Allen (2003) no existe una diferencia clara entre las mutaciones espontáneas y las inducidas; lo que parece ser una mutación espontánea podría ser una mutación inducida, ya que todas las plantas que existen en la naturaleza están sujetas a bajas dosis de radiación natural.
Como observación general, los resultados obtenidos en este estudio indican que los cromosomas rezagados fue la alteración que se presentó con mayor frecuencia en todos los tratamientos, mientras que los cromosomas aislados fue la alteración que presentó la menor frecuencia (Cuadro 5).
- Con la dosis de radiación de 100 Gy se obtuvo el mayor porcentaje de viabilidad de yemas, enraizamiento de microtallos, cantidad de hojas por explante, longitud de tallos, porcentaje de endurecimiento y de cromosomas rezagados en Physalis peruviana.
- Dosis de radiación entre 100 y 200 Gy son adecuadas para evaluación en futuras investigaciones, ya que a medida que aumenta la radiación, crece la frecuencia de alteraciones presentes en las células expuestas y disminuyen la viabilidad, el enraizamiento, la cantidad de hojas por explante, la longitud de tallos y el endurecimiento de las plántulas regeneradas.
- En células de ápices radicales de regenerantes de yemas irradiadas, se observaron alteraciones cromosómicas tales como puentes en anafase y telofase, cromosomas aislados, y cromosomas rezagados, siendo estos últimos los de mayor frecuencia.
Los autores de este trabajo agradecen a la Universidad Pedagógica y Tecnológica de Colombia, a los integrantes del Grupo de Investigación Bioplasma-UPTC por su valiosa y continua colaboración, y a los evaluadores del trabajo.
Almanza, P. J. 2000. Propagación. En: Flórez, R. V.; Fischer, G. y Sora R., A. (eds.). Producción, poscosecha y exportación de la uchuva (Physalis peruviana L.). Primera edición. Universidad Nacional de Colombia, Unibiblos, Bogotá. p. 27 - 40. [ Links ]
Cervantes, L.; Báez, J.; y Fernández, R. 1996. Efectos de radiación gamma en plantas de Diantus sp. propagadas por cultivo in vitro. Rev Cien. Des. 2 (3):46 - 54. [ Links ]
Contreras, I. y Almeida, J. 2003. Micropropagación del tomatillo (Physalis ixocarpa L.). Rev. Fac. Farm. 45(1):61 - 64. [ Links ]
Díaz, D. E.; González, D. C.; Rache, L. Y.; y Pacheco, J. 2008. Efecto citogenético de la colchicina sobre yemas vegetativas de Physalis peruviana L. Prospec Cient. 4:27 - 40. [ Links ]
Flórez, V. J.; Fischer, G.; y Sora, A. D. (eds.). 2000. Producción, poscosecha y exportación de la Uchuva (Physalis peruviana L.). Bogotá. Primera edición. Universidad Nacional de Colombia, Unibiblos. 175 p. [ Links ]
Fuchs, M.; González, V.; Castroni, S.; Díaz, E.; y Castro, L. 2002. Efecto de la radiación gamma sobre la diferenciación de plantas de caña de azúcar a partir de callos. Agron. Trop. 52 (3):311 - 323. [ Links ]
Hung, C. D. y Johnson, K. 2008. Effects of ionizing radiation on the growth and allyl isothiocyanate accumulation of Wasabia japonica in vitro and ex vitro. En: Vitro Cell Develop. Biol. - Plant. 44:51 - 58. [ Links ]
Kovács, E. y Keresztes, A. 2002. Effect of gamma and UV-B/C radiation on plant cells. Micron. 33:199 - 210. [ Links ]
Little, J. 2006. Cellular radiation effects and the bystander response. Mut. Res. 597:113 - 118. [ Links ]
Lu, G.; Zhang, X.; Zou, Y.; Zou, Q.; Xiang, X.; y Cao, J. 2007. Effect of radiation on regeneration of Chinese narcissus and analysis of genetic variation with AFLP and RAPD markers. Plant Cell Tiss Organ. Cult. 88:319 - 327. [ Links ]
Murashige, T. y Skoog, F. 1962. A revised medium for rapid growth and bioassays with tobacco tissue cultures. Physiol Plant. 15:473 - 493. [ Links ]
Otahola, G. V. 1999. Radiosesibilidad de las semillas y diferentes tipos de explantes en cultivo in vitro de parchita (Passiflora edulis f. flavicarpa Deg.) a radiaciones gamma. Tesis Magíster. Centro de Estudios de Posgrado del núcleo Monagas, Venezuela. 155 p. [ Links ]
Otahola, G. V.; Aray, M.; y Antoima, Y. 2001. Inducción de mutantes para el color de la flor en crisantemos (Dendranthema grandiflora (Ram.) Tzvelev) mediante radiaciones gamma. Rev UDO Agríc. 1(1):56 - 63. [ Links ]
Poehlman, J. y Allen, D. 2003. Mejoramiento genético de las cosechas. México, D.F. Segunda Edición. Editorial Limusa S.A. 511 p. [ Links ]
Raghava, R. P. y Raghava, N. 1989. Effects of gamma irradiation on fresh and dry weights of plant parts in Physalis L. Geobios. 16:261 - 264. [ Links ]
Raghava, R. P. y Raghava, N. 1990. Carotenoid content of husk tomato under the influence or growth regulators and gamma rays. Indian J. Plant Physiol. 33(1):87 - 89. [ Links ]
Ramírez, M. R. y Ochoa A. N. 1991. Adventitious shoot formation and plant regeneration from tissues of tomatillo (Physalis ixocarpa Brot.). Plant Cell Tiss. Organ. Cult. 25:185 - 188. [ Links ]
Rao, Y. V.; Ravi, A.; Lakshmi, T. V. R.; y Raja, K. G. 2004. Plant regeneration in Physalis pubescens L. and its induced mutant. Plant Tiss. Cult. 14 (1):9 - 15. [ Links ]
Rekha, K. y Langer, A. 2007. Induction and assessment of morpho-biochemical mutants in Artemisia pallens Bess. Genet. Resour. Crop Evol. 54:437 - 443. [ Links ]
Rodríguez, N. 2004. Estudio citogenético en Physalis peruviana L.: Uchuva (Solanaceae). Bogotá. Trabajo de grado (Biólogo). Universidad Nacional de Colombia. Sede Bogotá. Bogotá, Colombia. 78 p. [ Links ]
Statgraphics Plus for windows. 1996. Manugistics, Inc, Rockville, MD. Version 2 [ Links ]
Suprasanna, P.; Rupali, C.; Desai, N. S.; y Bapat, V. A. 2008. Partial desiccation augments plant regeneration from irradiated embryogenic cultures of sugarcane. Plant Cell Tiss. Organ Cult. 92:101 - 105. [ Links ]
Toker, C.; Uzun, B.; Canci, H.; y Ceylan, F. O. 2005. Effects of gamma irradiation on the shoot length of Cicer seeds. Radiat. Phys. Chem. 73:365 - 367. [ Links ]
Wi, S. G.; Chung, B. Y.; Kim, J. S.; Kim, J. H.; Baek, M. H.; Lee, J. W.; y Kim, Y. S. 2007. Effects of gamma irradiation on morphological changes and biological responses in plants. Micron. 38:553 - 564. [ Links ]
Yamaguchi, H.; Shimizu, A.; Hase, Y.; Degi, K.; Tanaka, A.; y Morishita, T. 2009. Mutation induction with ion beam irradiation of lateral buds of chrysanthemum and analysis of chimeric structure of induced mutants. Euphytica 165:97 - 103. [ Links ]
Zaka, R.; Chenal, C.; y Misset, M. T. 2002. Study of external low irradiation dose effects on induction of chromosome aberrations in Pisum sativum root tip meristem. Mutat. Res. 517:87 - 99. [ Links ]













