Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Agronómica
Print version ISSN 0120-2812
Acta Agron. vol.63 no.2 Palmira Apr./June 2014
https://doi.org/10.15446/acag.v63n2.36956
http://dx.doi.org/10.15446/acag.v63n2.36956
Agronomía
Efecto de la aplicación de roca fosfórica y la inoculación con bacterias solubilizadoras de fosfatos sobre el crecimiento del ají (Capsicum annum L.)
Effect of rock phosphate application and inoculation with phosphate solubilizing bacteria on growth of pepper (Capsicum annum L.)
Carlos Patiño Torres1*, Marina Sánchez de Prager2
1Departamento de Suelos y Aguas Facultad de Ingeniería Agronómica, Universidad del Tolima; 2Facultad de Ciencias Agropecuarias, Universidad Nacional de Colombia sede Palmira. *Autor para correspondencia: cpatinot@yahoo.com
Rec.: 31.01.2013 Acep.: 11.12.2013
Resumen
La utilización de roca fosfórica para la fertilización de los cultivos tropicales es una práctica eficaz y sostenible,cuyos efectos positivos sobre las plantas pueden aumentarse a través de su inoculación con microorganismos promotores del crecimiento vegetal. Para evaluar esta hipótesis, se estudió en invernadero el efecto de la fertilización con roca fosfórica en plantas de ají (Capsicum annum L.) variedad Cayena, inoculadas y sin inocular, con dos aislamientos bacterianos solubilizadores de fosfato (Burkholderia ambifaria y B. lata), utilizando como sustrato un suelo ácido altamente deficiente en fósforo, sobre variables asociadas con el crecimiento de las plantas. Los ensayos mostraron efecto significativo de la roca fosfórica (RF) sola y/o en conjunto con los aislamientos inoculados. La bioinoculación permitió disminuir la RF, a la mitad (12 g/unidad experimental) de la dosis más adecuada, sin afectar estadísticamente la media de las variables analizadas, igualmente, los contenidos de fósforo (15P) en los tejidos de las plantas inoculadas con las bacterias fueron superiores comparados con el de aquellas no inoculadas.
Palabras clave: Ají capsicum, biofertilizantes, biosolubilización, roca fosfórica.
Abstract
The use of phosphate rock for fertilization of tropical crops is an effective and sustainable practice, whose positive effects on plants can be increased by inoculation with plant growth promoting microorganisms. To test this hypothesis, the effect of greenhouse fertilization with rock phosphate in pepper plants (Capsicum annum L.) variety Cayenne, inoculated and uninoculated with two phosphate solubilizing bacterial isolates (Burkholderia ambifaria and B. lata), using a highly acidic and phosphorus deficient soil, on several variables associated with the growth of plants were studied. Greenhouse tests showed the significant effect of phosphate rock (PR) alone and / or together with the inoculated isolates. The RF bioinoculación allowed decrease to half (12 g / experimental unit) of the appropriate dose, without affecting the means of the variables, equally, the contents of P in the plant tissues inoculated with bacteria were higher compared with those not inoculated.
Key words: Biofertilizers, biosolubilization, capsicum ,phosphate rock.
Introducción
El alcanzar un nivel de producción agrícola adecuado para satisfacer la creciente demanda mundial de alimentos depende, en buena medida, de la aplicación racional de fertilizantes sintéticos a los cultivos, principalmente nitrogenados y fosfóricos (Lal, 2009; Fageria, 2009; FAO, 2004); no obstante en el caso de estos últimos, varios estudios prevén un escenario de escasez inminente a corto, mediano (Cordell et al., 2009; Gilbert, 2009) o largo plazo (Van Vuuren et al., 2010), situación que hace urgente proponer alternativas de fertilización fosfórica, especialmente en los países importadores de fertilizantes como Colombia. En este sentido, la fertilización directa con roca fosfórica (RF), sola o combinada con microorganismos solubilizadores de fósforo, se ha propuesto como una alternativa especialmente adecuada para los ambientes del trópico (FAO, 2004).
En el caso de los suelos tropicales existen tres condiciones que hacen ventajosa la utilización de la roca fosfórica para la fertilización de los cultivos: (1) la tasa de disolución de las rocas y minerales, y la reacción entre las superficies minerales y la solución del suelo, se incrementa bajo regímenes de alta humedad y altas temperaturas, prevalentes en el trópico; (2) el efecto positivo de la fertilización con rocas y minerales es mayor en suelos deficientes en nutrientes; y (3) las condiciones de alta acidez de un alto porcentaje de los suelos tropicales favorecen la solubilización de estas rocas (Edwards et al., 2010).
Como respaldo a su uso, existe considerable información sobre el empleo de RF para aplicación directa en el suelo (Rajan et al., 2006) o sobre técnicas de modificación de la RF antes de su aplicación directa en campo (FAO, 2004; Abouzeid, 2007). Las respuestas agronómicas varían desde efectos casi nulos, a efectos comparables con los producidos por superfosfato triple (Chien y Menon, 1995). Tal diversidad de respuesta es debida a varios factores que influyen en la efectividad agronómica de la RF, que van desde su manejo hasta factores edáficos y relacionados con la especie vegetal (Edwards et al., 2010).
Para solucionar los problemas de baja efectividad de la RF, debida a su lenta y baja solubilidad, se han diseñado varias estrategias para incrementar los niveles de solubilización, que incluyen entre otras: (1) modificaciones físicas como pulverización y activación mecánica (Abouzeid, 2010); (2) modificación fisicoquímica como fusión y calcinación (Abouzeid, 2010); (3) modificaciones químicas como acidulación, acidulación parcial, adición de azufre, mezclado y granulación (Rajan y Watkinson, 1992; Rajan y Warwaha, 1993); y (4) modificaciones biológicas como fosfo-compostaje, adición de desechos frescos, biosolubilización, fitoextracción e inoculación con micorrizas (FAO, 2004; Nziguheba, 2007; Agyin-Birikorang et al., 2007; Biswas y Narayanasamy, 2007).
La biosolubilización o aplicación conjunta de roca fosfórica con microorganismos que solubilizan el fosfato insoluble contenido en ella es una técnica que tiene varias ventajas, por lo que ha empezado a ser evaluada con interés. Esta técnica es efectiva, bien sea que se utilicen hongos (Singh y Reddy, 2011) o bacterias (Khan et al., 2013) como microorganismos solubilizadores de fosfato (MSF). Existen dos aproximaciones básicas de biosolubilización: en la primera, la RF se inocula directamente con MSF, los cuales facilitan la solubilización del fósforo contenido en ella; y la mezcla resultante es aplicada directamente en campo como fertilizante; en la segunda, los MSF se inoculan bien sea sobre las semillas o sobre el sustrato de siembra, previa aplicación de la RF en el suelo (Arcand y Schneider, 2006; Ivanova et al., 2006). Así se utilicen hongos o bacterias como MSF, los mecanismos involucrados en los procesos de solubilización del P insoluble contenido en la RF pueden incluir la producción de ácidos orgánicos, la acidificación del sustrato por excreción de protones y/o la producción de ácidos inorgánicos (Khan et al. 2013).
Entre las bacterias solubilizadoras de fosfatos (BSF) utilizadas en la mayoría de los ensayos de biosolubilización se destacan Pseudomonas, Bacillus, Rhizobium, Burkholderia, Pantoea,Achromobacter, Agrobacterium, Microccocus, Aereobacter, Flavobacterium, Enterobacter, Klebsiella, Rhodobacter, Arthrobacter, Serratia y Erwinia (Rodríguez y Fraga, 1999); mientras que entre los hongos se han reportado principalmente Aspergillus, Penicillium, Trichoderma y levaduras (Khan et al., 2010; Whitelaw, 2000). El presente estudio se efectuó con el objetivo de evaluar el efecto de la roca fosfórica, aplicada sola o en combinación con bacterias solubilizadoras de fosfato nativas, sobre varios parámetros de crecimiento de ají (Capsicum annum) con la finalidad de establecer potenciales programas de biofertilización en el cultivo.
Materiales y métodos
Inoculantes bacterianos
Se utilizaron como bioinoculantes las cepas Burkholderia ambifaria UNBS7 y B. lata, previamente aisladas de la rizosfera de plantas de chontaduro, las cuales en ensayos previos in vitro mostraron una efectiva capacidad solubilizadora de fosfatos (Patiño Torres y Prager, 2010). Los procedimientos de aislamiento y purificación de las cepas se describen en detalle en Patiño y Sánchez (2010). Para la multiplicación del inóculo, cada una de las cepas se sembró con un asa, en 75 ml de medio de cultivo líquido Pikovskaya (Patiño Torres y Prager, 2010), el cual fue colocado en agitación durante 48 h a 160 r.p.m., en condiciones adecuadas de luminosidad y temperatura ambientales (≈ 23 °C).
Determinación de actividad nitrogenasa
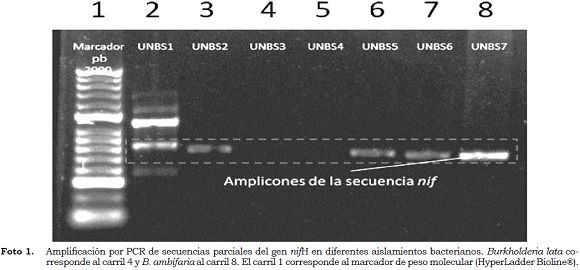
Debido a que algunos miembros del género Burkholderia presentan actividad diazotrófica, se evaluó por PCR la presencia de genes nif en el genoma de las cepas utilizadas. Para el aislamiento y purificación del ADN genómico de los aislados se utilizó el Wizard® Genomic DNA Purification Kit (Promega, USA), utilizando los protocolos sugeridos por el fabricante. Los detalles y condiciones para la amplificación de las secuencias nif fueron las siguientes: se usaron los cebadores nifH F y nifH R (5'- ACCCGCCTGATCCTGCACGCCAAGG- 3' y 5'-ACGATGTAGATTTCCTGGGCCTTGTT- 3', respectivamente) en un termociclador Biorad® modelo C100, se utilizó un primer paso de desnaturalización a 94 °C por 5 min, seguido por 30 ciclos de amplificación (desnaturalización a 94 °C por 45 s, alineación a 55 °C por 45 s, extensión a 72 °C por 45 s, y un paso final de elongación a 72 °C por 5 min); los amplicones fueron entonces mantenidos por 5 min a 4 °C. Los productos amplificados se corrieron luego en un gel de agarosa a 0.8%, por 60 min y 75 v, en una cámara Bio Rad Wide Mini-Sub Cell GT. Para las reacciones de PCR se utilizó el kit comercial Go Taq Green Master Mix (Promega) y las bandas electroforéticas se analizaron en un equipo Molecular Imager® Gel DocTM XR System (Biorad®).
Ensayos de inoculación en invernadero
Para evaluar el efecto de la fertilización con RF (fosforita 30P: 30% P2O5; 40% CaO; solubilidad en citrato de amonio neutro 3.1%) y la inoculación con las BSF sobre varios parámetros de crecimiento de plantas de ají se establecieron ocho tratamientos (Cuadro 1). Las plantas fueron establecidas en materas que contenían como sustrato 3.5 kg de suelo ácido no estéril altamente deficiente en P, pH = 4.76, MO (g/kg) = 87.59, PBray-II (mg/kg) = 3.97, K (cmol/kg) = 0.21, Ca (cmol/kg) = 2.87, Mg (cm/kg) = 4.76, Al (cmol/kg) = 1.46, CIC (cmol/kg) = 25.9, S (mg/kg) = 39.2, B (mg/ kg) = 0.78, Fe (mg/kg) = 36.34, Mn (mg/kg) = 23.32, Cu (mg/kg) = 0.81, y Zn (mg/kg) = 2.12. Las dosis de RF aplicadas fueron 12 y 24 g/unidad experimental y se instalaron en función de los requerimientos del cultivo, siendo 24 g la cantidad más adecuada. Las cepas evaluadas se inocularon sobre las semillas de ají variedad Cayena, para lo cual se sumergieron 50 semillas en un Erlenmeyer con 75 ml de cultivo microbiano líquido por 24 h y agitación a 120 r.p.m., que fue obtenido durante la fase de multiplicación de inóculo. Se partió del principio que las células microbianas formarían una biopelícula sobre la superficie de las semillas para favorecer los procesos de colonización de las raíces (Yaryura et al., 2008).
Una vez inoculadas, se sembraron dos semillas por unidad experimental consistente en materas plásticas con contenido de suelo no estéril. Quince días después de aplicado el tratamiento, se eliminó una de las plántulas en cada matera. El cultivo fue monitoreado constantemente y con aplicación de riegos periódicos para mantener el suelo a capacidad de campo. Las variables de crecimiento analizadas fueron, peso fresco total y de raíces, relación peso fresco raíz/peso fresco tallo, materia seca total, materia seca del tallo, área foliar y fósforo total en tejidos. El registro de los valores de las variables analizadas se hizo 68 días después de la siembra. Los tratamientos se dispusieron en un arreglo unifactorial, y en invernadero, con un diseño completamente aleatorio. Los datos se sometieron a análisis de varianza utilizando el software IBM SPSS v19. La diferencia entre medias se evaluó con la prueba de Duncan (α = 0.05), debido a su mayor poder en relación con la prueba de Tukey.
Recuperación de inoculantes
Para determinar la competitividad in situ de los bioinoculantes, se hicieron pruebas sobre el número de aislamientos con capacidad solubilizadora de fosfatos presentes en los sustratos de siembra de cada uno de los tratamientos, una vez se cosecharon las plantas. La recuperación de los aislados se hizo utilizando la técnica de dilución serial (Sánchez de Prager et al., 2006) y siembra en medio sólido Pikovskaya con fosfato tricálcico como única fuente de fósforo (15P). La solubilización de fosfatos identificada por la presencia de un halo de solubilización transparente alrededor de las colonias. Una vez purificados, los aislamientos se caracterizaron por pruebas microbiológicas estándar (Sánchez de Prager et al., 2006).
Resultados
Amplificación de secuencias nif
La reacción de PCR para la clonación de la secuencia parcial del gen nif amplificó a partir del ADN genómico del aislado B. ambifaria (UNBS7, carril 8) un segmento de aproximadamente 600 pb (Foto 1) el cual, no obstante, no fue secuenciado para determinar plenamente su identidad. No fue posible obtener un amplicón en el caso de B. lata (UNBS3, carril 4), lo cual podría indicar carencia del gen de la nitrogenasa en esta cepa particular, o baja especificidad de los cebadores utilizados.
Ensayos en invernadero
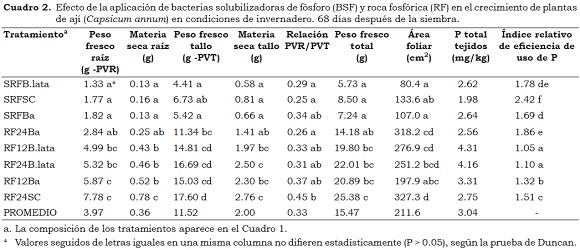
El análisis de varianza mostró que los tratamientos aplicados en condiciones de invernadero produjeron efectos significativamente diferentes (P < 0.05) sobre las variables de crecimiento analizadas, excepto para la relación peso fresco raíz/peso fresco tallo. Las medias de los tratamientos y su diferencia estadística según la prueba de Duncan aparecen en el Cuadro 2.
En todos los casos donde se presentaron diferencias significativas (P < 00.5) y altamente significativas (P < 0.01), el mayor efecto en las diferentes variables se logró con los tratamientos en los cuales se incorporó RF en el suelo. Es necesario destacar que la aplicación de las BSP permitió reducir a la mitad la dosis de RF necesaria para alcanzar los mismos valores estadísticos en materia seca y fresco del tallo, que el obtenido por las plantas fertilizadas con 24 g de RF no inoculadas. Un comportamiento similar se observó para las variables biomasa total (peso fresco total) y área foliar. Fue notable el efecto de la adición de RF sobre el crecimiento de la raíz, como se observa al comparar los tratamientos sin inóculo microbiano, con y sin adición de RF, donde el suministro de 24 g de RF significó un aumento de más de cuatro veces en el peso fresco de la raíz (1.77 g vs 7.78 g) y un incremento de aproximadamente 1.7 veces su volumen, efectos que significaron una mayor producción de materia seca en los tratamientos que recibieron la aplicación de RF.
La aplicación de solo RF (24 g) presentó un efecto notable en la producción de biomasa total y en área foliar (25.38 g y 327.3 cm2, respectivamente), mientras que la aplicación conjunta de RF con las BSP, disminuyó el área foliar (318.2 cm2 cuando se aplicó B. ambifaria y 251.2 cm2 cuando se inoculó el aislado de B. lata) y la biomasa total (14.18 g en el caso de la inoculación con B. ambifaria y 22.01 g cuando se aplicó B. lata). Igualmente se observaron diferencias (P < 0.05) para el efecto de la RF sobre el peso de la parte aérea de las plantas, tanto en base seca como en base fresca.
La aplicación de RF al sustrato en cualquiera de las dosis evaluadas conjuntamente con el bioinoculante redujo el valor de la relación peso fresco raíz /peso fresco tallo, de 0.45 a 0.26, con diferencia (P < 0.05) para el caso de B. ambifaria y a 0.3116 en B. lata, lo cual sugiere que para obtener una misma cantidad de biomasa aérea, las plantas inoculadas con las BSF requieren de una raíz con menor biomasa, pero más eficiente en los procesos de toma y absorción de nutrientes, procesos asociados con una arquitectura radical mejorada producida, probablemente, como respuesta a la acción microbiana. Lo anterior es confirmado por el hecho que las plantas inoculadas con solo BSP muestran, en relación con el testigo sin inocular, un mayor valor absoluto en el contenido de P total en los tejidos (2.62 mg/kg para las plantas tratadas con B. lata y 2.64 mg/kg en el caso de aquellas inoculadas con B. ambifaria, vs. 1.98 mg/kg para el testigo sin inocular).
Cuando la inoculación de las BSF fue acompañada de la aplicación de RF, el incremento en el contenido del P en los tejidos fue aún mayor. Así, las plantas suplementadas con 12 g de RF e inoculadas con B. lata presentaron 4.31 mg/kg de P, mientras que las fertilizadas con 24 g de RF y sin inocular sólo presentaron 2.75 mg/kg de fósforo (15P). Comparativamente las plantas inoculadas con B. ambifaria y suplementadas con 12 g de RF presentaron contenidos de P de 3.31 mg/kg, siendo superior también al testigo sin inocular y fertilizado con 24 g de RF.
En relación con la eficiencia en el uso del fósforo (15P) determinada como biomasa producida (g)/P total absorbido (g), fue evidente que las plantas fertilizadas con este nutriente fueron menos eficientes que aquellas no fertilizadas, independiente de que fueran o no inoculadas. Tomando como base la eficiencia en el uso del P en las plantas del tratamiento fertilizado con 12 g de RF e inoculado con B. lata, el cual presentó la eficiencia más baja, las plantas no inoculadas ni fertilizadas con RF presentaron una eficiencia 2.4 veces mayor. No se encontró, sin embargo, relación directa entre biomasa total y eficiencia de uso de fósforo (15P). Aunque las plantas no fertilizadas con RF presentaron una mayor eficiencia, no lograron producir una buena biomasa relativa a las plantas fertilizadas. En general, la aplicación de los aislados produjo un efecto negativo y significativo sobre la eficiencia en el uso de P en las plantas inoculadas (Cuadro 2).
Por otra parte, aunque la inoculación con BSF no favoreció una mayor biomasa radical, sí mejoró la arquitectura de la raíz, ya que aumentó la densidad de pelos radicales y de raíces secundarias y terciarias (Foto 2), necesarias para la toma y absorción de los nutrientes. Esta es la razón probable por la cual las plantas inoculadas presentaron mayores contenidos de P en tejidos. El incremento de raíces finas y pequeñas permite, además, a la planta un mejor aprovechamiento del volumen de suelo en busca de nutrientes y agua. Este efecto fue más notable cuando se utilizó adicionalmente RF como fuente de P (Foto 2).
Por el contrario, la aplicación de solo BSP, en particular el aislamiento de B. lata, ocasionó una reducción en términos absolutos, aunque no diferente estadísticamente, del área foliar y de la biomasa total en comparación con las plantas no inoculadas y no fertilizadas, un comportamiento similar al observado cuando las plantas recibieron fertilización con RF en las dosis evaluadas, lo que implica efectos negativos de las BSF sobre estas variables.
Recuperación de inoculantes
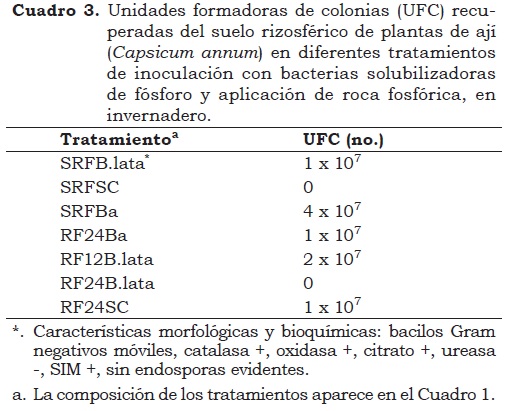
A excepción del tratamiento que incluyó la aplicación de 24 g de RF e inoculación con B. lata, del cual no fue posible obtener aislamientos bacterianos, de los demás tratamientos que incluyeron bioinoculantes, se recuperaron cantidades variables de poblaciones bacterianas (1 x 107 a 4 x 107 UFC) correspondientes taxonómicamente a los aislamientos inoculados, los cuales conservaron su capacidad solubilizadora de fosfatos (Cuadro 3). Del tratamiento testigo sin inóculo microbiano no fue posible recuperar BSF en medio de enriquecimiento PVK, lo cual apoya la hipótesis de que la inoculación de semillas antes de la siembra favorece el establecimiento de las poblaciones bacterianas sobre la superficie de las raíces de la planta.
Discusión
Los resultados en el presente ensayo confirman las respuestas positivas a la fertilización con RF y bioinoculación en campo y/o invernadero en diferentes cultivos (Rodríguez y Fraga, 1999; Dwivedi et al., 2004; Vassilev et al., 1996; Supanjani et al., 2006; Han et al., 2006; Leaungvutiviroj et al., 2010; Collavino et al, 2010). Este efecto sinérgico se puede explicar considerando que mientras la RF aporta principalmente fósforo, las BSP pueden tener efectos adicionales en la solubilización de este nutriente; por ejemplo, en la fijación de N, el biocontrol de patógenos y la producción de sustancias fitorreguladoras (Archand y Schneider, 2006). Aunque no se pudo comprobar en este estudio, es posible que B. ambifaria tenga actividad diazotrofa, según se deduce de los resultados de las pruebas moleculares efectuadas; de hecho, hay evidencia de que la diazotrofía es una característica ampliamente distribuida en varias especies de este género (Paungfoo-Lonhienne et al., 2014). Igualmente, las variaciones de la arquitectura radical en las plantas inoculadas indican la producción de sustancias con acción hormonal por las cepas de Burkholderia utilizadas en este ensayo, ya que se conocen evidencias circunstanciales de cambios morfológicos del sistema radical producidos en diferentes especies vegetales después de la inoculación con esta bacteria, que podrían estar relacionados con la producción de sustancias tipo auxinas (Coenye y Vandamme, 2006), hipótesis que puede ser tema de estudios futuros.
De otra parte, en el presente estudio la relación peso fresco de raíz/peso fresco del tallo, en la dosis máxima de RF (24 mg/kg) alcanzó un valor de 0.45; pero cuando la misma dosis se combinó con B. ambifaria, esta relación se redujo a 0.26, lo que sugiere una menor inversión de fotosintatos para la obtención de nutrientes y/o un incremento en la eficiencia de los procesos de toma y adquisición de nutrientes y agua a través de la raíz, debido a un mayor desarrollo radical lateral. Esta conclusión se apoya en el hecho de que los contenidos de P de los tejidos inoculados con las bacterias fueron mayores que los alcanzados por las plantas no inoculadas.
En resumen, los resultados del presente estudio ponen de manifiesto la importancia de usar la roca fosfórica como una fuente de fósforo alternativa a los fertilizantes sintéticos, particularmente en las condiciones del trópico, donde este estudio y otros han demostrado que es altamente eficiente en promover el crecimiento vegetal, especialmente cuando su aplicación se acompaña de la inoculación de microorganismos que, además de proveer de un suministro constante del nutriente a través de su actividad fisiológica normal, ejercen otras acciones benéficas sobre el metabolismo y la estructura vegetal. Es conveniente señalar que, además de ser una aproximación agronómicamente eficaz,la fertilización con RF y bioinoculantes es una práctica ambientalmente sostenible y poco costosa, adecuada a las condiciones socio-económicas y ambientales propias del trópico.
Conclusiones
- Los aislamientos bacterianos Burkholderia ambifaria y B. lata, solubilizadores de fosforo, cuando se inocularon en ají (Capsicun annum) se adaptaron a su rizosfera e incrementaron la eficiencia en el uso de roca fosfórica, lo que permitió reducir la aplicación de esta fuente de fósforo a la mitad, sin que ocurran diferencias significativas en la respuesta de las variables de crecimiento producción de biomasa total, área foliar y área y distribución de raíces.
- Del ADN genómico de los aislados de Burkholderia ambifaria se logró obtener por PCR, amplicones con potenciales secuencias del gen NifH, componente de la enzima Nitrogenasa.
Agradecimientos
Los autores agradecen a la Vicerrectoría de Investigaciones de la Universidad Nacional de Colombia sede Palmira por el apoyo financiero al proyecto, como uno de los ganadores de la Convocatoria Nacional de Investigación Año 2009.
Referencias
Abouzeid, A. Z. 2007. Physical and thermal treatment of phosphate ores - An overview. International journal of mineral processing 85(4):59 - 84. [ Links ]
Agyin-Birikorang, S.; O'Connor, G. A.; Jacobs, L. W.; Makris, K. C.; y Brinton, S. R. 2007. Long-term phosphorus immobilization by a drinking water treatment residual. J Environ. Qual. 36:316 - 323. [ Links ]
Arcand, M. M. y Schneider, K. D. 2006. Plant and microbial-based mechanisms to improve the agronomic effectiveness of phosphate rock: a review. Ann. Acad. Bras. Cienc. 78:791 - 807. [ Links ]
Biswas, D. R. y Narayanasamy, G. 2006. Rock phosphate enriched compost: An approach to improve lowgrade Indian rock phosphate. Bioresour. Technol. 97:2243 - 2251. [ Links ]
Chien, S. H. y Menon, R. G. 1995. Factors affecting the agronomic José de las Lajas, Cuba. Effectiveness of phosphate rock for direct application. Fert. Res. 41:227 - 234. [ Links ]
Coenye, T. y Vandamme, P. (eds.). 2006. Burkholderia: Molecular Microbiology and Genomics. Horizon Biosciences, U.K. 303 p. [ Links ]
Collavino, M.; Sansberro, P. A., Mroginski, L. A. y Aguilar, O. M. 2010. Comparison of in vitro solubilization activity of diverse phosphatesolubilizing bacteria native to acid soil and their ability to pro-mote Phaseolus vulgaris growth. Biol. Fert. Soils 46(7):727 - 738. [ Links ]
Cordell, D.; Drangert, J. A.; y White, S. 2009. The story of phosphorus: Global food security and food for thought. Global Environ. Change 19:292 - 305. [ Links ]
Dwivedi, B. S.; Singh, V. K.; y Dwivedi, V. 2004. Application of phosphate rock with or without Aspergillus awamori inoculation to meet phosphorus demands of rice-wheat systems in the indo-gangetic plains of India. Aust. J. Exp. Agr. 44: 1041 - 1050. [ Links ]
Edwards, A. C.; Walker, R. L.; Maskell, P.; Watson, C. A.; Rees, R. M.; Stockdale, E. A.; y Knox, O. G. 2010. Genetic engineering, biofertilisation, soil quality and organic farming. sustainable agriculture reviews. 4:99 - 117. [ Links ]
Fageria, N. K. 2009. The use of nutrients in crop plants. CRC Press. 448 p. [ Links ]
FAO (Food and Agriculture Organization of the United Nations). 2004. Use of phosphate rocks for sustainable agriculture. Fert. Plant Nutr. Bull. 13. [ Links ]
Gilbert, N. 2009. Environment: The disappearing nutrient. Nature, 461:716 - 718. [ Links ]
Han, S., Supanjani, H.; y Lee, K. D. 2006. Effect of co-inoculation with phosphate and potassium solubilizing bacteria on mineral uptake and growth of pepper and cucumber. Plant soil Environ. 52 (Suppl 3):130 - 136. [ Links ]
Ivanova, R.; Bojinova, D.; y Nedialkova, K. 2006. Rock phosphate solubilization by soil bacteria. J. University Chem. Technol. Metallurgy 41(3):297 - 302. [ Links ]
Khan, M. S.; Ahmad, E.; Zaidi, A.; y Oves, M. 2013. Functional aspect of phosphate-solubilizing bacteria: Importance in crop production. En: Maheshwari, D. K. et al. (eds.). Bacteria in agrobiology: crop productivity. Springer-Verlag Berlin Heidelberg. [ Links ]
Khan, M. S.; Zaidi, A.; Ahemad, M.; Oves, M.; y Wani, P. A. 2010. Plant growth promotion by phosphate solubilizing fungi-current perspective. Arch. Agron. Soil Sci. 56:73 - 98. [ Links ]
Lal, R. 2009. En: Climate change, intercropping, pest control and beneficial microorganisms. SpringerVerlag. 9 - 11. [ Links ]
Leaungvutiviroj, C.; Ruangphisarn, P.; Hansanimitkul, P.; Shinkawa, H. y Sasaki, K. 2010. Development of a new biofertilizer with a high capacity for N2 fixation, phosphate and potassium solubilization and auxin production. Biosci Biotechnol Biochem. 74(5):1098 - 1101. [ Links ]
Nziguheba G. 2007. Advances in integrated soil fertility management in Sub-Saharan Africa: Challenges and opportunities, Springer, Holanda. 149 - 160. [ Links ]
Patino Torres, C.; y Sánchez De Prager, M. 2012. Aislamiento e identificación de bacterias solubilizadoras de fosfatos habitantes de la rizosfera de chontaduro (B. gassipaes Kunth.). Rev. Biotecnol.Sector Agrop. Agroind. 9(2):176 - 186. [ Links ]
Paungfoo-Lonhienne, C.; Lonhienne, T. G.; Yeoh, Y. K.; Webb, R. I.; Lakshmanan, P. Chan, X.; Lim, P. E.; Ragan, M. A.; Schmidt, S. y Hugenholtz, P. 2014. A new species of Burkholderia isolated from sugarcane roots promotes plant growth. Microb. Biotechnol. 7(2):142 - 154. [ Links ]
Rajan, S. S. y Marwaha, B. C. 1993. Use of partially acidulated phosphate rocks as phosphate fertilisers. Fert. Res. 35:47 - 59. [ Links ]
Rajan, S. S. y Watkinson, J. H. 1992. Unacidulated and partially acidulated phosphate rock: agronomic effectiveness and the rates of dissolution of phosphate rock. Fert. Res. 33:267 - 277. [ Links ]
Rajan, S. S.; Watkinson, J. H. y Sinclair, A. G. 1996. Phosphate rock for direct application to soils. Adv. Agron. 57:78 - 159. [ Links ]
Rodriguez, H. y Fraga, R. 1999. Phosphate solubilizing bacteria and their role in plant growth promotion. Biotechnol. Adv. 17:319 - 339. [ Links ]
Sánchez De Prager, M.; Gallo, P. I.; Pineda Vasquez, M. E.; Pena, A.; Escarria, L.; Ramos, F. y Molina, O. 2006. Microbiología. En: Guías para el laboratorio 2006. Taller de Publicaciones Unal-Palmira. 115 p. [ Links ]
Singh, H. y Reddy, S. 2011. Effect of inoculation with phosphate solubilizing fungus on growth and nutrient uptake of wheat and maize plants fertilized with rock phosphate in alkaline soils. Europ. J. Soil Sci. 47:30 - 34. [ Links ]
Supanjani, H. H.; Jung, J. S.; y Lee, K. D. 2006. Rock phosphate-potassium and rock-solubilising bacteria as alternative, sustainable fertilizers. Agron. Sustain. Dev. 26:233 - 240. [ Links ]
Van Vuuren, D. P.; Bouwman, A. F.; y Beusen, A. H. 2010. Phosphorus demand for the 1970 - 2100 period: A scenario analysis of resource depletion. Global Environ. Change 20 (3):428 - 439. [ Links ]
Vassilev, N.; Franco, I.; Vassileva, M. y Azcon, R. 1996. Improved plant growth with rock phosphate solubilized by Aspergillus niger grown on sugarbeet waste. Biores. Technol. 55:237 - 241. [ Links ]
Whitelaw, M. A. 2000. Growth promotion of plants inoculated with phosphate solubilizing fungi. Adv. Agron. 69:99 - 151. [ Links ]
Yaryura, P. M.; León, M.; Correa, O. S.; Kerber, N. L.; Pucheu, N. L. y García, A. F. 2008. Assessment of the role of chemotaxis and biofilm formation as requirements for colonization of roots and seeds of soybean plants by Bacillus amylo-liquefaciens BNM339. Curr. Microbiol. 56(6):625 - 632. [ Links ]