Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Agronómica
Print version ISSN 0120-2812
Acta Agron. vol.63 no.3 Palmira July/Sept. 2014
https://doi.org/10.15446/acag.v63n3.42735
http://dx.doi.org/10.15446/acag.v63n3.42735
Agronomía
Quelato de hierro y agua de coco en la germinación in vitro de Rossioglossum grande (Orchidaceae)
Iron Chelate and coconut water in in vitro germination of Rossioglossum grande (Orchidaceae)
Vincenzo Bertolini1*, Anne Damon1 y Ángel Natanael Rojas Velázquez2
1Colegio de la Frontera Sur (ECOSUR). Carretera Antiguo Aeropuerto km. 2.5, CP: 30700, Tapachula, Chiapas, México. 2Facultad de Agronomía, Universidad Autónoma de San Luis Potosí, Álvaro Obregón # 64 Colonia Centro, CP: 78000, San Luis Potosí, S. L. P., México Tel. (444) 852 4058 Ext. 6. *Autor para correspondencia: Email: vbertolini@ecosur.mx Tel. (962) 628 9800 Ext. 5444, Fax (962) 628 9806.
Rec.:21.03.2014 Acep.:14.04.2014
Resumen
Rossioglossum grande (Lindl.) Garay & G.C. Kenn es una orquídea nativa mexicana, considerada en peligro de extinción por la NOM-059-Semarnat-2010. Teniendo en cuenta que la germinación asimbiótica in vitro es una herramienta estratégica para la conservación de orquídeas amenazadas, en este estudio se generó información básica mediante la comparación de la germinación de R. grande en medios Knudson C (KC) y Dalla Rosa y Laneri modificado con quelato de hierro y agua de coco (DR). Para el efecto se utilizaron un cultivo madre (CM) y dos subcultivos (C1 y C2) y los tratamientos se dispusieron en un diseño experimental totalmente aleatorio. Los resultados se analizaron mediante análisis de varianza y comparación de medias con la prueba de Tukey (P < 0.05) y Chi-cuadrada. A 60 días en el CM el medio de cultivo DR favoreció el desarrollo, la tasa de sobrevivencia y disminuyó la clorosis de los protocormos. A los 12 meses se presentó mayor desarrollo y mayor regeneración de protocormos. En los subcultivos C1 y C2 se registraron resultados similares lo que confirma que el DR acelera el desarrollo de los protocormos e incrementa su tamaño y tasa de regeneración. En síntesis, el empleo de hierro-quelato y agua de coco promueven el desarrollo in vitro de protocormos de R. grande.
Palabras clave: Chiapas, conservación, germinación, NOM-059-Semarnat-2010, protocormos.
Abstract
Rossioglossum grande (Lindl.) Garay & G.C. Kenn is a Mexican native orchid threatened to extinguish according to the NOM-059-Semarnat-2010. in vitro asymbiotic germination is a conservation tool widely used for threatened orchids. Generate basic knowledge about in vitro response of R. grande was the object of the work, comparing seed germination in Knudson C medium (KC) versus Dalla Rosa y Laneri medium (DR), modified adding iron chelate and coconut water. We distinguished three different stages of culture: the sowing culture (CM) and two subcultivated culture (C1 and C2). Experimental design was totally aleatory. Anova, Tukey's test (p< 0.05) y Chi-square were used to analyze germination variables averages. After 60 days from sowing (CM), seedling was more developed, and in general it had more percentage of green and vital protocorms using DR medium. After 12 months without subcultivate, we assist at regeneration of protocorms in DR medium in a significant way. In the subcultivation C1 and C2 we test similar responses. We assume that use of iron chelate and coconut water improves the protocorms development and their regeneration of R. grande in in vitro conditions.
Key words: Chiapas, conservation, germination, NOM-059-Semarnat-2010, protocorms.
Introducción
Orchidaceae es la segunda familia vegetal más grande por número de especies y comprende alrededor de 850 géneros y entre 20,000 y 30,000 especies (Dressler, 2005). México es el puente continental entre las Américas y posee una amplia diversidad biológica, favorecida por su alta variedad fisiográfica y climática (Rzedowski, 1986). La flora orquideológica de México se compone de 1.250 especies y subespecies, distribuidas en 168 géneros (Soto-Arenas et al., 2007; Salazar, 2013). Rossioglossum grande (Lindl.) Garay y Kenn es una orquídea epífita, distribuida en bosques de neblina entre México y Guatemala. En México es una de las especies registradas por el estado de Chiapas, específicamente en unos pocos sitios en la región del Soconusco (Damon et al., 2011). Se clasifica en peligro de extinción en el país (Semarnat, 2010) debido a la explotación no sostenible y a la pérdida de su hábitat. Para su conservación es urgente diseñar un método de propagación masiva. La propagación in vitro por semilla asegura la conservación de la diversidad genética y puede ser empleada para constituir bancos de germoplasma ex situ para fines de conservación (Wing-Yam y Arditti, 2009).
Las semillas de las orquídeas se encuentran entre las más pequeñas del reino vegetal, con dimensiones de décimas de milímetros y micras de gramos, características que les permiten una amplia dispersión espacial (Arditti y Abdul-Ghani, 2000). Debido a la falta de nutrimentos de reserva, su germinación en el medio natural se lleva a cabo a través de relaciones simbióticas obligadas con hongos micorrízicos tipo rhizoctonia (Hadley, 1997; Suárez et al., 2006). El empleo in vitro de estos hongos posiblemente es una herramienta útil, pero todavía no se han desarrollado protocolos efectivos para lograr una germinación simbiótica artificial y eficiente (Bertolini et al., 2011).
Se considera que el proceso de germinación empieza cuando la semilla se hincha y toma un color verde, lo que origina una estructura indiferenciada en forma esférica denominada protocormo. A su vez, este protocormo origina la plántula completa después de pasar por cinco etapas de desarrollo (Seaton y Ramsay, 2005). Estas etapas han sido descritas y divididas en: (1) formación del protocormo; (2) aparición de los rizoides; (3) aparición del meristemo apical; (4) desarrollo de la primera hoja; y (5) aparición de la primera raíz verdadera. De la etapa 5 en adelante se considera ya formada la plántula y se identifican tallos, hojas y raíces (Zettler y McInnis, 1994). A partir de las primeras orquídeas obtenidas por Knudson (1922, 1946, 1951), se ha producido abundante literatura sobre la germinación in vitro de orquídeas y se han desarrollado medios de cultivo para este fin. Sin embargo, el proceso puede ser lento antes de obtener plantas maduras (Sharma et al., 2004); por ejemplo, Buyun et al. (2004) reportan que el tiempo de cultivo in vitro de semillas de Cattleya sp. Es de 500 - 600 días y de 300 en Dendrobium sp. (Orchidaceae) antes de lograr aclimatar el material vegetal en condiciones de invernadero. Knudson (1951) observó que el rango de pH óptimo para el medio de cultivo de semillas de orquídeas varía entre 4.5 y 5.5, además, dicho medio tiende a acidificarse si se mantiene por tiempo prolongado. Este aspecto es importante si se considera que la germinación asimbiótica in vitro puede ser más o menos demorada, en función de la efectividad del protocolo.
En la germinación de algunas especies epífitas de la región Soconusco, se han empleado con éxito los medios C de Knudson (1946) y de Dalla Rosa y Laneri (1977) modificado por Damon et al. (2004). El primero es pobre en hierro, debido a que éste se encuentra presente en forma de sulfatos insolubles (FeSO4·H2O) (Hicks, 2007). El medio Dalla Rosa y Laneri modificado es una variante del medio Knudson C, que presenta fuentes de hierro en forma de quelatos (FeSO4.7H2O y NaEDTA), además, se emplea agua de coco en su formulación (Damon et al., 2004). No obstante el medio C de Knudson se ha empleado con éxito en la germinación de semilla de algunas especies de orquídeas (Seaton y Pritchard, 2011) y se sigue usando para probar la viabilidad de la semilla de orquídeas de diferentes especies (Hosomi et al., 2012; Nadarajan et al., 2011). Knudson (1922) observó que la sacarosa, la fructosa y otros complejos químicos de extractos vegetales favorecen la germinación y promueven el desarrollo de los protocormos. De igual manera, el endospermo líquido de la semilla de coco se ha usado en varios porcentajes y varias especies establecidas in vitro, incluyendo las orquídeas, ya que contiene vitaminas, enzimas, azúcares, fuentes nitrogenadas, reguladores de crecimiento y una fracción de sales inorgánicas (Hicks, 2007). El medio C de Knudson adicionado con NAA (1 mg/lt) y 15% de agua de coco, promueve la germinación de manera eficiente en la especie Dendrobium chrysantum Wall. (Orchidaceae) (De et al., 2006). Igualmente, el agua de coco empleada en Cattleya mendelii Dombrain (Orchidaceae) ha dado resultados significativos en la germinación, comparada con el testigo y con el uso de jugo de piña, AIA y GA3, respectivamente (Salazar-Mercado, 2012). En orquídeas terrestres de los género Habenaria y Ophrys se ha evidenciado el efecto positivo del agua de coco en el medio de cultivo, en término de formación y desarrollo de los protocormos (Stewart y Kane, 2006; Kitsaki et al., 2004). En la germinación de esporas de helecho, Smith y Yee (1975) observaron que el empleo de esa agua beneficia la germinación en términos de tiempo; además promueve la ramificación del gametofito, si se usa en concentraciones altas, debido a la acción conjunta de fuentes nitrogenadas (aminoácidos y aminas) y fuentes de azúcares. Los efectos promotores del agua de coco se deben a la presencia de compuestos orgánicos como citoquininas, zeatinas, kinetinas y purinas, que se consideran promotores del crecimiento vegetal (Yong et al., 2009; Hicks, 2007). Es un hecho que en la composición de esta agua extraída de cocos verdes, los fitorreguladores presentes son citoquininas, con un total de diez compuestos, seguidas por dos giberelinas y una auxina (Yong et al., 2009). Las citoquininas juegan un papel fundamental en la organogénesis vegetal, ya que inducen la formación de hojas y brotes y aumentan la velocidad de desarrollo y la germinación de la semilla (Werner et al., 2001; Huan et al., 2004).
Como hipótesis de este estudio se plantea que el hierro en forma de quelato y el agua de coco, añadidos al medio de cultivo C de Knudson (1946), incrementan el desarrollo in vitro de protocormos de R. grande y promueven su regeneración. El objetivo fue comparar el medio C de Knudson (1946) con el de Dalla Rosa y Laneri (1977) modificado (Damon et al., 2004) y conocer la respuesta en el desarrollo de los protocormos, para diseñar a mediano plazo un protocolo adecuado para la germinación in vitro de la especie.
Materiales y métodos
En marzo de 2012, se recolectó una cápsula (fruto) dehiscente de R. grande procedente de un sitio en la región terrestre prioritaria 135, corredor biológico Tacaná-Boquerón del Estado de Chiapas. Las semillas fueron desinfectadas sumergiéndolas en 100 ml de solución de NaOCl al 1% y tres gotas de emulsionante (Tween® 20) en agitación por 10 min. Un vez retiradas de la solución, se enjuagaron con agua desionizada estéril por tres veces consecutivas.
Los medios de cultivo Knudson (1946) (KC = Tratamiento 1) y Dalla Rosa y Laneri (1977) modificado (Damon et al., 2004) (DR = Tratamiento 2) fueron preparados ajustando el pH a 5.5 y esterilizados en autoclave a 121 °C, 101 kPa por 20 min. El agua de coco (Cocos nucifera L.) usada en el medio DR fue extraída y filtrada de frutos verdes producidos en la región del Soconusco.
Las semillas fueron sembradas el 13-03-2012 siguiendo el protocolo descrito por Seaton y Ramsay (2005) en cuatro cajas Petri por cada tratamiento. En cada caja Petri se colocaron aproximadamente 1.000 semillas. Al total de las placas se le denominó cultivo madre (CM). El desarrollo de los protocormos en CM fue evaluado a 30, 45 y 60 días desde la fecha de siembra. Después de transcurridos cien días de la siembra, se realizó la trasferencia de protocormos a medio fresco para obtener el primer subcultivo (C1), compuesto por cinco cajas Petri por tratamiento. Se emplearon protocormos homogéneos clasificables como etapa de desarrollo 2 (con rizoides), descrita por Zettler y McInnis (1994). Los protocormos no subcultivados fueron mantenidos en el CM. De esta manera el cultivo CM y el C1 fueron evaluados durante un año a partir de la siembra de la semilla. En cada caja Petri se cultivaron aproximadamente 150 protocormos.
El subcultivo 2 (C2) se obtuvo después de 110 días de haber originado el C1, para lo cual se utilizaron protocormos homogéneos clasificables como etapa 2 (con rizoides) (Zettler y McInnis, 1994) para un total de cinco cajas Petri por tratamiento. Cada mes, hasta doce meses después de la siembra inicial, se evaluó el estado de los protocormos. Todos los cultivos fueron mantenidos a 25° ± 2 °C, con un tiempo de iluminación de 16 h/día con tubos fluorescente de luz fría.
La calidad de los protocormos en los cultivos (CM, C1, C2) se evaluó como: número de protocormos muertos (PM), número de protocormos vivos (PV), número de protocormos en etapa de desarrollo 2 (E2), y número de protocormos en etapa 3 (con meristemo apical visible) en adelante (E3), número de protocormos pigmentados (Pver), número de protocormos albinos (PA), número de protocormos parcialmente albinos (protocormos cloróticos con zonas pigmentadas por arriba de 30% de su superficie total) (PpA), número de protocormos con un meristemo apical (Pmono), número de protocormos con dos meristemos (Pbi), número de protocormos con múltiples meristemos (Pmulti), y diámetro del protocormo (DP). Para el cultivo CM se consideraron además: el número de protocormos hinchados sin rompimiento de testa (PH), hinchados con rompimiento de testa (PHRT), oxidados (PO), cloróticos (PCl), con rizoides (PR), y con primordio foliar (PF). Igualmente, al finalizar cada ensayo se midió el pH del medio en los tres cultivos (CM, C1, C2) utilizando un potenciómetro digital y 5 mm3 de medio por tratamiento.
El diseño experimental utilizado fue totalmente aleatorio, la repetición consistió en cada protocormo analizado. Los datos fueron analizados mediante varianza, con el software Minitab 15® (2007). Para las variables de frecuencia se empleó la prueba no paramétrica de Chi-cuadrada de Pearson para comparar los tratamientos, mientras que en el caso del diámetro de protocormos se usó la prueba paramétrica de Tukey DHS (P < 0.05). La investigación se realizó en el laboratorio de Ecología y Cultivo Sustentable de las Orquídeas del Soconusco, en el Colegio de la Frontera Sur (Ecosur), Unidad Tapachula. La medición del pH de los medios se hizo en el campus Rosario Izapa, Tuxtla Chico, del Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias (INIFAP).
Resultados y discusión
Cultivo madre (CM)
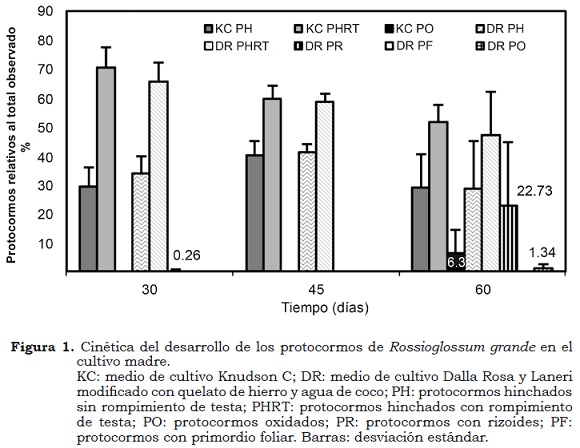
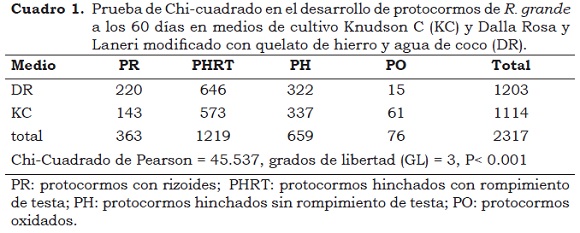
A los 60 días después de la siembra de las semillas, en el medio DR se presentó un menor porcentaje de protocormos oxidados que el medio KC (Figura 1 y Cuadro 1). Al mismo tiempo, a los 30 y 60 días, en el medio DR se produjeron el mayor número de protocormos con presencia de rizoides y primordios foliares, respectivamente (Figura 1). A 60 días, el análisis Chi-cuadrada mostró diferencias (P < 0.005) entre ambos tratamientos, en relación con las etapas de desarrollo alcanzadas por los protocormos (Cuadro 1), donde el medio DR mostró mayor cantidad de protocormos con rizoides (PR). A esta edad, el medio KC registró una reducción del pH mayor que el medio DR (pHKC = 4.3 vs. pHDR = 5.1), probablemente debido a la baja capacidad amortiguadora del medio KC, previamente observada por Hicks (2007).
Las observaciones a los 12 meses mostraron diferencias (P < 0.05) en la sobrevivencia, las etapas de desarrollo y la regeneración de los protocormos (Cuadro 2). No obstante que el medio DR generó valores inferiores de protocormos muertos con respecto al medio KC, ambos porcentajes no se consideran suficientes desde el punto de vista comercial; pero sí se debe valorar este resultado si se considera el alto valor ecológico de la especie y la falta de conocimiento previo de su respuesta en cultivo in vitro. En etapas más avanzadas de desarrollo, el medio DR produjo un mayor número de protocormos (P < 0.005) en comparación con el medio KC (Cuadro 2).
El diámetro de protocormos mostró diferencias (P < 0.001) entre tratamientos, con valores mayores en el medio DR; lo que no ocurrió con el grado de clorosis que fue similar entre tratamientos, ni con el pH (4.2) a 12 meses.
Subcultivo 1 (C1)
Al finalizar el periodo experimental C1 se observó nuevamente un porcentaje elevado de protocormos muertos en ambos tratamientos, lo que no ocurrió en el medio DR donde el desarrollo y la regeneración fueron mayores (P < 0.005) (Cuadro 3). El diámetro de los protocormos (DP) 12 meses después de la siembra fue mayor (P < 0.005), siendo de 5.28 ± 2.024 mm en el medio DR vs. 2.6 ± 0.902 mm en el medio KC. La clorosis fue similar (Chi-cuadrada = 4.266, P < = 0.118) y el pH en el medio KC fue menor (4.8) que en DR (5.1), valores que coinciden con los encontrados por Hicks (2007) y muestran que el medio KC tiene baja capacidad amortiguadora. No obstante Knudson (1951) considera que el pH óptimo para el cultivo de orquídeas se encuentra en el rango 4.5 < 5.5.
Subcultivo 2 (C2)
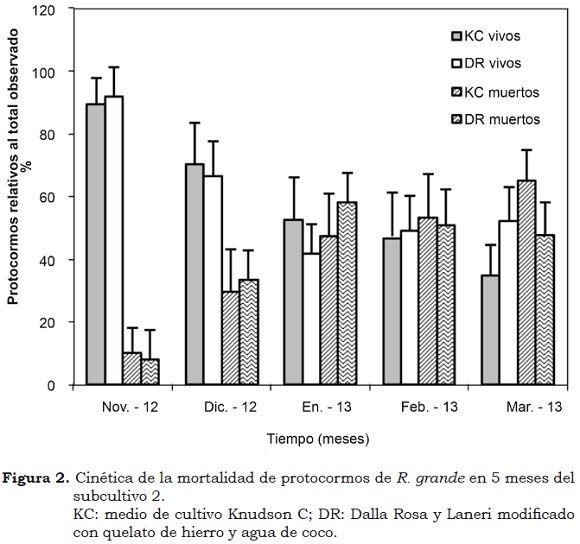
En ambos tratamientos se hallaron protocormos muertos. En el medio DR este fenómeno no se presentó después del tercer mes; mientras que en el KC continuó hasta el quinto mes (Figura 2 y Cuadro 4). Esta alta mortalidad probablemente sea el resultado del estrés ocasionado por el trasplante en medio fresco, ya que la densidad de protocormos por caja Petri fue menor. La clorosis también se presentó de forma significativa después de 12 meses de subcultivo de los protocormos (P < 0.001), siendo menos notable en el tratamiento DR (Cuadro 4). En este caso, el cultivo fresco y el contenido de quelato de hierro favorecieron la salud de los protocormos en este tratamiento.
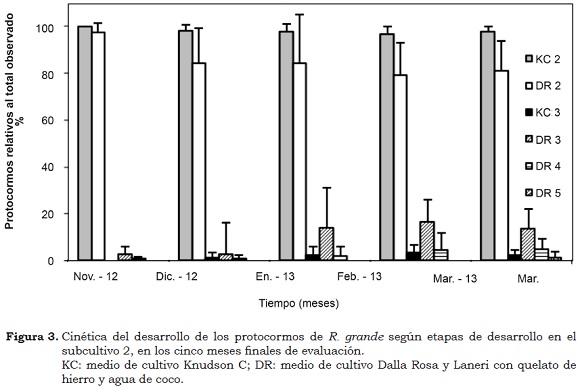
En los cinco meses finales de estudio, las variables de desarrollo de los protocormos mostraron mejores índices en aquellos subcultivados en el medio DR, en el que se presentaron en etapas 4 y 5, en comparación con el medio KC que sólo mostró protocormos en etapas 2 y 3 (Figura 3). A los 12 meses, la cantidad de protocormos en etapas avanzadas de desarrollo (E3) contrastaron (P < 0.002) entre los medios DR y KC, estando de nuevo a favor del medio DR (Cuadro 5). La regeneración de los protocormos fue significativo (P < 0.005) y mostró que, no obstante la elevada mortalidad, gracias a este proceso en el medio DR se pueden remplazar las pérdidas de estas estructuras (Cuadro 5).
El diámetro de los protocormos fue mayor (P < 0.001) en el medio DR, donde alcanzó un valor promedio de 5.8 ± 1.81 mm vs. 2.36 ± 0.54 mm en medio KC. El resultado mostró nuevamente el bajo poder de amortiguación del medio KC frente al DR (pHKC = 4.5, pHDR = 5.2).
En los medios de cultivo evaluados (CM, C1 y C2) los hallazgos coincidieron con los de Vacin y Went (1949) e Hicks (2007) en relación con la baja capacidad amortiguadora del pH en medio KC, el cual afecta la calidad del material vegetal cuando el cultivo es mantenido por prolongados periodos. En el CM, los protocormos en medio KC mostraron mayor clorosis y mortalidad, probablemente debido a la precipitación del hierro en forma de sulfato, siendo éste un riesgo existente en este tipo de medio (Hicks, 2007). El medio DR resultó menos sensible al descenso en pH que el medio KC, lo que se destacó en los protocormos del cultivo C2. Sin embargo, la mortalidad se dio en ambos tratamientos, con valores poco recomendables para el uso comercial de ambos medios en la especie evaluada, no obstante, para propósitos de conservación, estos resultados pueden considerarse aceptables.
Para desarrollo y regeneración de los protocormos, el medio DR presentó los valores más altos en todas las etapas del estudio, lo que ratifica los efectos benéficos del agua de coco sobre las variables del estudio. Los resultados en este trabajo concuerdan con los de Hicks (2007) quien encontró que el agua de coco puede promover la regeneración espontánea de protocormos in vitro del género Oncidium (Orchidaceae). El género Rossioglossum es filogenéticamente cercano a Oncidium y ambos pertenecen a la subfamilia Epidendroideae, subtribu Oncidinae (Soto Arenas et al., 2007). Por tanto, lo observado puede ser una característica propia de la especie estudiada, que se expresa mediante el empleo de agua de coco en el medio de cultivo in vitro.
Conclusiones
- El estudio proporciona un avance acerca de la respuesta en germinación y desarrollo de los protocormos de Rossioglossum grande (Lindl.) Garay & Kenn cultivado in vitro en medio Dalla Rosa y Laneri modificado y en medio C de Knudson.
- Se comprobó que la presencia de quelato de hierro y agua de coco (medio DR) promueve el desarrollo e induce una mayor regeneración de los protocormos, comparado con el medio C de Knudson.
- No obstante la alta mortalidad, la posibilidad de promover regeneración de protocormos puede ser interpretada como una ventaja productiva que permite aumentar el número de plántulas producidas a partir de una cantidad limitada de semillas.
- No obstante estos resultados positivos, se debe mejorar el protocolo de cultivo in vitro de semillas de R. grande, evaluando otros medios de cultivo con diferentes concentraciones de agua de coco e incluyendo carbón activado para limitar el fenómeno oxidativo y la alta mortalidad.
Agradecimientos
Al doctor Leobardo Iracheta Donjuán, Investigador titular de INIFAP, campus Rosario Izapa, Tuxtla Chico (Chiapas, México) por las sugerencias y aportes brindados en el estudio de las condiciones hídricas de los protocormos y su medio de cultivo.
Referencias
Arditti, J. y Abdul-Ghani, A. K. 2000. Transley Review No. 110. Numerical and physical properties of orchid seeds and their biological implications. New Phytol. 145:367 - 421. [ Links ]
Bertolini, V.; Damon, A. y Rojas Velázquez, A. N. 2011. Symbiotic germination of three species of epiphytic orchids susceptible to genetic erosion, from Soconusco (Chiapas, Mexico). Eur. J. Environ. Sci. 1(2):60 - 68. [ Links ]
Buyun, L.; Lavrentyeva, A.; Kovalska, L. E Ivannikov, R. 2004. in vitro germination of seeds of some rare tropical orchids. Acta Universitatis Latviensis, Biol. 676:159 - 162. [ Links ]
Dalla Rosa, M. y Laneri, U. 1977. Modification of nutrient solutions for germination and growth in vitro of some cultivated orchids and for the vegetative propagation of Cymbidium cultivars. Amer Orchid Soc. Bull. 46:813 - 820. [ Links ]
Damon, A.; Aguilar-Guerrero, E.; Rivera, L. y Nikolaeva, V. 2004. Germinación in vitro de semillas inmaduras de tres especies de orquídeas de la región del Soconusco, Chiapas, Mexico. Rev. Chapingo Serie Hortic. 10(2):195 - 203. [ Links ]
Damon, A.; Solano-Gómez, R.; García-González, A. 2011. Diversidad y conservación de las orquídeas del corredor biológico Tacaná-Boquerón. Fondos Mixtos, Chiapas. 37 p. [ Links ]
De, K. K.; Majumdar, S.; Sharma, R. N.; y Sharma, B. 2006. Green pod culture and rapid micropropagation of Dendrobium chrysantum Wall. - an horticultural and medicine orchid. Folia Hortic. 18(1):81 - 90. [ Links ]
Dressler, R. L. ¿How many orchid species? 2005. Selbyana 26:155 - 158. [ Links ]
Hadley, G. 1997. Orchid mycorrhiza. En: Arditti, J. y Pridgeon, A. M. (eds.). Orchid Biology: Reviews and Perspectives vol. 2. Cornell University Press. Ithaca, Nueva York. p:83 - 118. [ Links ]
Hicks, A. J. 2007.Orchid seed germination media, a compendium of formulations. The Orchid Seed Bank Project, Chandler, USA. 210 p. [ Links ]
Hosomi, S. T.; Custódio, C. C.; Seaton, P. T.; Marks, T. R.; y Machado-Neto, N. B. 2012. Improved assessment of viability and germination of Cattleya (Orchidaceae) seeds following storage. in vitro Cell. Dev. Biol.-Plant 48:127 - 136. [ Links ]
Huan, L. V. T.; Takamura, T.; y Tanaka, M. 2004. Callus formation and plant regeneration from callus through somatic embryo structures in Cymbidium orchid. Plant Sci. 166:1443 - 1449. [ Links ]
Kitsaki, C.; Zigouraki, S.; Ziobora, M.; y Chintziest, S. 2004. in vitro germination, protocorm formation and plantlet development of mature versus immature seeds from several Ophrys species (Orchidaceae). Plant Cell Rep. 23:284 - 290. [ Links ]
Knudson, L. 1922. Nonsymbiotic germination of orchid seeds. Bot. Gaz. 78(1):1 - 25. [ Links ]
Knudson, L. 1946. A new nutrient solution for orchid seed germination. American Orchid Society Bulletin 15:214 - 217. [ Links ]
Knudson, L. 1951. Nutrient solutions for orchids. Bot. Gaz. 112(4):528 - 532. [ Links ]
Minitab® 15.1.39.0 - © 2007 Minitab INC. [ Links ]
Nadarajan J.; Wood, S.; Marks, T. R.; Seaton, P. T.; y Pritchard, H. W. 2011. Nutritional requirements for in vitro seed germination of 12 terrestrial, lithophytic and epiphytic orchids. J. Trop. Forest Sci. 23(2):204 - 212. [ Links ]
Rzedowski, J. 1986. Vegetación de México. 3a. Edición. Limusa, México, D.F. 432 p. [ Links ]
Salazar, G. A. 2013. Two additions to the Mexican orchid flora. Nota Científica. Rev. Mex. de Biodiversidad 84(1):378 - 380. [ Links ]
Salazar-Mercado, S. A. 2012. Germinación asimbiótica de semillas y desarrollo in vitro de plántulas de Cattleya mendelii Dombrain (Orchidaceae). Acta Agronómica 61(1):69 - 78. [ Links ]
Seaton, P. T. y Pritchard, H. W. 2011. Orchid seed store for sustenaible use: a model for future seedbanking activities. Lankesteriana 11(3):349 - 353. [ Links ]
Seaton, P. T. y Ramsay, M. 2005. Growing orchid seed. Royal Botanic Garden, Kew, Londres. 82 p. [ Links ]
Semarnat (Secretaría de Medio Ambiente y Recursos Naturales). 2010. Norma Oficial Mexicana NOM-059-Semarnat-2010, Protección ambiental - Especies nativas de México de flora y fauna silvestres - Categorías de riesgo y especificaciones para su inclusión, exclusión o cambio - Lista de especies en riesgo. Diario Oficial de la Federación, 30 de diciembre de 2010. 78 p. [ Links ]
Sharma R. N.; Sharma, B.; y De, K. K. 2004. Micropropagation of Dendrobium fimbriatum Hook - an endangered orchid of Sikkim Himalaya. J. Hill. Res. 17(2):65 - 67. [ Links ]
Smith, C. W. y Yee, R. N. 1975. The effect of coconut milk on the germination and growth of spores of Nephrolepis hisutula. Am. Fern J. 65 (1):13 - 18. [ Links ]
Soto Arenas, M. A.; Hágsater, E.; Jiménez Machorro, R.; et al. 2007. Las Orquídeas de México. Catalogo Digital. Disco interactivo multimedia Win-Mac. Herbario AMO, Instituto Chinoin, A.C. México. [ Links ]
Stewart, S. y Kane, M.. 2006. Asimbiontic seed germination and in vitro seedling development of Habenaria macroceratitis (Orchidaceae), a rare Florida terrestrial orchid plant. Cell. Tiss. Organ Cult. 86:147 - 158. [ Links ]
Suárez, J. P.; Weib, M.; Abele, A.; Garnica, S.; Oberwinkler, F.; y Kottke, I. 2006. Diverse tulasnelloid fungi form mycorrhizas with epiphytic orchids in an Andean cloud forest. Mycol. Res. 110:1257 - 1270. [ Links ]
Vacin, E. y Went, F. W. 1949. Some pH changes in nutrient solution. Bot. Gaz. 110(4): 605 - 613. [ Links ]
Werner, T.; Motyka, V.; Strnad, M. y Schmulling, T. 2001. Regulation of plant growth by cytokinin. Proc. Natl. Acad. Sci. 98:10487 - 10492. [ Links ]
Wing-Yam, T. y Arditti, J. 2009. History of orchid propagation: a mirror of the history of biotechnology. Plant Biotec. Rep. 3:1 - 56. [ Links ]
Yong, J. W.; Ge, L.; Ng, Y. F.; y Tan, S. N. 2009. The chemical composition and biological properties of coconut (Cocos nucifera L.) water. Molecules 14:5144 - 5164. [ Links ]
Zettler L. W. y McInnis, T. M. 1994. Light enhancement of symbiotic seed germination and development of an endangered terrestrial orchid (Platanthera integrilabia). Plant Sci. 102:133 - 138. [ Links ]